Chia-Pet技术与应用研究
2020-07-04许立
许立

摘要:特定DNA调控元件之间的长距离染色质接触在基因表达调控中起着关键作用,在理解信号网络和细胞状态时,必须对这些三维(3D)染色质结构中的相互作用进行全局表征。利用成对末端标记序列(Chia-Pet)进行染色质相互作用分析是一种将功能染色质结构转化为数百万个短标记序列的方法。自2009年開发以来,在染色质相互作用分析中具有独特的优势,从而为转录调控的研究提供了新的视角。本文介绍了Chia-Pet的实验方案和数据分析过程,分析了几种常用工具各自的特点和适用范围,帮助研究人员选用合适的方法以获得更可靠的结果。
关键词: 基因表达调控; 三维染色质结构; Chia-Pet
【Abstract】 Long-distance chromatin contact between specific DNA regulatory elements plays a key role in gene expression regulation. Global characterization of the interactions in these three-dimensional (3D) chromatin structures is essential in understanding signal networks and cell states. Chromatin interaction analysis using Paired-End-Tag sequencing (Chia-Pet) is a method for transforming functional chromatin structures into millions of short labeling sequences. Since its development in 2009, it has unique advantages in chromatin interaction analysis, which provides a new perspective for the study of transcriptional regulation. This paper introduces the experimental scheme and data analysis process of Chia-Pet, analyses the characteristics and application scope of several commonly used tools, and helps researchers choose appropriate methods to obtain more reliable results.
【Key words】 gene expression regulation; three-dimensional chromatin structures; Chia-Pet
0 引 言
转录调控是真核生物中一个复杂而有序的过程,其中染色质相互作用起着关键作用,从而调节基因表达,并进一步影响其他细胞的活动。许多研究转录因子(tf)与转录调控的结合的技术已经被开发出来。例如染色质免疫沉淀(chip)微阵列(chip chip)[1]、chip pet[2]和chip seq[3],但却无法确定远端tf结合位点的靶基因。另一个挑战是确定这种远端结合位点是否具有功能性,即通过染色体环在物理上接近靶基因启动子,或吸引RNA聚合酶Ⅱ复合物进行基因转录。因此,鉴定全基因组远端染色质相互作用,将调控元件引导至目标基因,可能为转录调控的研究提供新的视角。染色体构象捕获(3c)[4]及其衍生物,4c[5-6]和5c[7]可以揭示参与转录调控的长程染色质相互作用,但这些技术受到限制,或者是因为其整体性较低,如3c,或者是因其无法在整个基因组中绘制高分辨率的相互作用区域[8]。染色质相互作用分析与配对末端标记测序(Chia-Pet)方法就能够符合分析高吞吐量和高分辨率基因组水平上染色质相互作用这些要求。与HI-C[9]相比,Chia-Pet在与功能研究相关的蛋白质相关的更高分辨率上更好,确定TF结合位点和染色质相互作用,为以三维(3D)方式研究长程染色质相互作用奠定了坚实的基础,并提供了更可靠的方式。目前,Chia-Pet已成功应用于人MCF7细胞[10]、人癌细胞[11]、人T细胞[12]、小鼠胚胎干细胞[13]、小鼠神经祖细胞[14]和小鼠B细胞[15]以及其他细胞[16]。
为了系统评价Chia-Pet的方法,本文将详细探讨该方法的实验方案,与此同时,为方便后续研究分析,很多分析Chia-Pet数据的计算方法被提出,本文对这些计算方法进行了较为全面的研究与论述。
1 Chia-Pet实验方案介绍
对端测序的结果存储在2个fastq文件中,可以使用Chia-Pet工具[17]或其他方法[18]进行处理。通常,Chia-Pet数据处理有7个步骤(见图1),分别是:连接子过滤;Pet映射;冗余去除;自连和互连Pet分类;结合位点分析自连Pet;用互连Pet进行染色质相互作用分析;染色质相互作用数据的可视化。
在第一步中,连接体将与参考半连接体核苷酸序列对齐。除标签序列外,有2种半连接体,分别命名为A和B,而且具有相同的核苷酸。因此,根据连接体的组成将PET分为2类:相同的连接体(AA或BB)和不同的连接体(AB或BA)。然后将连接体从原始测序片段中排除,并保留剩余的DNA片段以供进一步分析。在连接体过滤后,使用BWA[19]、Bowtie[20]、Batmis[21]或其他绘图工具将短DNA序列与参考基因组对齐。使用samtools[22]和bedtols[23]过滤掉冗余和低质量的映射序列。自连PET是指从两端循环的单个DNA片段的测序片段,并在同一染色体上的短距离内映射到基因组。互连PET是指来自不同DNA片段的测序片段,通常2个标签位于不同染色体中或长距离位于同一染色体中。虽然使用自连PET来确定基因组上的蛋白质结合位点,但是互连PET可以通过聚类来预测染色质相互作用。在此基础上还须确保2个结合位点之间的交互集群确实存在或者是偶然发生的。Li等人[17]使用基于超几何分布的Fisher精确检验来量化相互作用频率。Paulsen等人[18]提出了一种基于非中心超几何分布的新统计模型,该模型将基因组距离依赖关系考虑在内进行p值估计。最后,构建Chia-Pet浏览器来报告数据并可视化结合位点以及交互集群。
通过数据处理获得的相互作用需通过湿实验室进行验证。短基因组距离中DNA元件间的相互作用可以通过3C实验验证。对于远距离相互作用中的DNA片段(位于不同染色体或同一染色体中的两个锚点,距离超过100万碱基对),可以使用显微镜技术,如DNA荧光原位杂交(DNA-FISH)[24]直接观察相互作用锚的位置和核中的相对空间距离。
2 Chia-Pet数据分析方法
2.1 Chia-Pet Tool介绍
正如预期的那样,这种方法识别的交互要比CPT少得多。虽然这种方法能够产生准确的交互,但是软件只执行Chia-Pet数据分析、交互评分中的最后一步。因此,用户必须编写自己的软件来查找和删除链接器序列、对齐宠物、删除重复项、调用峰值、将宠物分组到交互中并确定宠物距离的下限。因此,该软件仅对具有重要编程技能的研究人员有用。已经描述了其他软件包,但这些软件包或者不公开,或者与CPT和Chiasig有类似的限制。
2.3 Mango介绍
Mango[25]将基因组位点间相互作用的可能性作为距离和峰深的函数进行建模,并使用该模型为相互作用分配统计置信度。值得注意的是,Mango用一种简单而健壮的贝叶斯方法取代了计算上昂贵的距离匹配重布线方法。
由于使用方便和准确性的提高,Mango将通过对Chia-Pet数据集的分析,大幅提升揭示三维染色质结构特征和功能的能力。同时也纠正了非特定的相互作用,可以作为一个基因组接近和峰深的函数。本次研究证明,与CPT(现有的Chia-Pet分析管道)和Chiasig(为Chia-Pet交互提供统计置信度估计的软件包)相比,Mango表现出更高的准确性。将Mango应用于多个Chia-Pet数据集,可以独立复制与NAT相关的发现。三维染色质环的结构,包括对具有内向基序的CTCF结合位点的强富集。
除了提高准确性之外,Mango的可用性也颇受青睐。Mango被设计成所有的研究人员都可以使用。Mango很容易安装,只需一个命令就可以完成从fastq到交互的所有步骤。
2.4 MICC介绍
MICC[26],一种易于使用的R包,用于处理Chia-Pet数据。MICC旨在以高灵敏度检测染色质相互作用,同时将错误发现率(FDR)控制在合理水平。 MICC的输入是源自Chia-Pet数據的原始PET簇。 MICC的最终输出包括:将PET簇描述为真实相互作用簇的后验概率列表和相应的FDR。在不同数据集的相同FDR上,MICC总能检测到比Chia-Pet工具和ChiaSig更多的相互作用。此外,MICC检测到的相互作用在生物学重复之间也更加一致。
2.5 各种工具之间的性能比较
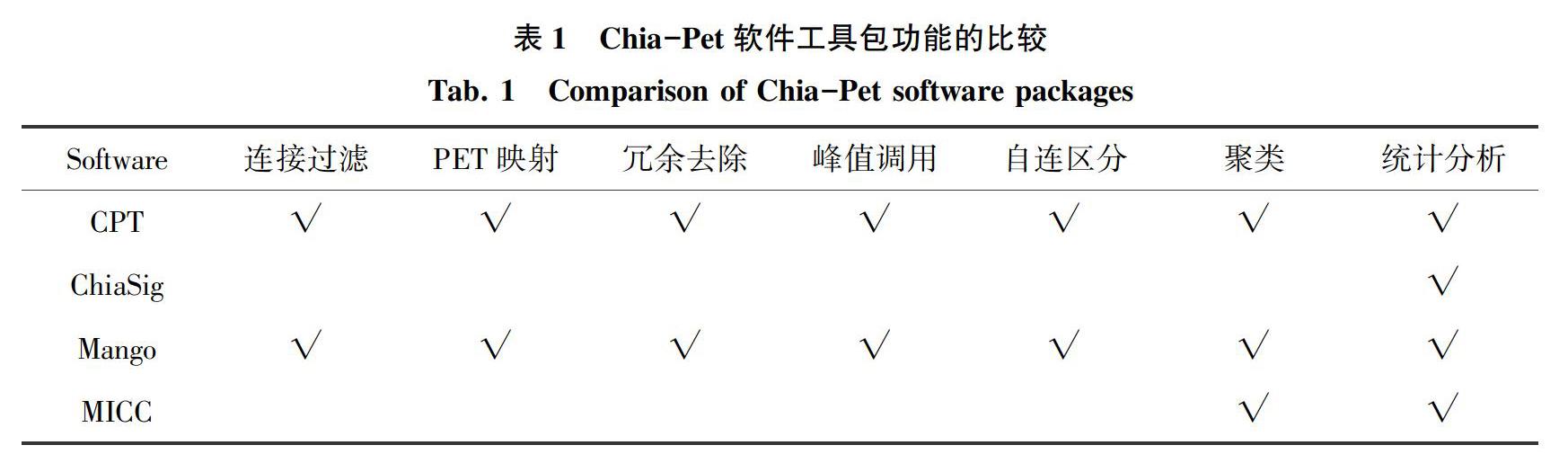
Mango仅依赖4个广泛使用且易于安装的软件包。相比之下,CPT需要具体的操作系统配置,主要有复杂的编程语言和环境阵列,包括C、Perl、Python、R、 Mysql、Apache Web Server和Php,并附带7页的安装指南。Chiasig可以轻松安装,但只执行分析Chia PET数据所需的单个步骤。因此,用户要编写自己的代码来执行大多数处理步骤,包括连接解析、PET映射、冗余去除、峰值调用和距离过滤,详见表1。
MICC,从Chia-Pet的数据中检测显著染色质相互作用。与Chia-Pet工具相比,MICC使用较低深度的测序库恢复了较高深度测序库中检测到的交互作用的显著比例。同时,还为宠物集群提供了更一致的排序,从而可以提高实验复制之间的再现性。通过与5C数据的比较,分析后发现MICC能比Chiasig更有效地检测相互作用。此外,MICC检测到的低PET计数的相互作用与5C数据有很大的重叠,这表明MICC寻找弱相互作用是可行的。这些特性使MICC优于其他现有的工具,特别是在以较少的排序深度处理ChiaPET数据时。
3 Chia-Pet技术应用
3.1 研究DNA片段之间的相互作用
Chip Seq用于分析DNA和蛋白质之间的相互作用,而Chia-Pet则从根本上研究DNA片段之间的相互作用。Fullwood等人[27]使用Chia-Pet技术构建了由人乳腺癌细胞系MCF7的雌激素受体α(ER-a)结合的染色质相互作用网络,发现长程ER-α结合位点主要位于启动子区域。Handoko等人[28]发现CTCF介导的小鼠胚胎多能干细胞相互作用。Chia-Pet揭示的5个不同的染色质结构域为染色体结构组织提供了新的CTCF功能模型,并将增强子与基因转录调控的启动子连接起来。
在描述人类T细胞中增强子-启动子相互作用后,Chepelev等人[29]提出增强子以细胞特异性的方式增加其靶基因的表达,相互作用的启动子是共存的。此外,细胞核中的染色体在多个层次上被组织起来发挥作用,除CTCF外,还有许多因素可能参与T细胞的这一过程。在未来的研究中,需要对详细的机制进行探讨。
He等人[30]根据Chip Seq获得的ER-α结合峰计算DNA环化的可能性,继而预测ER-α介导的染色质相互作用。这是第一个使用Chip Seq预测染色质相互作用的工作,为Chia-Pet提供了补充。
3.2 构建染色质相互作用网络
与许多细胞网络一样,染色质交互网络[31]具有无标度和模块化拓扑结构,多数节点仅参与一个或两个交互,而一些节点与不成比例的大量节点连接。染色质相互作用网络被组织成“社区”,社区内的基因以协调方式执行相关功能并对外部刺激做出反应,意味着这些社区可能在数百万年进化过程中被塑造。
在未来的研究中,不仅可以将该方法应用于其他特定类型的基因,还可以将相互依赖的网络结合起来,因为细胞活动一起发生并且相互联系。 此外,染色质相互作用网络可能奠定3D或甚至4D基因组波的基础,从静态转变为动态[31]。
3.3 染色质相互作用的功能研究
目前,已有多种方法用于研究Chia-Pet鉴定的染色质相互作用的功能,即:荧光素酶报告基因测定[11]、目的蛋白的表达水平敲定实验[11]、来自转基因实验的增强子测定法鉴定的调控元件[15]、基因组编辑方法(如锌指核酸酶基因组编辑,TALENs和CRISPR / Cas9)干扰染色质相互作用[16]。
3.4 染色质三维结构的重建
染色质的精确三维结构提供了更好的生物学功能景观。到目前为止,远距离相互作用的数据适合于重建三维基因组结构。2个3c衍生物,即hi-c[10]和Chia-Pet[9],实际上反映了整个基因组的结构。Hi-C技术可以捕获所有的交互,但是分辨率很低。Chia-Pet技术大大提高了分辨率,但只能识别已知蛋白质介导的相互作用。因此,Chia-Pet数据可用于进行更为密集的建模。
对染色质的三维结构进行建模主要有2种方法[32]。一种是物理模型,如用于解释实验结果的珠子串模型;另一种是用于重建结构的非线性优化模型。其中,物理模型方法中必须考虑许多物理性质。重建结构的非线性优化模型的第一步是将染色质相互作用频率转换为空间距离,基于此将空间距离转换为三维结构。由于缺乏直接参数来评估在全基因组范围内建立的三维结构,电子显微镜的发展将在促进染色质三维结构的研究中发挥重要作用。染色质相互作用的可视化与功能测定结合是一种重要的方式,可以让人们对基因組结构有更直观的印象,并全面了解基因组的功能。
4 结束语
本文介绍了Chia-Pet的实验方案和数据分析过程,分析了几种常用工具的特点和适用范围,有助于研究中选用合适的方法以获得更可靠的结果。现已成功地应用于转录调控分析的许多研究中,并已鉴定出不同的染色质相互作用模型。尽管如此,在Chia-Pet协议和分析管道方面仍有亟待改进之处,使协议更加简洁和易于执行,数据分析过程更加自动化和可定制。
参考文献
[1] REN B, ROBERT F, WYRICK J J, et al. Genome-wide location and function of DNA binding proteins[J]. Science, 2000, 290(5500): 2306.
[2]WEI C L, WU Q, VEGA V B, et al. A global map of p53 transcription-factor binding sites in the human genome[J]. Cell, 2006, 124(1): 207.
[3]JOHNSON D S, MORTAZAVI A, MYERS R M, et al. Genome-wide mapping of in vivo protein-DNA interactions[J]. Science, 2007, 316(5830): 1497.
[4]DEKKER J, RIPPE K, DEKKER M, et al. Capturing chromosome conformation[J]. science, 2002, 295(5558): 1306.
[5]ZHAO Z, TAVOOSIDANA G, SJLINDER M, et al. Circular chromosome conformation capture (4C) uncovers extensive networks of epigenetically regulated intra-and interchromosomal interactions[J]. Nature genetics, 2006, 38(11): 1341.
[6]SIMONIS M, KLOUS P, SPLINTER E, et al. Nuclear organization of active and inactive chromatin domains uncovered by chromosome conformation capture-on-chip (4C)[J]. Nature genetics, 2006, 38(11): 1348.
[7]DOSTIE J, RICHMOND T A, ARNAOUT R A, et al. Chromosome conformation capture carbon copy (5C): A massively parallel solution for mapping interactions between genomic elements[J]. Genome research, 2006, 16(10): 1299.
[8]de WIT E, De LAAT W. A decade of 3C technologies: Insights into nuclear organization[J]. Genes & development, 2012, 26(1): 11.
[9]LIEBERMAN-AIDEN E, Van BERKUM N L, WILLIAMS L, et al. Comprehensive mapping of long-range interactions reveals folding principles of the human genome[J]. Science, 2009, 326(5950): 289.
[10]LI G, RUAN X, AUERBACH R K, et al. Extensive promoter-centered chromatin interactions provide a topological basis for transcription regulation[J]. Cell, 2012, 148(1-2): 84.
[11]CHEPELEV I, WEI G, WANGSA D, et al. Characterization of genome-wide enhancer-promoter interactions reveals co-expression of interacting genes and modes of higher order chromatin organization[J]. Cell research, 2012, 22(3): 490.
[12]HANDOKO L, XU H, LI G, et al. CTCF-mediated functional chromatin interactome in pluripotent cells[J]. Nature genetics, 2011, 43(7): 630.
[13]DOWEN J M, FAN Z P, HNISZ D, et al. Control of cell identity genes occurs in insulated neighborhoods in mammalian chromosomes[J]. Cell, 2014, 159(2): 374.
[14]KIEFFER-KWON K R, TANG Z, MATHE E, et al. Interactome maps of mouse gene regulatory domains reveal basic principles of transcriptional regulation[J]. Cell, 2013, 155(7): 1507.
[15]PAPANTONIS A, KOHRO T, BABOO S, et al. TNF[WT6BZ]α[WT6BZ]signals through specialized factories where responsive coding and miRNA genes are transcribed[J]. The EMBO Journal, 2012, 31(23): 4404.
[16]DEMARE L E, LENG J, COTNEY J, et al. The genomic landscape of cohesin-associated chromatin interactions[J]. Genome research, 2013, 23(8): 1224.
[17]LI G, FULLWOOD M J, XU H, et al. ChIA-PET tool for comprehensive chromatin interaction analysis with paired-end tag sequencing[J]. Genome biology, 2010, 11(2): R22.
[18]PAULSEN J, RDLAND E A, HOLDEN L, et al. A statistical model of ChIA-PET data for accurate detection of chromatin 3D interactions[J]. Nucleic acids research, 2014, 42(18): e143.
[19]LI H, DURBIN R. Fast and accurate short read alignment with Burrows–Wheeler transform[J]. Bioinformatics, 2009, 25(14): 1754.
[20]LANGMEAD B, TRAPNELL C, POP M, et al. Ultrafast and memory-efficient alignment of short DNA sequences to the human genome[J]. Genome biology, 2009, 10(3): R25.
[21]TENNAKOON C, PURBOJATI R W, SUNG W K. BatMis: A fast algorithm for k-mismatch mapping[J]. Bioinformatics, 2012, 28(16): 2122.
[22]LI H, HANDSAKER B, WYSOKER A, et al. The sequence alignment/map format and SAMtools[J]. Bioinformatics, 2009, 25(16): 2078.
[23]QUINLAN A R, HALL I M. BEDTools: A flexible suite of utilities for comparing genomic features[J]. Bioinformatics, 2010, 26(6): 841.
[24]LANGER-SAFER P R, LEVINE M, WARD D C. Immunological method for mapping genes on Drosophila polytene chromosomes[J]. Proceedings of the National Academy of Sciences of the United States of America , 1982,79:4381.
[25]PHANSTIEL D H, BOLE A P, HEI DARI N, et al. Mango: A bias-correcting Chia-Pet analysis pipeline[J]. Bioinformatics, 2015, 31(19):3092.
[26]HE C, ZHANG M Q, WANG X. MICC: An R package for identifying chromatin interactions from ChIA-PET data[J]. Bioinformatics, 2015, 31(23): 3832.
[27]FULLWOOD M J, LIU M H, PAN Y F, et al. An oestrogen-receptor-α-bound human chromatin interactome[J]. Nature, 2009, 462(7269): 58.
[28]HANDOKO L, XU H, LI G, et al. CTCF-mediated functional chromatin interactome in pluripotent cells[J]. Nature genetics, 2011, 43(7): 630.
[29]CHEPELEV I, WEI G, WANGSA D, et al. Characterization of genome-wide enhancer-promoter interactions reveals co-expression of interacting genes and modes of higher order chromatin organization[J]. Cell research, 2012, 22(3): 490.
[30]HE C, WANG X, ZHANG M Q. Nucleosome eviction and multiple co-factor binding predict estrogen-receptor-alpha-associated long-range interactions[J]. Nucleic acids research, 2014, 42(11): 6935.
[31]SANDHU K S, LI G, POH H M, et al. Large-scale functional organization of long-range chromatin interaction networks[J]. Cell reports, 2012, 2(5): 1207.
[32]PENG C, LI G L, ZHANG H Y, et al. Reconstruction of three-dimensional structures of chromatin and its biological implications[J]. Scientia Sinica Vitae, 2014, 44(8): 794.
