高中化学中的微观思维及培养
2020-07-04田胜勇
田胜勇
摘 要:化学高考越来越注重对学生学科思维的考查,高中化学教师在日常教学中应当顺应这种改变,培养学生用微观思维来理解物质变化,从而实现学生整体、全面的素质提高。
关键词:学科思维;微观思维;守恒思想
学生经常会有这样的疑问:平时课堂上所学的知识,在高考试题中很少涉及,那我们高中的学习是为了什么?高考是学科思维的考查,而学科思维就包括微观思维,既包含物质的溶解、水解、电离等物理变化过程,也包含中和、水解、氧化、还原等化学变化过程。要能准确把握物质变化的本质,就应从微观的角度去理解和把握变化过程。
一、微观思维的考查
1.微观变化过程
微观是相对宏观而言。宏观只能描述现象,微观才能解释本质。用微观思维来理解变化过程,能帮助我们回答物质的变化到底是怎么进行的。这种靠微观思维来理解物质变化的考查,高中考题中无处不在。
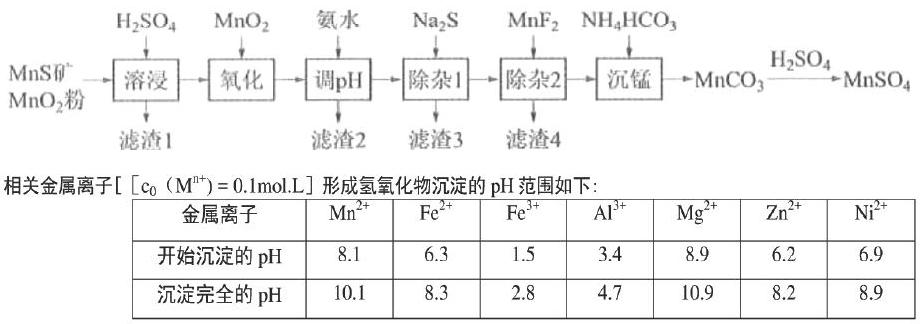
如,【2019全国卷Ⅲ第26题节选】高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备。工艺如下图所示。
(3)“调pH”除铁和铝,溶液的pH范围应调节为 ~6之间。
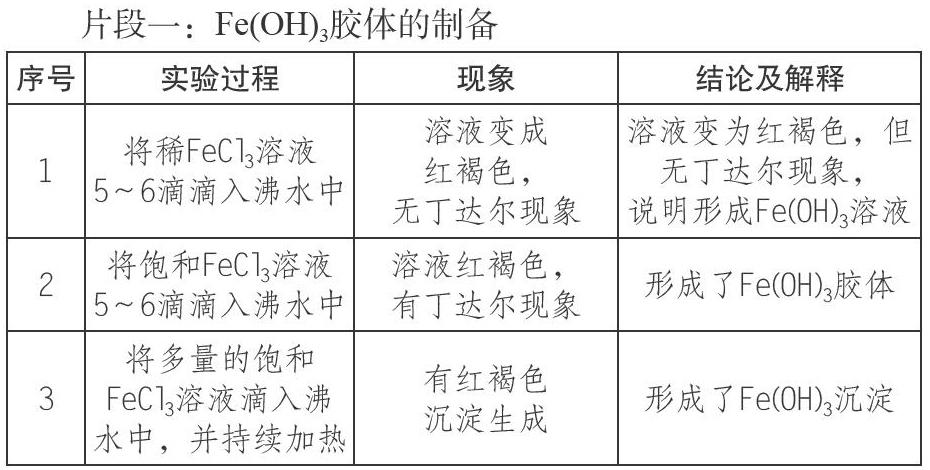
【解析】以Fe(OH)3为例,Fe(OH)3通常以沉淀的形式存在,但如果Fe3+和OH-的浓度很低,比如c(Fe3+)=0.1mol/L,只要pH不高于1.5,即c(OH-)≤10-12.5mol/L,该溶液也只是Fe(OH)3的不饱和或者饱和溶液。如果c(OH-)增大,则变为Fe(OH)3的过饱和溶液,沉淀也开始产生。当pH=2.8时,随着Fe3+不断沉淀,最终c(Fe3+)≤10-5 mol/L,即认为Fe3+沉淀完全。
同理,c(Al3+)=0.1mol/L时,pH=3.4开始形成沉淀,pH=4.7时Al3+沉淀完全。而本题的目的是只沉淀Fe3+和Al3+,所以pH范围应调节为4.7~6之间。
2.守恒思想
守恒思想是人的重要意识体现,其意义在于让学生认识到客体即使外观发生了变化,但其特有的属性不会改变。这就要求能够进入化学反应的微观世界,去理解化学变化中的质量为什么会恒定?氧化还原反应过程中的电子是如何转移?溶液中的阴阳离子的电荷完全中和等,守恒思想是微观思维的重要表现形式。
2.1电荷守恒:溶液中的阳离子所带的正电荷与阴离子所带的负电荷相等,溶液呈电中性。
如【2019全国卷Ⅲ】11.设NA為阿伏伽德罗常数的值。关于常温下pH=2的H3PO4溶液,下列说法正确的是( )
A.每升溶液中的H+数目为0.02NA
B.c(H+)=c(H2PO4-)+2c(HPO42-)+3c(PO43-)+c(OH-)
C.加水稀释使电离度增大,溶液pH减小
D.加入NaH2PO4固体,溶液酸性增强
其中B选项,H3PO4溶液中阳离子只有H+,阴离子有H2PO4-、HPO42-、PO43-、OH-。离子浓度乘以每个离子所带的电荷数是相等的。学生若具备电荷守恒思维,就能快速准确地得出结论。
2.2未知方程式的书写过程对守恒思维的考查:未知方程式的书写严格按照依据题意判断主反应物和主产物→依据电子守恒完成氧化还原反应部分配平→依据电荷守恒完成离子部分配平→依据原子守恒完成整个方程式的配平顺序。
如【2019全国卷Ⅲ第26题节选】
【解析】根据题意可以判断该反应的主反应物和主产物:MnS+MnO2+H2SO4-S+MnSO4,其中MnS中的S体现还原性,MnO2体现氧化性,1 mol 的MnS失2 mol e-,1 mol 的MnO2得2 mol e-,依据电子守恒确定MnS和MnO2系数都为“1”。再根据原子守恒依次配MnSO4、H2SO4的系数“2”,MnS+MnO2+2H2SO4-S+2MnSO4。并最终确定产物有2mol H2O生成,MnS+MnO2+2H2SO4=S+2MnSO4+2mol H2O
二、微观思维的培养
化学学科思维不是一朝一夕培养起来的,这就要求我们教师在日常教学中把握基础教学的每一个机会,不断地指导学生去理解、探索物质变化的微观过程。
1. Na作为金属性很强的金属,在化学反应中都表现为强烈的失去电子的还原性。投入水中,H2O作为弱电解质发生:H2O?H++OH-,H+具有一定氧化性,得到电子转化成H2,溶液剩下Na+和OH-。由于H2~2e-~2H+~2H2O,故Na的系数确定为“2”。
2. 用饱和食盐水来代替H2O进行实验。由于H2O的浓度降低,Na接触H+的机率降低,反应速率减慢。
3. 对于NaCl饱和溶液,即为Na+和Cl-的饱和溶液。在NaOH生成过程中伴随着Na+浓度的增大和溶剂H2O的量的减少,形成NaCl过饱和溶液,从而溶液变浑浊,有部分晶体析出。
教师对化学方程式的解读不应该只停留在肤浅的宏观物质变化上面,而是要带着学生走进化学反应的微观世界,从电子、离子、原子的角度去理解变化过程,寻找化学反应规律。每个方程式都是生动有趣的“活”的个体,都理应成为我们教学中的重要资源。
教育的最终目的是育人,是对人的思维的锻炼和培养的过程。化学课程的本质就是如何利用化学学科资源培养学生的学科思维,从而提升学生的思维品质,由此实现人的进步与提高。
