闭塞节段对慢性颈内动脉闭塞血管再通治疗的影响
2020-07-03祁鹏尹晓亮陆军胡深王俊杰杨希孟陈鲲鹏王海峰王大明
祁鹏 尹晓亮 陆军 胡深 王俊杰 杨希孟 陈鲲鹏 王海峰 王大明
慢性颈内动脉闭塞(CICAO)是缺血性卒中的重要原因,尽管施以积极的药物治疗,脑卒中年复发风险仍达6%~20%[1⁃2],若存在血流动力学障碍则复发风险更高[3]。慢性颈内动脉闭塞患者的累积生存率较低,5 年全因病死率为30%~40%[4]。随着血管再通理念与技术的发展,慢性颈内动脉闭塞的治疗日益受到重视,血管再通治疗为其主要方法。慢性颈内动脉闭塞的闭塞节段通常较长,血管再通技术存在较大挑战;不同闭塞节段对血管再通成功率、再通技术、再通风险及预后的影响尚不明确。北京医院近3 年来采用血管再通技术共治疗39 例慢性颈内动脉闭塞患者,本文拟探讨闭塞节段对血管再通治疗的影响。
对象与方法
一、研究对象
1.纳入标准 (1)均经CTA 或DSA 证实单侧颈内动脉闭塞。(2)发病至血管再通治疗时间>3 周。(3)颈内动脉闭塞导致的相应缺血症状反复发作,并经规范化药物治疗无效。(4)CTP 显示闭塞侧相应区域低灌注。(5)行血管再通治疗。(6)所有患者及其家属对手术方案和风险知情并签署知情同意书。
2.排除标准 (1)非闭塞侧颈内动脉缺血症状,或经规范化药物治疗症状稳定。(2)CTP 显示闭塞侧脑灌注正常。(3)合并重要脏器功能障碍而无法耐受手术或预期寿命<2 年。
3.一般资料 选择2017 年1 月至2020 年1 月在北京医院神经外科行血管再通治疗的慢性颈内动脉闭塞连续病例共39 例,男性35 例,女性4 例;年龄39 ~80 岁,平均(63.52±10.14)岁。既往高血压者29 例(74.36%)、冠心病16 例(41.03%)、糖尿病18 例(46.15%)、高脂血症21 例(53.85%),吸烟18 例(46.15%)。入院时美国国立卫生研究院卒中量表(NIHSS)评分0 ~10 分,中位评分2(1,3)分;改良Rankin 量表(mRS)评分1 ~4 分,中位值1(1,2)分。
二、研究方法
1.血管再通治疗 患者平卧位,于局部或全身麻醉下行脑血管造影和血管再通治疗,全身麻醉仅用于预判闭塞节段较远或配合度较差,影响手术操作的患者。采用改良Seldinger 法经右股动脉穿刺,置入8F 股动脉鞘,全身肝素化,全脑血管造影明确闭塞部位、闭塞节段、闭塞段起始部形态和侧支代偿等:(1)闭塞节段,颈总动脉造影明确闭塞段起点,全脑血管造影并根据向闭塞侧颈内动脉远端代偿(如眼动脉、后交通动脉和前交通动脉)的正向或逆向血流综合判断闭塞段终点。(2)闭塞近端残端形态,分为无残端、圆钝型和尖削型共3 种类型。其中,无残端自颈总动脉向颈外动脉顺滑过度,无颈内动脉残端;圆钝型残端,可见残端,呈光滑圆钝状,无明确起点指示血管再通部位和方向;尖削型残端,可见残端,呈“尖削”状、“火焰”状,提示血管再通治疗起点。闭塞段起点位于颈内动脉起始部的患者,将8F 导引导管送至颈总动脉远端;闭塞段起点位于颈内动脉眼段者,将6F 导引导管送至颈内动脉颈段末端。在路径图引导下,根据闭塞节段、走行、闭塞近端残端形态和远端位置等信息而确定再通治疗方案。经导引导管将Echelon⁃10 微导管(美国EV3 公司)或SL⁃10 微导管(美国Stryker 公司)配合0.014 in Asahi 微导丝(日本Asahi Intecc 公司)或Synchro 微导丝(美国Stryker 公司),尝试通过闭塞段起点进入闭塞段内;若通过颈段残端困难,则经导引导管将4F 或5F 多功能导管(美国Cordis 公司)配合0.035 in 超滑导丝,尝试通过闭塞近端残端起点。突破闭塞近端残端起点并穿过闭塞段时,应轻柔操控导丝,在阻力适中的情况下逐步前行直至闭塞段远端,切忌暴力操控和过度旋转。经同侧眼动脉、后交通动脉代偿血流逆向充盈显示闭塞远端位置的情况下,操控导丝通过闭塞远端,撤除微导丝,经微导管造影确定微导管进入闭塞段真腔后,留置交换导丝、撤回微导管。据闭塞段正常管径选取直径偏小的球囊,常规选择直径1.50 或2.00 mm,长度15、20 或30 mm 的球囊,由远及近全程扩张闭塞段。球囊扩张后根据造影显示的管径、管壁是否光滑、有无废用性萎缩、有无动脉夹层、有无多发附壁血栓等判断是否应用并选取适合的栓子保护装置。再选取与管腔相适应的更大直径球囊进一步扩张闭塞段使狭窄血管更好成形。然后,根据闭塞节段、附壁血栓负荷量、是否存在动脉夹层、残留狭窄程度等,必要时可行支架植入术。术后即刻行DSA,闭塞段管腔内血流充盈、远端血流通畅,即可结束手术。对于病变节段较长,管壁多发不规整、多发动脉夹层、管腔内血栓负荷量较大等情况,在保证血流稳定的前提下,对非原发性动脉粥样硬化性狭窄病变可留待二期处理,术后1 ~2 个月复查造影,残留症状性狭窄的患者再次手术治疗。
2.围手术期处理 术前均常规服用阿司匹林100 mg/d 和氯吡格雷75 mg/d,连续口服5 d,并根据血小板聚集抑制率试验调整用药。术中常规全身肝素化,术后不中和肝素。术后6 h 复查头部CT 以排除颅内出血,继续服用阿司匹林100 mg/d 和氯吡格雷75 mg/d,治疗3 ~6 个月改为阿司匹林100 mg/d长期维持。
3.评价指标 (1)血管再通:闭塞段血管完全开通,术后即刻复查DSA 显示改良脑梗死溶栓血流分级(mTICI)2b ~3 级,至少维持10 min 前向血流,为血管再通治疗成功。(2)围手术期并发症:包括动脉栓塞、颅内出血、导丝穿破血管、血流限制性动脉夹层、视网膜栓塞、颈内动脉海绵窦瘘、腹膜后血肿等。(3)动脉再狭窄:术后3 和6 个月复查CTP、CTA或MRA,术后12 个月复查CTP、CTA 或DSA,观察有无动脉再狭窄或再闭塞,其中,再通血管残留狭窄率≥50%为动脉再狭窄。
结 果
本组39 例患者,左颈内动脉闭塞21 例(53.85%),右颈内动脉闭塞18 例(46.15%);闭塞节段分别为颈内动脉C1 段、C1 ~C2 段或C1 ~C3 段(颅外短节段闭塞)11 例(28.21%),C1 ~C4 段(中节段闭塞)10 例(25.64%),C1 ~C5 段或C1 ~6 段(长节段闭塞)14 例(35.90%),C6 段或C6 ~C7 段(颅内短节段闭塞)4 例(10.26%);闭塞近端残端形态呈尖削型者29 例(74.36%)、圆钝型8 例(20.51%)、无残端2 例(5.13%)。
血管再通治疗时间78 ~300 min,平均(155.13±51.49)min;30 例血管再通成功,血管再通成功率为76.92%;7 例(23.33%)行单纯球囊扩张术、15 例(50%)行单纯支架植入术、8 例(26.67%)行球囊扩张术联合支架植入术,且闭塞节段不同,单纯球囊扩张术比例不同,分别为颅外短节段闭塞0/9、中节段闭塞1/8、长节段闭塞3/9、颅内短节段闭塞3/4,单纯支架植入术比例亦不同,分别为颅外短节段闭塞9/9、中节段闭塞4/8、长节段闭塞1/9、颅内短节段闭塞1/4;术中应用栓子保护装置18 例(60%);共植入支架44 枚,平均每例植入支架1.46 枚。3 例(10%)发生围手术期并发症,其中,术中栓子脱落致远端栓塞1 例,术后对侧肢体肌力轻度下降,至出院时基本自行恢复;术中过度灌注1 例,术后2 h 突发意识丧失,CT 显示再通侧基底节区出血,术后32 d 死亡;术后闭塞侧视力减退、视野缺损1 例,眼底检查显示视网膜中央动脉栓塞,经眼科对症治疗后有所改善。30 例血管再通成功病例中仅1 例(3.33%)因术后过度灌注而诱发基底节区出血,于术后32 d 死亡。本组30 例血管再通成功患者治疗情况参见表1。本组有9 例(23.08%)患者血管再通失败,失败原因分别为:3 例导丝未通过闭塞近端残端;4 例导丝未通过闭塞远端;1 例术中出现颈动脉海绵窦瘘而终止操作;1 例导丝穿过闭塞段全程,小球囊扩张后出现运动性失语、左侧肢体偏瘫,10 min 后自行好转,终止操作。9 例患者均未出现围手术期并发症。
本组有4 例患者因病变节段较长、管腔内血栓负荷量较大等原因,血管再通治疗后对残留狭窄或夹层等病变留待复查再决定是否行二期手术,原始闭塞段位于颈内动脉C1 ~C4 段2 例、C1 ~C5 段1 例和C1 ~C6 段1 例;单纯球囊扩张术2 例,球囊扩张术联合支架植入术2 例。4 例患者均于术后1 ~2 个月行DSA 检查,1 例管腔进一步修复、血流改善,未予进一步处理;3 例管壁修复后残留局限性重度狭窄,进一步行支架植入术,术后恢复良好。
对29 例生存的血管再通成功患者共随访2 ~37 个月,中位时间16(4,27)个月。随访期间新发梗死1 例,术前右颈内动脉C1 ~C4 段闭塞,行单纯支架植入术,血管再通成功,术后6 个月再发左侧肢体无力,MRI 显示左侧额叶新发梗死灶,DSA 显示右颈内动脉破裂孔段重度支架内再狭窄(狭窄率95%),行药物球囊扩张术,术后恢复良好,二次术后7 个月复查CTA 和CTP 均正常;其余28 例患者随访期间病情平稳,无新发脑缺血事件。21 例获得影像学(CTA、MRA 或DSA)随访1 ~24 个月、中位时间5.50(3.50,8.00)个月,动脉再狭窄2 例(9.52%)、动脉再闭塞3 例(14.29%),余16 例(76.19%)病变稳定或好转。2 例动脉再狭窄,1 例为上述随访期间新发梗死患者,1 例闭塞段位于左颈内动脉C1 ~C4 段,均行单纯球囊扩张术,血管再通成功,术后4 个月DSA 显示管腔较前变细,但血流稳定,术后11 个月复查CTA 仍稳定,无临床症状,未进一步处理。3 例动脉再闭塞患者,1 例原始闭塞段位于右颈内动脉C1 ~C4 段,行球囊扩张术联合支架植入术(右颈内动脉起始部植入1 枚支架),血管再通成功,至术后5 个月复查CTA 显示支架内再闭塞,无临床症状,未进一步处理;2 例原始闭塞段位于右颈内动脉C1 ~C5 段,行球囊扩张术联合支架植入术,各植入2 枚(颈总动脉末端至颈内动脉颈段远侧部)和1 枚(颈总动脉末端至颈内动脉起始部)支架,血管再通成功,术后3 天内复查颈动脉超声显示支架内再闭塞,无临床症状,未予进一步处理。

表1 30 例血管再通成功患者的治疗情况Table 1. Details of 30 patients with successful endovascular recanalization
典型病例
患者 男性,74 岁。因右上肢活动不利伴言语不清1 月余,于2017 年10 月6 日入院。患者入院前1 个月出现右上肢肌力减弱伴言语模糊。入院时NIHSS 评分为2 分(右上肢力量评分1 分、言语评分1 分),mRS 评分1 分。头部DWI 显示左侧额叶新发梗死灶(图1),CTP 显示左侧额顶区低灌注(图2),临床诊断为左颈内动脉慢性闭塞,脑梗死,高脂血症;于2017 年10 月11 日行脑血管造影和血管再通治疗。术中可见左颈内动脉自起始部至破裂孔段闭塞,经同侧眼动脉代偿逆向反流至海绵窦段(图3)。经SL⁃10 微导管在Asahi⁃14 微导丝导引下经由闭塞起始部通过闭塞段,以2.50 mm × 30.00 mm Ryujin 球囊由远及近扩张闭塞段,置入Spider 6.0 保护伞,经保护伞导丝以4 mm×30 mm Viatrac 球囊扩张闭塞段,于颈内动脉颈段植入1 枚9 mm×50 mm Wallstent 支架、于颈内动脉起始部或颈总动脉植入1 枚9 mm×40 mm Precise 支架(图4,5)。术后即刻DSA 显示颈段和颅内段显影良好(图6,7),血管再通成功。术后5 天出院,出院后随访至术后2 年,CTP 显示双侧额顶叶灌注正常(图8);颈部CTA 显示再通节段管腔显影良好,无支架内再狭窄(图9)。
讨 论

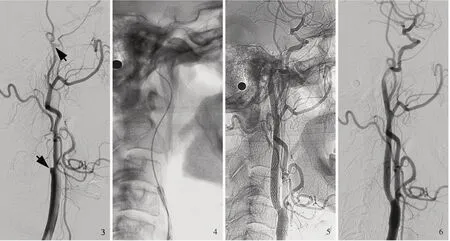
图1 术前横断面DWI 显示,左侧额叶和岛叶新发梗死灶(箭头所示) 图2 术前横断面MTT 图和TTP 图显示,左侧额顶区低灌注(左图为MTT 图,绿色区域所示;右图为TTP 图,红色区域所示) 图3 术前DSA 显示,左颈内动脉自起始部至破裂孔段闭塞(箭头所示),闭塞段远端经同侧眼动脉代偿逆向充盈显影 图4 术中将微导丝通过闭塞段 图5 术中分别于左颈内动脉颈段、左颈内动脉起始部至颈总动脉各植入1 枚支架 图6 术后即刻复查DSA 显示,左颈内动脉颈段显影良好Figure 1 Preoperative axial DWI showed newly developed infarct of left frontal lobe and insular lobe (arrows indicate). Figure 2 Preoperative axial MTT map and TTP map showed decreased cerebral perfusion of left frontal⁃temporal⁃parietal lobe (MTT map is on the left, green areas indicate; TTP map is on the right, red areas indicate).Figure 3 Preoperative left CCA DSA showed occlusion of ICA C1-C3 segment (arrows indicate), with distal artery perfused by collateral flow through ipsilateral ophthalmic artery. Figure 4 Microwire been successfully placed through the whole occluded segment during operation.Figure 5 Telescoped stenting in ICA and distal CCA with successfully recanalized artery during operation. Figure 6 Immediately postoperative DSA showed successfully recanalized cervical flow.
本研究所纳的病例血管再通成功率为76.92%(30/39),不同闭塞节段的血管再通成功率差异较大,颅外短节段闭塞(C1 段、C1 ~C2 段或C1 ~C3 段)和颅内短节段闭塞(C6 段或C6 ~C7 段)由于闭塞节段相对较短,血管再通成功率较高,分别达9/11 和4/4;而长节段闭塞(C1 ~C5 段或C1 ~C6 段)血管再通成功率最低,仅9/14;此外,不同闭塞节段的血管再通治疗方式也显示出明显差异,闭塞节段不同,单纯球囊扩张术比例不同,分别为颅外短节段闭塞0/9、中节段闭塞1/8、长节段闭塞3/9、颅内短节段闭塞3/4,单纯支架植入术比例亦不同,分别为颅外短节段闭塞9/9、中节段闭塞4/8、长节段闭塞1/9、颅内短节段闭塞1/4。围手术期并发症发生率(10%,3/30)和病死率(3.33%,1/30)均较低,中远期预后相对较好,仅1 例(3.33%,1/30)因支架内再狭窄新发梗死,影像学随访5 例发生动脉再狭窄或再闭塞,均为中长节段闭塞再通患者,提示中长节段慢性颈内动脉闭塞患者的血管再通技术仍有待进一步改进,密切的影像学随访有助于提高远期血管再通成功率。
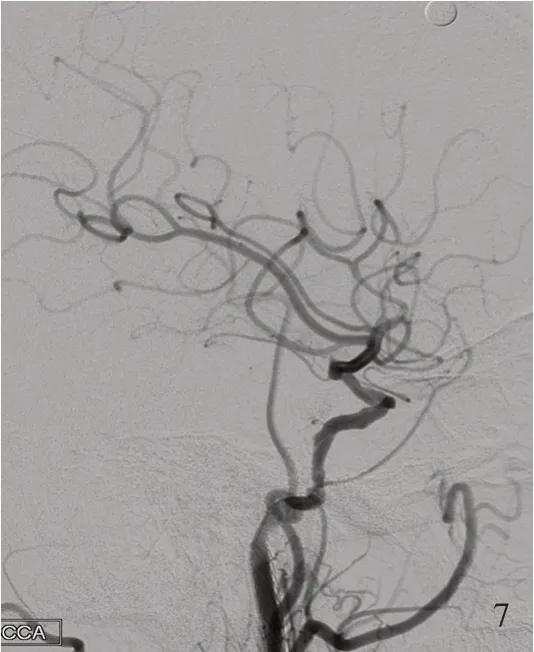
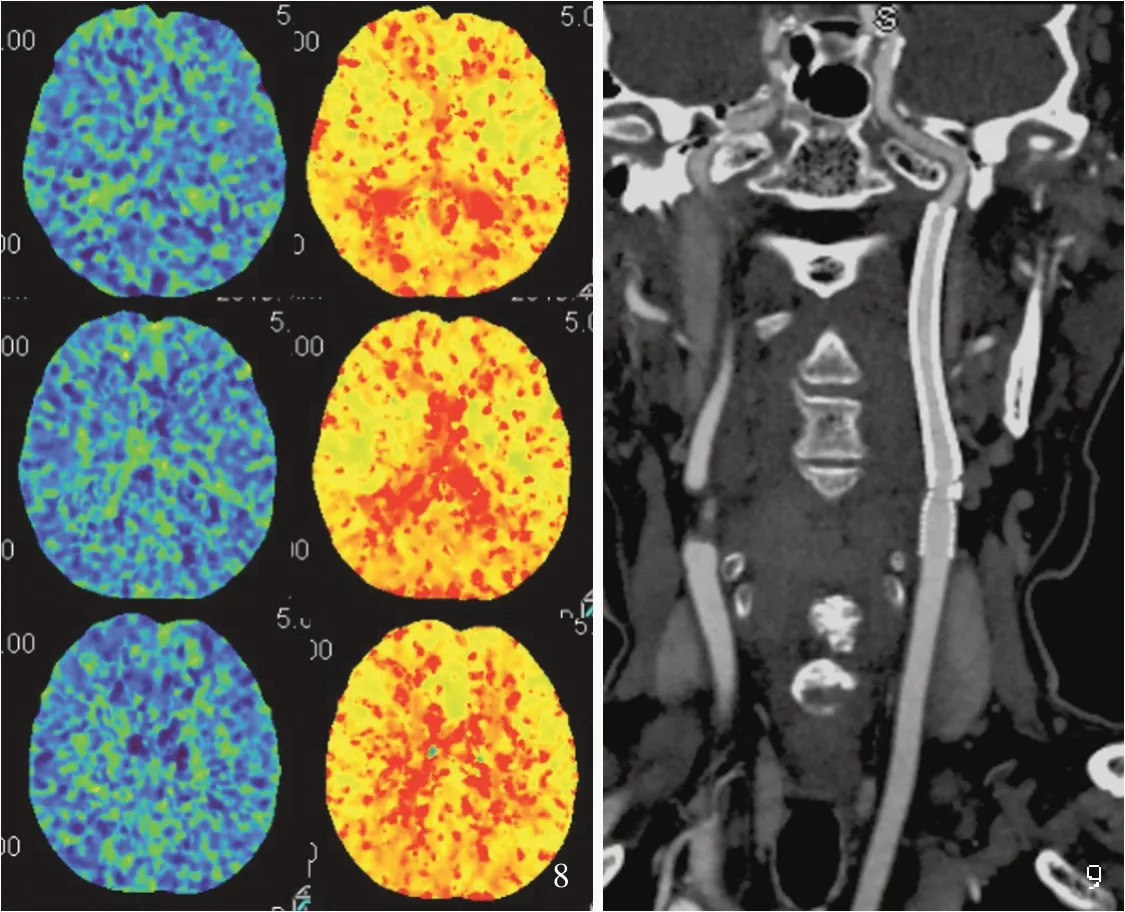
图7 术后即刻复查DSA,左颈内动脉颈段和颅内段均显影良好 图8 术后2 年复查横断面MTT 图 和TTP 图,双侧额顶叶灌注对称(左图为MTT 图,右图为TTP 图) 图9 术后2 年复查颈部CTA,未见支架内再狭窄Figure 7 Immediately postoperative DSA showed favorable development at cerical and intracranial segment of ICA.Figure 8 Axial MTT map and TTP map at 2 years after operation showed normal cerebral perfusion (MTT map is on the left, TTP map is on the right). Figure 9 Cervical CTA at 2 years after operation showed favorable recanalized artery lumen without in⁃stent restenosis.
研究显示,闭塞时间、闭塞节段、闭塞近端残端形态、钙化程度和患者是否存在症状性缺血性卒中症状均 是 血 管 再 通 成功的影响因素[1,5⁃8],其 中 以 闭塞节段是最为重要且直接的影响因素,闭塞节段越长、血管再通成功率越低。Chen 等[8]对138 例慢性颈动脉闭塞患者血管再通治疗经过进行回顾,经统计闭塞远端位于岩骨段及以下、海绵窦段、床突段、眼动脉段、交通段及以上的患者血管再通成功率依次为93%、80%、73%、33%、29%。Lee 等[6]采用血管再通技术共治疗41 例慢性颈动脉闭塞患者,CTA 显示反流至床突段及以上的患者血管再通成功率为52%,反流至床突段以下的患者为89%。本研究闭塞近端位于颈内动脉起始部的患者,其闭塞远端位于破裂孔段及以下(颅外短节段闭塞)、海绵窦段(中节段闭塞)、床突段和眼段(长节段闭塞)的血管再通成功率分别为9/11、8/10、9/14,呈下降趋势;而颅内短节段闭塞(C6 段或C6 ~C7 段)患者由于闭塞节段较短,血管再通成功率为4/4。
血管再通成功首先取决于微导丝顺利通过闭塞段全程,而对其后的血管成形术方式尚无统一意见,对于管腔内可能存在斑块、陈旧性附壁血栓、动脉夹层等严重病变,根据术者经验可采取单纯球囊扩张术、单纯支架植入术或二者联合的方式。本研究血管再通成功的患者中7 例(23.33%)行单纯球囊扩张术、16 例(53.33%)行单纯支架植入术、8 例(26.67%)行球囊扩张术联合支架植入术,其中,颅外短节段闭塞、中节段闭塞、长节段闭塞和颅内短节段闭塞患者单纯球囊扩张术比例分别为0/9、1/8、3/9 和3/4,单纯支架植入术比例分别为9/9、4/8、1/9 和1/4,提示随着闭塞节段的延长,临床更倾向于球囊扩张术。理论上,微导丝通过长节段闭塞时潜在发生动脉夹层、管壁损伤的风险增加[9],血管再通后管腔内可能存在陈旧性血栓、斑块、动脉夹层等复杂成分,此时行血管成形术的目的是稳定血流、降低栓子脱落风险,因此,随着闭塞节段的延长,球囊扩张术可能是较为稳妥的方式。
慢性颈内动脉闭塞血管再通治疗常见的围手术期并发症有远端栓塞、高 灌 注 出 血、低 灌 注 梗 死 等[8,10]。本研究围手术期症状性颅内出血发生率为3.33%(1/30),为致死性基底节区出血。围手术期颅内出血风险主要是由于脑高灌注综合征和导丝刺破血管,其中,脑高灌注综合征的发生机制尚不清楚,可能与颅内动脉血流自动调节(CA)能力受损有关。Chen 等[8]对138 例慢性颈内动脉闭塞患者行血管再通治疗,2 例术后发生迟发性高灌注出血,因此认为,围手术期严格控制血压可以降低高灌注风险。导丝刺破血管则与闭塞节段有关,闭塞节段越长、导丝刺破血管的可能性越大,需术者准确综合判断闭塞病变及术中仔细操控导丝,如术中发生导丝刺破血管,处置不当可导致严重后果。本研究围手术期栓塞事件发生率为6.67%(2/30),1 例为非症状性远端栓塞、1 例为视网膜中央动脉栓塞,经对症治疗后均恢复良好。术中栓子脱落致远端栓塞是慢性颈内动脉闭塞最常见的围手术期并发症,且多为非症状性栓塞[11⁃12],这是由于血管再通后管腔内多为陈旧性血栓,不易发生较大的远端栓塞,因此症状性栓塞的可能性较小。尽管如此,仍应警惕严重栓塞事件的发生,栓子保护装置是减少远端栓塞的有效措施[12],目前常用的远端栓子保护装置适用于颈内动脉颈段短节段闭塞,而对于长节段闭塞则难以发挥全程保护作用,因此,积极探索近端栓子保护装置的应用策略和效果有助于进一步降低栓塞风险。与颅内外血管搭桥术相比,血管再通治疗可最大程度地改善和恢复慢性颈内动脉闭塞患者的脑灌注,且最符合生理需求,从而对中远期缺血性卒中复发有更好的预防作用。小样本病例回顾分析显示,慢性颈内动脉闭塞血管再通治疗后,随访期间极少发生同侧缺血性事件[10,13⁃14]。有 研 究 显 示,血 管 再 通 后 脑 灌 注 改 善 可以 有 效 改 善 认 知 功 能[15⁃18]。在 本 研 究 中,仅1 例 患者(3.33%,1/30)术后5 个月出现同侧缺血性卒中,DSA 提示支架内再狭窄,进一步行球囊扩张术后病情稳定。慢性颈内动脉闭塞开通后中远期血管再通率对维持良好的脑灌注、降低缺血性卒中复发率有重要意义。本组有21 例患者获得CTA 或DSA 随访,16 例病变稳定或好转、2 例动脉再狭窄、3 例动脉再闭塞,这5 例动脉再狭窄或再闭塞患者均为中长节段闭塞再通,2 例再闭塞发生于术后3 天内、1 例再闭塞发生于术后5 个月、2 例再狭窄发生于术后6和11 个月,提示对于此类患者应采取密切的复查策略,有助于及时发现影像学改变并积极处理。
慢性颈内动脉闭塞的血管再通治疗仍在积累经验和不断探索中,治疗经验大多来自单中心研究数据,病例数仍较少,且为回顾性研究。本研究初步显示出不同闭塞节段对血管再通成功率、血管再通方式、围手术期并发症和影像学预后的影响趋势,尚待前瞻性多中心大样本随机对照试验的进一步验证。
利益冲突无