瑞舒伐他汀钙片对映异构体检测方法
2020-06-28徐慧娟张晓燕
徐慧娟,张晓燕,夏 莉,王 菲
(1.瀚晖制药有限公司,浙江 杭州 310020;2.杭州和泽医药科技有限公司,浙江 杭州 318000)
瑞舒伐他汀(rosuvastatin),其化学名为(E)-7-[4-(4-氟基苯基)-6-异丙基-2-[甲基(甲磺酰基)氨基]-嘧啶-5-基](3R,5S)-3,5-二羟基庚-6-烯酸,CAS号:147098-20-2,分子式:C22H28N3O6S[1]。最早由日本盐野义制药公司研发,2003年在美国正式获批上市,以钙盐给药,是一种选择性HMG-CoA还原酶抑制剂,用于治疗高脂血症、高胆固醇血症及动脉硬化症等相关疾病[2]。其结构式中有两个手性碳,贮藏期间可能转变为非对映异构体和对映异构体,瑞舒伐他汀钙片刚被收载到USP41[3]中,该标准仅对非对映异构体进行控制,暂不确定对映异构体是否有相同的临床疗效,因此参考EP9.0[4]瑞舒伐他汀钙原料质量标准[4]建立瑞舒伐他汀钙片对映异构体检测质控方法具有研究意义。
1 实 验
1.1 仪器与试剂
U3000高效液相色谱仪,戴安;MS105DU十万分之一电子天平,ME104E万分之一电子天平,梅特勒-托力多;色谱柱CHIRALCEL OJ-RH(4.6×150mm,5μm),大赛璐;供试品:瑞舒伐他汀钙片(批号:71705141,规格10mg),浙江海正药业股份有限公司;对照品:瑞舒伐他汀钙(批号:2.0),EP;对映异构体(P1101-2),浙江海正药业股份有限公司;非对映异构体(批号:P1401-1),浙江海正药业股份有限公司;氧化杂质(批号:20-DEC-16-03),美国QTY;内酯杂质(批号:140421),加拿大MC;光降解杂质S(批号:15-NOV-16-5),美国QTY;瑞舒伐他汀乙酯(批号:20170529 RE08),深圳博泰尔;乙腈(色谱纯),默克;三氟醋酸(色谱纯),美国天地有限公司;其他试验均为色谱纯。
1.2 实验方法
1.2.1 测定方法
取本品细粉适量(约相当于瑞舒伐他汀25 mg),置25 mL量瓶中,加乙腈-水(25:75)超声使溶解并稀释至刻度,摇匀,滤过,取续滤液作为供试品溶液;另取瑞舒伐他汀钙对照品适量,用乙腈-水(25:75)稀释制成每1 mL约含瑞舒伐他汀2 μg的对照品溶液;另取瑞舒伐他汀钙对照品与对映异构体对照品各适量,加乙腈-水(25:75)溶解并稀释制成每1 mL中约含瑞舒伐他汀1 mg,对映异构体4 μg的混合溶液,作为系统适用性试验溶液。照高效液相色谱法(中国药典 2015年版四部通则0512)试验,用CHIRALCEL OJ-RH纤维素衍生物手性柱(4.6 mm×150 mm,5 μm),以乙腈-0.1%(V/V)三氟醋酸水溶液(25:75)为流动相;流速为每分钟0.5 mL;检测波长为242 nm;柱温35℃。 取系统适用性试验溶液10 μ1,注入液相色谱仪,记录色谱图,出峰顺序依次为对映异构体峰与瑞舒伐他汀峰,瑞舒伐他汀峰与对映异构体峰之间的分离度应不低于1.5,瑞舒伐他汀峰拖尾因子不得过1.8。分别精密量取供试品溶液与对照品溶液各10 μ1,分别注入液相色谱仪,供试品溶液色谱图中如有与对映异构体保留时间一致的色谱峰,按外标法以峰面积计算不得过0.1%。
1.2.2 溶液配制
(1)稀释剂:乙腈-水(25:75)
空白辅料溶液:称取空白辅料(总混)170 mg,置10 ml量瓶中,加稀释剂超声,放冷至室温,用稀释剂稀释至刻度,摇匀,滤过,弃去初滤液,取续滤液即得。
(2)供试品溶液:取本品细粉适量(约相当于瑞舒伐他汀25 mg),置25 ml量瓶中,加稀释剂超声使溶解并稀释至刻度,摇匀,滤过,取续滤液,即得。
(3)对照品溶液:精密量取瑞舒伐他汀钙对照品10 mg,置100 ml量瓶中,用稀释剂超声使溶解并稀释至刻度,摇匀,精密量取1 ml,置50 ml量瓶中,用稀释剂稀释至刻度,摇匀,即得。
(4)系统适用性溶液:称取对映异构体对照品4 mg,置50 ml量瓶中,加稀释剂溶解并稀释至刻度,摇匀,精密量取1 ml,置20 ml量瓶中,称取瑞舒伐他汀钙对照品20 mg,置同一量瓶中,加稀释剂超声使溶解并稀释至刻度,摇匀,即得。
(5)准确度对照品储备液①:精密称取对映异构体对照品10 mg,置100 ml量瓶中,加乙腈适量超声使溶解,放冷至室温,用稀释剂稀释至刻度,摇匀,即得。(0.1 mg/ml)
(6)准确度对照品储备液②:精密量取对照品储备液①5ml,置50 ml量瓶中,用稀释剂稀释至刻度,摇匀,即得。(10 μg/ml)
对映异构体检测限(LOD)储备液:精密量取对映异构体对照品储备液②1 ml,置10 ml量瓶中,用稀释剂稀释至刻度,摇匀,即得。
(7)LOD溶液:精密量取2 ml对映异构体LOD储备液、1.2 ml对照品溶液,置同一50 ml量瓶中,用稀释剂稀释至刻度,摇匀,即得。
(8)定量限(LOQ)溶液:精密量取2 ml对映异构体LOD储备液、1.2 ml对照品溶液,置同一10 ml量瓶中,用稀释剂稀释至刻度,摇匀,即得。
12.4 空白试剂干扰试验
精密量取稀释剂和空白辅料溶液各10 μ1,注入液相色谱仪,记录色谱图。
1.2.4 已知杂质干扰试验
加入有限度浓度的各已知杂质(对映异构体限度0.1%,非对映异构体限度0.2%,氧化杂质限度1.0%,光降解杂质S限度0.2%,瑞舒伐他汀内酯限度1.0%,瑞舒伐他汀乙酯限度0.2%)和瑞舒伐他汀钙,配制成每ml含1 mg瑞舒伐他汀的混合溶液,精密量取10 μ1,注入液相色谱仪,记录色谱图。
1.2.5 系统适用性试验
取对照品溶液10 μ1,注入液相色谱仪,记录色谱图,并连续测定对照品数次,计算峰面积的RSD%。
1.2.6 检测限(LOD)和定量限(LOQ)
分别精密量取LOD和LOQ溶液10 μ1,注入液相色谱仪,记录色谱图。
1.2.7 线性与范围
(1)线性对照品储备液①:取准确度对照品储备液①稀释配制25 ml(0.1 mg/mL)。
(2)线性储备液:精密量取对线性照品储备液①瑞舒伐他汀钙对照品储备液各5 m L,置25 mL量瓶中,用稀释剂稀释至刻度,摇匀,即得。(20 μg/mL)
(3)线性溶液1(定量限):精密量取以上线性储备液适量,用稀释剂制成定量限浓度,即得。
(4)线性溶液2(50%)、3(100%)、4(150%)、5(200%):精密量取线性储备液0.5 mL、1 mL、1.5 mL、2 mL,分别置10 mL量瓶中,用稀释剂稀释至刻度,摇匀,分别制成1 μg/mL、2 μg/mL、3 μg/mL、4 μg/mL。
精密量取上述线性溶液1~6(各1针)10 μl,注入液相色谱仪,记录峰面积,以浓度为横坐标,峰面积为纵坐标,作线性回归方程,并计算对映异构体的校正因子。
1.2.8 准确度试验
(1)定量限浓度溶液:称取空白辅料170 mg(处方量),置10 mL量瓶中,加稀释剂适量,超声使溶解,放冷至室温,精密量取准确度对照品储备液②适量,置同一量瓶中,摇匀,用稀释剂稀释至刻度,摇匀,滤过,弃去初滤液,取续滤液,即得。(平行3份,各进1针)
(2)50%限度溶液、100%限度溶液、150%限度溶液:称取空白辅料170 mg(处方量),置10 mL量瓶中,加稀释剂适量,超声使溶解,放冷至室温,分别精密量取准确度对照品储备液;②1 mL、2 mL、3 mL,置同一量瓶中,摇匀,用稀释剂稀释至刻度,摇匀,滤过,弃去初滤液,取续滤液,即得。(最终浓度分别为1 μg/mL、2 μg/mL、3 μg/mL,每种浓度平行3份,各进1针)
精密量取定量限浓度溶液、150%限度溶液、对照品溶液各10 μl,注入液相色谱仪,记录峰面积,通过理论加入量及实际测得量计算各浓度下的对映异构体的回收率,并计算RSD%,考察方法的准确度。
1.2.9 重复性(加样)试验
加样供试品溶液:称取本品研细粉末适量(约相当于瑞舒伐他汀10 mg),置10 mL量瓶中,加稀释剂适量,超声使溶解,放冷至室温,精密量取准确度对照品储备液;②2 mL,置同一量瓶中,摇匀,用稀释剂稀释至刻度,摇匀,滤过,弃去初滤液,取续滤液,即得。(平行配制6份)
精密量取上述加样供试品溶液(6份,各1针)10 μl注入液相色谱仪,按主成分外标法以峰面积计算对映异构体含量及RSD%。
1.2.10 溶液稳定性试验
将对照品溶液、供试品溶液、加样供试品溶液三者置室温(15℃~25℃)避光放置,约在0、12、24、48、72小时,分别精密量取以上3个溶液10 μl,注入液相色谱仪,依法测定,并计算各时间点与0小时峰面积的比值。
1.2.11 色谱条件耐用性试验
对色谱条件分别做如下变动考察:(1)流动相组成-有机相比例±2%,即(0.1%三氟醋酸水溶液-乙腈(77:23)和(73:27);(2)柱温(35±2℃);(3)流速(0.5±0.1 mL/min);(4)同型号其他色谱柱。
2 结果与讨论
2.1 空白试剂、空白辅料干扰试验
图1显示空白试剂不干扰样品检测,空白辅料出峰时间约为主峰的相对保留时间1.8,对其无干扰,专属性好。
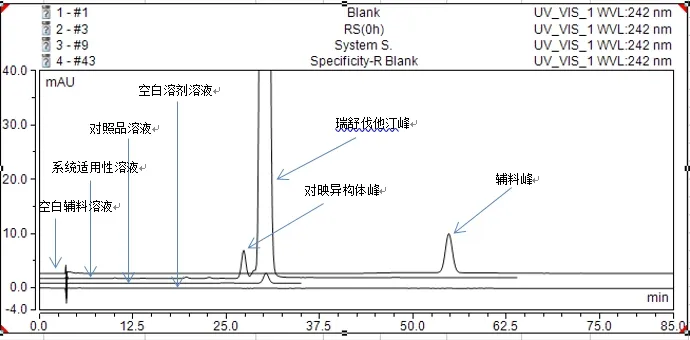
图1 空白辅料、空白溶剂、系统适用性、对照品溶液图谱
2.2 已知杂质干扰试验
图2显示各已知杂质限度浓度下的液相图,各已知杂质出峰在主峰后,对映异构体在主峰前,因此各已知杂质不干扰检测。

图2 各已知杂质定位图
2.3 系统适用性试验
表1表明,瑞舒伐他汀钙对照品5次进样峰面积的RSD%小于1,系统适用性符合要求。

表1 系统适用性试验
2.4 线性和范围
线性和范围结果见表2,相关系数、截距均符合要求,校正因子为1.09;可不予校正。
2.5 检测限与定量限
当对映异构体和瑞舒伐他汀对照品浓度低至0.04 μg/mL(即含量0.004%)时,两物质的吸收峰信噪比均不3.2,大于3,符合检测限要求。
表3表明本品中对映异构体含量低至0.02%时可有效定量,信噪比大于10。
2.6 准确度试验
表4表明,定量限浓度下回收率为91.1%,其他浓度下回收率平均值为93.3%,本方法准确度良好。
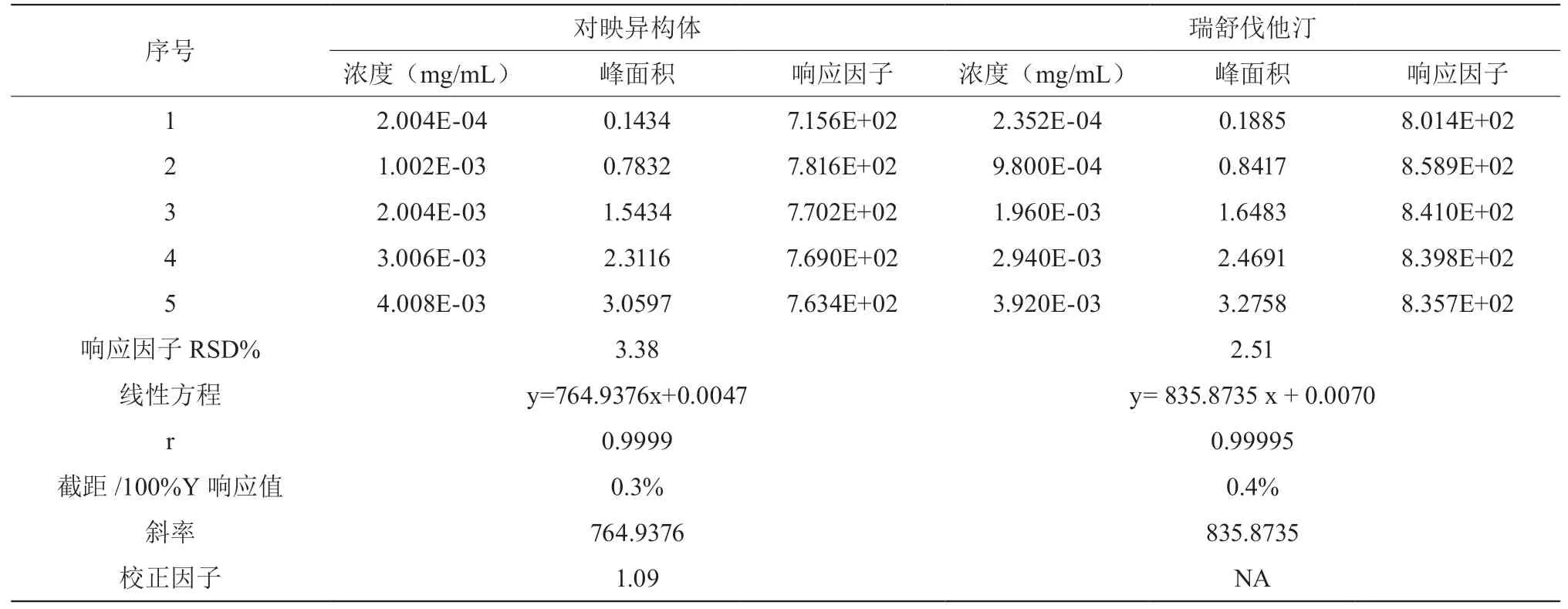
表2 线性与范围实验结果

表3 定量限实验结果
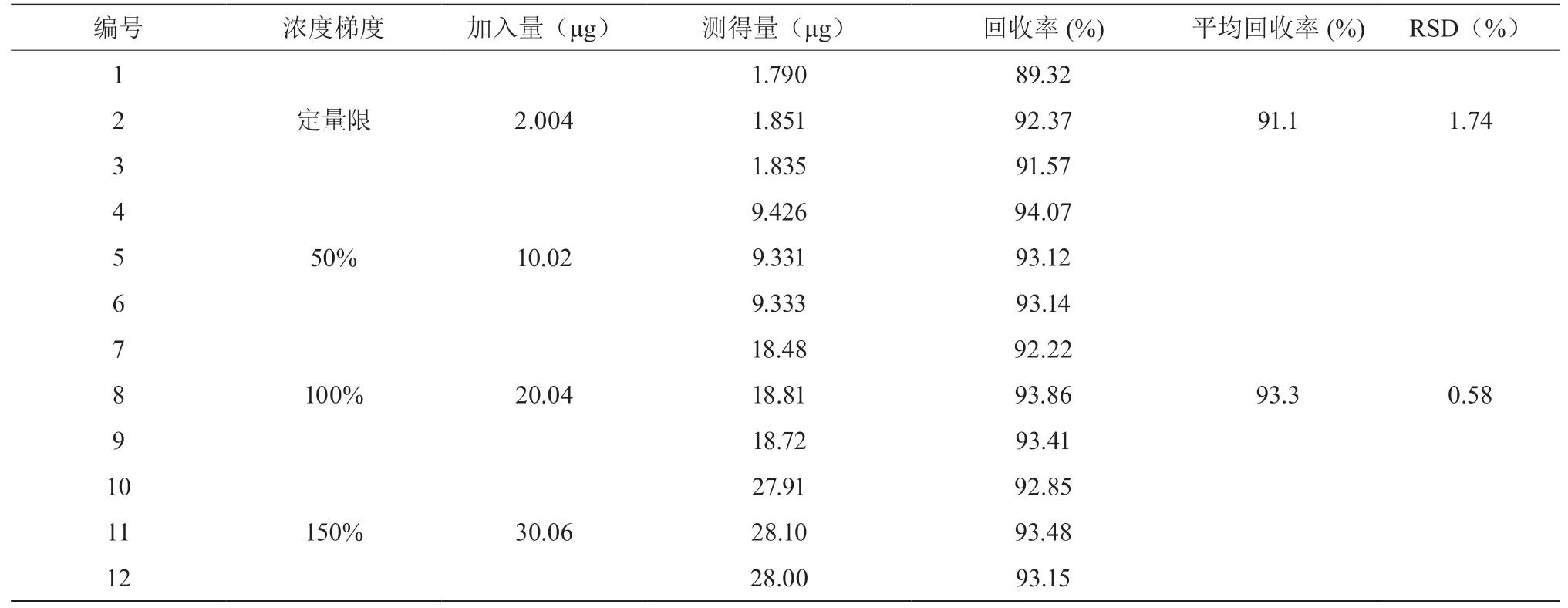
表4 准确度实验结果
2.7 重复性试验
加入量为0.02004mg,实验重复6次,回收率分别是107.7%、108.0%、108.6%、107.6%、108.0%、107.5%,平均回收率为107.9%,RSD%为0.36%,说明本方法重复性良好。
2.8 溶液稳定性
表5表明瑞舒伐他汀钙对照品溶液、供试品(加样)溶液在室温(15-25℃)条件下72小时内稳定。

表5 对照品溶液、供试品(加样)溶液中对映异构体稳定性
2.9 色谱条件耐用性试验
表6表明在各条件下系统适用性结果均符合要求;每个色谱条件下的测定结果与原条件测定结果的绝对差值均不大于0.05%;但需注意的有机相比例变化2%,保留时间的影响很大,需注意控制有机相比例。

表6 色谱条件耐用性对映异构体实验结果
3 结 论
空白试验和空白辅料不干扰样品检测。对照品溶液和供试品溶液在室温条件下72小时内稳定。
耐用性主要考察方法本身对于可变试验因素的抗干扰能力,分别考察柱温37℃和33℃,流速0.6 ml/min和0.4 ml/min,有机相比例23%和27%,测定同一批样品,结果显示有机相比例的轻微改变引起瑞舒伐他汀钙和对映异构体保留时间较大漂移,日常检测时需注意。其他条件的轻微改变对测定结果无显著影响。
本实验通过制备10%、50%、100%、150%浓度的供试品溶液,考察峰面积与溶液中瑞舒伐他汀和对映异构体浓度的线性关系,瑞舒伐他汀在浓度为0.2352 μg/mL-3.920μg/mL的浓度范围内,浓度与峰面积成线性,线性方程为y=835.8735x+0.0070,r为0.99995,响应因子的RSD为2.51%,截距为100%响应值的0.4%。对映异构体在浓度为0.2004~4.008 μg/mL的浓度范围内,浓度与峰面积成线性,线性方程为y=764.9376x+0.0047,r为0.9999,响应因子的RSD为3.38%,截距为100%响应值的0.3%,校正因子为1.09;可不予校正。表明在上述浓度范围内瑞舒伐他汀钙和对映异构体线性关系良好。
本文通过对瑞舒伐他汀对映异构体分析方法的验证,确定了此方法的合理性、有效性,对瑞舒伐他汀钙片的质量监控提供方法。
