铜基石墨烯复合催化剂的合成与表征
2020-06-22王永胜兰小林邱天张新平吴莹莹陈莉徐伟祥郭栋杰段正康
王永胜,兰小林,邱天,张新平,吴莹莹,陈莉,徐伟祥,郭栋杰,段正康
(湘潭大学化工学院,环境友好与资源高效利用化工新技术湖南省协同创新中心,湖南湘潭411105)
引 言
亚氨基二乙酸是农药草甘膦的生产原料,存在多种合成方法,其中二乙醇胺脱氢法是一种经济且环保的工艺方法,此工艺一般采用Cu 基催化剂,其所用的Cu 基催化剂具有高效、廉价等优点[1-3]。Cu基纳米材料导电性好,耐腐蚀、耐压性强且价格低廉,广泛应用于催化有机转化、电催化和光催化[4-7]。尤其在催化脱氢和加氢领域,Cu基催化剂由于其优异的性能得到了广泛的关注[8-9]。但同时存在一些待解决问题,比如在二乙醇胺脱氢中,由于反应过程中会放出大量的热,使得具有催化活性的铜纳米粒子(Cu NPs)在反应时易团聚甚至烧结,导致催化剂失活,因此需引入载体以增强催化剂的稳定性[10-13]。
石墨烯一种单层的sp2 碳晶格,具有比表面积大,本征流动性高,自由电子密度大等优点[14-15],其表面具有大量吸附位点(—OH、—COOH 等),可通过化学相互作用和静电吸引锚定Cu2+[16],使Cu2+均匀分散在石墨烯表面,是一种理想的载体材料[17-20]。多层石墨烯纳米片可以包覆Cu NPs,或将其嵌入氧化石墨烯(GO)片层间,防止Cu NPs 聚集,以提高催化剂的抗氧化性和催化活性[21-23]。同时,片层间的Cu NPs 能防止GO 因π-π 键堆叠和范德华力相互作用而导致石墨烯纳米片层再次堆叠[24]。
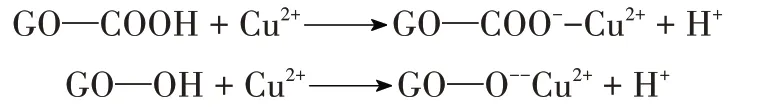
石墨烯负载Cu NPs 及其衍生物的合成可分为原位合成与非原位合成。非原位合成是先将GO 还原得到还原氧化石墨烯(rGO),再将金属Cu NPs沉积在rGO 上,这种方法得到的材料往往存在密度低,Cu NPs 分散不均匀的缺点[25]。原位合成法是通过GO或rGO表面功能化,从而进一步控制其表面成核位点,从而使Cu NPs 分散均匀,但该法尚未得到广泛研究[24]。本课题组在之前的工作中制备出Cu/rGO 催化剂用于二乙醇胺脱氢制备亚氨基二乙酸,虽然亚氨基二乙酸选择性达到80%以上,但是二乙醇胺转化率较低[23]。
因此,本文采用原位合成法制备了Cu/rGO 纳米催化剂并用于二乙醇胺脱氢合成IDA。为了提高二乙醇胺转化率,通过引入有机配体对苯二甲酸(TPA)对GO 表面进行修饰,使其功能化,经水热反应,在GO 片层间及表面形成有机配位键,再通过N2氛围下焙烧去除有机配位键,将Cu物种锚定在rGO 的褶皱层的表面,提高催化剂的抗烧结性能。最后由化学还原得到Cu/rGO 纳米催化剂。采用XRD、FTIR、XPS、SEM 等表征手段对所制备的Cu/rGO 催化剂进行表征,考察了溶剂、水热时间、沉淀pH 以及TPA 的添加对材料微观结构特性及催化性能的影响。
1 实验材料和方法
1.1 材料
石墨粉,青岛金日来石墨有限公司;高锰酸钾、硝酸铜[Cu(NO3)2·3H2O],广东汕头市西陇化工厂;硝酸钠,台山市化工厂有限公司;硫酸[98%(质量)]、盐酸[31%(体积)],衡阳市凯信化工试剂有限公司;双氧水[50%(体积)],西陇科学股份有限公司;氨水[25%(体积)],上海沃凯生物技术有限公司;对苯二甲酸,上海阿拉丁生化科技股份有限公司;硝酸银,天津市光复科技发展有限公司;实验用水为双重去离子水,电阻率达到18 MΩ·cm。
1.2 氧化石墨烯的制备
采用改进Hummers 法制备氧化石墨烯:称取3.0 g 石墨粉,1.5 g NaNO3于三口烧瓶,并将三口烧瓶置于冰水浴中。向三口烧瓶内缓慢加入69 ml 浓硫酸,通过机械搅拌(300 r/min)使其和混合均匀。保持瓶内温度在0~4℃,将9.0 g KMnO4少量多次加入三口烧瓶内,在该温度下,低温反应1 h。将烧瓶内温度升到35℃,中温反应1 h。向三口烧瓶内缓慢加入200 ml 去离子水,并控制温度逐渐升到98℃左右,保持98℃反应1 h 后,结束高温反应。最后加入少量双氧水,溶液变为亮黄色。用10%的盐酸离心过滤至上清液滴加Ba(NO3)2无沉淀产生,再用去离子水清洗至上清液滴加AgNO3溶液无沉淀产生。将离心得到的沉淀物置于50℃烘箱中干燥数日后,再研磨成粉末状,即得氧化石墨烯。
1.3 有机配体修饰的Cu/rGO前体的制备
称取0.3 g 氧化石墨于200 ml 烧杯,加入75 ml H2O,25 ml 乙醇,超声分散2 h,可得氧化石墨烯溶液。称取0.02 mol Cu(NO3)2·3H2O,适量对苯二甲酸于500 ml 烧杯,加入150 ml 乙醇,25 ml H2O,搅拌混合1 h,该过程作用机理如图1。再与GO 分散液混合搅拌1 h 后,逐滴加入1 mol/L NaOH 溶液至一定pH(pH=7.0,12.0,13.0)。再将溶液转入聚四氟乙烯内衬的水热釜,在160℃下反应数小时(2、6、10 h)。待反应液冷却至室温,经水洗、醇洗,滤饼置于50℃烘箱干燥。将沉淀物研磨成粉状后,在N2氛围下,350℃焙烧2 h,得到Cu/rGO前体。
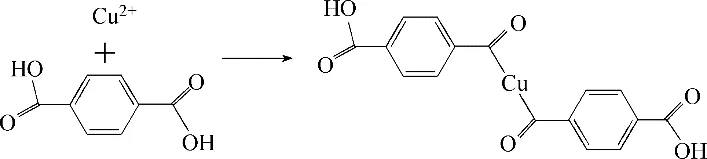
图1 有机配体与Cu2+的相互作用关系图Fig.1 Diagram of interaction between organic ligand and Cu2+
1.4 Cu/rGO催化剂的制备
将催化剂前体分散于300 ml H2O 中,室温下搅拌30 min。称取0.01 mol CuCl 于30 ml H2O 中,在机械搅拌下,逐滴加入到前体溶液中。称取0.02 mol NaBH4溶于30 ml H2O,再缓慢滴加入到上述混合溶液中,继续反应1 h。反应完成后,用水和乙醇清洗数次,将滤饼置于40℃真空干燥箱干燥,得到Cu/rGO催化剂。图2为催化剂制备流程图。
1.5 催化剂的评价及产物分析
将10 g 二乙醇胺、2 g 催化剂、8.5 g 氢氧化钠(溶于80 ml去离子水)加入至高压反应釜中。检查反应釜气密性,通入N2排空5~6 次后加压至1 MPa,4℃/min 的升温速率下,升温至160℃, 在转速为400 r/min 进行搅拌,用转子流量计计量排出的气体体积。当气压升高至1.5 MPa 后打开排气阀,降压至1 MPa后关闭排气阀,并记录每次排气的体积和排气温度。反应过程中反应釜内压力在20 min 内无变化即视为反应结束。采用液相色谱进行定量分析,用强阴离子交换色谱柱(Hypersil SEX, 5 μm, 4.6 mm×250 mm),固定流动相为0.030 mol/L 的磷酸二氢钾-磷酸溶液,流速为1 ml/min,柱温25℃,采用紫外检测器,检测波长为200 nm。
2 实验结果与讨论
2.1 Cu/rGO催化剂的表征
2.1.1 Cu/rGO 催化剂的XRD 表征分析 图3(a)为水热2、6、10 h后,水热产物的XRD 谱图,由图可知,经160℃水 热 反 应2 h,样 品 在2θ=32.4°、35.5°、38.6°、48.8°、53.4°、58.2°、61.5°、66.2°、67.9°、72.4°、74.9°处出现CuO 特征衍射峰(PDF#48—1548)。随着水热时间增加,水热6 h的样品在2θ=36.3°、42.3°、73.4°处出现Cu2O 特征衍射峰(PDF#05—0667)。继续增加水热时间,在2θ=32.4°处有微弱的出峰,为Cu2O 特征衍射峰(PDF#05—0667)。综上所述可知,水热时间会对Cu物种的形成产生影响,增加水热时间,会提高Cu2O 的含量,说明随着水热时间延长,催化剂中部分Cu2+能够经水热反应还原为Cu+。图3(b)为水热10 h 后,催化剂前体及还原后的催化剂XRD 衍射图。经过N2氛围下焙烧,NaHB4还原后,催化剂中CuO 的衍射峰消失,保留了2θ=36.3°、61.4°处Cu2O 的特征衍射峰,在2θ=42.3°、50.3°、74.1°处出现Cu0的特征衍射峰(PDF#04—0836),表明NaHB4作为还原剂,通过化学还原可以将铜的氧化物还原成Cu0。
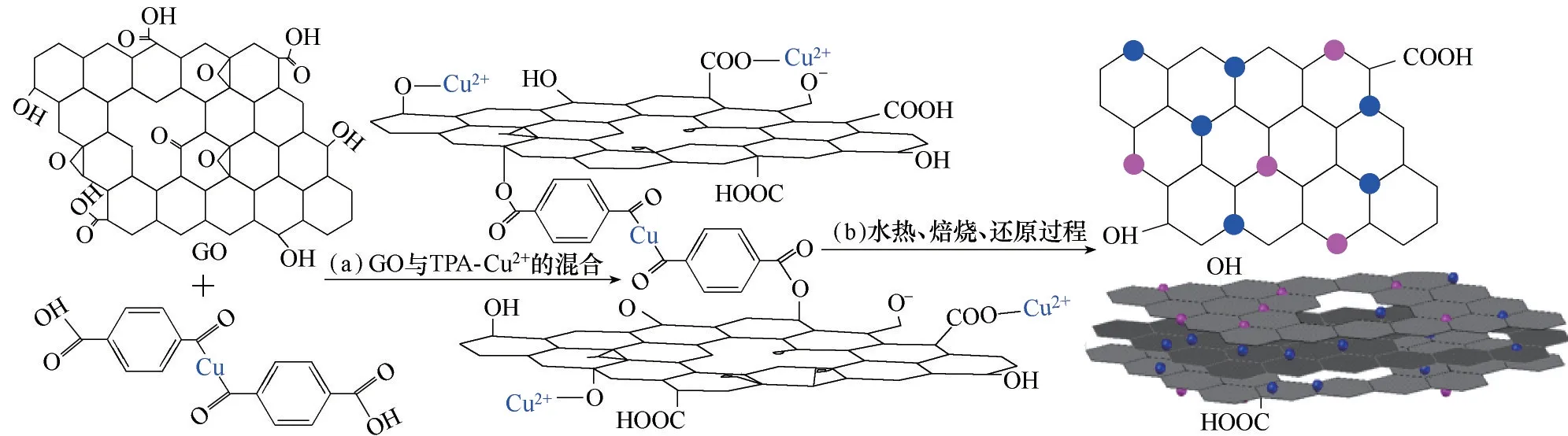
图2 Cu/rGO催化剂制备流程图,其中红色小球为Cu0,蓝色小球为Cu2OFig.2 Preparation flow chart of Cu/rGO catalyst,wherein red pellet is Cu0 and blue pellet is Cu2O
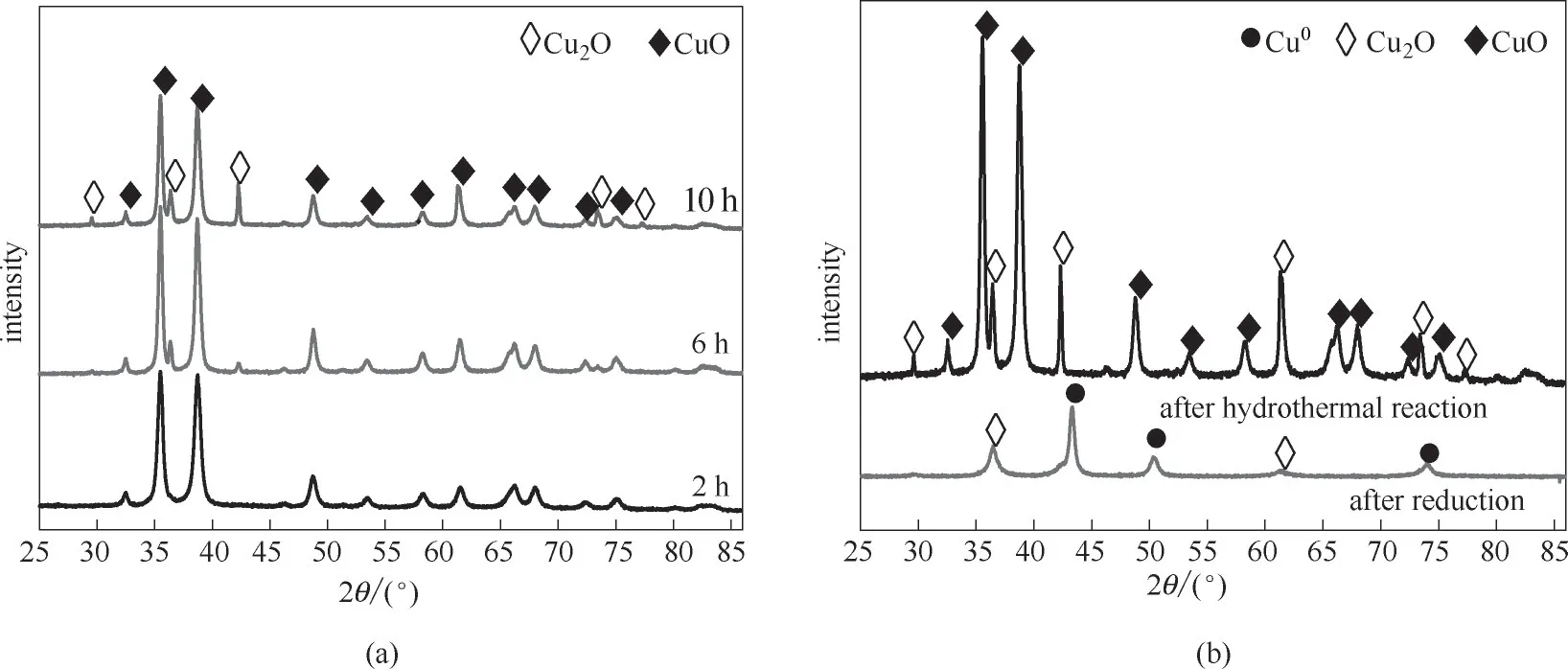
图3 不同水热时间后水热产物(a)与水热后催化剂前体及还原后Cu/rGO催化剂(b)XRD谱图Fig.3 XRD patterns of hydrothermal products after different hydrothermal times(a),precursor of hydrothermal catalyst and reduced Cu/rGO catalyst(b)
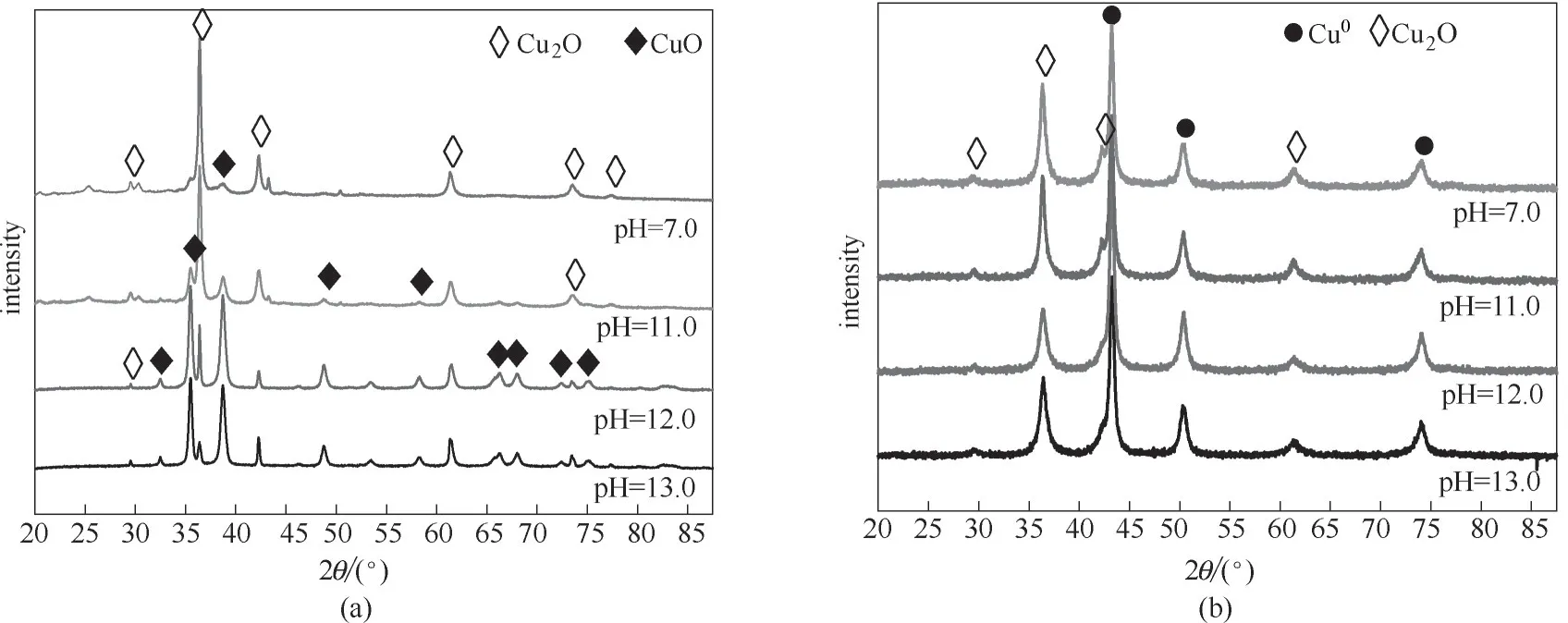
图4 不同pH下水热产物(a)及其还原产物(b)的XRD谱图Fig.4 XRD patterns of hydrothermal products(a)and their reduction products(b)at different pH
图4(a)为不同pH 沉淀后,经10 h 水热反应的水热产物的XRD 谱图。当沉淀pH 为7.0 时,在2θ=29.4°、36.3°、42.3°、61.3°、73.6°、77.3°出现Cu2O 特征衍射峰(PDF#05—0667),仅在2θ=38.7°处出现了CuO 衍 射 峰(PDF#48—1548)。当pH 为11.0 时,在2θ=35.5°,48.7°,58.2°处新出现了CuO 衍射峰(PDF#48—1548)。当 沉 淀pH 为12.0 时,在2θ=66.2°、67.9°、72.4°、74.9°处出现了CuO 衍射峰(PDF#48—1548)。随着pH 继续升高,样品中CuO 含量增加,Cu2O 含量降低。而TPA 在常温下不溶于水和乙醇,但溶于强碱性溶液,结合实验过程观察,发现pH 为7.0时,还能观察到TPA颗粒,且溶液颜色为蓝灰色,当pH 为12.0 时,TPA 完全溶于溶剂中,且溶液颜色变棕黑色,所以pH增加,TPA溶解度增强,水热反应时含氧官能团增加,对铜物种的还原性降低。图4(b)为还原后催化剂的XRD 谱图,从图中可以看出,当pH 为7.0 时,在2θ=29.5°、36.3°、42.2°、61.4°处出现Cu2O 特征衍射峰(PDF#05—0667),在2θ=42.3°、50.3°、74.1°出现Cu0特征衍射峰(PDF#04—0836)。当pH 为12.0 时,2θ=42.2°处的Cu2O 特征衍射峰消失。随着沉淀pH 增加,催化剂中Cu2O 含量降低,Cu0含量增加。对比还原前,随着沉淀pH 增加,前体中Cu2O 含量降低,CuO 含量增加,因此,Cu0的增加来自NaHB4的作用,CuO 和Cu+被还原为Cu0,催化剂中Cu2O 能够稳定存在而不被还原。这是由于在石墨烯表面形成金属有机配位键经碳化后,将Cu2O 包裹在石墨烯片层间,有利于Cu2O 的稳定存在。
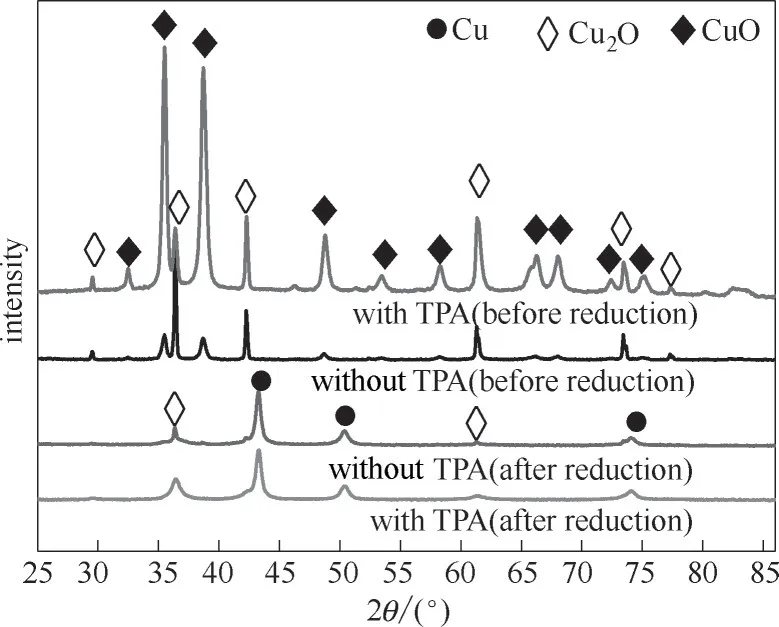
图5 有无添加TPA的两种催化剂在还原前、后的XRD谱图Fig.5 XRD patterns of the two catalysts with or without addition of TPA before and after reduction
图5 对比了有无添加TPA 的两种催化剂,水热反应后,未添加TPA 的样品在2θ=29.5°、36.3°、42.2°、61.2°、73.4°、77.3°处出现Cu2O 特征衍射峰(PDF#05—0667),在2θ=35.5°、38.6°、48.6°处出现CuO 特征衍射峰(PDF#48—1548),与添加TPA 的样品相比,未添加TPA 的样品中CuO 相对含量明显较少。这是因为TPA 加入后,催化剂中含氧官能团增加,对铜物种的还原程度降低。在还原后,于未添加TPA 的催化剂相比,添加TPA 的催化剂中Cu2O衍射峰的面积较大,说明结晶度较好,且半峰宽较宽可以说明其粒径较小,说明TPA 的加入、金属有机配位键的形成、碳化等过程会影响Cu2O结晶度。
2.1.2 Cu/rGO 催化剂的FT-IR 表征 图6为有无添加TPA 对催化剂性质的影响。在FT-IR 谱图中,3420~3600 cm-1吸收峰为GO 片层间吸附的水分子中O—H 以及GO 自身携带O—H 的伸缩振动[26]。1384、1087 cm-1附近的吸收峰分别来自C—OH 的弯曲振动和伸缩振动,1268 cm-1附近的吸收峰来自于GO 表面C—O—C 碳骨架振动[27]。1400 cm-1左右属于C—OH 的伸缩振动,1140 cm-1左右属于C—O 的伸缩振动,在2929 cm-1附近吸收峰来自于烷基链的C—H 拉伸振动[28]。1534 cm-1来自于rGO 中石墨的片层结构[29]。1724、1620、1400 和1024 cm-1处的吸收峰分别来自的伸缩振动、H—O—H 的弯曲振动振动和C—O 的伸缩振动[26]。1224 cm-1处 为C—OH,1056 cm-1处 为C—O[24]。1633 cm-1、1730 cm-1处分别代表GO 中类苯环结构上的的伸缩振动峰和伸缩振动特征峰[27]。
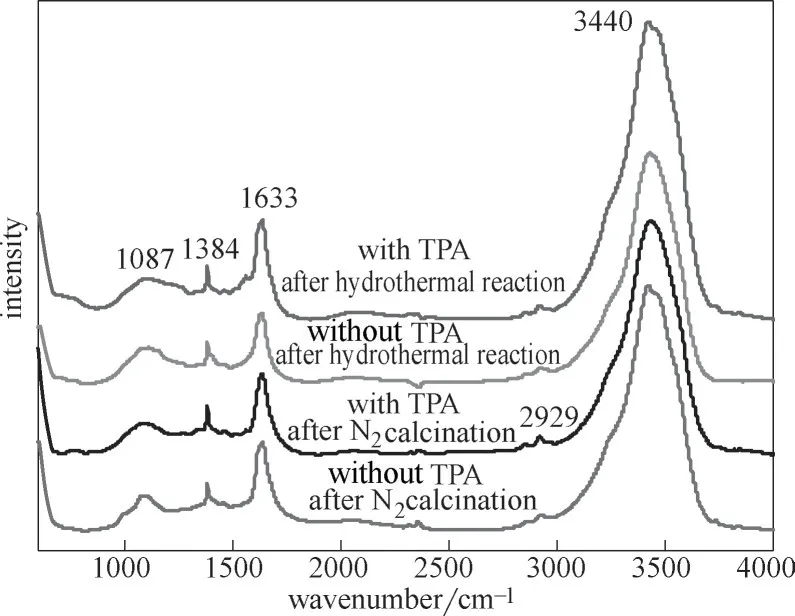
图6 有无添加TPA的两种催化剂在水热后与N2焙烧后的FT-IR谱图Fig.6 FT-IR spectra of two catalysts with and without TPA after hydrothermal and N2 calcination
由于GO 片层间含有大量含氧官能团,能够与溶剂中的水分子形成氢键,使其具有较好的亲水性。在添加TPA 的样品中,水热反应后的曲线在3440 cm-1处吸收峰相对增强,来自于TPA 与氧化石墨烯片层间的含氧官能团相互作用,使其层间距增加,对水分子的亲和力也相对增加;同时也说明有机配体TPA 在GO 材料中成功配位。而在N2氛围焙烧后,添加TPA 样品中3440 cm-1附近的吸收峰减弱,与无TPA 样品的出峰情况一致,这是由于N2焙烧后,去除掉了石墨烯片层间的部分含氧官能团。说明TPA 的加入,增加了石墨烯片层间的有机官能团,在水热过后,形成了金属有机配位键,而N2焙烧能够有效除去金属有机配位键。
图7 为在不同溶剂下,经水热反应与N2氛围焙烧所得样品的FT-IR 谱图。当溶剂为H2O 时,在3440 cm-1附近的吸收峰减弱,即是O—H 的振动减弱,而以V(乙二醇)∶V(水)=1∶1,或者V(乙醇)∶V(水)=1∶1 作为溶剂时,在3440 cm-1附近的吸收峰强度增加且一致。说明以水作溶剂时,样品中O—H 减少,还原程度较高,但相反,有机配位键与rGO 的相互作用减弱,形成金属有机配位键的可能性降低。1087 cm-1附近有较宽的出峰带,属于C—O、C—OH 及C—O—C 的振动。1630 cm-1,1730 cm-1处分别代表rGO 中类苯环结构上的的伸缩振动峰和C O 伸缩振动特征峰[23]。在谱图中,以V(乙醇)∶V(水)=1∶1为溶剂时,水热后和N2焙烧后的样品均在1630 cm-1处出峰,即rGO 中类苯环结构上的的伸缩振动峰最强且稳定,说明在高温焙烧下,石墨烯的结构没有破坏。1400 cm-1左右属于C—OH 的伸缩振动,以V(乙醇)∶V(水)=1∶1 为溶剂时,N2焙烧后,在1453 cm-1处出现新的特征峰,同时3440 cm-1处O—H 振动减弱,这是由于高温焙烧后,水分子的脱除使得水中O—H 减少,而rGO 上C—OH 的增加。综合rGO 的稳定性和还原性,因此选择V(乙醇)∶V(水)=1∶1为溶剂。
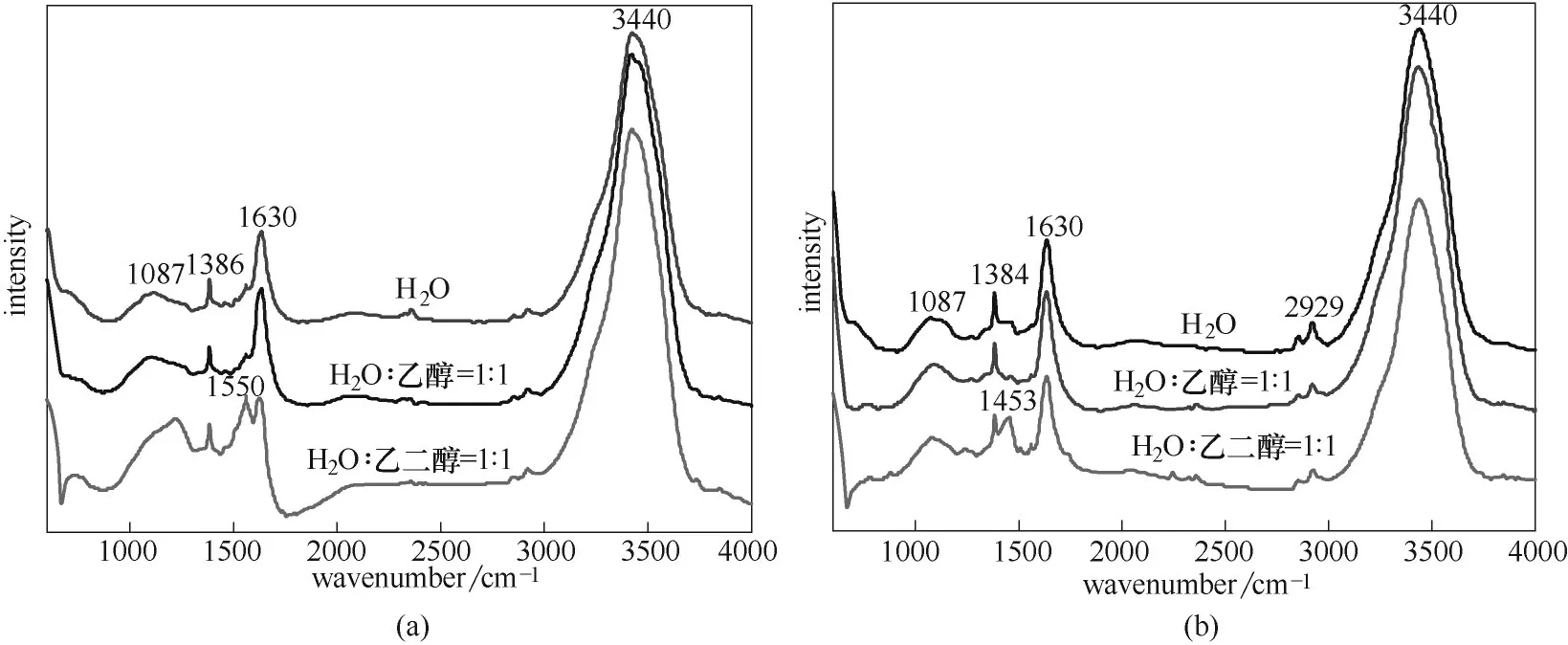
图7 不同溶剂条件下催化剂在水热后(a)与N2焙烧后(b)的FT-IR谱图Fig.7 FT-IR spectra of the catalysts after hydrothermal(a)and N2 calcined(b)under different solvent conditions
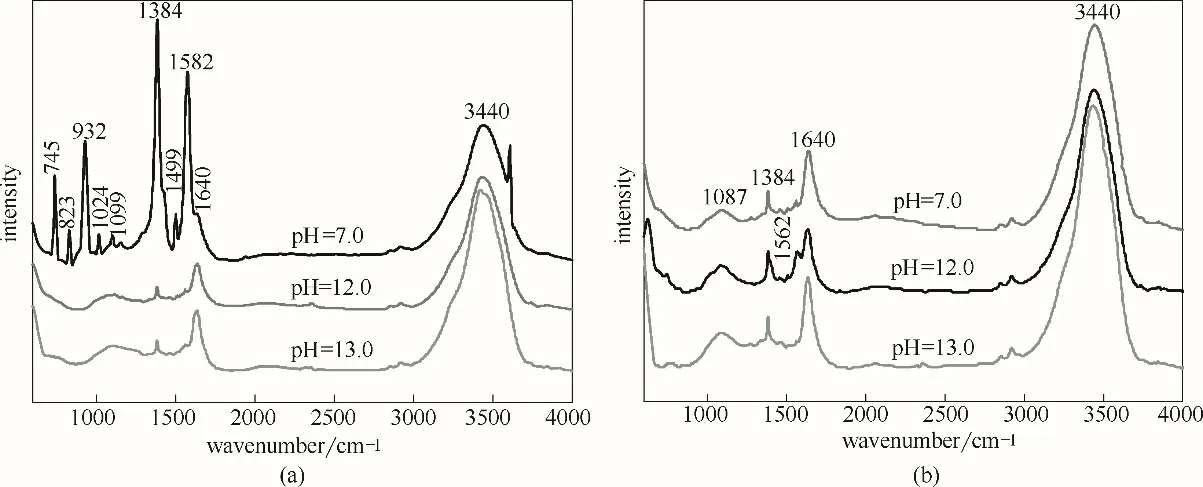
图8 不同沉淀pH条件下催化剂在水热后(a)与N2焙烧后(b)的FT-IR谱图Fig.8 FT-IR spectra of the catalysts after hydrothermal(a)and N2 calcined(b)with different precipitation pH
图8为在不同沉淀pH 条件下,经过水热反应和N2氛围焙烧所得样品的FT-IR 谱图。在800~1800 cm-1之间的出峰带为含氧官能团,如羟基、环氧基、醚键[30],当pH 为7.0时,水热反应后的红外谱图在上述区间出峰较多,表示该条件下,GO 上的含氧官能团未能有效去除,还原程度较低。当pH=13.0 时,3440 cm-1、1440 cm-1处出峰强度增加,说明此时金属有机配位键形成较好,且经过N2焙烧后,能有效去除,与图6 结论一致,所以选择在强碱性条件下沉淀。
图9 为在不同水热时间条件下,经水热反应和N2氛围焙烧所得样品的FT-IR谱图。从图中可以看出,随着水热时间的增加,在3440 cm-1、1640 cm-1处特征衍射峰强度增加,分别归因于O—H振动、C C振动强度增加[27]。由此表明,水热时间的延长有利于氧化石墨烯的还原及有机配体与氧化石墨烯之间的相互作用。
2.1.3 Cu/rGO催化剂的形貌分析 图10(a)为GO的SEM 图和XRD 谱图。将5 mg 氧化石墨溶于5 ml 乙醇中,超声分散1 h,使其剥落成片后,取其上清液滴在硅片上进行SEM 分析。从图中可以看到GO 呈褶皱状的片层结构。通过XRD 可知,GO 的衍射出峰位置在10.8°,表明GO 层与层之间距离约为0.82 nm[31]。图10(b)、(c)分别为水热和还原后Cu/rGO 的SEM 图,图中可以看到堆叠或弯曲成块状,这可能是由于水热过程中,GO 片层间含氧官能团减少,因π-π 键堆叠和范德华力相互作用而导致石墨烯纳米片层再次堆叠[21];在rGO 片层间或者其表面,有铜物种存在。为了更清晰的观察Cu NPs 的形貌,对催化剂进行TEM 表征,图10(d)为催化剂Cu/rGO 的TEM 图,可以看到粒径约为10 nm 左右的Cu NPs 分布在褶皱层状的rGO表面。
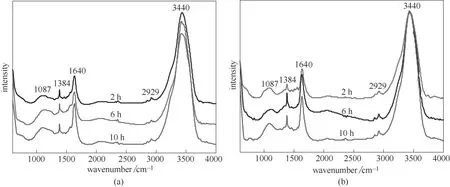
图9 不同水热时间条件下催化剂经水热(a)与N2焙烧(b)的FT-IR谱图Fig.9 FT-IR spectra of catalysts hydrothermal(a)and N2 calcined(b)under different hydrothermal conditions

图10 GO(插图为GO的XRD图)(a)、水热后CuO/rGO(b)和还原后的Cu/rGO的SEM图(c);Cu/rGO的TEM图(d)Fig.10 SEM images of GO(inset:XRD pattern of GO)(a),hydrothermal products CuO/rGO(b)and Cu/rGO after reduction(c);TEM image of Cu/rGO(d)
2.1.4 Cu/rGO 催化剂的XPS表征 图11(a)、(b)为催化剂还原前后Cu 2p 的XPS 谱图,其中图11(a)为未还原的催化剂前体的XPS 谱图,通过软件拟合,将933 eV 附 近 的Cu 2p3/2处 的 主 峰,分 为 在932.5 和934.0 eV 处出峰,分别对应Cu0/Cu+和Cu2+。在953.4 eV 处的Cu 2p1/2的主峰以及940~945 eV 的卫星峰,都对应Cu2+[32-35]。经过还原,Cu0/Cu+(932.5 eV、952.3 eV)峰强增加,Cu2+(934.7 eV、940~945 eV、953.9 eV)峰强减弱,说明经过化学还原,Cu2+还原成了Cu0/Cu+。
图11(c)为未还原的催化剂前体的Cu Auger 谱图,从图中可以看到主峰在动能为917.4 eV处,对应Cu2+,在动能为915.5 eV 处有较弱的副峰,对应Cu+,而在动能为918.0 eV(Cu0)处,尚未有拟合峰出现,与XRD 和Cu 2p分析一致,催化剂前体在还原之前,铜主要以Cu2+形式存在,只有少量Cu+,没有Cu0。在还原后的Cu Auger 谱图中,通过软件拟合分峰,在动能为916.5、917.2、918.7 eV 处的峰分别对应Cu+、Cu2+、Cu0,且主要以Cu0为主[29]。
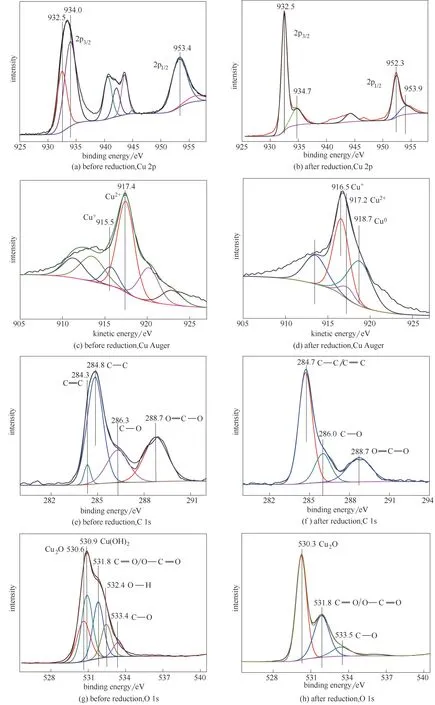
图11 样品的XPS谱图Fig.11 XPS spectra of samples
图11(e)、(f)为催化剂的C 1s 谱图,催化剂在还原之前,在结合能为284.3、284.8、286.3、288.7 eV 处分别对应、C—C、C—O、—O,经过NaBH4还原,催化剂中的C—O 和—O 减少,表明NaBH4能够除去石墨烯上的含氧官能团,起到还原GO作用。
图11(g)、(h)为催化剂的O 1s 谱图,催化剂在还原之前,在结合能较低的位置(小于531 eV),即530.6、530.9 eV处分别对应Cu2O、Cu(OH)2;在结合能较高的位置(大于531 eV),即531.8、532.4、533.4 eV处分别对应/O—、O—H、C—O。同时,催化剂前体中Cu2+所占比例明显较大,含氧官能团多。而催化剂还原后,Cu2+消失,含氧官能团减少。
2.2 催化剂性能测试
采用单因素实验,改变溶剂、沉淀pH 以及水热反应时间,将得到的催化剂用于二乙醇胺脱氢反应,测定催化剂的催化性能,结果如表1 所示。1 条件为:水与乙醇体积比为1∶1 为溶剂,pH 为13.0,在160℃下水热10 h。2~4 条件为:n(Cu)∶n(TPA)=1∶2,pH 为13.0,在160℃下水热10 h。5~7 条件为:以V(乙醇)∶V(水)=1∶1 为溶剂,n(Cu)∶n(TPA)= 1∶2,在160℃下水热10 h。8~9 条件为:以V(乙醇)∶V(水)=1∶1 为溶剂,n(Cu)∶n(TPA)=1∶2,pH为13.0。
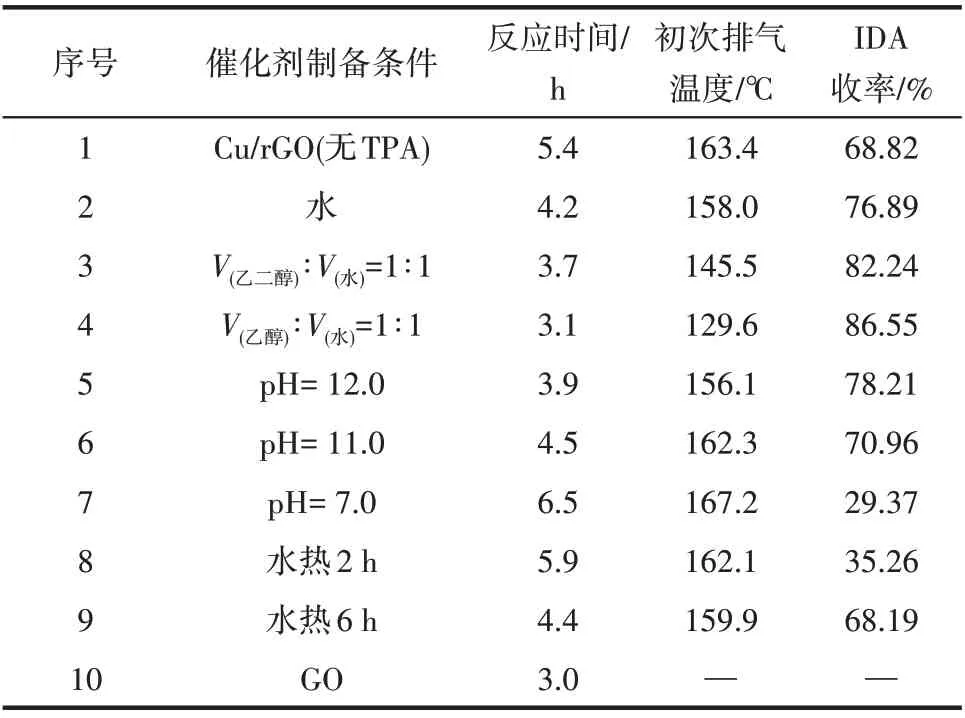
表1 催化剂用于催化二乙醇胺脱氢制亚氨基二乙酸的性能测试结果Table 1 Catalytic performance of samples in dehydrogenation of diethanolamine
由表1 可知,通过TPA 修饰后,Cu/rGO 在二乙醇胺脱氢反应中的催化活性显著提高。以V(乙醇)∶V(水)=1∶1 作为溶剂时,初次排气温度最低,反应时间最短,IDA 收率最高,证明该方法制备的Cu/rGO 在二乙醇胺脱氢反应中具有较好的催化效果。改变催化剂制备条件,当pH 为7.0 以及水热2 h 时,催化效果最差,一方面由于GO 还原不够充分,另一方面,TPA、Cu2+与GO 的相互作用不强,降低了催化剂的催化活性。与前文表征分析一致,V(乙醇)∶V(水)=1∶1作为溶剂、pH 为13.0、水热时间10 h 时,GO 还原效果最好且TPA、Cu2+与GO 的相互作用越强,催化活性越高。
3 结 论
本文通过Hummers 法制备了氧化石墨,经超声剥离得到单片的GO 分散液,再与TPA-Cu2+充分混合后,经水热、N2氛围焙烧、NaHB4还原得到Cu/rGO纳米催化剂。与未经TPA 修饰的催化剂相比,经TPA 修饰后制得的Cu/rGO 催化剂用于二乙醇胺脱氢时,IDA 收率由68.82%提升至86.55%,反应时间明显缩短。结合表征分析及性能测试,确定在V(乙醇)∶V(水)=1∶1 作为溶剂、pH 为13.0、水热10 h 条件下,制得催化剂催化性能较好。一方面TPA 的加入,增强了GO 片层间的相互作用,增加了GO 片层间的有机官能团,并且经过N2氛围焙烧后,能够有效除去有机配位键;另一方面,TPA 的加入能够稳定Cu2O,使其结晶度较好,增加了催化剂活性位点,提高反应速率。通过改变溶剂、沉淀pH 及水热时间发现,以水作溶剂时,还原程度较高,但有机配位键与rGO 的相互作用减弱。与乙二醇相比,以V(乙醇)∶V(水)=1∶1 为溶剂时,石墨烯的结构更加稳定;沉淀pH 为7.0 时,rGO 还原程度较低,pH 为13.0 时,金属有机配位键形成最好;水热时间延长有利于GO的还原及有机配体与GO 之间的相互作用。褶皱层状的rGO 可以更好地锚定Cu NPs 可以提高催化剂的抗烧结性能和活性。因此,将TPA 引入铜基石墨烯纳米复合催化剂在催化脱氢反应中具有良好的发展前景。
