染色体微阵列分析联合全外显子组测序在胎儿骨骼发育异常产前诊断的应用
2020-06-21王桂喜胡矩锋
王桂喜,胡矩锋
(临沂市妇幼保健院,山东 临沂 276000)
骨骼系统发育异常(Skeletal abnormalities,SA)是人类最常见的出生缺陷之一。其原因包括遗传或环境因素(包括药物或机械作用)[1]。目前,已有学者将染色体微阵列分析技术应用于胎儿SA的产前诊断,与单纯染色体核型分析相比,明显提高了致病基因的检出率[2]。但仍无法检出因单基因病导致的胎儿SA;另外,目前尚未见全外显子组测序(Whole exome sequencing,WES)应用于胎儿SA的报道。本文将核型分析、染色体微阵列分析(Chromosomal microarray analysis,CMA)和WES同时用于产前胎儿SA的临床诊断,现将结果报道如下。
1 资料与方法
1.1一般资料 选择本院2017年12月—2019年12月因胎儿SA就诊的11例孕妇,孕周18~26周,平均22.55周。所有孕妇均签订知情同意书,胎儿SA均在分娩或引产后经随访证实。
1.2方法 11例孕妇中9例行羊水穿刺,2例直接引产,引产后胎儿组织进行取样。所有病例均行染色体核型+CMA检测,其中4例加用WES检测。染色体核型检测:羊水穿刺病例经接种、培养和收获细胞,采用G显带技术对染色体核型进行染色,计数30个核型,分析5个,遇异常核型则计数分析数量加倍。CMA检测:对引产后的胎儿,取2块组织块(带皮肤的肌肉组织3 cm×3 cm),抽取胎儿父母静脉血,乙二胺四乙酸真空采血管采血,各5 mL,标本经处理后保存-80℃待测。进行低覆盖度全基因组测序并结合生物信息学分析,准确定位100kb以上的微缺失/微重复片段。若在胎儿组织中检测出100 kb以上与疾病相关的微缺失/微重复,则使用其父母样本用相同方法进行验证。WES检测:提取胎儿组织DNA和父母外周血DNA,所有DNA浓度>50 ng/μL,总量>1.5μg,吸光度(A260/280 nm)为1.8~2.0。后超声打断基因组DNA,经过建库、杂交捕获、质控等过程后进行测序。测序过程由博圣公司完成。样本的来源与取血检查方式均已通过医院伦理委员会批准,患者填写知情同意书后接受产前诊断。
2 结果
2.1染色体核型及CMA检测情况 所有核型均提示正常(46,XN),仅2例染色体微阵列分析结果提示异常,均为微重复。详见表1。
2.2WES检查结果 行WES检查的4例中,3例(基因型均为het)查出基因突变,其中2例为致病性突变:1例为携带ECEL1的突变,分别位于c.2023G>A,P.a675t和c.2152-3C>G,1例为SLC25A13的突变,位置为c.852-855del、p.R284fs及c.1264-1C>A;另1例为NPR2基因意义不明确的突变。见表2。

表1 胎儿骨骼发育及染色体异常情况
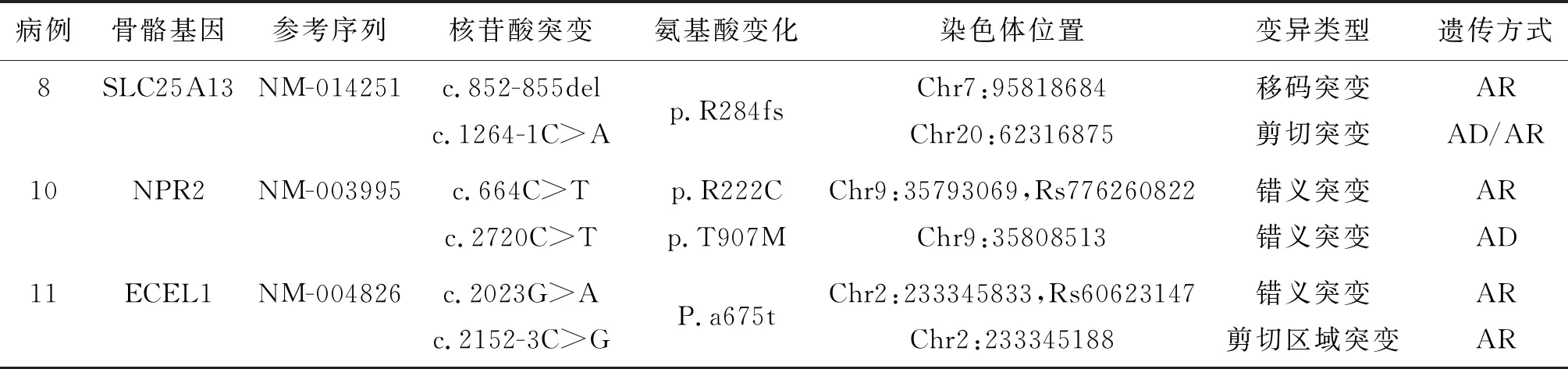
表2 WES检测出的异常者情况
3 讨论
SA包括骨发育异常、软骨发育异常和骨发育不全等,分型不同其表型亦不同。国内文献报道胎儿SA发生率为1.18%[3]。其病因尚不明确,2010年修订的骨发育异常的国际分类标准指出,绝大部分的骨骼发育异常均和已发现的致病基因相关[4]。传统的染色体核型分析仅可以检测到染色体数目异常及较大片段的结构异常,故检出率较低。而染色体微阵列分析具有较大优势,可检测染色体不平衡畸变,包括染色体非整倍体、染色体微缺失或微重复,可检测到常规染色体核型分析无法检测的拷贝数变异[5]。本研究11例病例中,染色体核型均未见异常,行CMA检测提示2例染色体异常,均为微重复。
众所周知,人类85%的致病基因变异位于外显子区。WES是利用序列捕获技术将全基因组外显子区域脱氧核糖核酸(DNA)捕捉并富集后进行高通量测序的基因组分析技术,与染色体微阵列分析相比,有它独特的优势。本研究4例行WES检查的病例中,3例WES结果异常,1例捕获到NPR2基因NM-003995中的错义突变,但意义不明确;1例捕获到ECEL1基因的15号外显子在NM-004826序列的杂合变异,其中c.2023G>A(P.a675t)为错义突变,该变异位于重要的蛋白质功能结构区域,依据美国医学遗传学与基因学学会(ACMG)变异分类标准与指南,此变异为致病性变异,此类变异可导致远端关节挛缩5D型,主要表现为严重的手部屈曲指、轻度的脚趾屈曲、内翻足、膝关节伸展性挛缩、髋关节脱位等;1例检测到SLC25A13的移码变异,多种计算机辅助分析预测这个变异可能影响蛋白质结构/功能的可能性较大,较多数据库认为此变异具有致病性。
综上所述,染色体微阵列分析联合WES检测可明显提高染色体异常的检出率,尤其是胎儿骨骼发育异常诊断的阳性率明显增加。此技术的应用,不仅为产前诊断及遗传咨询提供了指导,也为及早进行出生缺陷干预及再发生育风险评估提供了理论依据。
