阔鳞鳞毛蕨黄酮类化学成分的分离与鉴定
2020-06-17李焕勇陈能花
王 林,李焕勇,梁 妮,陈能花
1暨南大学分析测试中心,广州 510632;2珠海市斗门区新盈中等职业学校,珠海 519100;3暨南大学中药及天然药物研究所,广州 510632
阔鳞鳞毛蕨Dryopterischampionii(Benth.) C.Chr.为鳞毛蕨科(Dryopteridaceae)鳞毛蕨属(Dryopteris)植物,广泛分布于我国山东、江苏、浙江、江西、福建、河南、湖南、湖北、广东、香港、广西、四川、贵州、云南、西藏等地,日本、朝鲜也有分布[1]。该植物作为中药资源被收录于《中国中药资源志要》,具有清热解毒、止咳平喘的功效,可用于治疗感冒、气喘、便血、烧烫伤等病症[2]。现代研究显示,阔鳞鳞毛蕨中主要含有间苯三酚、脂肪酸、甾醇等化学成分,其中间苯三酚是其特征性成分,并对多种肿瘤细胞显示出较强的抑制活性[2,3]。前期本课题组对该植物95%乙醇提取物的石油醚萃取部位进行了系统研究,发现其中部分间苯三酚化合物表现出显著的抑菌活性[4,5]。为了进一步研究分析阔鳞鳞毛蕨的化学成分,寻找活性成分,本实验对阔鳞鳞毛蕨95%乙醇提取物中的乙酸乙酯萃取部位进行了研究。
1 仪器与材料
Bruker AV-500/400型核磁共振波谱仪(瑞士Bruker公司);JASCO P 2000旋光仪(日本JASCO公司);Agilent 6210 LC/MSD TOF高分辨质谱仪(美国Agilent公司);Shimadzu LC-20AD型分析型高效液相色谱仪(日本Shimadzu公司);Shimadzu LC-20AP型制备型高效液相色谱仪(日本Shimadzu公司);EYALA旋转蒸发仪(日本EYALA公司)。
柱层析材料:硅胶(80~100,200~300目,青岛海洋化工厂)、ODS(Merck公司)、Sephadex LH-20(Pharmacia公司);硅胶GF254薄层预制板(烟台化学工业研究所);分析和制备高效液相所用试剂为色谱级;其他均为分析纯。
实验所用药材阔鳞鳞毛蕨(地上部分)于2014年4月采自贵州省贵阳市,经暨南大学药学院周光雄教授鉴定为鳞毛蕨科鳞毛蕨属植物阔鳞鳞毛蕨Dryopterischampionii的地上部分,药材标本(No.2014041705)存于暨南大学中药及天然药物研究所。
2 提取与分离
取干燥阔鳞鳞毛蕨地上部分药材(10 kg),充分粉碎,经95%乙醇于室温下浸渍提取4次,合并所得提取液,减压浓缩得粗提物(1.12 kg)。将所得粗提物加适量水进行混悬,并依次用体积比约3∶1的石油醚、乙酸乙酯进行萃取,分别减压回收得石油醚(0.25 kg)、乙酸乙酯(0.35 kg)萃取部位。取乙酸乙酯萃取部位浸膏进行硅胶柱层析(200~300目),以石油醚-乙酸乙酯为洗脱剂进行梯度洗脱(100∶0→0∶100),经TLC检测分析合并后得14个馏分(Fr.1~Fr.14)。其中馏分Fr.6~Fr.7分别经Sephadex LH-20柱层析(100%甲醇)纯化得到子馏分(Fr.6-S1~Fr.6-S8,Fr.7-S1~Fr.7-S10)。纯化后的子馏分Fr.6-S6经制备型高效液相[甲醇-水(0.1%乙酸)=53∶47]得到化合物3(6.0 mg),4(5.6 mg),6(5.2 mg)和7(8.5 mg);Fr.7-S4经制备型高效液相[甲醇-水(0.1%乙酸)=53∶47]得到化合物2(10.0 mg)和5(11.2 mg)。馏分Fr.9和Fr.10分别通过ODS柱层析并以甲醇-水(20∶80→100∶0)梯度洗脱进行纯化,得到子馏分(Fr.9-O1~Fr.9-O17,Fr.10-O1~Fr.10-O15)。纯化后的子馏分Fr.9-O3通过制备型高效液相[甲醇-水(0.1%乙酸)=30∶70]分离得到化合物1(16.2 mg);子馏分Fr.9-O7通过制备型高效液相[甲醇-水(0.1%乙酸)=35∶65]得到化合物13(13.2 mg);Fr.9-O13通过制备型高效液相[甲醇-水(0.1%乙酸)=40∶60]得到化合物8(10.8 mg)和9(11.3 mg);Fr.10-O10通过制备型高效液相[甲醇-水(0.1%乙酸)=39∶61]分离得到化合物10(9.2 mg)和11(8.8 mg);Fr.10-O13通过制备型高效液相[甲醇-水(0.1%乙酸)=40∶60]分离得到化合物12(6.5 mg)。
3 结构鉴定
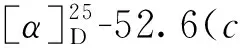
化合物2黄色粉末;HR-ESI-MS:m/z309.037 2[M+Na]+(calcd for C15H10O6Na,309.037 0);1H NMR(500 MHz,CD3OD)δ:7.30(2H,overlapped,H-2′,6′),6.87(1H,d,J=8.1 Hz,H-5′),6.45(1H,s,H-3),6.37(1H,d,J=1.9 Hz,H-8),6.16(1H,d,J=1.9 Hz,H-6);13C NMR(125 MHz,CD3OD)δ:165.9(C-2),103.8(C-3),183.7(C-4),163.1(C-5),100.1(C-6),166.2(C-7),95.0(C-8),159.3(C-9),105.2(C-10),123.6(C-1′),114.1(C-2′),146.9(C-3′),150.9(C-4′),116.7(C-5′),120.2(C-6′)。以上数据与文献[7]报道数据一致,故鉴定该化合物为木犀草素。
化合物3黄色粉末;HR-ESI-MS:m/z273.076 7[M+H]+(calcd for C15H13O5,273.075 7);1H NMR(500 MHz,CD3OD)δ:7.31(2H,d,J=8.4 Hz,H-2′,6′),6.82(2H,d,J=8.4 Hz,H-3′,5′),5.90(1H,d,J=2.1 Hz,H-6),5.88(1H,J=2.1 Hz,H-8),5.35(1H,dd,J=13.0,3.0 Hz,H-2),3.15(1H,dd,J=17.1,13.0 Hz,H-3a),2.72(1H,dd,J=17.1,3.0 Hz,H-3b);13C NMR(125 MHz,CD3OD)δ:80.5(C-2),44.0(C-3),197.8(C-4),164.9(C-5),97.1(C-6),168.4(C-7),96.2(C-8),165.4(C-9),103.3(C-10),131.1(C-1′),129.0(C-2′,6′),116.3(C-3′,5′),159.0(C-4′)。以上数据与文献[8]报道数据一致,故鉴定该化合物为柚皮素。
化合物4黄色粉末;HR-ESI-MS:m/z289.070 8[M+H]+(calcd for C15H13O6,289.070 7);1H NMR(500 MHz,CD3OD)δ:6.92(1H,s,H-2′),6.79(2H,s,H-5′,6′),5.90(1H,d,J=1.8 Hz,H-6),5.88(1H,d,J=1.8 Hz,H-8),5.29(1H,dd,J=12.8,3.0 Hz,H-2),3.10(1H,dd,J=17.1,12.8 Hz,H-3a),2.72(1H,dd,J=17.1,3.0 Hz,H-3b);13C NMR(125 MHz,CD3OD)δ:80.5(C-2),44.1(C-3),197.7(C-4),165.5(C-5),97.0(C-6),168.5(C-7),96.2(C-8),164.8(C-9),103.3(C-10),131.8(C-1′),114.7(C-2′),146.5(C-3′),146.9(C-4′),116.2(C-5′),119.2(C-6′)。以上数据与文献[9]报道数据一致,故鉴定该化合物为圣草酚。
化合物5黄色粉末;HR-ESI-MS:m/z303.050 2[M+H]+(calcd for C15H11O7,303.049 9);1H NMR(500 MHz,DMSO-d6)δ:7.68(1H,d,J=2.2 Hz,H-2′),7.55(1H,dd,J=8.4,2.2 Hz,H-6′),6.88(1H,d,J=8.4 Hz,H-5′),6.41(1H,d,J=2.0 Hz,H-8),6.19(1H,d,J=2.0 Hz,H-6);13C NMR(125 MHz,DMSO-d6)δ:146.8(C-2),135.8(C-3),175.9 (C-4),156.2(C-5),98.2(C-6),163.9(C-7),93.4(C-8),160.8(C-9),103.1(C-10),122.0(C-1′),115.1(C-2′),145.1(C-3′),147.7(C-4′),115.6(C-5′),120.0(C-6′)。以上数据与文献[9]报道数据一致,故鉴定该化合物为槲皮素。
化合物6黄色粉末;HR-ESI-MS:m/z271.061 2[M+H]+(calcd for C15H11O5,271.060 1);1H NMR(500 MHz,CD3OD)δ:7.86(2H,d,J=8.5 Hz,H-2′,6′),6.94(2H,d,J=8.5 Hz,H-3′,5′),6.59(1H,s,H-3),6.46(1H,br s,H-8),6.21(1H,br s,H-6);13C NMR (125 MHz,CD3OD)δ:166.3(C-2),103.8(C-3),183.9(C-4),163.3(C-5),100.2(C-6),166.1(C-7),95.1(C-8),159.4(C-9),105.3(C-10),123.3(C-1′),129.4(C-2′,6′),117.0(C-3′,5′),162.8(C-4′)。以上数据与文献[10]报道数据一致,故鉴定该化合物为芹菜素。
化合物7黄色粉末;HR-ESI-MS:m/z309.038 5[M+Na]+(calcd for C15H10O6Na,309.037 0);1H NMR(500 MHz,CD3OD)δ:8.09(2H,d,J=8.4 Hz,H-2′,6′),6.91(2H,d,J=8.4 Hz,H-3′,5′),6.39(1H,br s,H-8),6.18(1H,br s,H-6);13C NMR(125 MHz,CD3OD)δ:148.0(C-2),137.2(C-3),177.4(C-4),162.5(C-5),99.3(C-6),165.7(C-7),94.5(C-8),158.3(C-9),104.5(C-10),123.8(C-1′),130.7(C-2′,6′),116.3 (C-3′,5′),160.5(C-4′)。以上数据与文献[11]报道数据一致,故鉴定该化合物为山奈酚。
化合物8黄色粉末;HR-ESI-MS:m/z431.113 6[M+H]+(calcd for C21H21O11,431.112 9);1H NMR(500 MHz,CD3OD)δ:8.07(2H,d,J=8.9 Hz,H-2′,6′),6.90(2H,d,J=8.9 Hz,H-3′,5′),6.41(1H,d,J=2.1 Hz,H-8),6.21(1H,d,J=2.1 Hz,H-6),5.26(1H,d,J=7.5 Hz,H-1″),3.71(1H,dd,J=11.8,2.3 Hz,H-6″a),3.55(1H,dd,J=11.8,5.5 Hz,H-6″b),3.43(2H,m,H-4″,5″),3.20(2H,m,H-2″,3″);13C NMR(125 MHz,CD3OD)δ:159.1(C-2),135.5(C-3),179.5(C-4),163.1(C-5),99.9(C-6),166.1(C-7),94.8(C-8),158.5(C-9),105.7(C-10),122.8(C-1′),132.3(C-2′,6′),116.1(C-3′,5′),161.6(C-4′),104.1(C-1″),75.7(C-2″),78.1(C-3″),71.4(C-4″),78.4(C-5″),62.6(C-6″)。以上数据与文献[12]报道数据一致,故鉴定该化合物为黄芪苷。
化合物9黄色粉末;HR-ESI-MS:m/z457.074 4[M+Na]+(calcd for C20H18O11Na,457.074 1);1H NMR(500 MHz,CD3OD)δ:7.53(1H,d,J=2.1 Hz,H-2′),7.51(1H,dd,J=8.4,2.1 Hz,H-6′),6.91(1H,d,J=8.4 Hz,H-5′),6.40(1H,d,J=2.1 Hz,H-6),6.21(1H,d,J=2.1 Hz,H-8),5.47(1H,s,H-l″),4.34(1H,dd,J=3.0,0.7 Hz,H-2″),3.92(1H,dd,J=5.2,3.0 Hz,H-3″),3.87(1H,m,H-4″),3.50(2H,m,H-5″);13C NMR(125 MHz,CD3OD)δ:159.4(C-2),134.9(C-3),180.0(C-4),163.1(C-5),99.9(C-6),166.1(C-7),94.8(C-8),158.6(C-9),105.6(C-10),123.0(C-l′),116.4(C-2′),146.4(C-3′),149.9(C-4′),116.8(C-5′),123.1(C-6′),109.5(C-l″),83.3(C-2″),78.7(C-3″),88.0(C-4″),62.5(C-5″)。以上数据与文献[13]报道数据一致,故鉴定该化合物为广寄生苷。
化合物10黄色粉末;HR-ESI-MS:m/z487.085 7[M+Na]+(calcd for C21H20O12Na,487.084 7);1H NMR(500 MHz,DMSO-d6)δ:7.57(2H,overlapped,H-2′,6′),6.85(1H,d,J=8.9 Hz,H-5′),6.40(1H,br s,H-8),6.20(1H,br s,H-6),5.47(1H,d,J=7.0 Hz,H-1″),3.57(2H,overlapped,H-6″),3.22(2H,overlapped,H-2″,3″),3.08(2H,overlapped,H-4″,5″);13C NMR(125 MHz,DMSO-d6)δ:156.3(C-2),133.3(C-3),177.4(C-4),161.2(C-5),98.7(C-6),164.1(C-7),93.5(C-8),156.2(C-9),104.0(C-10),121.6(C-1′),115.2(C-2′),144.8(C-3′),148.5(C-4′),116.2(C-5′),121.2(C-6′),100.8 (C-1″),74.1(C-2″),76.5(C-3″),69.9(C-4″),77.6(C-5″),61.0(C-6″)。以上数据与文献[14]报道数据一致,故鉴定该化合物为槲皮素-3-O-β-D-葡萄糖苷。
化合物11黄色粉末;HR-ESI-MS:m/z431.112 7[M+H]+(calcd for C21H21O10,431.112 9);1H NMR(500 MHz,DMSO-d6)δ:8.04(2H,d,J=8.8 Hz,H-2′,6′),6.90(2H,d,J=8.8 Hz,H-3′,5′),6.78(1H,s,H-3),6.28(1H,s,H-6),5.01(1H,d,J=4.2 Hz,H-1′′),3.80(2H,m,H-6′′),3.53(1H,m,H-2′′),3.39(1H,overlapped,H-4′′),3.26(2H,overlapped,H-3′′,5′′);13C NMR(125 MHz,DMSO-d6)δ:164.0(C-2),102.5(C-3),182.1(C-4),160.4(C-5),98.2(C-6),162.6(C-7),104.6(C-8),156.0(C-9),104.1(C-10),121.6(C-1′),129.0(C-2′,C-6′),115.8(C-3′,C-5′),161.2(C-4′),73.4(C-1″),70.9(C-2″),78.7(C-3″),70.6(C-4″),81.9(C-5″),61.3(C-6″)。以上数据与文献[15]报道数据一致,故鉴定该化合物为牡荆素。
化合物12黄色粉末;HR-ESI-MS:m/z433.114 5[M+H]+(calcd for C21H21O10,431.112 9);1H NMR(500 MHz,DMSO-d6)δ:7.97(2H,d,J=8.8 Hz,H-2′,6′),6.95(2H,d,J=8.8 Hz,H-3′,5′),6.87(1H,s,H-3),6.83(1H,d,J=2.1 Hz,H-8),6.45(1H,d,J=2.1 Hz,H-6),5.40(1H,d,J=5.0 Hz,H-1′′),3.73(1H,dd,J=10.5,5.0 Hz,H-6′′a),3.47(2H,overlapped,H-2′′,6′′b),3.26(1H,overlapped,H-4′′),3.19(2H,overlapped,H-3′′,5′′);13C NMR(125 MHz,DMSO-d6)δ:163.0(C-2),103.1(C-3),182.0(C-4),156.9(C-5),99.5(C-6),164.3(C-7),94.8(C-8),161.1(C-9),105.3(C-10),121.0(C-1′),128.6(C-2′,6′),116.0(C-3′,5′),161.4(C-4′),99.9(C-1′′),73.1(C-2′′),76.4(C-3′′),69.5(C-4′′),77.2(C-5′′),60.6(C-6′′)。以上数据与文献[16]报道数据一致,故鉴定该化合物为芹菜素-7-O-β-D-葡萄糖苷。
化合物13黄色粉末;HR-ESI-MS:m/z779.180 6[M+Na]+(calcd for C36H36O18Na,779.179 4);1H NMR(500 MHz,CD3OD)δ:7.44(1H,d,J=15.9 Hz,H-7′′′′),7.35(1H,d,J=1.8 Hz,H-2′),7.24(1H,dd,J=8.4,1.8 Hz,H-6′),7.21(2H,d,J=8.5 Hz,H-2′′′′,6′′′′),6.93(1H,d,J=8.4 Hz,H-5′),6.68(2H,d,J=8.5 Hz,H-3′′′′,5′′′′),6.16(2H,s,H-6,8),6.06(1H,d,J=15.9 Hz,H-8′′′′),5.74(1H,br s,H-1′′),4.52(1H,dd,J=11.8,2.0 Hz,H-6′′′a),4.46(1H,d,J=7.8 Hz,H-1′′′),4.39(1H,br d,J=2.2 Hz,H-2′′),4.15(1H,dd,J=11.8,6.2 Hz,H-6′′′b),3.92(1H,dd,J=9.8,3.0 Hz,H-3′′),3.73(1H,m,H-5′′),3.46(1H,m,H-5′′′),3.40(1H,t,J=9.8 Hz,H-4′′),3.32(3H,overlapped,H-2′′′,3′′′,4′′′),1.09(1H,d,J=6.2 Hz,H-6′′);13C NMR(125 MHz,CD3OD)δ:158.2(C-2),136.7(C-3),179.5(C-4),163.0(C-5),99.7(C-6),165.5(C-7),94.8(C-8),158.3(C-9),105.9(C-10),122.8(C-1′),117.0(C-2′),146.2(C-3′),149.6(C-4′),116.3(C-5′),123.0(C-6′),102.5(C-1′′),83.6(C-2′′),71.7(C-3′′),73.5 (C-4′′),71.9(C-5′′),17.7(C-6′′),107.1(C-1′′′),75.1(C-2′′′),77.5(C-3′′′),71.9(C-4′′′),75.2(C-5′′′),64.3(C-6′′′),126.9(C-1′′′′),130.9(C-2′′′,6′′′′),116.6(C-3′′′′,5′′′′),160.9 (C-4′′′′),146.6(C-7′′′′),114.6(C-8′′′′),168.9(C-9′′′′)。以上数据与文献[17]报道数据一致,故鉴定该化合物为槲皮素-3-O-6-反式-对香豆酰基-β-D-葡萄糖-(1→2)-α-L-鼠李糖苷。
4 结果与讨论
本实验对阔鳞鳞毛蕨地上部分的乙醇提取物进行了系统的化学成分研究,从乙酸乙酯萃取部位分离鉴定了13个黄酮类化合物,均为首次从该植物中得到。阔鳞鳞毛蕨为鳞毛蕨属植物,被收录于《中国中药资源志要》,具有清热解毒、止咳平喘的功效。目前仅有少量文献报道对其化学成分的研究,且主要集中于其挥发性成分和间苯三酚类结构,同时其药理活性的物质基础也主要以间苯三酚类成分作为评价指标。本实验通过对阔鳞鳞毛蕨极性中等的乙酸乙酯部位进行分离纯化,得到了多种黄酮类结构,丰富了该植物的化学成分类型,同时也可为寻找新的生物活性和临床应用的开发提供重要的依据。
黄酮类化合物是泛指一类以两个苯环通过中间三个碳原子连接而形成的结构为基本母核的化合物,根据结构中间三碳链的氧化程度可将其进一步分为黄烷醇、黄酮、黄酮醇、二氢黄酮和二氢黄酮醇等[18]。该类化合物广泛存在于自然界植物中,是多种中药和天然药物的活性成分之一,具有抗氧化、抗菌、抗病毒、抗炎等多种药理活性[18]。如表儿茶素结构中存在的酚羟基,可提供氢质子与自由基结合,形成稳定的氢键,抑制自由基连锁反应,发挥抗氧化作用[19];柚皮素可干扰金黄色葡萄球菌和大肠杆菌膜脂成分的变化,以及改变细胞膜的通透性,同时还能作用于细菌细胞内的基因组DNA,使其发生聚集,导致细胞死亡[20];槲皮素可与流感病毒的血球凝集素相互作用从而抑制流感病毒入侵宿主细胞[21];黄芪苷可通过抑制丝裂原活化蛋白激酶(MAPKs)、NF-κB等相关信号通路的激活,降低促炎细胞因子表达发挥抗炎作用[22]。黄酮类化合物作为重要的天然有机化合物,具有多种生物活性,应用广泛,临床上可被用于感染性疾病、慢性炎症等疾病的治疗,工业领域可被制作成营养粉或食疗粉等保健品,还可作为天然的甜味剂和抗氧化剂等[23-25]。
鳞毛蕨科的鳞毛蕨属为我国的蕨类大属之一,该属植物广泛分布于全国各地,其最初的药用价值主要是作为驱虫药使用,而随着对该属植物研究的不断深入,更多的化学成分及其药理功效被发现,其中较低极性的间苯三酚类成分一直被认为是该属植物的特征性成分及药理活性的主要成分,而较中等极性及含量较高的常见黄酮类成分则易被忽视。因此本实验从阔鳞鳞毛蕨研究中对具有多种显著药理活性的黄酮类成分的发现,则可促进对该药用植物的开发和应用,并为其提供一定的指导和科学依据,使该蕨类资源能得到充分有效的利用。
