N-正丁基乙醇胺合成工艺的改进
2020-06-15唐英武钱莉苹吴世刚
唐英武,黄 勇,钱莉苹,吴世刚
1.宿州亿帆药业有限公司,安徽宿州,234000;2.合肥亿帆生物制药有限公司,安徽合肥,231200
N-正丁基乙醇胺,N,N-二正丁基乙醇胺是两种重要的精细化工中间体和医药中间体,在纺织、医药、农用化学品等方面具有广泛的应用,可生产医药、涂料、表面活性剂等,也可作为脱碳、脱硫剂等使用[1]。近年来,N-正丁基乙醇胺作为金属切削液的助剂成分和涂料调节剂被开发利用,而随着中国工业加工和建筑行业的迅猛发展,N-正丁基乙醇胺的市场需求也有了迅速扩大。本产品主要来源于国外进口,国外主要生产厂家为BASF等[2]。本文就提高N-正丁基乙醇胺的收率,降低N-正丁基乙醇胺的制备成本进行研究。
1 N-正丁基乙醇胺合成进展
本文根据起始原料不同将其合成路线分为两大类:以正丁胺为原料进行羟乙基化合成;以乙醇胺为原料进行胺烷基化合成[3]。下面就各合成路线进行分析比较。
1.1 以乙醇胺、溴代正丁烷为原料路线
乙醇胺和溴代正丁烷的反应属于卤代烷的亲核取代反应[4-5]。溴代正丁烷先和一分子乙醇胺反应生成目标产物N-正丁基乙醇胺,但N-正丁基乙醇胺的亲核性大于乙醇胺,会继续与体系中未反应的溴代正丁烷发生进一步亲核取代反应,生成N,N-二正丁基乙醇胺。为了提高N-正丁基乙醇胺的收率,必须大大增加乙醇胺的摩尔配比,以抑制N,N-二正丁基乙醇胺的生成,因此产品收率不高,生产成本较高。
1.2 以氯乙醇、正丁胺为原料路线
以氯乙醇、正丁胺为原料有二取代的副产物生成[6],比例与反应原料的摩尔比有关,正丁胺的比例越高,得到的主产品比例越高,但不能完全抑制副产物。从各原料和产物来看,正丁胺沸点为77 ℃,氯乙醇需要完全转化而不需要考虑分离,主产物N-正丁基乙醇胺沸点为200 ℃,副产物N-正丁基二乙醇胺沸点为274 ℃,而为反应的乙醇胺沸点为170.5 ℃,因此产品分离需要较高的蒸馏柱。并且氯乙醇属于剧毒化学品,购买使用需要特殊许可证,经多方面打听都未买到该原料,并考虑最后大生产的方便,最后放弃了该路线。
1.3 以乙醇胺、正丁醛为原料路线
以乙醇胺、正丁醛为原料合成N-正丁基乙醇胺分两步[7],第一步,正丁醛与乙醇胺生成烯胺,这是一个平衡反应,在有水的存在时是可逆的,在生成烯胺同时也会形成一个五元环的副产物。第二步,烯胺加氢反应,进而被加氢生成目标产物N-正丁基乙醇胺,但水过多后形成烯胺受到影响,收率也会降低。在此加氢反应中,β-羟基不够稳定,因此形成较多的其他不明杂质,给分离带来困难,质量达不到指标。
1.4 以环氧乙烷、正丁胺为原料路线
采用环氧乙烷和正丁胺合成N-正丁基乙醇胺路线[8-9],环氧乙烷和正丁胺价格相对便宜,而且两者是加成反应,原子经济效益高,无需其他溶剂,只要控制好N,N-二正丁基乙醇胺的生成量,就可以显著降低成本。文献报道的工艺比较古老,工艺条件苛刻,不适合工业化,本文采用循环反应和边反应边分离的生产工艺,及时移走反应产物,有效抑制N,N-二正丁基乙醇胺的生成量,以达到N-正丁基乙醇胺高收率低成本的目的。
综合上面反应结果,路线一:由溴代正丁烷和乙醇胺合成N-正丁基乙醇胺的路线需要大大过量的乙醇胺而造成所需的反应设备大,产能低,回收乙醇胺需要大量的能量,同时在后处理过程中需要用到大量的二氯甲烷来萃取产物,二氯甲烷沸点低,只有约40 ℃,挥发性也特别大,回收率非常低,所以成本高。同时由于中和时产生大量的含盐和乙醇胺的废水,需要另外的治理成本,所以综合成本比较高;路线二:由氯乙醇和正丁胺合成N-正丁基乙醇胺的路线中原料氯乙醇毒性大,不易购买;路线三:由正丁醛和乙醇胺合成N-正丁基乙醇胺的路线由于产生大量的副产物而使得收率太低,同时加氢反应需要高压反应釜,设备投入也比较大;路线四:采用环氧乙烷和正丁胺合成N-正丁基乙醇胺的路线,由于两个原材料价格相对比较便宜,原子经济效益高,同时采用特殊设备后可以提高产品的选择性,反应过程中也不产生太多的废弃物,对环保压力也比较小,综合成本显著降低。所以本文采用该路线合成N-正丁基乙醇胺。
本文在路线四的基础上,优化合成工艺条件,在原料物质量之比正丁胺:环氧乙烷为1∶1.6~1.8,环氧乙烷通入时间为5~6 h,反应压力为0.05 MPa~0.06 MPa,反应和分离同步升温由78 ℃至最后控制到134~140 ℃时,产品收率高,纯度达99%,其结构经1H HMR确证。
2 实验部分
2.1 仪器与试剂
GC-2014C 岛津气相仪(岛津企业管理(中国)有限公司);Varian-400MH 核磁共振仪(美国Varian公司)。正丁基胺、环乙烷为化学纯;N-正丁基乙醇胺(对照,分析纯)。
2.2 合成过程
在装有回流冷凝管、温度计、精馏柱以及循环泵和环氧乙烷导气管的500 mL四口烧瓶中加入定量的正丁胺,用氮气置换体系空气,然后抽真空至-0.08 MPa关闭真空阀门,放入电热套中加热至所需温度,然后开启循环泵,打开环氧乙烷阀门,将计量好的环氧乙烷缓慢通入系统中,通完后将反应维持适当温度,持续反应一定时间后,气相色谱中控反应,当基本检测不到有产物增加时终止反应,降温至室温。将物料转入精馏装置,先常压回收正丁胺,然后真空精馏得N-正丁基乙醇胺,收率为82%(与标准品图谱一致),产品纯度为99%(GC面积归一法)。由N-正丁基乙醇胺1HMR图谱(图1)可知,b.p.204~205 ℃; 1H HMR(CDCl3,400 MHz),δ3.59(t,2H),δ2.67(t,1H),2.55(t,4H),1.41(m,2H),δ1.28(dd,2H),δ0.85(t,3H)。
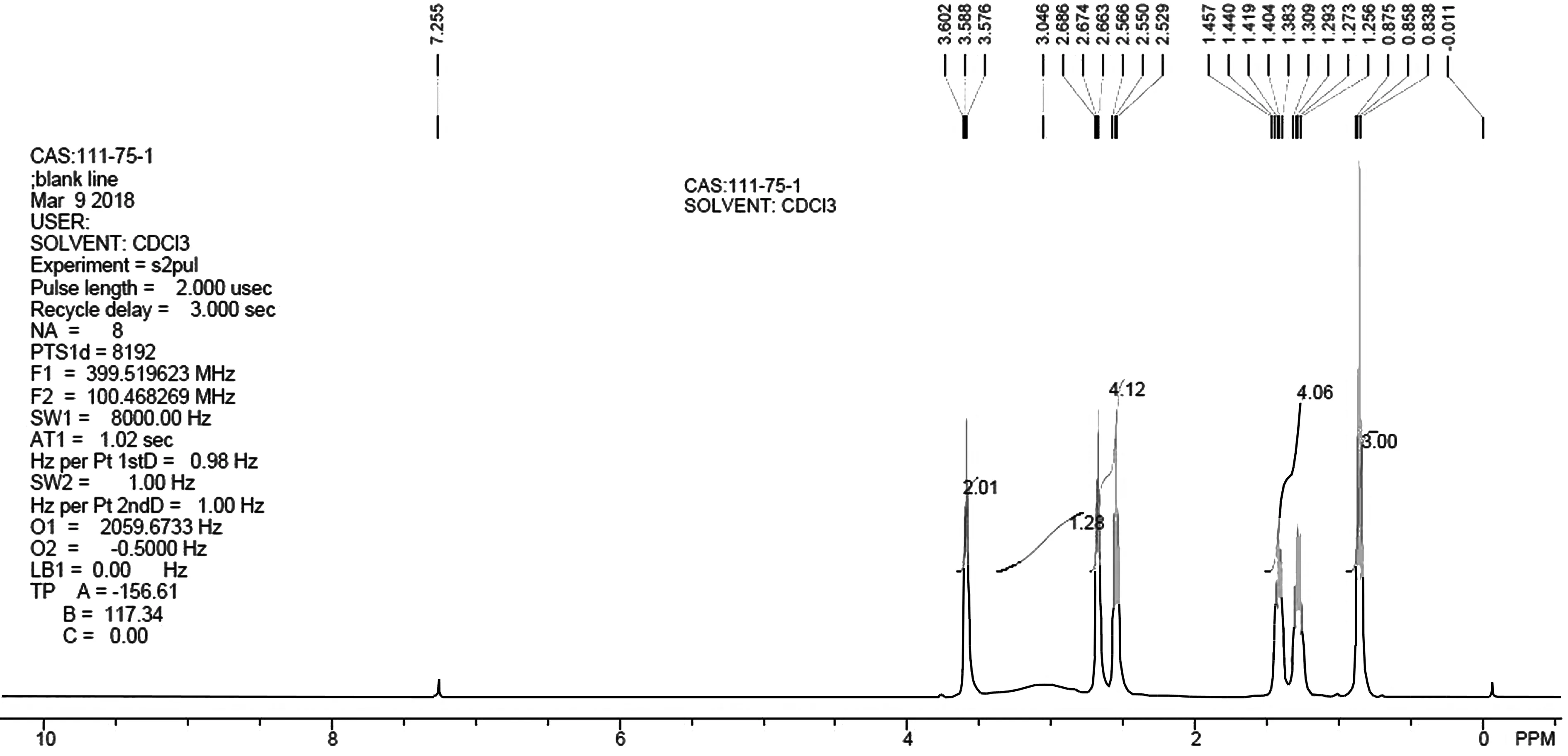
图1 N-正丁基乙醇胺1HMR图谱
3 影响因素控制
为了提高收率和适于工业放大,分别对正丁胺与环氧乙烷摩尔配比、环氧乙烷通入时间(物质量不变,加入时间变化)、反应温度与压力对选择性影响进行了优化。
3.1 正丁胺与环氧乙烷摩尔配比的影响
由图2可知,随着正丁胺加入量的增加,正丁胺的转化率越来越低,但生成N-正丁基乙醇胺的选择性逐步提高,综合考虑正丁胺的回收成本,工艺确定正丁胺与环氧乙烷摩尔比为1∶1.6~1.8为宜。

图2 转化率与选择性和正丁胺与环氧乙烷摩尔配比的关系曲线
3.2 环氧乙烷通入速度的影响
环氧乙烷的通入速度是影响反应的主要因素,由图3可以看出,环氧乙烷加入量不变,通入时间短,反应区域内的环氧乙烷含量过高,导致区域内正丁胺与环氧乙烷摩尔配比变低,使得副产增多,产品选择性变差。而环氧乙烷通入时间过长,产品选择性增加不多并趋于稳定,但带来能耗增加,不利于生产成本控制,故本工艺确定均速5~6 h加完为宜。
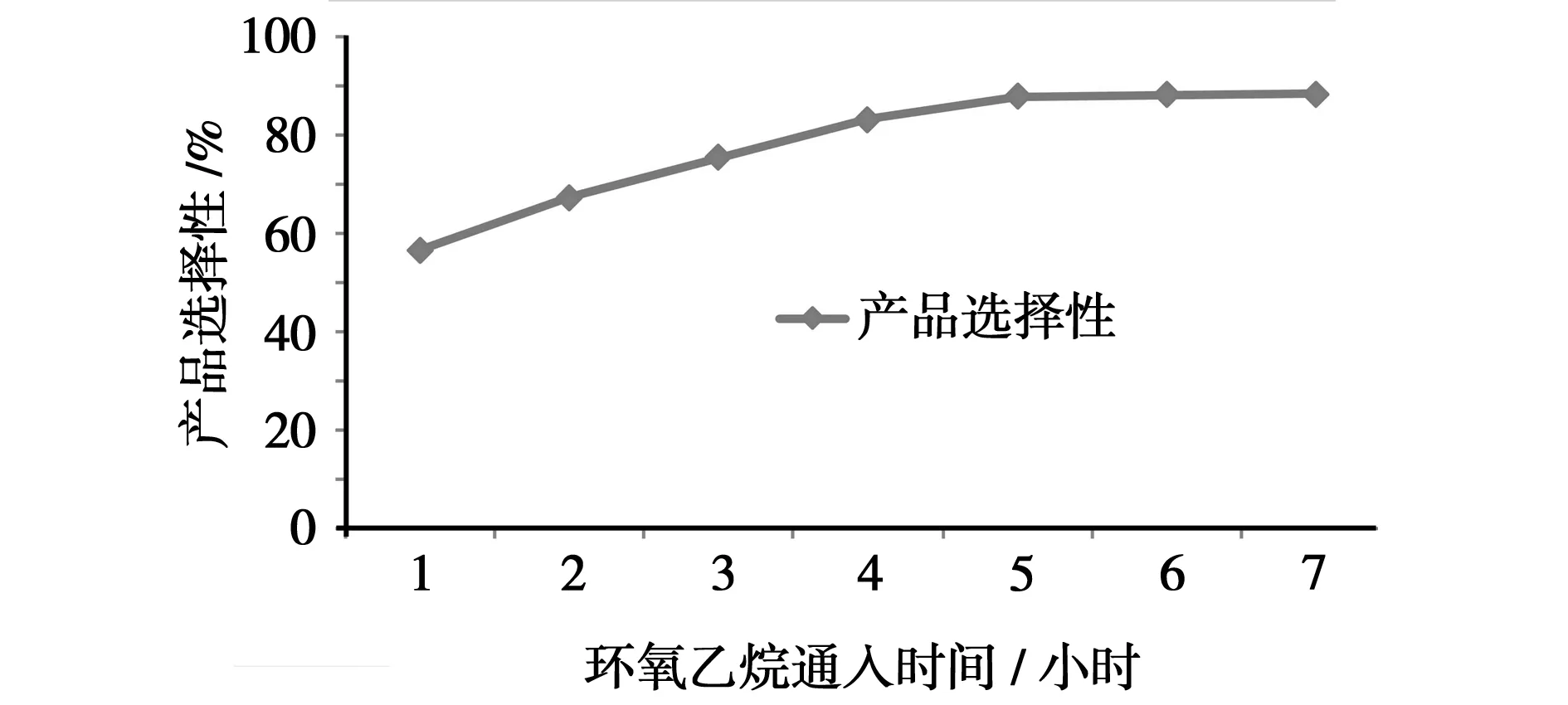
图3 产品选择性和定量环氧乙烷通入时间的关系曲线
3.3 反应温度与压力对反应选择性的影响
本工艺采用循环反应和边反应边分离的生产工艺,及时移走反应产物,有效抑制N,N-二正丁基乙醇胺的生成量,对温度的控制主要决定于正丁胺的气化量,正丁胺的气化量越大,在反应区域正丁胺的摩尔比也越大,使得选择性越高。而体系的压力正好直接指示了正丁胺的气化量,因此本文采用对体系压力的控制来控制正丁胺的气化量,图4显示了压力与选择性的关系。由图4可以看出,反应压力低,产品选择性差,而反应压力过高,对设备要求也高,能耗成本也相应增加,所以本工艺确定最佳反应压力为0.05 MPa~0.06 MPa间。
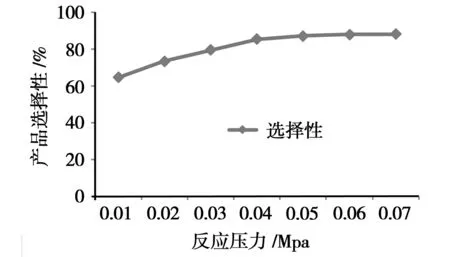
图4 选择性与反应压力关系曲线
为了保持适当的正丁胺气化量,在反应过程中采取逐步提高釜温,由于初始时,体系中是正丁胺,故温度基本控制在78 ℃,随着反应的进行,产物越来越多,而产物沸点为198 ℃,所以必须逐步提高釜内物料的温度,以保证正丁胺的气化量,本实验中最后控制到134~140 ℃就可在保证气化量的情况下是环氧乙烷充分转化反应。
4 结 论
本研究首次使用连续反应,连续精馏移除产品产物,推进了反应正向进行,提供了一个无溶剂的产业化工艺(图5)。对反应的主物料摩尔比、环氧乙烷的通入时间,反应温度与压力四个方面进行了优化,得到最佳的工艺参数为:在正丁胺与环氧乙烷摩尔比1∶1.6~1.8,环氧乙烷通入时间为5~6 h,反应温度为134~140 ℃,压力控制为0.05~0.06 MPa为最佳工艺参数,产品质量指标达到99.0%以上,实现本精细化学品顺利国产化。
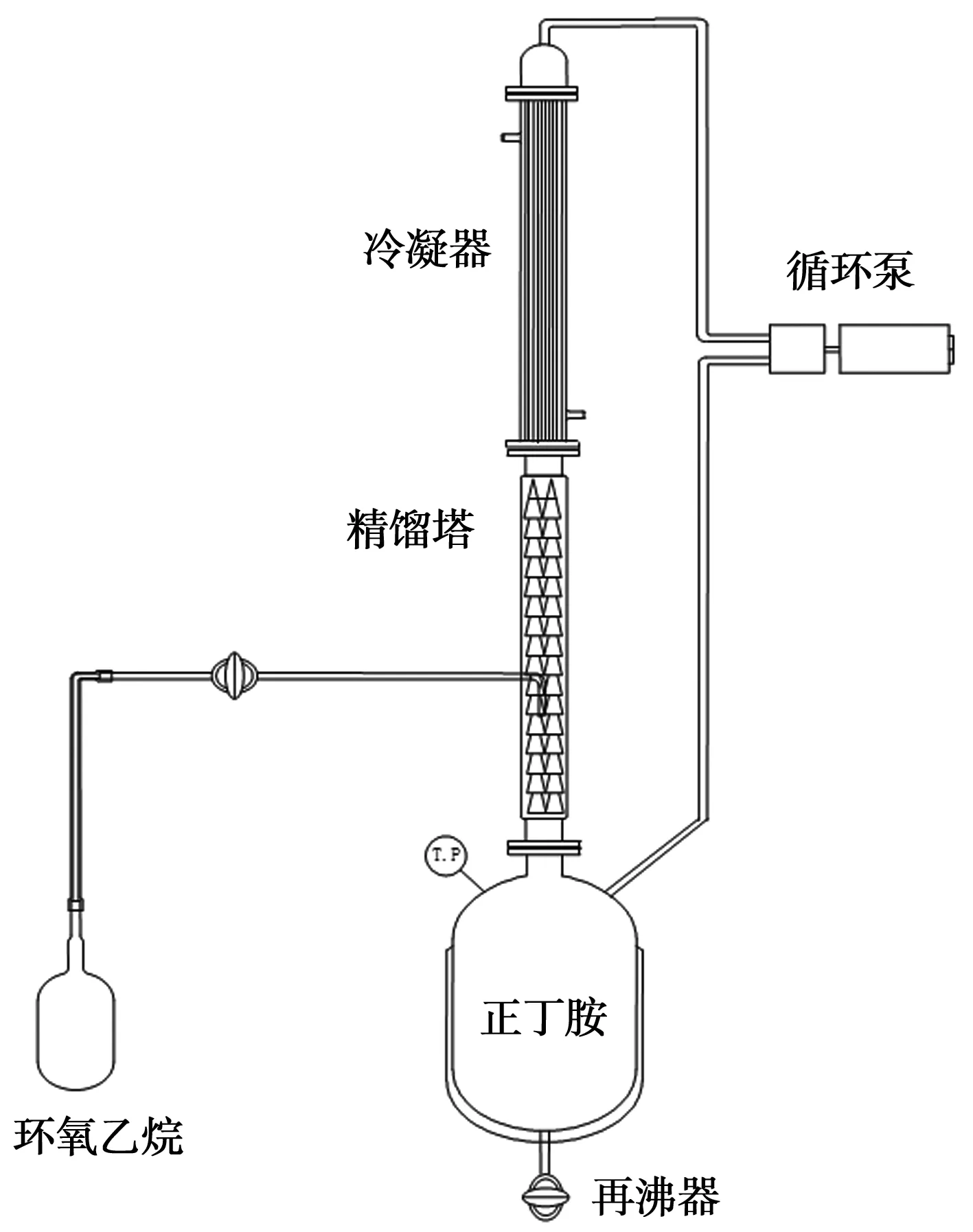
图5 设备工艺流程图
