共沉积法制备Al–Tm合金的可行性研究
2020-06-13郑家宁
◎ 郑家宁
一、实验部分
1.试剂与仪器。
实验过程中使用的药品:
LiCl、KCl、AlCl3、Tm2O3、HCl、HNO3、CH3COCH、AgNO3、Mo、C、刚玉坩埚、刚玉套管。
实验过程中使用的设备:
电化学工作站、X-射线衍射仪、坩埚式电阻炉、电子天平、电感耦合等离子体发光谱仪、电热恒温鼓风干燥箱。
2.电解质与电极体系。
本实验所采用的电解质为等质量比的LiCl-KCl。
采用经典的三电极体系,即研究电极、参比电极和辅助电极。本论文中的工作电极为W,Ag/AgCl为参比电极,辅助电极为石墨棒。
主要的电化学测试方法包括循环伏安、方波伏安。通过循环伏安曲线可以判定各金属离子的还原顺序,以及还原电位的范围,由方波伏安曲线可以计算出某反应的转移电子数。
二、Al(III)和Tm(III)共沉积过程的研究
1.Tm2O3的氯化。
在LiCl–KCl熔盐体系中Tm2O3可以被AlCl3氯化而释放出Tm(III)离子。反应如下:

2.循环伏安曲线。
图1为上述熔盐体系中,在753K下W电极上得到的典型循环伏安曲线。在图中没有观察到图4.20中位于 1.0V左右对应于Al(III)/Al的信号,表明AlCl3已经被成功地从熔盐体系中去除。
图2为753K时,在LiCl–KCl–AlCl3(2wt.%)熔盐体系中加入1wt.%Tm2O3前(实线)后(虚线)在 W电极(S=0.32cm2)上得到的循环伏安曲线。其中C[Al(III)]=2.14×10-4,C[Tm(III)]=7.40×10-5molcm-3。从图中的虚线可以清晰地看到三对信号A/A′、B/B′和C/C′。信号A/A′和C/C′分别是由Al(III)/Al和 Li(I)/Li的还原 /氧化引起的。我们在-1.7V到-2.1V范围内改变循环伏安曲线的换向电位(图3)。当阴极换向电位比-2.00V更正的时候,除了Al(A/A′)的氧化/还原信号外,仅仅能观察到一对氧化/还原信号IV/IV′。但当阴极换向电位变得更负,达到-2.20V时,曲线中出现了一个新的氧化信号V′。因此,阳极信号V′和阴极信号V是一对氧化/还原信号。阴极信号IV和V应该是对应于两种Al-Tm合金的形成。
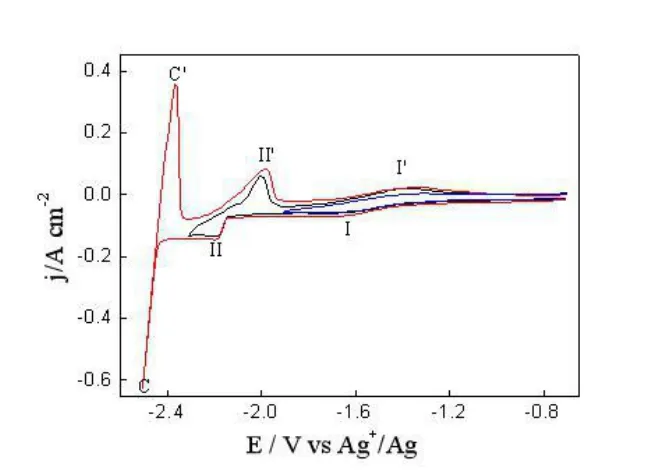
图 1在含有 Tm (III)(9.30×10–5mol/cm3)的LiCl–KCl熔盐体系中不同换向电位下得到的循环伏安曲线;工作电极为W电极(S=0.32cm2),实验温度为753K,扫描速度为0.2Vs-1。
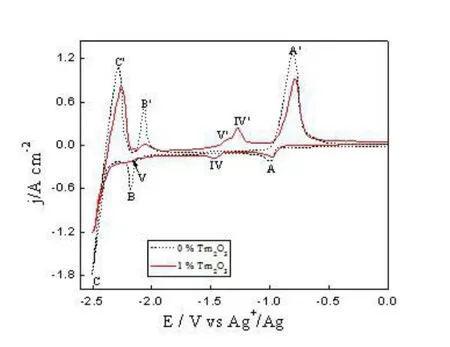
图2在LiCl-KCl-AlCl3(2wt.%)熔盐体系中加入1wt.%Tm2O3前(虚线)后(实线),在W电极(S=0.32cm2)上得到的循环伏安曲线;扫描速度为0.2Vs-1。
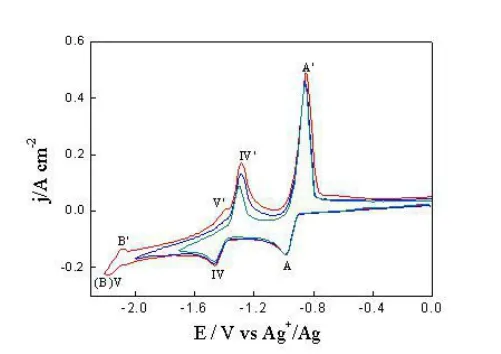
图3753K时,在LiCl-KCl-AlCl3(2wt.%)-Tm2O3(1wt.%)熔盐体系中不同换向电位下得到的循环伏安曲线;扫描速度为0.2Vs-1。
3.方波伏安曲线。
在图2和3中无法清晰的分辨出的阴极信号B和Ⅴ因此,采用比循环伏安更加灵敏的方波伏安法来进一步研究该熔盐体系。图4为在LiCl-KCl-AlCl3(2wt.%)熔盐体系中加入1wt.%Tm2O3前(虚线)后(实线)在W电极(S=0.32cm2)上得到的方波伏安曲线。在添加Tm2O3之前,可以观察到两个信号A和B(曲线肩部),分别对应于Al和一种Al–Li合金的形成。在添加Tm2O3之后,除了信号A和B之外,在信号A和B之间观察到了两个新的信号IV和V,它们对应于两种Al–Tm金属间化合物的形成。
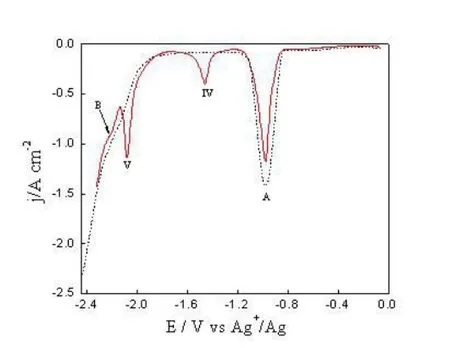
图4在LiCl-KCl-AlCl3(2wt.%)熔盐体系中加入1wt.%Tm2O3前(虚线)后(实线)在W电极(S=0.32cm2)上得到的方波伏安曲线;脉冲高度,25mV;电位阶跃,1mV;频率15Hz。
四、小结
本章探究了在W电极上,Li-Cl-KCl-AlCl3熔盐中 Tm(III)的沉积过程。在-1.28V和-1.36V点位上析出两种Al–Tm合金。证实了Tm(III)与Al(III)形成合金的可行性。
