用单壁羟基碳纳米管/壳聚糖内涂层分析柱毛细管电泳法测定药剂中的盐酸金刚烷胺含量
2020-06-12马永钧
王 荣,马永钧
(西北师范大学 化学化工学院, 甘肃省生物电化学与环境分析重点实验室,甘肃 兰州 730070)
盐酸金刚烷胺( Amantadine Hydrochloride,AH)是一种人工合成的抗病毒类药物[1],主要用于治疗帕金森病[2]、帕金森病异动症[3]、小脑功能障碍[4]等神经系统类疾病。同时它也被添加在各类感冒药中用于预防、治疗病毒性流感引起的呼吸道感染[5-6]。另外,盐酸金刚烷胺与其它抗病毒类药物共同使用还有治疗丙型肝炎[7-9]的作用。但是,盐酸金刚烷胺的用法或用量不当可能会引发晕厥、水肿、睡眠障碍[10-11]等不良反应,因此试样中盐酸金刚烷胺的含量测定对该药品在临床治疗中的安全使用具有重要意义,同时也能为该药品在日常生活中的合理应用提供依据[12]。
《中国药典》中规定一般采用酸碱电位滴定法进行盐酸金刚烷胺的含量测定[13],该方法的操作较为复杂繁琐,用于前处理的样品取样量大。此外,国内外也有报道采用质谱法[14]、色谱法[15-16]、高效液相色谱-蒸发光检测器法[17-18]、高效液相色谱-示差折光检测器法[19]、液相色谱-质谱联用法[20-21]等测定盐酸金刚烷胺含量的仪器分析方法。通常对成分复杂的含盐酸金刚烷胺的药品试样可采用高效液相色谱-蒸发光检测器法[17-18]、高效液相色谱-示差折光检测器法[19]等来进行含量测定。虽然HPLC法具有灵敏度高、分离效能高等优点,但设备昂贵,分析成本高,分析时间也较长。
目前,毛细管电泳-电致化学发光(CE-ECL)法因其分离高效、快速、低成本的优势,已在复杂药物成分的分离测定中发挥出巨大作用[22-23],但用此方法测定盐酸金刚烷胺尚未见报道。因此,本文采用柱前N-甲基化衍生方法[24],将盐酸金刚烷胺转化为具有强发光信号的单一衍生产物,并借助于一种新合成的MTS-gel凝胶电泳分离添加剂和一种单壁羟基碳纳米粒子/壳聚糖复合物壁涂毛细管为分离柱,建立了柱前衍生CE-ECL法对实样药剂中盐酸金刚烷胺进行含量测定的新方法。
1 实验部分
1.1 仪器与试剂
MPI-A型多参数分析测试系统(西安瑞迈电子科技有限公司,中国);CHI760B型电化学工作站(上海辰华仪器公司,中国);熔融石英毛细管(50 cm×75 μm i.d.河北永年光导纤维厂,中国);pH-10型酸度计(赛多利斯有限公司,德国);化学发光信号检测采用三电极系统:工作电极采用含稀土类普鲁士蓝(Er-PBAs)修饰的铂盘电极(Φ=0.3 mm),修饰所用的试剂中仅将稀土离子Eu3+更换为Er3+后即可按原文献方法进行制备[25];辅助电极为铂丝;参比电极为Ag/AgCl (1.0 mol/L KCl盐桥)电极。
盐酸金刚烷胺(AH,含量>98.0 %)(上海阿拉丁生化科技股份有限公司,中国);肌氨酸(Sar,含量> 99.0 %),六水合二氯联吡啶钌(含量>98.0 %)和壳聚糖(脱乙酰度>95 %)(百灵威科技有限公司,中国);单壁羟基碳纳米管(含量>90 %,平均粒度约1~2 nm)(北京德科岛金科技有限公司,中国);1-己基-3-甲基咪唑四氟硼酸盐离子液体(ImidBF4 IL,纯度>99 %),(兰州中科凯特科工贸有限公司,中国);D-(+)海藻糖二水合物(纯度>99 %)(上海阿拉丁生化科技股份有限公司,中国);其余试剂均为分析纯,实验用水均为超纯水(>18 MΩ·cm)。
1.2 电泳测定条件

MTS-gel的合成方法:在一只10 mL的比色管中加入10.0 mmol/L的硝酸镁1.00 mL+20.0 mmol/L的海藻糖溶液0.50 mL+20.0 mmol/L的硅酸钠溶液3.00 mL后用水定容,并置于32 ℃的水浴锅中保温反应13 min,取出后自然冷却至室温备用。
石英毛细管采用了壳聚糖/单壁羟基碳纳米管做内壁修饰材料,具体修饰步骤参见文献[24],所有制备环节中仅将含10.0 mg/mL的壳聚糖稀冰醋酸溶液(1.0 %,体积分数)置换为含10.0 mg/mL壳聚糖+1.0 mg/mL单壁羟基碳纳米管的稀冰醋酸溶液(1.0 %,体积分数),而保持其它制备条件完全一致,即可制备出符合分析要求的内壁涂饰毛细管。
1.3 标准溶液和试样溶液的配制与衍生反应步骤
用标准品试剂分别配制1.00 mmol/L盐酸金刚烷胺溶液和1.00 mmol/L肌氨酸溶液储备液,置于4 ℃冰箱中保存备用。
取片状药片精确称取后研细成粉末置于50 mL小烧杯中,之后再加入2.0 mL无水乙醇,加水搅拌至充分溶解后全部转移至25 mL比色管中以水定容,自然放置达到自然沉降分层,定量吸取上层清液备用。胶囊状药品和冲剂类药品可准确称取其内容物后直接置于50 mL小烧杯中,同样采用以上方法充分溶解后定容于25 mL比色管中。所有预处理后的待测溶液应先加适量内标物用于下步衍生反应。
在一只10 mL比色管中先加入1.00 mL 0.25 mol/L的磷酸盐缓冲溶液(pH值=5.95),用移液管准确加入一定体积的混合标准溶液(含内标物)或待测样溶液(加入溶液的体积应不大于2.0 mL),再加入1.00 mL 0.5 mol/L的甲醛溶液并用水稀释到5.0 mL刻度处后于室温下放置60 min;然后,在比色管中依次加入1.0 mL 0.20 mol/L的氢氧化钠(用于调整反应液的酸度)和0.60 mL 0.01 mol/L的顺丁烯二酸溶液,摇匀后放入57 ℃恒温水浴中加热反应50 min,取出冷却至室温;再逐次加入0.25 mL 0.1 mol/L醋酸铵,1.0 mL 0.25 mol/L硼氢化钠(使用时临时配制)以及0.50 mL 0.2 mol/L的硼酸溶液,注意这三种试剂的加入间隔时间相应保持为10 min,20 min和10 min。最后,直接以水定容至10.0 mL刻度处,取此溶液经由滤膜过滤后就可进样测定,也可于冰箱中保存至2周内进行测定。
2 实验结果
2.1 盐酸金刚烷胺与肌氨酸衍生产物的电致化学发光响应特性
首先,采用CE-ECL法对盐酸金刚烷胺和肌氨酸的混合标准溶液进行了衍生反应前后的对比试验。如图1所示,a曲线和b曲线分别表示100 μmol/L盐酸金刚烷胺和25.0 μmol/L肌氨酸混合标准溶液衍生前后的电泳图。由a曲线只能观察到来源于肌氨酸的微弱杂质峰,而没有来源于盐酸金刚烷胺的任何发光峰。然而,由b曲线可见有三个强的ECL电泳峰,经过加标实验反复确定得出1号峰属于衍生反应中存留的甲醛试剂,而2、3号电泳峰则是待测物盐酸金刚烷胺和内标物肌氨酸各自的衍生产物。通过对比实验曲线a、b就可以得出,经N-甲基化衍生反应后的盐酸金刚烷胺由不发光到产生了高达2500(a.u.)的强电化学发光信号峰,且发光衍生产物单一。

图1 盐酸金刚烷胺与肌氨酸混合标准溶液>经衍生反应前后的对比电泳图
Fig.1 Contrastive electropherograms of the AH and Sar mixture standard solution before and after the derivatization reaction.a.For the sample solution containing 100 μmol/L AH and 25.0 μmol/L Sar,b.For the same sample solution to be undergone through a pre-column N-methylation derivatization process
2.2 柱前衍生反应关键实验条件的优化
一般而言,N-甲基化衍生反应主要分为三个步骤:α-伯胺基通过亲核加成反应形成氨基醇中间体、氨基醇中间体脱水形成亚胺中间体、使用硼氢化钠将亚胺中间体再还原具有更高ECL发光强度N-甲基化衍生产物[26]。因盐酸金刚烷胺本身就含有盐酸成分,样品加入量较大时就会对影响衍生反应溶液的pH值,导致反应不彻底进而影响到衍生产物的ECL发光峰强度。因此,衍生反应过程中的所加入的NaOH量必须进行实验优化(参见实验部分1.3)。从图2中的结果可知,衍生反应中NaOH的加入量在0.16~0.2 mmol范围内时,标样的ECL发光强度逐渐增大,当加入量超过0.2 mmol后,相应的发光强度值又有下降趋势,此时的电泳峰也有展宽现象。因此,可确定NaOH的最佳加入量为0.2 mmol。
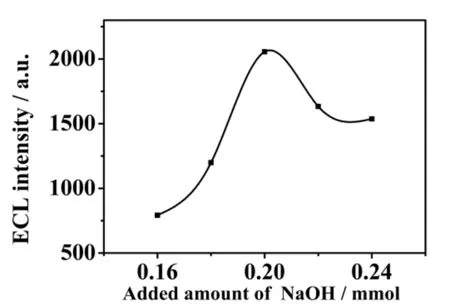
图2 NaOH加入量对盐酸金刚烷胺衍生物电泳峰强度的影响Fig.2 Effect of the addition amount of NaOH on the ECL peak intensity of AH derivative
2.3 背景电解质中分离添加剂的优化
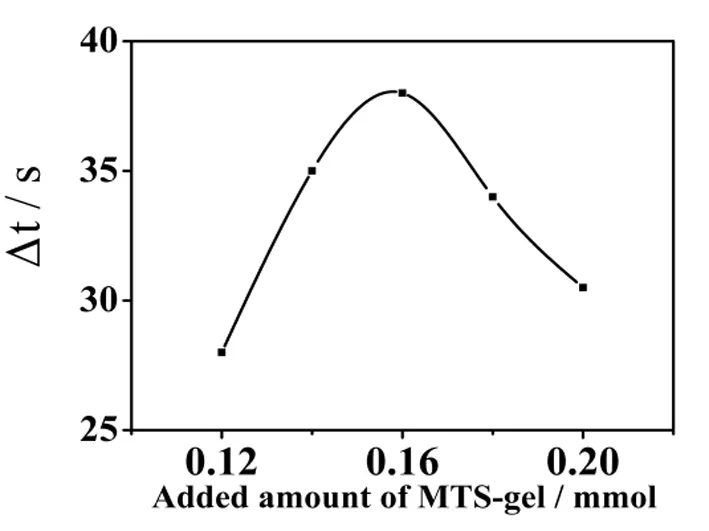
图3 MTS-gel凝胶添加剂浓度对盐酸金刚烷胺和肌氨酸衍生物电泳峰分离程度的影响Fig.3 Effect of the additive dosage of MTS-gel on the separating degree of electrophoretic peaks of AH and Sar derivatives
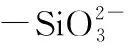
2.4 测定盐酸金刚烷胺的工作曲线
以一系列不同浓度的盐酸金刚烷胺并各加入25.0 μmol/L的肌氨酸内标物的混合标准溶液为测试液进行柱前衍生CE-ECL分析并纪录其电泳图。数据结果如图4(a)和图4(b)所示:由两种衍生产物的电泳峰所得到的峰面积比AAH/ASar与盐酸金刚烷胺的初始浓度在10~250 μmol/L和400~750 μmol/L之间有良好的线性关系,线性回归方程分别为AAH/ASar=-0.1509 + 0.0942 CAH(μmol/L)(R2=0.9995)和AAH/ASar=-30.1729 + 0.1133 CAH(μmol/L)(R2=0.9991),经计算得出的检测限为2.4 μmol/L(S/N=3)。此外,以含100 μmol/L盐酸金刚烷胺+25.0 μmol/L肌氨酸的混合衍生样平行进样测定6次,经统计得到盐酸金刚烷胺和肌氨酸峰面积度值的标准偏差分别小于3.8%和2.1%,而相应电泳峰迁移时间的平均标准偏差值分别为3.1%和2.6%,表明本法的测定精密度良好。
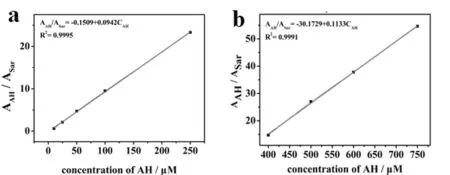
图4 盐酸金刚烷胺原始浓度和盐酸金刚烷胺衍生物与肌氨酸衍生物峰面积比值之间的定量关系Fig.4 Quantitative relationship curve between the ratio value of AAH/ASar and original concentration of AH
2.5 实际样品测定
在最优条件下,采用内标法对市购的几种成人及小儿感冒药中的盐酸金刚烷胺含量进行了定量测定,样品的测定值、加标量和加标回收率结果如表1所示,由实样回收率值表明本法的准确度尚令人满意。通过与所测药品金刚烷胺药剂标识含量的对比可知,这几种市售的感冒药中盐酸金刚烷胺含量均在标识值的91%~95% 范围内,符合国家药品标准工作手册及《中国药典》中对药品中盐酸金刚烷胺含量的限度要求[27]。
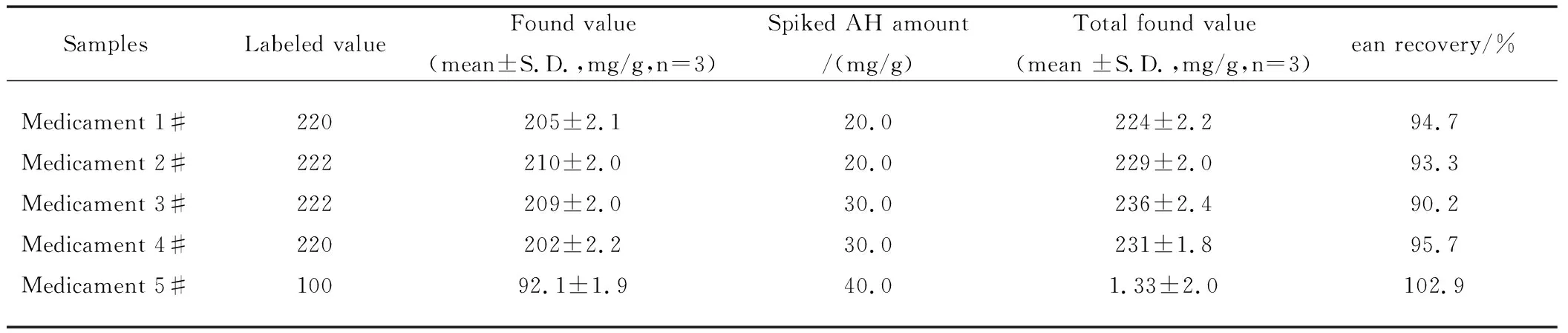
表1 几种实际样品中盐酸金刚烷胺含量的测定结果Table 1 Determination results of amantadine hydrochloride content in the several real samples
3 结论
本文选用单壁羟基碳纳米管/壳聚糖修饰的毛细管柱,以MTS-gel为主要分离添加剂分析测定了几种药品中的金刚烷胺含量,成功建立了柱前衍生毛细管电泳-电致化学发光法测定药品试样中盐酸金刚烷胺含量的一种分析方法。此外,实验中使用的单壁羟基碳纳米管/壳聚糖修饰的毛细管能提高分析结果的重现性,还证明了新合成的MTS-gel凝胶可作为电泳分离添加剂用于定量分析。该方法准确、快速,分析成本低,可完全适用于不同种类药品中盐酸金刚烷胺含量的检测。
