CuNi纳米晶的可控合成及Pt/CuNi催化剂催化肉桂醛加氢性能
2020-06-09张欢阮露娜裴安艾文斌吴锋顺熊晚枫朱丽华
张欢,阮露娜,裴安,艾文斌,吴锋顺,熊晚枫,朱丽华
(江西理工大学材料冶金化学学部化学化工学院,江西赣州341000)
在多相催化反应中,催化剂的形貌及表面缺陷位对催化剂性能有重要影响,如具有花状或海胆状形貌的负载型纳米催化剂具有丰富的缺陷位,可有效地提高催化剂性能[1-5]。在非贵金属催化剂中,镍、铜等金属催化剂因其价格低廉受到研究者们的广泛关注,而催化剂的表面形貌、电子结构和金属间的相互作用对催化剂性能有重要影响[6-13]。由于CuNi双金属催化剂存在金属间的协同作用,因此,与Cu或Ni单金属纳米催化剂相比,CuNi双金属纳米催化剂具有更高的催化活性[14-15],CuNi双金属纳米催化剂在许多重要的化工反应中得到广泛应用[16-18],如CO 加氢制甲醇[19]、乙醇水蒸气的重整[20]、甲烷部分氧化[21]以及不饱和醛的加氢反应[22-23]。因Cu 纳米颗粒相比于Ni 纳米颗粒在空气中更易被氧化,于是研究者们开始合成CuNi 双金属纳米颗粒以防止Cu被氧化,并用于催化反应中。如Wu 等[24]以聚乙烯吡咯烷酮(PVP)为表面活性剂及苯胺为还原剂,采用溶剂热法制备了六方纳米片和纳米线等不同形貌的Cu-Ni双金属纳米晶,其中,在邻二甲苯催化燃烧生成CO2和H2O 的反应中,Cu-Ni双金属纳米线的T90(邻二甲苯的转化率达到90%的温度)低于常规形貌的催化剂,展现出优异的催化活性。此外,人们还采用不同的制备方法合成了不同形貌的CuNi 双金属催化剂纳米颗粒,如海绵状[25]、球形[26]和片状[17]。本文通过改变水热合成中添加的表面活性剂种类及合成温度来控制CuNi 纳米晶的形貌,并以肉桂醛加氢为模型反应研究Pt/CuNi纳米催化剂的催化性能[27-32]。
1 实验部分
1.1 CuNi二元金属纳米晶的合成
采用水热法制备CuNi二元金属纳米晶;首先,称 取 一 定 量 的NiCl2·6H2O 和Cu(NO3)2·3H2O 溶 于30mL 去离子水中形成混合溶液,搅拌30min,然后称取1.8130g NaOH 溶解于5mL 去离子水配制成NaOH 溶液,并加入至上述溶液中,磁力搅拌10min,向上述液体中加入一定量的表面活性剂[0.2000g 聚乙烯吡咯烷酮(PVP)、0.2000g 十六烷基三甲基溴化铵(CTAB) 或2mL 乙二胺(EDA)],10min 后将混合物转移至100mL 聚四氟乙烯内衬中,缓慢滴加2mL 85%的水合肼溶液,整个合成过程都在剧烈搅拌下进行。将水热反应釜安装好,并使其在设定温度下(60℃、90℃、120℃、150℃、180℃)保持2h。最后将混合物进行离心、洗涤,再将得到的黑色固体在真空干燥箱中60℃烘干6h。研磨,称重,得到粉末,记作CuNi-T-S[T为水热合成温度,分别为60℃、90℃、120℃、150℃、180℃;S为合成过程中加入的表面活性剂,分别为No(未加入)、EDA、PVP、CTAB]。
Pt/CuNi 催化剂的合成:将一定量的H2PtCl2·6H2O (AR) 溶 解 于200mL 去 离 子 水 中,再 将0.3000g已制备好的CuNi 二元金属纳米晶加入上述溶液,连续搅拌6h使得CuNi 粉末在溶液中高度分散;过滤,同时用去离子水和无水乙醇洗涤数次。再将获得的黑色固体置于真空干燥烘箱60℃保持6h,得到Pt/CuNi样品,记作:Pt/CuNi-T-S[T为水热合成温度,T=60℃、90℃、120℃、150℃、180℃;S为水热合成过程所加入的表面活性剂,S=No(未加入)、EDA、PVP、CTAB]。
1.2 催化剂分析测试方法及仪器
测试前将待测样品装入带有凹槽的载玻片上,并用平整的玻璃片将样品压平整;利用Rigaku Ultima IV X射线衍射仪(XRD)进行物相分析。以Cu Kα为X射线源,λ=0.15406nm,工作电压为40kV、电流为30mA;2θ扫描范围为10°~90°。
首先将粉末加入到乙醇溶剂中超声15min,然后用滴管滴到硅片上,室温下晾干后,利用扫描电镜(SEM,MLA650F 型)进行测试。加速电压100V~30kV,放大倍数20~900000 倍;探测电流4pA~10nA。进行形貌分析时,扫描电镜(MLA650F型)附带X 射线能谱(EDS),对样品进行SEMEDS测试。
为了检测催化剂表面各元素化学价态及其相对含量,对催化剂进行X射线光电子能谱(XPS)表征。用配备单色Al Kα(hv=1486.6eV)X 射线源的PHI-Quantum 2000 能谱仪对样品进行X 射线光电子能谱测试。
对Pt/CuNi 催化剂进行高角度环形暗场扫描透射(HAADF-STEM)和STEM-EDS 元素面扫分析;测试过程在Tecnai F30透射电镜上进行,测试中加速电压为300kV;将样品分散于乙醇溶液中,采用超声使其分散,再取数滴附于包覆碳膜的金栅上,待干燥后用于测试。
1.3 催化剂性能测试
在高压反应釜(Parr 4848)装置中对催化剂性能进行测试。首先将10mL 肉桂醛的乙醇溶液(0.4mL 肉桂醛溶于9.6mL 乙醇中)加入反应釜中,再加入0.5000g 催化剂并使其均匀分散在溶液中。安装好反应装置,用99.999% N2吹扫2min,排出反应器中的空气,再用99.999% H2净化2min,排尽N2及剩余的少量空气;在搅拌速率为500r/min下,H2初始压力为5.0MPa,设定程序使反应温度升至80℃并反应1h;反应完成后,待装置冷却至室温,过滤分离催化剂和反应液体,收集反应液作为气相色谱(GC)的待测样,产物定量定性分析采用气相色谱(Agilent GC 7820A)。
2 结果与讨论
2.1 物相组成和微观结构
2.1.1 催化剂的XRD表征
图1为60℃和90℃水热温度下,使用不同的表面活性剂制备的CuNi 二元金属纳米晶的XRD 图。由 图1 可 见,在CuNi 二 元 金 属 中,2θ=19.3°、33.1°、38.5°、59.1°与62.7°分别归属于Ni(OH)2(001)、Ni(OH)2(100)、Ni(OH)2(101)、Ni(OH)2(110)与Ni(OH)2(111)晶面的特征衍射峰(JCPDS card No.14-0117)[33-36]。其中,在90℃水热反应下,使用不同表面活性剂制备的CuNi 二元金属纳米晶的XRD图[图1(b)]比图1(a)(60℃)中各物相对应的衍射峰更尖锐。2θ=43.4°、50.6°和74.3°分别对应Cu(111)、Cu(200)与Cu(220)晶面的特征峰(JCPDS card No.65-9743)[37],2θ=44.3°、51.7°和76.1°分别归属于Ni(111)、Ni(200)与Ni(222)晶面的特征衍射峰(JCPDS card No.04-0850)。60℃时,EDA 作为表面活性剂时[图1(a)],Cu 对应的衍射峰较明显,但Ni的衍射峰几乎未出现,可能的原因主要如下:①Ni 可能是高度分散的纳米颗粒,且尺寸相对较小或为非晶态;②Ni2+与EDA之间存在较强的配位作用,阻碍了Ni2+的还原。以PVP作为表面活性剂合成的CuNi二元金属纳米晶,在2θ=35.5°、19.3°、38.5°、59.1°和62.7°处 分 别 呈 现 出CuO(002)、Ni(OH)2(001)、Ni(OH)2(101)、Ni(OH)2(110)和Ni(OH)2(111)的衍射峰(JCPDS card No. 48-1548 和14-0117)[38-39],原因可能是在PVP 表面活性剂的较强包裹作用下,使得CuO 和Ni(OH)2未被完全还原;在90℃,以PVP 作为表面活性剂合成的CuNi 二元金属纳米晶呈现出Ni(OH)2的强峰,且出现了fcc结构Ni 的衍射峰,表明高温有利于Ni 的还原。而Ni(111)、Ni(200)与Ni(220)晶面所对应的衍射峰[40-41],其强度相较于CTAB、EDA作为表面活性剂时强度较小[图1(b)],说明在PVP 体系中Ni 可能高度分散于Ni(OH)2纳米颗粒中,且尺寸相对较小。在CTAB与EDA体系中(90℃),未见有明显的CuO与Ni(OH)2物相的衍射峰出现,形成了尖锐的Cu(111)、Cu(200)、Cu(220)、Ni(111)、Ni(200)与Ni(220)特征衍射峰[42]。从以上结果可知,Cu2+相比Ni2+更容易被还原,且PVP 的存在会阻碍Ni2+的还原,CTAB 与EDA存在不会阻止Ni2+的还原。此外,在所有样品的XRD 图中,未见明显Cu 氧化态晶相的衍射峰,可能的原因是在低温水热合成时,因Cu2+较Ni2+更易被还原,Cu2+先被还原生成Cu,Ni2+后被还原生成Ni将Cu包覆,二者形成了Cu@Ni核壳结构,阻止了Cu进一步被氧化。

图1 不同水热合成温度合成的CuNi二元金属样品的XRD图
图2分别是在120℃和150℃水热反应下,使用不同的表面活性剂制备的CuNi 二元金属纳米晶的XRD 图。从图中可知,以PVP 为表面活性剂时,120℃水热温度下制备的CuNi 二元金属纳米晶的XRD 图中,2θ=19.3°、33.1°、38.5°、59.1°与62.7°分别归属于Ni(OH)2(001)、Ni(OH)2(100)、Ni(OH)2(101)、Ni(OH)2(110)与Ni(OH)2(111)晶面的特征衍射峰(JCPDS card No.14-0117)[43]。以PVP为表面活性剂时,150℃水热温度下合成的CuNi二元金属纳米晶的XRD 图中还出现了CuO(002)晶面的衍射峰(2θ=35.5°;JCPDS card No.48-1548),说明以PVP为表面活性剂制备的CuNi 二元金属纳米晶中Ni(OH)2未被完全还原;以CTAB为表面活性剂制备的CuNi二元金属纳米晶的XRD图中CuO和Ni(OH)2衍射峰不太明显。而以EDA 作为表面活性剂的体系中,未见有明显的Ni(OH)2和CuO 出现,形成了明显的Cu(111)、Ni(111)、Cu(200)、Ni(200)特征衍射峰,可能CuNi 二元金属纳米晶形成了Cu@Ni 核壳结构,阻止先被还原生成的Cu被氧化。
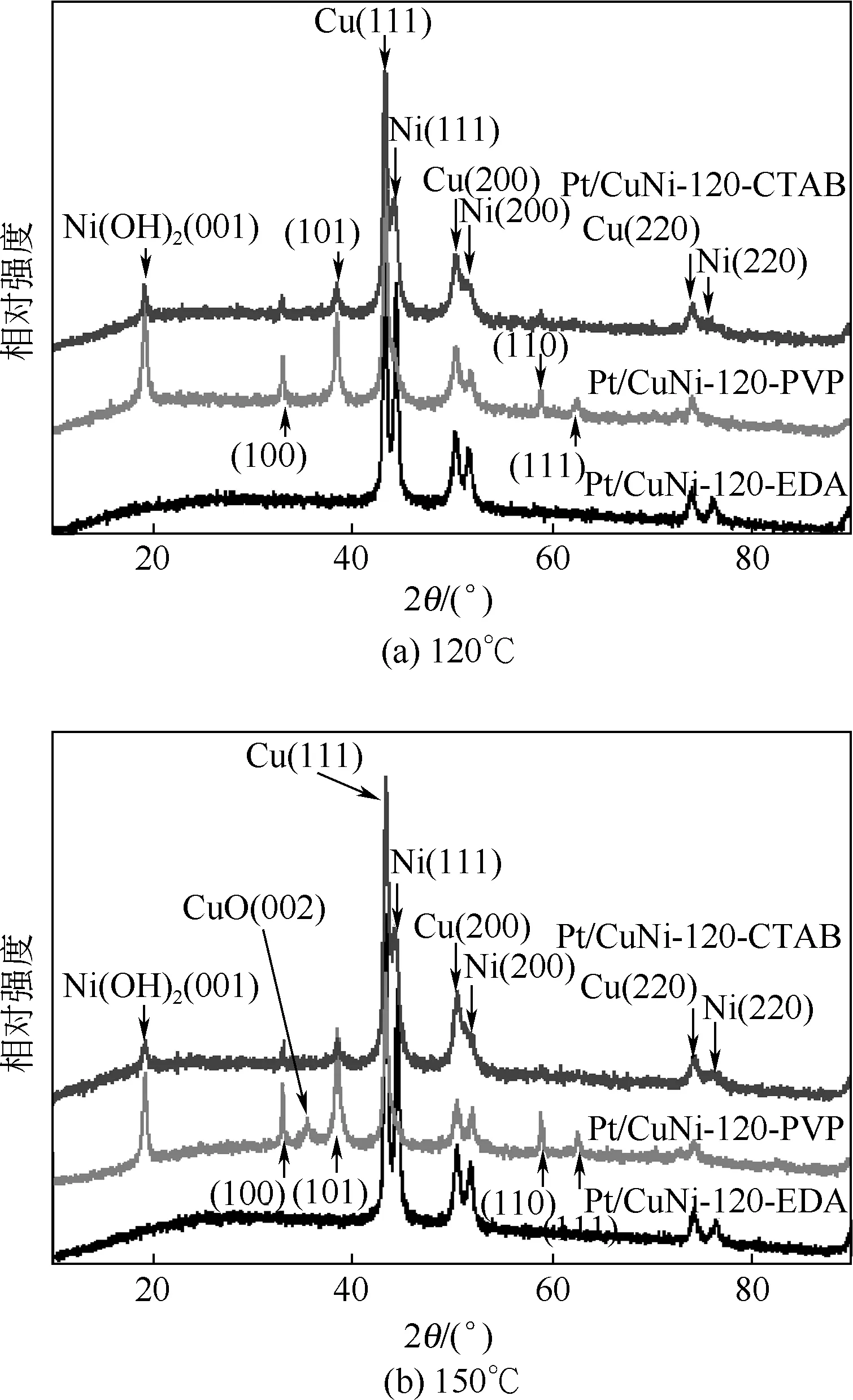
图2 不同温度合成的CuNi纳米晶的XRD图
图3(a)中的衍射峰情况与图1与图2基本一致,但其中以PVP 为表面活性剂制备的CuNi 二元金属纳米晶的XRD 图中CuO 和Ni(OH)2衍射峰强度相较于其他温度下制备的明显更低。图3(b)是不加表面活性剂时,分别在不同的水热温度下制备的CuNi二元金属纳米晶的XRD 图,在60℃与90℃下未见有明显的Ni(OH)2晶面的衍射峰出现,在2θ=43.4°、50.6°、74.3°、44.5°、51.8°和76.4°处出现了尖锐的Cu(111)、Cu(200)、Cu(220)、Ni(111)、Ni(200)和Ni(220)特征衍射峰(JCPDS card No. 65-9743 和04-0850)[44]。随着温度升高(120℃、150℃与180℃),有CuO(002)、CuO(111)衍射峰出现,并在150℃时达到最高值[图3(b)]。形成这一结果的原因主要是:随着温度的升高,加快了Ni2+与Cu2+还原反应的反应速率,加快了Cu与Ni的还原进程,已还原的Cu未被Ni完全包裹,致使部分Cu暴露在空气中被氧化,从而出现了CuO 衍射峰,且可能在150℃水热合成温度时,Ni 包裹Cu 的程度最差,导致更多的Cu原子暴露在晶体表面被氧化。
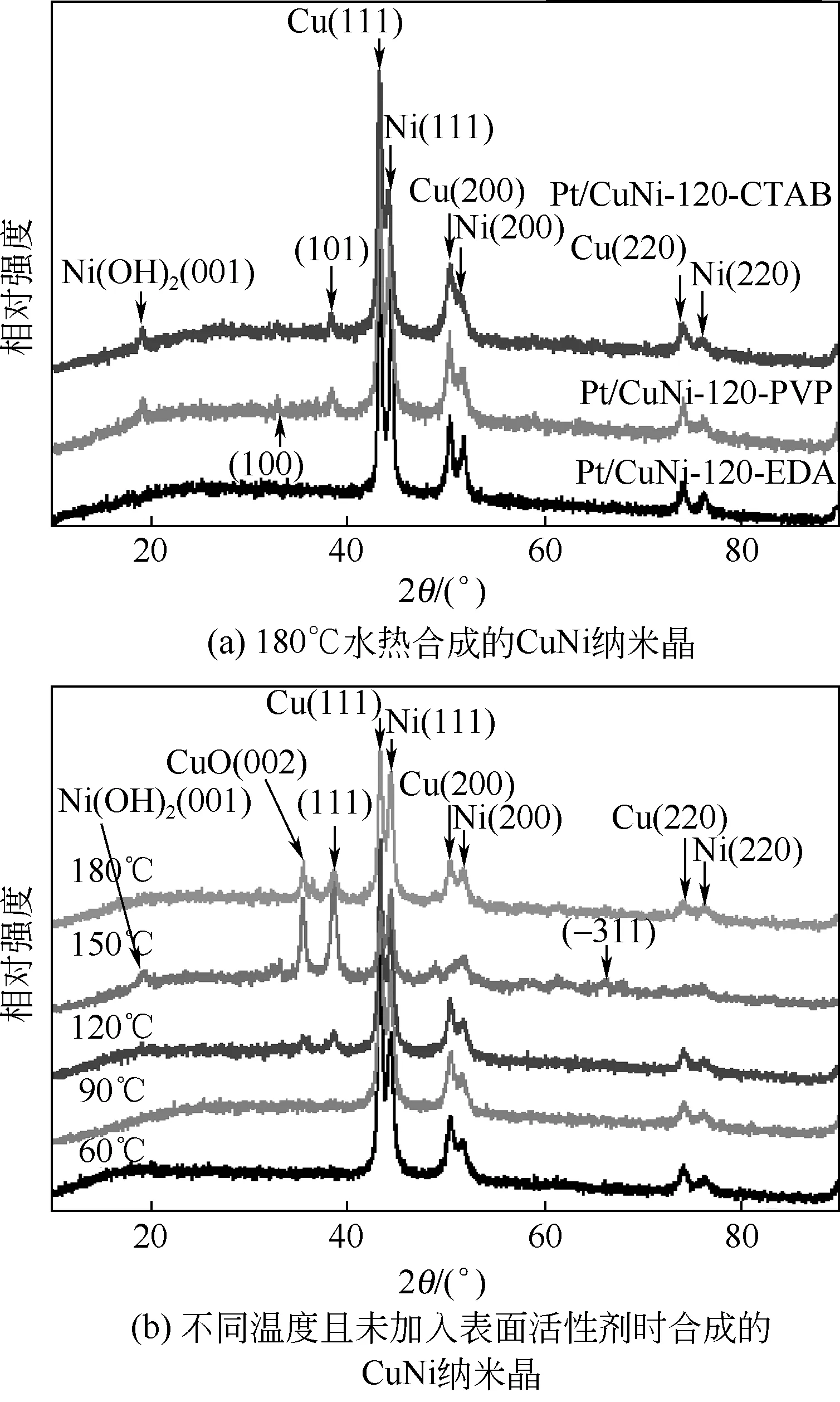
图3 不同合成条件下制备的CuNi纳米晶的XRD图
图4为Pt/CuNi-120-S催化剂的XRD图。在Pt/CuNi-120-PVP 与Pt/CuNi-120-CTAB 催 化 剂 的XRD 图中,在2θ=19.3°、59.1°与62.7°处出现较强的Ni(OH)2(001)、Ni(OH)2(110)与Ni(OH)2(111)晶面的特征衍射峰(JCPDS card No. 14-0117),Cu(OH)2(020)晶面的衍射峰仅出现在Pt/CuNi-120-PVP 的XRD 图中。在所有样品的XRD 图中,2θ=43.4°、50.6°、74.3°、44.5°、51.8°和76.4°分别对应的Cu(111)、Cu(200)、Cu(220)、Ni(111)、Ni(200)和Ni(220)晶面(JCPDS card No. 65-9743 和04-0850),且衍射峰较明显。更重要的是所有Pt/CuNi 催化剂的XRD 图中,未发现任何属于Pt 物种相关的衍射峰,表明催化剂中Pt 很可能主要以纳米团簇或单原子的形式高度分散于CuNi 双金属纳米晶上。对于Pt/CuNi-120-PVP 催化剂,同时存在Cu(OH)2、Ni(OH)2、Ni 与Cu 物相,这可能是造成Pt/CuNi-120-PVP催化剂催化肉桂醛加氢反应中对苯丙醇产率较低(30.7%)的原因之一。

图4 Pt/CuNi-120-EDA、Pt/CuNi-120-PVP、Pt/CuNi-120-CTAB和Pt/CuNi-120-No的XRD谱图
2.1.2 催化剂的XPS表征
图5 为Pt/CuNi-120-S 催化剂的Ni 2p XPS 能谱图。从图中可知,结合能位于857.1eV、855.4eV、853.9eV 及852.7eV 的峰,分别对应于催化剂表面的NiOOH、Ni(OH)2、NiO及Ni(0)物种[45]。此外,Ni(0)物种对应的峰面积明显小于Ni 氧化态物种[NiOOH、Ni(OH)2、NiO]相应的峰面积,表明催化剂表面Ni 物种主要以氧化态形式存在。原因可能是催化剂表面的Ni 原子与空气中的氧气和水发生反应导致的。其中,Pt/CuNi-120-PVP 催化剂表面中NiO(853.9eV)所对应的峰面积远小于其他3种Pt/CuNi-120-S催化剂,且其表面Ni(OH)2物种的比例最高,可能是在CuNi 晶体制备过程中较多的Ni(OH)2未被还原成Ni(0),使得催化剂表面主要以Ni(OH)2物种为主。

图5 Pt/CuNi-120-S催化剂的Ni 2p XPS能谱图
图6为Pt/CuNi-120-S催化剂的Cu 2p XPS能谱图。从图中可知,结合能位于933.6eV 与932.6eV的衍射峰分别归属于催化剂表面的CuO 与Cu(0)物种[46]。对于Pt/CuNi-120-EDA与Pt/CuNi-120-CTAB催化剂,CuNi 纳米晶合成过程中Cu2+与Ni2+还原较完全,且XRD 表征结果说明可能已形成Cu@Ni 核壳结构,对样品中的Cu 起到一定的保护作用,使其不易被空气氧化。因此,催化剂表面上Cu 的氧化态的含量相比于Pt/CuNi-120-No 与Pt/CuNi-120-PVP催化剂较低。
图7 为Pt/CuNi-120-S 催化剂的Pt 4f XPS 能谱图。结合能为73.5eV、72.4eV 及71.5eV 分别对应于催化剂表面的Pt4+、Pt2+与Pt(0)物种[47],从各物种对应的峰面积之比,可发现Pt/CuNi-120-No[图7(a)]和Pt/CuNi-120-CTAB[图7(d)]催化剂表面Pt(0)所占比例低于Pt/CuNi-120-EDA[图7(b)]和Pt/CuNi-120-PVP[图7(c)]催化剂,且Pt/CuNi-120-PVP催化剂表面Pt2+的含量较高。
2.1.3 CuNi样品的SEM及SEM-EDS表征
图8 为采用不同表面活性剂在90℃下合成的CuNi 晶体的SEM 图。从图中可知,以EDA 为表面活性剂时,CuNi 主要为不规则形状。而采用PVP或CTAB 为表面活性剂时,晶体的形貌均为类球形,颗粒分散均匀,粒径较小。以CTAB为表面活性剂制备的CuNi二元金属粒径最小,小于200nm。在CuNi-90-EDA的SEM-EDS能谱图中,可得各元素的含量,Ni元素的含量为Cu元素含量的1/2,原因是部分Ni(OH)2未被还原,使得Ni在CuNi中的量较少,这与其XRD的表征结果相符。
图9 为采用不同表面活性剂在120℃下合成的CuNi 晶体的SEM 图。由图可见,其中CuNi-120-EDA 整体为类球状,且表面有毛刺状的花瓣(类似于花状结构)[图9(a)],可以增大催化剂的比表面积,从而增加与反应物接触的活性位点,提高催化性能。以EDA 为表面活性剂制备的CuNi 晶体粒径相对较大,在同一温度下以CTAB 为表面活性剂时制备的CuNi 晶体粒径最小,约100nm[图9(c)]。从CuNi-120-EDA的SEM-EDS能谱图[图9(d)]可知,氧元素的质量分数仅为1.42%,且Cu 与Ni含量相当,说明该催化剂中含有Cu、Ni 的氧化物和氢氧化物较少,Cu2+、Ni2+被水合肼还原较为完全。

图6 Pt/CuNi-120-S催化剂的Cu 2p XPS能谱图
图10是采用不同表面活性剂在150℃下合成的CuNi 晶体的SEM 图。由图可见,CuNi-150-EDA晶体呈现明显的海胆状[图10(a)],比表面积增大,使得其表面暴露更多缺陷位和配位不饱和的Ni 原子,有利于提高催化剂的催化性能。以PVP 和CTAB作为表面活性剂制备的CuNi晶体形貌呈现均匀的球状,且粒径较小,高度分散[图10(b)和(c)]。结合图10(d)中的SEM-EDS结果,以EDA作为表面活性剂制备的CuNi 二元金属中含氧量较其他温度下稍高,且Cu与Ni含量接近,结合其XRD分析结果,初步推断形成了以Cu为核,Ni包覆于Cu表面的二元金属核壳结构(Cu@Ni)。

图9 采用不同表面活性剂在120℃下合成的CuNi晶体的SEM图及SEM-EDS能谱图
图11是采用不同表面活性剂在180℃下合成的CuNi 晶体的SEM 图。由图可见,其中以EDA 为表面活性剂时,CuNi双金属纳米晶形貌主要为柱状,PVP及CTAB表面活性剂参与制备的CuNi晶体都呈现规则的球状,且以PVP和CTAB为表面活性剂制备的CuNi 晶体的纳米颗粒粒径更小,原因是合成过程中,PVP 和CTAB 可以起到更好的保护作用,使得纳米颗粒不易长大。结合CuNi-180-EDA双金属纳米晶的SEM-EDS能谱图可知,180℃时,CuNi晶体的海胆形貌消失,说明随着温度的不断上升,晶体颗粒表面的针状Ni 金属发生了团聚,形成了较大尺寸的柱状结构,高温不利于形成具有更多缺陷位的花状和海胆状CuNi双金属纳米晶。

图10 采用不同表面活性剂在150℃下合成的CuNi晶体的SEM图及SEM-EDS能谱图

图11 采用不同表面活性剂在180℃下合成的CuNi晶体的SEM图及SEM-EDS能谱图
2.1.4 Pt/CuNi催化剂的SEM和SEM-EDS表征
图12 为Pt/CuNi-120-EDA 催化剂的SEM 图及SEM-EDS 能谱图。从图中可知,Pt/CuNi-120-EDA 与CuNi-120-EDA 的形貌和结构类似(花状的),此种结构增大了其比表面积,提高了催化剂表面的活性位点数目,有利于促进其催化加氢反应,表明Pt的负载基本未影响CuNi-120-EDA的形貌和纳米结构。根据CuNi-120-EDA 的SEM-EDS能谱图可知,Pt元素的实际负载量为2.41%。

图12 Pt/CuNi-120-EDA催化剂的SEM及SEM-EDS能谱图
2.1.5 催化剂的HAADF-STEM和STEM-EDS表征图13、图14 为Pt/CuNi-120-EDA 催 化 剂 的HAADF-STEM 图和STEM-EDS 元素面扫结果。从各元素的面扫结果图可知,纳米颗粒中同时存在Pt、Cu、Ni元素且高度均匀分布。此外,Pt元素的分布区域明显小于Cu与Ni元素的分布区域。进一步说明成功合成了CuNi 双金属纳米晶,且Pt 原子通过化学置换法成功负载于CuNi 双金属纳米晶表面,形成了Pt-on-CuNi 纳米结构。Pt 与CuNi 之间的协同作用有利于提高Pt/CuNi 催化剂的催化加氢性能。

图13 Pt/CuNi-120-EDA催化剂的HAADF-STEM图
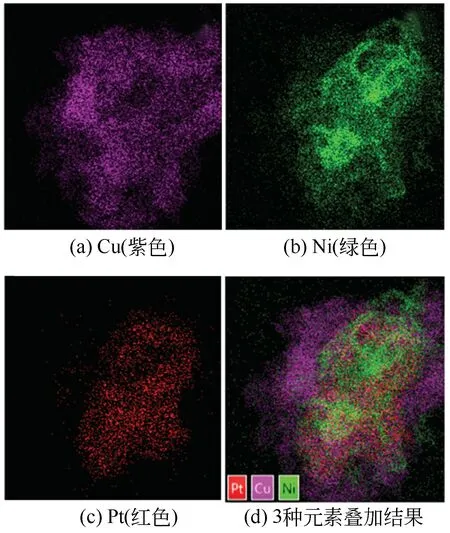
图14 Pt/CuNi-120-EDA催化剂的STEM-EDS图
2.2 各催化剂催化肉桂醛加氢性能的比较
通过对比表1 中Pt/CuNi-120-S 催化剂催化肉桂醛选择性加氢结果(包括肉桂醛的转化率及苯丙醛、肉桂醇与苯丙醇的产率)可知,各催化剂对肉桂醛的转化率几乎相同,原因是反应时间较长及反应温度较高(80℃),使得所有反应物均被加氢,苯丙醇产率大小顺序为Pt/CuNi-120-EDA>Pt/CuNi-120-CTAB>Pt/CuNi-120-No>Pt/CuNi-120-PVP,原因是EDA 和CTAB 表面活性剂阻止了CuNi 晶体进一步团聚,PVP 表面活性剂的作用不明显。Pt/CuNi-120-EDA催化剂形貌为花状,且尺寸相对较小,使得催化剂表面具有更多的活性位点、缺陷位和配位不饱和的金属原子;Pt/CuNi-120-EDA催化剂活性较高,温度较高(80℃)时更有利于肉桂醛的深度加氢,使得产物苯丙醇的产率高达100%。对Pt/CuNi-120-EDA催化剂进行稳定性测试,发现其催化肉桂醛加氢的反应性能基本不变,对产物苯丙醇的产率仍为100%,说明该催化剂的稳定性非常好。

表1 Pt/CuNi-120-S催化剂催化肉桂醛选择性加氢性能①
3 结论
采用水热法(以水合肼为还原剂)合成了CuNi 双金属纳米晶体,探究了不同水热合成温度和表面活性剂对CuNi 形貌和结构的影响规律,发现合适的温度(120℃或150℃)及EDA 有利于形成表面缺陷位及不饱和配位原子数量较多的花状或海胆状Cu@Ni 双金属纳米晶。通过化学置换法进一步合成了Pt/CuNi-120-S 三元金属纳米催化剂,评价了Pt/CuNi-120-S 催化剂催化肉桂醛选择性加氢性能,研究表明Pt/CuNi-120-EDA催化剂具有最高的苯丙醇收率(100%),原因是具有Pt-on-CuNi纳米结构的Pt/CuNi-120-EDA催化剂中含有较多的表面缺陷位及配位不饱和的原子,Pt 与Cu@Ni 之间存在协同作用,且Pt/CuNi-120-EDA催化剂具有很好的稳定性,有着重要的工业化应用价值。
