低浓度阿托品联合角膜塑形镜矫治近视的临床观察
2020-06-08唐文婷李世贝
唐文婷,田 美,李世贝,喻 谦
0引言
近视作为最常见的屈光不正类型,其患病率呈现逐年上升的趋势,按照目前的进展趋势到2050年全球将有50%(50亿)左右的人群被近视困扰[1]。这在东亚地区更为突出,目前已有约80%~90%的人患有近视[2]。青少年为近视的高发人群,目前尚无有效治愈近视的方法。有研究认为低浓度阿托品(0.01%)滴眼液能够有效控制青少年近视进展[3-5],虽然在中国台湾及新加坡已经上市并应用于临床,但在我国尚缺乏足量的、长期的安全性及有效性研究观察,并未正式进入临床应用。角膜塑形镜因良好的控制低中度近视进展的效果[6]、低风险、可逆性等优势成为研究的热点,并已在临床中广泛应用。本文探讨两者联合使用矫治近视的有效性及安全性。
1对象和方法
1.1对象前瞻性随机对照试验。选取2016-05/2018-08我院眼科门诊收治的青少年近视患者126例126眼(均取右眼数据进行研究),年龄8~14(平均11.05±2.13)岁,其中女66例(52.4%),男60例(47.6%)。入选标准:(1)近3mo内未采取任何相关治疗方法的患者;(2)全身情况正常,无器质性眼疾;(3)双眼矫正视力均≥1.0,近视力正常,调节能力正常;(4)屈光度检查:球镜度-1.00~-6.00D,顺规散光≤1.5D,逆规散光≤-0.75DC,且球镜度数/柱镜度数>2,无屈光参差;(5)角膜曲率K1值40~45D,角膜e值>0.2;(6)瞳孔大小正常(2.5~4mm),暗室环境下不能过小(<4mm)或过大(>光学区);(7)依从性好,能按时治疗及随访。排除标准:(1)患有眼部或全身疾病不适宜配戴角膜塑形镜或滴用阿托品滴眼液者;(2)患有全身疾病需长期用药(如激素、阿托品、非甾体类抗炎药等)或观察期内需使用影响近视度数变化的治疗方案;(3)近视力不佳,调节能力异常者;(4)近3mo内配戴过角膜接触镜或应用其他相关治疗措施的患者;(5)个人卫生习惯不良,依从性差,不能配合检查、按时治疗及定时来院复查者;(6)相关药物过敏的患者。所有患者配戴角膜塑形镜后1mo采取双盲及随机的原则将患者编号并分为试验组(63例63眼,每晚联合应用0.01%阿托品滴眼液1次)和对照组(63例63眼,每晚联合应用聚乙二醇滴眼液1次)。本研究经成都医学院第一附属医院医学伦理委员会审批通过,自制药品由成都医学院第一附属医院制剂科配制,符合药品制剂管理规定。治疗前向所有患者及其监护人讲解可能出现的并发症,并签署知情同意书。
1.2方法
1.2.1治疗方法入选对象均配戴角膜塑形镜,材料为Boston XO(氟硅丙烯酸酯),内表面反几何四弧设计,试戴及复查均达到理想适配,患者均在每日夜间至少戴镜8h,随访期间若有镜片破损或镜片划痕较重的情况则及时更换镜片。戴镜1mo后,每晚配戴角膜塑形镜前30min,试验组患者联合应用低浓度(0.01%)阿托品滴眼液(1mL∶0.5mg硫酸阿托品与聚乙二醇滴眼液按比例稀释配制,严格按照无菌操作要求在制剂室生物安全柜进行操作)1次;对照组患者联合应用聚乙二醇滴眼液1次。向患者及家属强调使用滴眼液的重要性,并建立微信群及QQ群按时提醒,每月漏点次数不能大于5次。每次点眼后闭眼按压泪囊部5min。滴眼液均遮盖药品标签进行编号,试验统计分析结束后明确各组所用药品。
1.2.2观察指标所有患者均完善眼科相关检查,排除治疗禁忌证。嘱患者每3mo到院复查,观察眼轴(AL)、等效球镜度(SE)、最佳矫正近视力(BCNVA)、瞳孔直径(PD)、调节幅度(AMP)、泪膜破裂时间(BUT)、眼压(IOP)的改变情况,其中联合治疗1a后等效球镜度的检测需在停止治疗3wk后进行。检查时间统一为8∶00~10∶00am。检查者均为同一名资深眼科主治医师,并经过严格培训及考核,检查时对其设盲。(1)眼轴:不散瞳情况下用IOL Master光学生物测量仪检查,至少连续测量5次,取平均值。(2)等效球镜度(SE=S+1/2C):客观验光和主观验光结合检查。前者在室内光线下散瞳前后(初诊及联合治疗1a后需散瞳)应用全自动电脑验光仪,测量3次,取平均值,并在充分散瞳后暗室中同时使用点、带状检影镜检影验光3次,取平均值。室内光线下小瞳下使用综合验光仪进行主观验光。记录验光结果,初诊时依据此结果让患者试戴角膜塑形镜30~60min,得到初诊最终验光结果。复查时可用自动验光仪快速了解屈光状态及角膜曲率变化,均测量3次,取平均值,如误差或增长大于0.5D则进行检影验光及综合验光。(3)最佳矫正近视力:应用标准近视力表检查单眼近视力,检查距离为33cm,自然光或人工照明均可,结果转换为LogMAR视力进行统计分析。(4)瞳孔直径:双眼完全放松(不戴镜),室内适应5min后,用AR-1自动电脑验光仪检查,设置受检眼平面的光照度为300~310Lx,单眼检查,测量3次,取平均值。(5)调节幅度:采用移近法测量,单眼全矫状态下,注视近视力表最佳视力的上一行单个视标,视力表缓慢向受检者移近(2cm/s),直至视标持续模糊,视力表与被检眼距离的倒数即为调节幅度,测量3次,取平均值。(6)眼压:采用非接触眼压计测量眼压,测量3次,取平均值。(7)泪膜破裂时间:荧光素钠试纸经生理盐水湿润后置于下睑结膜囊,裂隙灯钴蓝光下观察并记录泪膜破裂时间。

2结果
2.1基线资料以戴镜后1mo检查结果为基线水平(等效球镜度以戴镜前检测结果为基线水平),两组中不同程度近视患者基线资料比较,差异均无统计学意义(P>0.05),具有可比性,见表1。
2.2治疗情况本研究过程中,纳入患者均未出现中止或退出情况,未发生严重的眼前节并发症,1例患者出现镜片划痕较重,1例患者出现镜片丢失,均在1wk内予以更换。试验组中用药1wk后出现轻微眼痒、眼红者1眼(1.6%),未予特殊处理,密切随访3d后症状消失;早期主诉有户外畏强光症状者7眼(11.1%),随着治疗时间的延长(4wk后),症状逐渐消失;主诉重影或眩光者4眼(6.3%);无视近模糊和室内畏光症状。
2.3治疗后眼轴变化情况联合治疗6mo,试验组和对照组低度近视患者眼轴分别增长0.07±0.06、0.11±0.07mm,中度近视患者眼轴分别增长0.05±0.04、0.09±0.07mm。联合治疗1a,两组患者眼轴均有所增加,但试验组患者眼轴较对照组增加较少,试验组和对照组低度近视患者眼轴分别增长0.13±0.03、0.22±0.05mm,中度近视患者眼轴分别增长0.12±0.03、0.20±0.05mm,两组之间比较差异均有统计学意义(t=6.983、8.940,均P<0.001)。随访期间,两组患者眼轴变化趋势见图1。
表1 不同程度近视患者基线资料的比较

近视程度组别眼数男/女(例)AL(x±s,mm)SE(x±s,D)BCNVA(x±s,LogMAR)PD(x±s,mm)AMP(x±s,D)BUT(x±s,s)IOP(x±s,mmHg)低度近视试验组208/1223.72±0.31-2.56±1.150.03±0.026.13±0.6213.02±2.3111.17±0.9413.22±1.48对照组2211/1123.70±0.29-2.59±1.120.03±0.016.15±0.5812.98±2.2411.14±1.0313.20±1.78 t/χ20.4230.2160.0860.710-0.1080.0570.0980.039P0.5160.8300.9320.4820.9150.9550.9220.969中度近视试验组4320/2324.69±0.34-4.90±1.160.04±0.016.16±0.6712.93±2.1611.10±1.0513.21±1.59对照组4121/2024.71±0.37-4.92±1.210.04±0.016.19±0.5612.91±2.3311.12±1.1713.20±1.80 t/χ20.186-0.2580.0771.009-0.2220.041-0.0830.027P0.6660.7970.9390.3160.8250.9680.9340.979
注:低度近视:-1.00D≤球镜度数≤-2.75D;中度近视:-3.00D≤球镜度数≤-6.00D。试验组:每晚联合应用0.01%阿托品滴眼液1次;对照组:每晚联合应用聚乙二醇滴眼液1次。
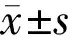

近视程度组别眼数BCNVA(LogMAR)PD(mm)AMP(D)BUT(s)IOP(mmHg)低度近视试验组200.04±0.026.88±0.5611.44±1.5911.07±1.0213.31±1.61对照组220.04±0.016.19±0.5412.79±1.9011.15±1.0313.28±1.58t0.4324.064-2.483-0.4380.106P0.668<0.0010.0170.6620.916中度近视试验组430.05±0.026.90±0.5111.41±1.5711.06±0.9413.20±1.61对照组410.04±0.026.23±0.5512.75±1.9311.08±1.0113.18±1.58t1.3065.793-3.498-0.1150.070P0.195<0.001<0.0010.9090.944
注:低度近视:-1.00D≤球镜度数≤-2.75D;中度近视:-3.00D≤球镜度数≤-6.00D。试验组:每晚联合应用0.01%阿托品滴眼液1次;对照组:每晚联合应用聚乙二醇滴眼液1次。

图1 联合治疗前后两组患者眼轴变化趋势对比。
2.4治疗后等效球镜度变化情况联合治疗1a,停止治疗3wk检测发现,两组患者等效球镜度均有所增加,但试验组患者的等效球镜度较对照组增加较少,试验组和对照组低度近视患者等效球镜度分别增加0.16±0.07、0.21±0.08D,中度近视患者等效球镜度分别增加0.16±0.05、0.20±0.09D,两组之间比较差异均有统计学意义(t=-2.146,P=0.038;t=-2.534,P=0.013)。
2.5治疗后两组患者各观察指标的比较联合治疗1a后,两组患者最佳矫正近视力、泪膜破裂时间、眼压比较,差异均无统计学意义(P>0.05),但两组患者泪膜破裂时间均较基线水平有所降低;试验组患者瞳孔直径较对照组明显增大,调节幅度较对照组降低,差异均有统计学意义(P<0.05),见表2。此外,随访1a,试验组患者主诉眼干涩不适13眼(20.6%),对照组11眼(17.5%)。
3讨论
阿托品及角膜塑形镜控制近视进展的机制不尽相同,前者通过作用于巩膜上的毒蕈碱受体(主要抑制M1和M4亚型受体)影响巩膜重塑而延缓眼轴增长[7];后者使周边视网膜呈近视离焦状态,延缓眼轴增长。本研究评估将这两种最有效控制近视的方法联合使用是否能提高疗效(应用眼轴、等效球镜度指标评估),并观察其安全性(应用最佳矫正近视力、瞳孔直径、调节幅度、泪膜破裂时间、眼压指标评估)。
本研究发现,联合治疗1a,试验组低度近视患者等效球镜度增加了0.16±0.07D,对照组低度近视患者等效球镜度增加了0.21±0.08D,试验组中度近视患者等效球镜度增加了0.16±0.05D,对照组中度近视患者等效球镜度增加了0.20±0.09D,试验组与对照组比较均有统计学差异,这与Wan等[8]研究结果一致,但Tan等[9]研究认为球镜度数增加无差异,但该研究观察时间仅为1mo,还有待后续观察统计。此外,本研究中,联合治疗1a,试验组低度近视患者眼轴平均延长0.13mm,对照组低度近视患者眼轴平均延长0.22mm,延缓眼轴增长率为40.91%,试验组中度近视患者眼轴延长0.12mm,对照组中度近视患者眼轴延长0.20mm,延缓眼轴增长率为40.00%。Kinoshita等[10]研究1a发现,试验组(0.01%阿托品滴眼液联合角膜塑形镜)眼轴延长0.09mm,对照组(单纯角膜塑形镜治疗)眼轴延长0.19mm,延缓眼轴增长率为52.63%。石梦海等[11]研究1a发现,试验组(0.01%阿托品滴眼液联合角膜塑形镜)眼轴延长0.12mm,对照组(单纯角膜塑形镜治疗)眼轴延长0.22mm,延缓眼轴增长率为45.45%。故可以认为经过1a联合治疗的患者眼轴增长明显减缓,因此对于近视进展快速(目前普遍认为增长快速是每年球镜度数增长大于1.00D或者眼轴增长超过0.36mm)或单纯角膜塑形镜控制效果不佳的患者,可以在密切随访的前提下联合使用0.01%阿托品滴眼液。上述研究中联和疗法延缓眼轴增长率不完全相同,可能与研究对象的平均年龄及屈光度不同有关,今后的研究应在继续延长观察时间的同时,加大样本量,根据年龄及屈光度更为详细地分组分层,还可以将父母遗传、视觉习惯、户外活动时间等混杂因素考虑进实验设计。
随访1a期间,本研究纳入患者均无严重眼前节并发症,无视近模糊和室内畏光症状,眼红、眼痒、户外畏强光、眩光等不适发生率低,无需采取治疗措施,且随治疗时间延长症状消失,不影响正常学习及生活。联合治疗对患者的眼压无影响,会出现眼干不适,但较单纯使用角膜塑形镜的干眼程度并未加重,因此虽然角膜塑形镜会影响泪膜稳定性,但加用0.01%阿托品滴眼液并未加重干眼。联合治疗对瞳孔直径有轻度影响,较治疗前增大约0.75mm,调节幅度降低约1.55D,但因为保留了功能性调节能力,并不影响最佳矫正近视力。这与符爱存等[12]和Wan等[8]研究结果一致。但石迎辉等[13]研究认为,调节幅度不受影响,分析原因可能与该研究纳入的研究对象年龄[9~16(平均12.5±3.6)岁]、研究时间(6mo)以及调节幅度的测量方法(雾视法,本研究采用移近法,通常雾视法测量结果略低于移近法)等有关,也可能与瞳孔测定的光照度及检查的时间点不同有关。因本次研究尚未停止治疗4wk以上进行各观察指标的检测,未观察到停药较长时间之后有无近视反跳及调节能力、瞳孔直径是否有恢复,后续的研究会增加上述内容。
综上,低浓度阿托品滴眼液联合角膜塑形镜矫治青少年近视在短期内应用是安全有效的,在严格掌握适应证及专业人员熟练验配、严密随访的情况下,可以考虑在临床上先应用于近视进展较快或单纯角膜塑形镜控制效果不理想的患者。
