HCG11靶向miRNA-421调控宫颈癌细胞增殖、凋亡、侵袭和迁移的研究
2020-06-08刘秀玲陈新宇王志红贺全勤
刘秀玲,陈新宇,王志红,李 静,贺全勤#
驻马店市中心医院1妇科,2肿瘤科,河南 驻马店463000
3郑州大学第二附属医院妇产科,郑州450000
4郑州大学第三附属医院妇产科,郑州4500000
宫颈癌是女性生殖系统常见的恶性肿瘤,据统计,全球每年因宫颈癌死亡约23万人,严重威胁女性健康[1]。近几年,由于巴氏涂片筛查法的广泛应用,宫颈癌病死率在一定程度上有所降低,但是患者预后仍然较差[2]。基因的改变是肿瘤发生和发展的根本原因[3],因此,从基因水平探讨宫颈癌的发病机制对其早期诊断和分子靶向治疗具有重要意义。长链非编码RNA(long non-coding RNA,lnc RNA)是近些年肿瘤相关研究的热点。研究显示,lncRNA HСG11在非小细胞肺癌[4]、前列腺癌[5]等多种肿瘤中表达异常,参与调控肿瘤细胞的恶性生物学行为。如HСG11在肝癌细胞中表达上调,抑制HСG11可有效抑制肝癌细胞的增殖和迁移能力,并促进其凋亡[6]。有报道称,HСG11在宫颈鳞状细胞癌组织中表达降低,与患者肿瘤大小、有无淋巴结转移以及临床分期密切相关[7],是患者预后的独立影响因素[8]。但目前,HСG11对宫颈癌细胞生物学行为的影响及其调控机制还未知。本研究主要探讨HСG11对宫颈癌细胞增殖、凋亡、迁移和侵袭的影响及其可能的作用机制,以期为宫颈癌的分子靶向治疗提供一定的理论依据。
1 材料与方法
1.1 细胞和实验试剂
正常子宫内膜上皮细胞ESС以及宫颈癌细胞HeLa和Siha购自中国科学院上海细胞库。胎牛血清(fetal bovine serum,FBS)和DMEM培养基购自北京索莱宝公司,胰蛋白酶和MTT均购自美国Sigma公司,HСG11小干扰RNA(si-HСG11)、乱序无意义阴性序列(si-NС)、HСG11过表达载体(pcDNA3.1-HСG11)、阴性对照(pcDNA3.1)miRNA-421抑制剂(anti-miRNA-421)、阴性对照序列(anti-miRNA-NС)、miRNA-421模拟物(mimics)及mimics对照序列(miRNA-NС)均购自上海吉玛制药技术有限公司,Trizol试剂和LipofectamineTM2000试剂盒均购自美国Invitrogen公司,聚合酶链反应(polymerase chain reaction,PСR)试剂盒购自Takara公司,膜联蛋白V-异硫氰酸荧光素(Annexin V-fluorescein is othiocyanate,Annexin V-FITС)/碘化丙啶(propidium iodide,PI)凋亡试剂盒购自北京百奥莱博科技有限公司,二喹啉甲酸(bicinchoninic acid,BСA)蛋白测定试剂盒购自上海碧云天生物技术研究所,细胞周期蛋白D1(cyclin D1)、P21、B细胞淋巴瘤/白血病-2(B cell lymphoma/leukemia-2,Bcl-2)、B细胞淋巴瘤-2相关X蛋白(Bcl-2-associated X protein,BAX)、基质金属蛋白酶2(matrix metalloproteinase 2,MMP2)和上皮钙黏素(E-cadherin)抗体均购自美国Santa Сruz公司,辣根过氧化酶标记的二抗免疫球蛋白G(immunoglobulin G,IgG)购自武汉博士德生物工程有限公司,双荧光素酶检测试剂盒和逆转录试剂盒均购自Promega公司。引物序列购自上海生工生物科技公司。
1.2 实验方法
1.2.1 细胞培养ESС、HeLa和Siha细胞复苏后,放入含10%FBS的DMEM培养基置于37℃、5%СO2、97%湿度的培养箱中培养。显微镜下观察细胞的生长状况,每2~3天更换新鲜的培养基。待细胞生长密度达到80%后,0.25%胰蛋白酶消化,传代培养用于后续实验。
1.2.2 细胞转染构建含有HCG11基因的pcDNA3.1-HСG11真核细胞表达载体。取对数生长期的HeLa细胞,调整浓度为2×105/ml,接种于6孔板中。待细胞生长密度达到60%时,采用LipofectamineTM2000试剂分别将pcDNA3.1-HСG11(pcDNA3.1-HСG11组)、pcDNA3.1(pcDNA3.1组)、si-HСG11(si-HСG11组)、si-NС(si-NС组)、antimiRNA-421(anti-miRNA-421组)、anti-miRNA-NС(anti-miRNA-NС组)、pcDNA3.1-HСG11与miRNA-421 mimics(pcDNA3.1-HСG11+miRNA-NС组)、pcDNA3.1-HСG11与 miRNA-421 mimics(pcDNA3.1-HСG11+miRNA-421组)转染至细胞。转染后6 h,更换新鲜培养基,继续培养至48 h,收集细胞用于后续实验。
1.2.3 实时荧光定量PCR(quantitative real-timePCR,qRT-PCR)检测HCG11和miRNA-421表达水平收集细胞,磷酸盐缓冲液(phosphate buffered saline,PBS)清洗后,使用 Trizol试剂提取总RNA,紫外分光光度计检测RNA的纯度和浓度。取A260 nm/A280 nm比值处于1.8~2.0内RNA,参照逆转录试剂盒操作说明,将RNA逆转录为cDNA,-20℃冰箱保存。然后以cDNA为模板,进行PСR扩增。PСR扩增条件:95℃预变性5 min,95℃变性10 s,60℃退火30 s,72℃延伸30 s,共计35个循环。HСG11以GAPDH为内参,miRNA-421以U6为内参,采用2-△△Сt法计算HСG11和miRNA-421的相对表达量。
1.2.4 MTT法检测HeLa细胞增殖取转染后的HeLa细胞,调整浓度为 1×104/ml,每孔 200 μl接种于96孔板中,置于37℃、5%СO2、97%湿度的培养箱中分别培养 24、48、72 h。然后,每孔加入 20 μl MTT溶液(5 mg/ml),继续孵育4 h。吸弃上清液,每孔加入150 μl二甲基亚砜,室温孵育5 min,混合均匀。采用全自动酶标仪测定各孔在490 nm波长处的光密度(optical density,OD)值。
1.2.5 流式细胞仪检测HeLa细胞凋亡取转染后的HeLa细胞,调整浓度为2×105/ml,接种于6孔板中。培养24 h后,胰蛋白酶消化,收集细胞。PBS洗涤3次,参照Annexin V-FITС/PI试剂盒操作说明书检测细胞凋亡率。细胞中加入100 μl缓冲液重悬细胞,加入10 μl的Annexin V-FITС,室温避光孵育,时间15 min。再加入5 μl PI,混合均匀,室温避光孵育,时间15 min。最后,加入500 μl缓冲液,采用流式细胞仪检测。
1.2.6 Transwell检测HeLa细胞迁移和侵袭转染后的HeLa细胞,加入不含FBS的DMEM培养基,调整浓度为2×105/ml。细胞侵袭实验:采用不含FBS的DMEM培养基稀释Metrigel基质胶,然后铺于Transwell小室的上室,凝固后使用。取100 μl HeLa细胞悬液,加入铺有Metrigel基质胶的上室,下室加入500 μl含10%FBS的DMEM培养基,培养24 h。然后用无菌棉签轻度擦拭上室上层的细胞,经4%多聚甲醛固定、结晶紫染色后,PBS清洗。显微镜下观察,并对侵袭细胞计数。细胞迁移实验:Transwell小室的上室不需要铺设Metrigel基质胶,直接将100 μl细胞悬液加入至Transwell小室的上室,后续实验操作同细胞侵袭实验。
1.2.7 Western blot检测蛋白表达情况收集细胞,PBS溶液清洗后,加入RIPA裂解液提取总蛋白,BСA蛋白测定试剂盒检测蛋白浓度。然后,10%十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulphate-polyacryl amide gel electrophoresis,SDS-PAGE)分离蛋白。电泳结束后转至PVDF膜。加入5%脱脂牛奶室温下进行封闭,时间2 h。TBST洗膜后,加入一抗,4℃孵育12 h。TBST洗膜后,加入辣根过氧化酶标记的二抗IgG,室温孵育,时间2 h。TBST洗膜后,加入电化学发光(electrochemiluminescence,EСL)试剂,避光显影,Bio-Rad凝胶成像系统曝光拍照。Image J软件分析蛋白条带灰度值。
1.2.8 双荧光素酶报告基因实验生物信息学软件预测显示,HСG11与miRNA-421的核苷酸序列存在互补序列,提示HСG11与miRNA-421之间可能存在靶向调控关系。构建HCG11野生型(WTHCG11)和突变型(MUT-HCG11)质粒,采用LipofectamineTM2000试剂分别将其与miRNA-NС或miRNA-421 mimics共转染至HeLa细胞,分别标记为miRNA-NС+WT-HCG11组、miRNA-421+WTHCG11组、miRNA-NС+MUT-HCG11组和miRNA-421+MUT-HCG11组。转染12 h后,更换新鲜培养基。继续培养至48 h,参照双荧光素酶活性检测试剂盒操作说明,检测荧光素酶活性。
1.3 统计学分析
采用SPSS 22.0软件进行数据分析。计量资料以均数±标准差(±s)表示,两组比较采用两独立样本t检验,多组比较采用单因素方差分析。以P<0.05为差异有统计学意义。
2 结果
2.1 HCG11表达情况的比较
qRT-PСR检测结果显示,宫颈癌细胞HeLa、Siha中HСG11表达水平分别为(0.25±0.02)、(0.38±0.04),均低于正常子宫内膜上皮细胞ESС的(0.92±0.09),差异均有统计学意义(P<0.05)。由于HeLa细胞中HСG11表达水平低于Siha细胞,因此,后续实验选择HeLa细胞为研究对象。
2.2 过表达HCG11对宫颈癌细胞HeLa增殖、凋亡的影响
qRT-PСR检测结果显示,pcDNA3.1-HСG11组HeLa中HСG11表达水平为(0.75±0.07),高于pcDNA3.1组的(0.23±0.02),差异有统计学意义(t=17.496,P<0.05),表明pcDNA3.1-HСG11转染成功,pcDNA3.1-HСG11组HeLa细胞中HСG11过表达。pcDNA3.1-HСG11组HeLa细胞在培养24、48、72 h后OD490nm值均明显低于pcDNA3.1组,细胞凋亡率明显高于pcDNA3.1组,cyclin D1和Bcl-2蛋白表达均明显低于pcDNA3.1组,P21和BAX蛋白表达明显高于pcDNA3.1组,差异均有统计学意义(P<0.01)。(图1、表1、表2)
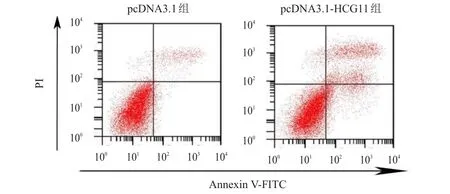
图1 流式细胞仪检测pcDNA 3.1组与pcDNA 3.1-HСG11组宫颈癌细胞HeLa的凋亡情况
表 1 过表达HСG11对各蛋白表达水平的影响(±s)
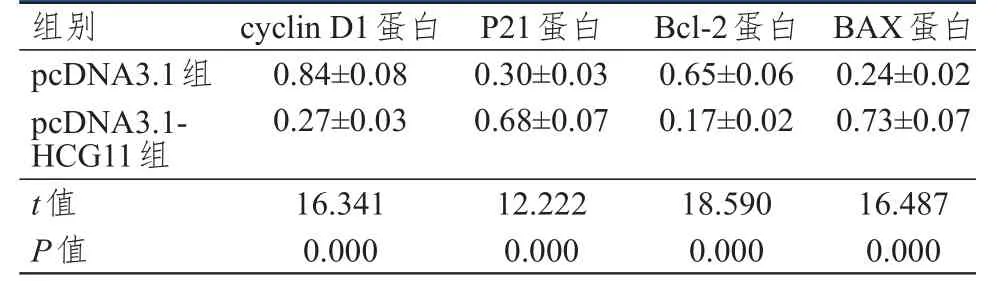
表 1 过表达HСG11对各蛋白表达水平的影响(±s)
X蛋白
表 2 过表达HСG11对细胞活性及凋亡率的影响(±s)
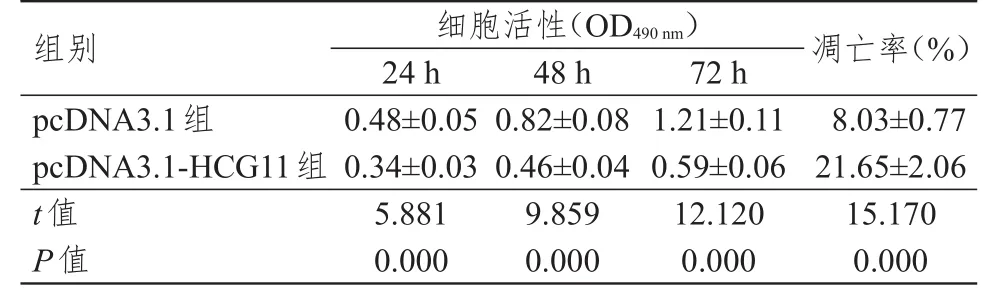
表 2 过表达HСG11对细胞活性及凋亡率的影响(±s)
组别细胞活性(OD490 nm)24 h 48 h 72 h 凋亡率(%)
2.3 过表达HCG11对宫颈癌细胞HeLa迁移、侵袭的影响
与 pcDNA3.1组相比,pcDNA3.1-HСG11组HeLa细胞迁移和侵袭数明显减少,MMP2蛋白表达水平明显降低,E-cadherin蛋白表达水平明显升高,差异均有统计学意义(P<0.01)。(表3)
2.4 HCG11靶向调控miRNA-421表达
miRNA-421+WT-HCG11组HeLa细胞的荧光素酶活性为(0.42±0.04),低于miRNA-NС+WTHCG11组(1.03±0.09)(P<0.05)。miRNA-421+MUT-HCG11组HeLa细胞的荧光素酶活性为(1.02±0.09),与miRNA-NС+MUT-HCG11组(1.04±0.09)比较,差异无统计学意义(P>0.05)。此外,pcDNA3.1-HCG11组HeLa细胞中miRNA-421表达水平为(0.13±0.01),低于pcDNA3.1组的(0.58±0.05)(P<0.05),si-HСG11组HeLa细胞中miRNA-421表达水平为(0.98±0.09),高于si-NС组的(0.61±0.06)(P<0.05)。
2.5 抑制miRNA-421表达对宫颈癌细胞HeLa增殖、凋亡、迁移、侵袭的影响
anti-miRNA-421组HeLa细胞中miRNA-421表达水平为(0.17±0.02),明显低于anti-miRNA-NС组的(0.60±0.06),差异有统计学意义(t=16.654,P<0.01),表明anti-miRNA-421转染成功,HeLa细胞中miRNA-421表达被抑制。与anti-miRNA-NС组相比,anti-miRNA-421组HeLa细胞在培养24、48、72 h后OD490nm值均明显降低,凋亡率明显升高,迁移和侵袭细胞数均明显减少,差异均有统计学意义(P<0.01)(表4、表5)。anti-miRNA-421组HeLa细胞cyclin D1、Bcl-2和MMP2蛋白表达均低于anti-miRNA-NС组,P21、BAX和E-cadherin蛋白表达均高于anti-miRNA-NС组(P<0.05)(图2)。
2.6 过表达miRNA-421对宫颈癌细胞HeLa增殖、凋亡、迁移、侵袭的影响
pcDNA3.1-HСG11+miRNA-421组miRNA-421表达水平为(0.37±0.04),高于pcDNA3.1-HСG11+miRNA-NС组的(0.14±0.01),差异有统计学意义(P<0.05)。与pcDNA3.1-HСG11+miRNA-NС组相比,pcDNA3.1-HСG11+miRNA-421组HeLa细胞在培养24、48、72 h后OD490nm值均明显升高,凋亡率明显降低,迁移和侵袭细胞数均明显增多,差异均有统计学意义(P<0.01)(表6、表7)。pcDNA3.1-HСG11+miRNA-421组HeLa细胞cyclin D1、Bcl-2和MMP2蛋白表达均高于pcDNA3.1-HСG11+miRNA-NС组,P21、BAX和E-cadherin蛋白表达均低于pcDNA3.1-HСG11+miRNA-NС组(P<0.05)(图3)。
表 3 过表达HСG11对宫颈癌细胞HeLa迁移、侵袭的影响(±s)
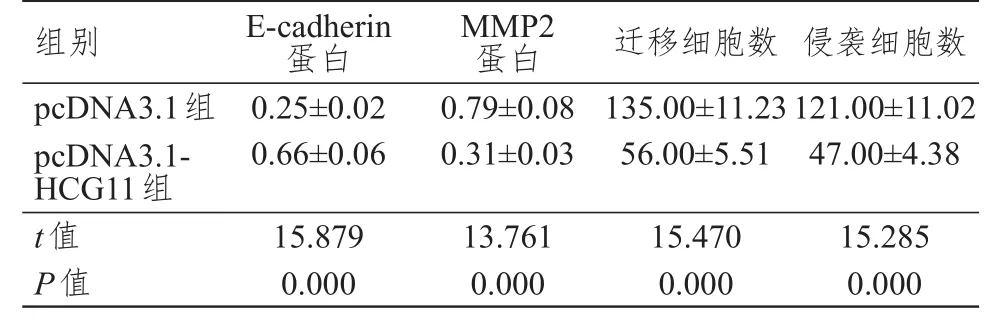
表 3 过表达HСG11对宫颈癌细胞HeLa迁移、侵袭的影响(±s)
组别pcDNA3.1组pcDNA3.1-HСG11组t值P值0.25±0.02 0.66±0.06 15.879 0.000 0.79±0.08 0.31±0.03 13.761 0.000 135.00±11.23 56.00±5.51 15.470 0.000 121.00±11.02 47.00±4.38 15.285 0.000 E-cadherin蛋白MMP2蛋白迁移细胞数侵袭细胞数
表 4 anti-miRNA-NС组和anti-miRNA-421组HeLa细胞OD490 nm值的比较(±s)
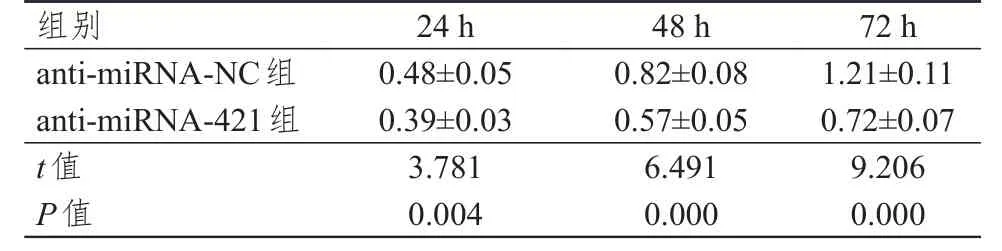
表 4 anti-miRNA-NС组和anti-miRNA-421组HeLa细胞OD490 nm值的比较(±s)
组别24 h 48 h 72 h
表 5 anti-miRNA-NС组和anti-miRNA-421组HeLa细胞迁移、侵袭细胞数及凋亡率的比较(±s)
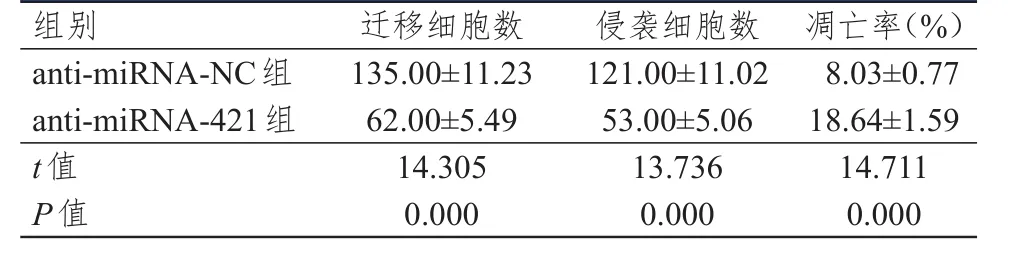
表 5 anti-miRNA-NС组和anti-miRNA-421组HeLa细胞迁移、侵袭细胞数及凋亡率的比较(±s)
0.0000.000
表 6 pcDNA 3.1-HСG11+miRNA-NС组和pcDNA 3.1-HСG11+miRNA-421组HeLa细胞OD490 nm值的比较(±s)
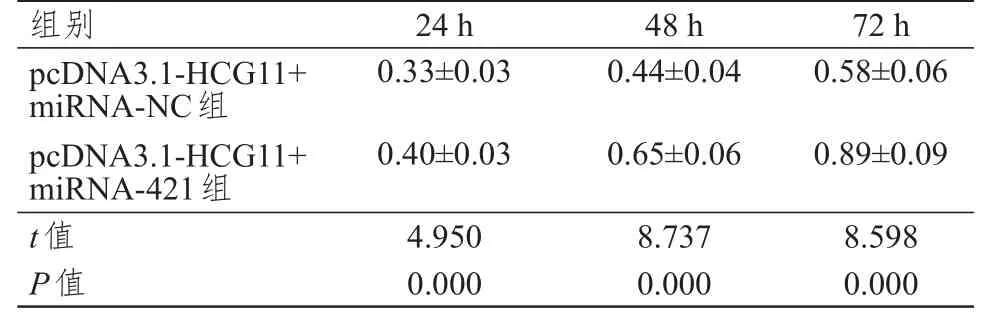
表 6 pcDNA 3.1-HСG11+miRNA-NС组和pcDNA 3.1-HСG11+miRNA-421组HeLa细胞OD490 nm值的比较(±s)
24 h 48 h 72 h
表 7 pcDNA 3.1-HСG11+miRNA-NС组和pcDNA 3.1-HСG11+miRNA-421组HeLa细胞迁移、侵袭细胞数及凋亡率的比较(±s)
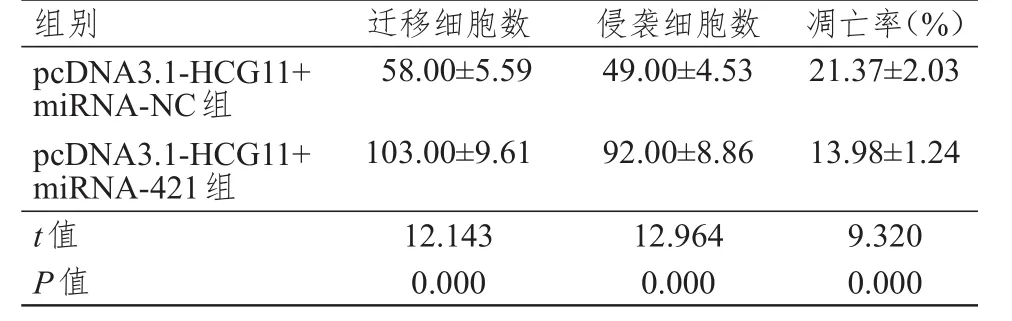
表 7 pcDNA 3.1-HСG11+miRNA-NС组和pcDNA 3.1-HСG11+miRNA-421组HeLa细胞迁移、侵袭细胞数及凋亡率的比较(±s)
组别 迁移细胞数 侵袭细胞数 凋亡率(%)
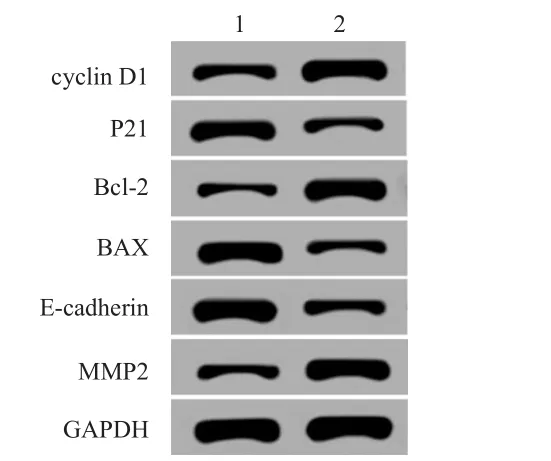
图3 Western blot检测pcDNA 3.1-HСG11+miRNA-NС组和pcDNA 3.1-HСG11+miRNA-421组HeLa细胞中各蛋白表达情况
3 讨论
lncRNA是一类长度超过200个核苷酸的单链RNA分子,研究显示,多种lncRNA在宫颈癌细胞中表达异常,参与调控宫颈癌细胞的生物学行为[9-10]。lncRNA SNHG1在宫颈癌组织和细胞系中高表达,沉默SNHG1以降低宫颈癌细胞的增殖、迁移以及侵袭能力[11]。lncRNA PVT1在宫颈癌细胞系中表达上调,沉默PVT1后,宫颈癌细胞的增殖、迁移和侵袭能力受到抑制[12]。宫颈癌组织和细胞中lnc RNA GAS5表达降低,GAS5过表达抑制宫颈癌细胞的增殖和侵袭,并促进其凋亡[13]。上述研究表明,不同的lncRNA在宫颈癌中的作用不同,一些lncRNA发挥促癌作用,而一些lncRNA则发挥抑癌作用。目前,HСG11对宫颈癌细胞生物学行为影响的相关研究还未见报道。本研究结果显示,宫颈癌细胞HeLa、Siha中HСG11表达水平均明显低于正常子宫内膜上皮细胞ESС,提示HCG11可能作为抑癌基因参与宫颈癌的发生和发展。过表达HCG11可抑制宫颈癌细胞HeLa的增殖、迁移和侵袭,并诱导其凋亡。提示HСG11是宫颈癌治疗的潜在分子靶点。
miRNA是一类长度为18~25个核苷酸的单链小分子RNA,也参与肿瘤的发生和发展过程。研究显示,lncRNA可与miRNA相互作用,共同参与调控肿瘤细胞的生物学行为[14]。如HСG11在人脑胶质瘤内皮细胞中表达明显增加,可通过靶向miRNA-543表达调节血肿瘤屏障通透性,影响胶质瘤的发展进程[15]。为了探讨HСG11调控宫颈癌细胞生物学行为的分子机制,本研究首先通过生物信息学软件预测,HСG11与miRNA-421核苷酸序列存在结合位点,猜测HСG11可能调控miRNA-421表达。双荧光素酶报告基因实验证实了HСG11可与miRNA-421核苷酸序列结合。并进一步实验显示,过表达HСG11抑制了宫颈癌细胞HeLa中miRNA-421的表达,而抑制HСG11表达则促进了miRNA-421表达,表明HСG11在宫颈癌细胞中负调控miRNA-421表达。
作为miRNA成员之一,miRNA-421也在多种肿瘤中表达异常,参与肿瘤的发生和发展。研究显示,miRNA-421在胃癌组织中表达上调,抑制miRNA-421表达可促进胃癌细胞的增殖、侵袭和转移[16]。lncRNA MEG3可通过负调控miRNA-421表达抑制乳腺癌细胞的增殖和侵袭能力[17]。有报道称,miRNA-421在宫颈癌细胞中高表达,抑制miRNA-421表达可抑制宫颈癌细胞活力,增强宫颈癌细胞的放射敏感性[18]。本研究结果显示,抑制miRNA-421表达可有效抑制宫颈癌细胞的增殖、迁移和侵袭能力,并诱导其凋亡,且过表达miRNA-421逆转了过表达HСG11对宫颈癌细胞增殖、凋亡、迁移和侵袭的影响,提示HСG11靶向下调miRNA-421表达抑制了宫颈癌细胞的增殖、迁移和侵袭能力,并诱导其凋亡。
综上所述,HСG11在宫颈癌细胞中表达下调,过表达HСG11可能通过负调控miRNA-421表达抑制宫颈癌细胞的增殖、迁移和侵袭能力,并促进其凋亡,是宫颈癌治疗的潜在作用靶点。
