泡沫铁对碱性废水中Cr(Ⅵ)的电还原
2020-06-03郭明林
郭明林,陈 倩,高 建
(1.天津工业大学 化学与化工学院,天津 300387;2.天津工业大学 中空纤维膜材料与膜过程国家重点实验室,天津 300387;3.天津工业大学 环境科学与工程学院,天津 300387)
铬是一种具有出色的物理化学性质的金属,在自然界中以化合物形态存在。铬也是一种人体必需的微量元素,Cr(Ⅲ)对维持身体健康具有重要作用,能够促进身体生长发育,增强胰岛素功能,糖尿病人甚至还需要额外补充身体所需的Cr(Ⅲ)[1-3]。但是,摄入过量的Cr(Ⅵ)会对人类的身体健康产生极大危害[4],可致畸、致癌、致突变[5],Cr(Ⅵ)来源主要是电镀、鞣革、纺织、涂料、铬酸盐生产等行业排放的工业废水[6]。国家规定的含铬废水排放标准要求Cr(Ⅵ)质量浓度不得超过0.5 mg/L,铬总含量上限为 1.5 mg/L[7-9]。目前,Cr(Ⅵ)的过量累积已经对地球的水生条件和生态系统造成了严重的环境污染问题[10-11],含铬废水的处理已经受到人们越来越多的关注与重视。铬最常见的化合价有 0、+Ⅱ、+Ⅲ、+Ⅵ。Cr(0)和 Cr(Ⅱ)基本无毒性或毒性很小;Cr(Ⅲ)毒性也较小,易于在碱性条件下从溶液中析出;Cr(Ⅵ)毒性最大,是 Cr(Ⅲ)毒性的 100 倍以上。因此,将废水中的Cr(Ⅵ)还原到Cr(Ⅲ),并使其絮凝沉淀从水系中排出,是处理含铬废水的有效方法。
近年来,为了去除污水中的Cr(Ⅵ),研究者开发了大量工艺。如王会才等[12]制备表面带有正电荷的铵盐功能化氧化石墨烯,对Cr(Ⅵ)的吸附量高达102 mg/g;廖小深等[13]采用紫外光辐照接枝法制备聚砜中空纤维滤膜,对Cr(Ⅵ)的截留率会随pH 值增大而增大;孙波等[14]以双铁为电极,通过脉冲交流电在pH 值为4 的含铬废水中进行电絮凝;赵丽等[15]以普通铁板作为阴阳极,在pH=3 的Fe2SO4溶液中,将废水中的Cr(Ⅵ)电还原为Cr(Ⅲ)。此外,还有生物过程[16]、离子交换[17]和光催化[18]等工艺。其中,电还原法是一种成熟、有效、廉价的工艺,其高效性很大程度上取决于电极材料的选择。目前,已经报道的电极材料有含铁化合物[17,19-20]、铝[21-24]、碳材料[8,10]等。铁材料是最为有效的电极材料,诸如磁铁矿[25]、四方硫铁矿[26]、零价铁[27]和生铁锈[28]等,都能够还原Cr(Ⅵ)。然而,无论考虑哪种电极材料,Cr(Ⅵ)的去除多是在酸性条件下进行的。传统上,电还原法去除废水中Cr(Ⅵ)的过程分为两步:在酸性条件下还原Cr(Ⅵ),在碱性条件下将Cr(Ⅲ)絮凝沉淀并排出水系。这种方法在处理酸性含铬工业废水方面非常有效,目前尚未有碱性条件下电还原Cr(Ⅵ)的报导。通常情况下,含Cr(Ⅵ)的碱性废水需要先对其进行酸性调节再进行电还原去除Cr(Ⅵ),这无疑又增加了工艺成本。因此,探索碱性废水中直接采用电还原法去除Cr(Ⅵ)的工艺条件显得尤为重要。
传统以铁材料为电极电还原去除Cr(Ⅵ)时,依靠铁阳极溶解产生的Fe2+还原Cr(Ⅵ),之后加入碱性物质,或者随着阴极表面水被还原产生OH-调节溶液为碱性,Cr(Ⅲ)才会发生絮凝沉淀,进而排出体系。本文结合电催化析氢(HER)原理,探索了一种适用于处理碱性含Cr(Ⅵ)废水、操作简单的电化学除铬方法。以泡沫铁为工作电极和对电极,在电化学工作站上进行碱性环境下Cr(Ⅵ)的还原实验,考察泡沫铁和不锈钢网作为对电极、不同电流密度对Cr(Ⅵ)去除效果的影响,并对其动力学进行研究,分析碱性环境下电还原去除Cr(Ⅵ)的机理。
1 实验部分
1.1 试剂与仪器
试剂:泡沫铁,厚度 3 mm,孔径 0.1~10 mm,益阳式菲美特新材料有限公司产品;不锈钢网,精度3 μm,河北腾德金属丝网制品有限公司产品;盐酸、氢氧化钠、重铬酸钾,均为分析纯,天津市风船化学试剂科技有限公司产品;无水乙醇,分析纯,天津市科密欧化学试剂有限公司产品。
仪器:TG16B 型超声仪,湖南凯达科学仪器有限公司产品;HZT-A200 型电子天平,福州华志科学仪器有限公司产品;TU1900 型紫外可见分光光度计,北京普析通用仪器有限公司产品;CHI760E 型电化学工作站,上海辰华仪器有限公司产品;722S 型可见分光光度计,上海菁华科技仪器有限公司产品。
1.2 电极制备
裁取3 cm×3 cm 大小的泡沫铁和不锈钢网若干块,浸入洗衣粉溶液中,超声清洗20 min 后取出,并用蒸馏水清洗数次;将泡沫铁放入盐酸溶液中浸泡2~3 min,取出后用蒸馏水和无水乙醇洗涤数次,干燥备用。
1.3 Cr(Ⅵ)的去除实验
首先采用TU1900 型紫外可见分光光度计分析含Cr(Ⅵ)溶液在添加NaOH 后光谱的变化。
使用处理过的泡沫铁作为工作电极和对电极,银/氯化银作为参比电极,将电极置入70 mL 氮气饱和的20 mg/L Cr(Ⅵ)溶液中,加入NaOH 至浓度为0.02 mol/L。在电还原过程中,采用磁力搅拌器对反应液讲行搅拌,使溶液的理化性质接近均匀一致。每隔10 min 取样,采用722S 型可见分光光度计在波长为372 nm 处测定样品溶液的吸光度。根据Cr(Ⅵ)溶液反应前后吸光度的变化,计算Cr(Ⅵ)的去除率T,如式(1)所示。

式中:T 为 Cr(Ⅵ)的去除率(%);C0为溶液中 Cr(Ⅵ)的初始质量浓度(mg/L);C 为溶液中Cr(Ⅵ)的质量浓度(mg/L)。
实验中测量的电势需要根据Nernst 方程校准到可逆氢电极电势(RHE),如式(2)所示:
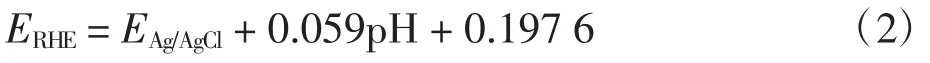
式中:ERHE为可逆氢电极电位(Vvs.RHE);EAg/AgCl为以银/氯化银电极为参比电极测得的电位(Vvs.Ag/AgCl);pH 为溶液的 pH 值。
1.4 反应动力学分析实验
采用泡沫铁或不锈钢网作为对电极,泡沫铁作为工作电极,考察不同电流密度对反应动力学的影响。电还原Cr(Ⅵ)的反应属于非均相反应,反应过程可用Langmuir-Hinshelwood 准一级动力学方程(式(3))来描述[29-30]:

对式(3)进行积分得到式(4):

式中:υ 为Cr(Ⅵ)的去除速率(mg/(L·h));C 为反应t时间后溶液中Cr(Ⅵ)的质量浓度(mg/L);C0为溶液中Cr(Ⅵ)的初始质量浓度(mg/L);t 为还原反应进行的时间(min);ln(C/C0)与时间 t 成线性关系,斜率 kobs为准一级动力学常数(min)。
2 结果与讨论
2.1 Cr(Ⅵ)物种的吸收峰分析
通常情况下,Cr(Ⅵ)在溶液中的物种会随着酸碱性的改变而发生变化[7,31-32],如式(5)所示:

当pH 值为1~6 时,平衡反应逆向移动,Cr(Ⅵ)主要以形式存在;当pH 值的范围为6~7.5 时,C(rⅥ)以形式存在;当pH 值在7.5 以上时,平衡反应正向移动,Cr(Ⅵ)主要以形式存在。
图1 为20 mg/L 的Cr(Ⅵ)溶液在添加NaOH 前后的紫外光谱图。

图1 Cr(Ⅵ)溶液在添加NaOH 前后的UV-Vis 曲线Fig.1 UV-Vis curve of Cr(Ⅵ)solution before and after adding NaOH
由图1 可以看出,重铬酸钾原溶液检测结果与文献[33]一致,在350 nm 处显示出强烈的吸收带,该吸收带归属于铬酸在四面体构象结构中的O-Cr(Ⅵ)电子电荷转移[34-35]。但是,当NaOH 添加到重铬酸钾溶液中后,吸收峰增加并转移到更高的波长值372 nm 处。由此表明,在本文实验条件下,NaOH 促进了分子内O-Cr(Ⅵ)电子电荷转移。
2.2 不同电流密度对Cr(Ⅵ)去除效果的影响
图2、图3 所示分别为在pH 值为13、以泡沫铁为工作电极和对电极、银/氯化银为参比电极、Cr(Ⅵ)初始质量浓度为20 mg/L 的条件下,不同电流密度对Cr(Ⅵ)的去除效果和动力学曲线。
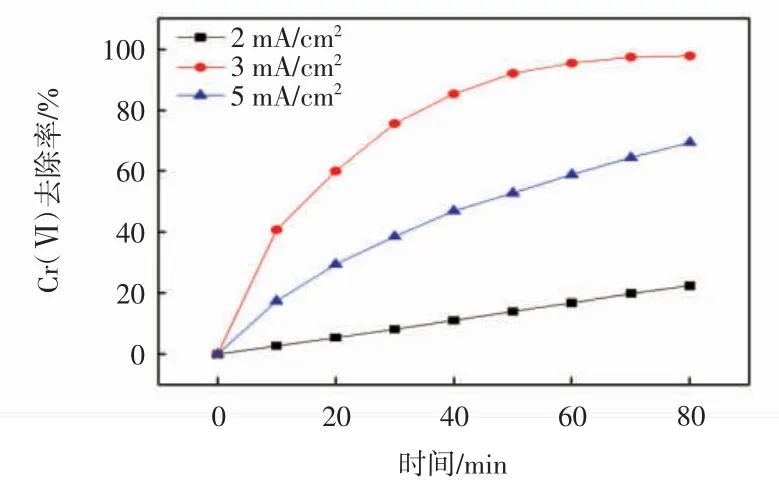
图2 不同电流密度对Cr(Ⅵ)去除效果的影响Fig.2 Effect of different current densities on Cr(Ⅵ)removal efficiency

图3 碱性条件下Cr(Ⅵ)电还原去除的动力学曲线Fig.3 Kinetic curve of Cr(Ⅵ)removal by electroreduction under alkaline conditions
由图2 可知,80 min 时,在 2、3、5 mA/cm2的电流密度下,Cr(Ⅵ)的去除率分别达到22.49%、97.89%、69.42%,kobs分别为 0.003、0.050、0.014。明显可以看出,随着电流密度的增加,Cr(Ⅵ)的去除率呈现先升高后降低的趋势,在电流密度为3 mA/cm2时达到最高的还原反应速率。这是因为与高电流条件相比,低电流强度条件下泡沫铁和铁的氢氧化物对Cr(Ⅵ)的吸附效率更高,更有利于对电极铁表面发生的还原Cr(Ⅵ)反应。此外,结合HER 原理可知,工作电极电解水过程中产生的氢中间体H*会随着电流强度的升高而逐渐减少,形成H2析出。2 mA/cm2的电流密度相对较小,只能产生少量具有强还原性的氢中间体;随着电流密度增加到3 mA/cm2,氢中间体H*的生成速率增加,工作电极附近Cr(Ⅵ)的还原速率也逐渐提高,而且在对电极表面,作为电子供体的Fe(Ⅱ)生成速率加快,电子转移速率也随之加快,Cr(Ⅵ)还原加速,因而,在电流密度3 mA/cm2的条件下,Cr(Ⅵ)的去除效果比电流密度为2 mA/cm2时更好;当电流密度增加到5 mA/cm2时,此时的电流密度已经能够电解水析出H2,这就导致了工作电极处的氢中间体H*产量减少,Cr(Ⅵ)到Cr(Ⅲ)的还原反应变弱,从而Cr(Ⅵ)的去除效果变差。Ya 等[36]以钛网包裹的废铁作为阳极,以不锈钢板作为阴极,在pH=1.1 酸性溶液中进行电还原去除Cr(Ⅵ),相应电流密度范围为1.18 ~3.54 mA/cm2。当电流强度从0.25 A 增加到0.5 A 时,Cr(Ⅵ)被还原并完全去除所需时间从176 min 减少到80 min。对比可知,本文在碱性条件下以泡沫铁为电极材料同样可以实现Cr(Ⅵ)的高效去除。
2.3 泡沫铁电还原Cr(Ⅵ)的重复使用性
在pH 值为13、使用三电极体系、以泡沫铁作为电极材料、Cr(Ⅵ)初始质量浓度为20 mg/L 的条件下,考察泡沫铁重复使用3 次电还原去除Cr(Ⅵ)的效果,结果如图4 所示。
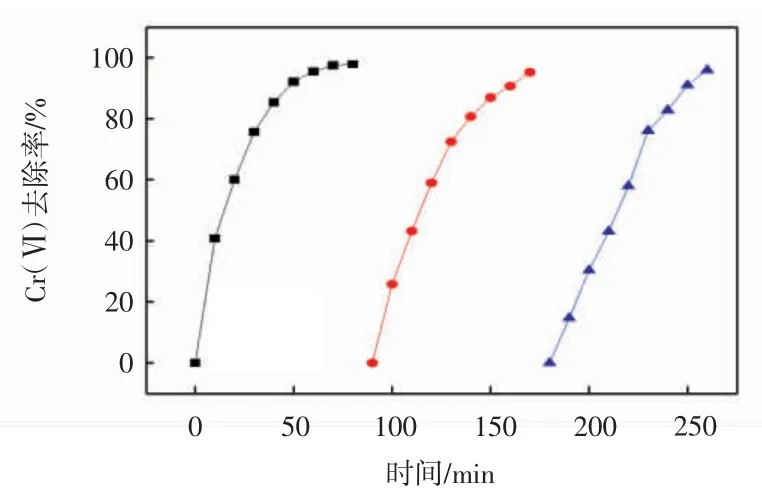
图4 泡沫铁重复使用对Cr(Ⅵ)的电还原去除效果Fig.4 Effect of electroreduction to remove Cr(Ⅵ)with foamed iron to reused
由图4 可知,经过3 次重复实验,80 min 时泡沫铁对Cr(Ⅵ)的去除率分别为97.89%、95.22%、95.95%。可以看出,使用相同的两块泡沫铁电极在碱性条件下进行3 次电还原去除Cr(Ⅵ)实验,去除效果比较稳定,说明泡沫铁电极可以重复使用,且去除Cr(Ⅵ)效果良好。
2.4 碱性条件下泡沫铁电还原Cr(Ⅵ)的机理
图5 所示为碱性条件下以泡沫铁为电极材料电还原去除Cr(Ⅵ)的机理。
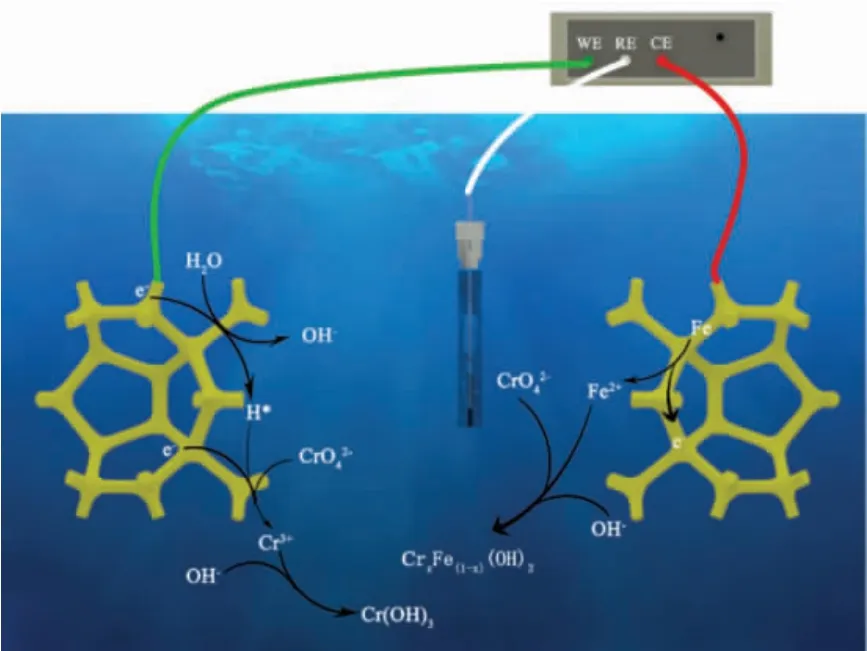
图5 碱性条件下以泡沫铁为电极材料电还原去除Cr(Ⅵ)的机理Fig.5 Mechanism of electroreduction of Cr(Ⅵ)by using foamed iron as electrode material under alkaline conditions

泡沫铁对电极在电还原去除Cr(Ⅵ)过程中,起主要作用的是Fe(Ⅱ),既起到了吸附作用,又是Cr(Ⅵ)的电子供体。首先,泡沫铁发生电化学溶解,如式(7)[37-39]所示:

生成的Fe2+和溶液中的OH-在泡沫铁对电极的表面生成 Fe(OH)2沉淀,如式(8)所示:

而Fe(OH)2的存在瞬时完成了 Cr(Ⅵ)的吸附和固定化[40],吸附的Cr(Ⅵ)被Fe(Ⅱ)还原为Cr(Ⅲ),如式(9)[41-42]所示:
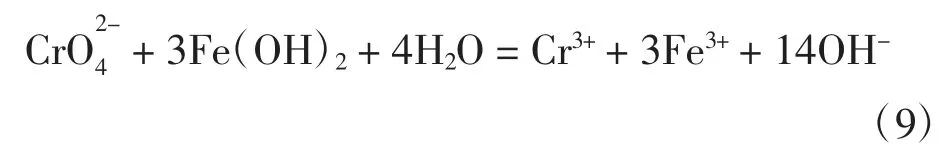
并以CrxFe1-x(OH)3的形式沉淀,如式(10)所示:

CrxFe1-x(OH)3在对电极上发生沉淀,保证了Cr(Ⅲ)不会被释放到溶液中发生再生,但是也对铁颗粒表面起到了钝化作用[43-45],这导致泡沫铁对Cr(Ⅵ)的还原能力受到电极限制,使得Cr(Ⅵ)去除速率逐渐降低[37]。
作为工作电极的泡沫铁主要充当电子传递介质,结合HER 原理可知,将电势控制在适当范围内可以产生足够的氢中间体H*,有利于还原反应的进行,如式(11)所示:

电位过高则会进一步产生H2析出,如式(12):


电解水产生的OH-与Cr3+结合,生成Cr(OH)3沉淀,如式(14)所示:

2.5 不同对电极对Cr(Ⅵ)去除效果的影响
为进一步确认在电还原去除Cr(Ⅵ)中起主要作用的电极,在pH 值为13、电流密度为3 mA/cm2、工作电极为泡沫铁、Cr(Ⅵ)初始质量浓度为20 mg/L 的条件下,研究泡沫铁和不锈钢网分别作为对电极对Cr(Ⅵ)的去除情况对比,结果如图6 所示。

图6 泡沫铁和不锈钢网分别作为对电极对Cr(Ⅵ)的去除情况Fig.6 Removal effect of Cr(Ⅵ)by foamed iron and stainlesssteel mesh respectively as counter electrode
由图6(a)可以看出,泡沫铁作为工作电极,泡沫铁和不锈钢网分别作为对电极时,对应的LSV 极化曲线没有明显差异。这意味着泡沫铁作为工作电极在上述两个电还原去除Cr(Ⅵ)过程中所起的作用是基本相同的。由图6(b)可知,经过80 min 还原反应后,泡沫铁和不锈钢网分别作为对电极时,Cr(Ⅵ)的去除率分别为 97.89%、39.76%;由图 6(c)可以看出,泡沫铁和不锈钢网对铬的还原反应遵循准一级动力学,kobs分别为0.051 和0.006,以泡沫铁作为对电极的还原反应速率是不锈钢网的8 倍以上。结合图6(b)和图6(c),可以进一步得出结论,在对电极上发生的反应对电还原Cr(Ⅵ)起主要作用,即Cr(Ⅵ)的去除主要以Fe(Ⅱ)还原Cr(Ⅵ)为主。此外,泡沫铁作为对电极时Cr(Ⅵ)的去除率和还原速率远远大于不锈钢网作为对电极时,这是因为作为对电极,泡沫铁和不锈钢网的面积虽然都是3 cm×3 cm,但是泡沫铁通透多孔,具有更大的比表面积,因而具有更多的活性位点还原Cr(Ⅵ)。由于泡沫铁的吸附性和更多的活性位点,使Cr(Ⅵ)与Fe(Ⅱ)能够快速接触并发生还原反应(式(9))。而不锈钢网由于其比较稳定,不易生成Fe(Ⅱ)和Fe(Ⅲ),因而难以实现Fe(Ⅱ)对Cr(Ⅵ)的还原和Fe(OH)3对Cr(Ⅲ)的吸附。因此,泡沫铁作为对电极对Cr(Ⅵ)的去除速率比不锈钢网高。
此外,由图2 可知,工作电极上产生的氢中间体H*对电还原Cr(Ⅵ)速率也有一定影响,而且受电流密度影响较大。
3 结 论
(1)将HER 原理与电还原相结合,实现了碱性条件下高效去除Cr(Ⅵ)。在保证铁阳极实现高效还原Cr(Ⅵ)的基础上,根据HER 原理选择还原态氢H*产生最高效的电压,阴极反应为还原Cr(Ⅵ)提供了又一动力,加快了反应速率。
(2)泡沫铁作为对电极还原Cr(Ⅵ)的反应速率是不锈钢网的8 倍以上。这归因于泡沫铁通透多孔的结构,一方面保证了其具有更大的比表面积,进而能够吸附大量的Cr(Ⅵ)在电极表面;另一方面,能够提供更多的活性位点进行还原反应。
(3)在HER 电压范围内电还原,Cr(Ⅵ)的去除效果和还原速率随着电流密度的增加呈现先升高后降低的趋势。这归因于还原态氢H*的数量在一定范围内会随着电流密度的增加而增加,但电流密度过大会导致H+直接还原为H2,还原态氢H*减少。当电流密度为3 mA/cm2时,pH=13 条件下电还原20 mg/L的Cr(Ⅵ)溶液,80 min 时去除率可达到97.89%.
