Y3+掺杂TiO2柱撑膨润土光催化氧化甲基橙的降解过程
2020-05-29董倩茹蒋惠忠
董倩茹, 韩 冰, 冯 威, 蒋惠忠
(1.吉林大学 新能源与环境学院, 长春130021; 2.吉林建筑大学 市政与环境工程学院, 长春 130118)
染料废水为难降解有机废水, 处理方法主要有生物法、物理法和化学法[1-3].但常规处理方法效率较低[4], 目前大多数使用高级氧化法[5], 如光催化降解有机废水[6-7].TiO2是一种优良的光催化剂[8-11], 但其禁带宽度大、光谱响应范围窄、反应过程中易团聚难回收, 且光生电子-空穴极易复合[12].通过对TiO2金属离子掺杂[13]、非金属掺杂[14]、双元素共掺杂[15]和表面修饰[16]等改性可改善其光催化能力.卢维奇等[17]用溶胶-凝胶法制备了钇掺杂TiO2光催化剂降解甲基橙, 并对其降解性能和影响条件进行了研究; 王瑞芬等[18]用水热法制备了钇掺杂TiO2光催化剂, 并研究了其光催化性能; 吴忠杰等[19]用溶胶凝胶法制备了钇掺杂TiO2光催化剂, 并研究了其光催化活性及影响因素.
膨润土主要成分为蒙脱石, 掺杂后可提高TiO2的吸附性[20-21].掺杂过渡金属离子可增大光谱响应范围、抑制光生电子-空穴复合、抑制TiO2团聚并增强对光的吸收能力[22].因此本文在钇掺杂TiO2材料的基础上加入膨润土, 并研究其对甲基橙废水的光催化降解机理.对反应过程中的化学需氧量(COD)、总有机碳(TOC)、电导率和pH值等进行测定, 通过紫外-可见分光光度法(UV-Vis)、液相色谱质谱联用(LC-MS)及紫外可见漫反射光谱(UV-Vis DRS)分析催化剂及降解过程中的中间产物, 并给出可能的降解途径.
1 实 验
1.1 试剂与仪器
钠基膨润土(Na-MMT, 分析纯, 天津光复精细化工厂); 掺杂钇离子的二氧化钛柱撑膨润土(自制); 钛酸四正丁酯(C16H36O4Ti, 化学纯, 上海国药集团化学试剂有限公司); 异丙醇((CH3)2CHOH, 分析纯, 北京化工厂); 硝酸钇(Y(NO3)3·6H2O, 分析纯, 上海国药集团化学试剂有限公司); 浓盐酸(HCl, 分析纯, 沈阳市联邦试剂厂); 甲基橙(C14H14N3SO3Na, 分析纯, 上海青析化工科技有限公司).
紫外-可见分光光度计(L5S型, 上海仪电分析仪器有限公司); 电子天平(PTX-FA210S型, 福州华志科学仪器有限公司); 马弗炉(SX-25-10型, 山东龙口先科仪器公司); pH计(PHS-3C 型, 上海仪电科学仪器股份有限公司); 电导率仪(DSCⅡ型, 瑞士梅特勒-托利多公司); COD加热装置(HY-7012型, 青岛尚德环保仪器有限公司); TOC测定仪(LiquidTOC型, 德国元素分析系统公司); 电热鼓风干燥箱(GZX-9070MBE型, 上海博讯实业有限公司医疗设备厂); 离子色谱(HIC26A型, 日本岛津公司); 高效液相色谱仪(Agilent1100型, 美国Agilent公司); 质谱仪(Agilent1200型, 美国Agilent公司).
1.2 掺杂钇离子的TiO2柱撑膨润土制备
将钛酸四正丁酯(42.5 mL)与异丙醇(37.5 mL)混合并充分搅拌20 min, 向所得溶液中缓慢滴加165 mL溶解了0.70 g硝酸钇的去离子水, 并搅拌20 min使其混合均匀, 先用2 mol/L盐酸调节溶液的pH=2.8, 再将溶液置于50 ℃烘箱中烘干12 h, 使其形成透明溶胶.
用500 mL去离子水浸泡10 g钠基膨润土过夜, 使其形成膨润土悬浮液, 将上述溶胶加入其中, 剧烈搅拌3 h后, 室温放置20 h, 以7 000 r/min离心30 min, 然后在烘箱中于50 ℃烘干.将烘干的复合物磨碎, 在马弗炉中于200 ℃焙烧3 h后冷却, 置于暗处待用.所得产物即为掺杂Y3+的TiO2柱撑膨润土(简称Y-TiO2-MMT), 其中Y3+在TiO2中的摩尔分数为1.50%.
1.3 光催化反应
由于光催化最佳反应条件为酸性条件[23], 因此将初始pH值设为5.0.将200 mL质量浓度为200.0 mg/L的甲基橙(MO)溶液与0.40 g Y-TiO2-MMT在反应器中混合, 避光搅拌30 min使染料分子充分吸附在催化剂上.取一定量样品经5 000 r/min离心后, 测定上清液的pH值、电导率、COD值和TOC值.同时测定悬浊液的COD值, 将分离出已吸附染料的Y-TiO2-MMT于60 ℃烘干, 测定催化剂的漫反射光谱和TOC值.测定值作为本次实验的初始值.剩余样品以100 W高压汞灯为光源进行光催化实验.分别在0.5,1,2,3,4,5,6 h取出少量样品对上述指标进行测定, 观察各项指标随光照时间延长的变化, 以确定甲基橙光催化降解途径.
2 结果与讨论
2.1 复合材料的扫描电镜照片
图1为复合材料的扫描电镜(SEM)照片.由图1(A)可见, TiO2-MMT保留了膨润土的层状结构[24], 但TiO2出现团聚现象, 粒径增大, 表面较粗糙.由图1(B)可见, 材料表面相对光滑, 表明Y3+已掺杂到复合材料中, 掺杂Y3+抑制了TiO2的团聚, 增强了材料对光的吸收能力.

图1 TiO2-MMT(A)和Y-TiO2-MMT(B)的扫描电镜照片Fig.1 SEM images of TiO2-MMT (A) and Y-TiO2-MMT (B)
2.2 掺杂Y3+对吸附及光催化效果的影响
图2为Y-TiO2-MMT和TiO2-MMT对甲基橙溶液降解率的对比结果.光照开始前, 先将Y-TiO2-MMT置于MO溶液中, 于暗处放置0.5 h, 此时溶液中仅存在Y-TiO2-MMT的吸附作用, MO溶液的降解率为21.2%, 用TiO2-MMT吸附0.5 h后, MO溶液的降解率为12.1%, 表明掺杂Y3+可提高复合材料的吸附性能, 使更多的有机物吸附在催化剂表面.光照6 h后, 用Y-TiO2-MMT的MO溶液降解率达99.6%, 比用TiO2-MMT的MO溶液降解率提高了17.7%.因此, Y-TiO2-MMT优于TiO2-MMT的吸附及光催化效果.表明掺杂钇离子可增强TiO2的光响应能力, 有利于进行光催化反应, 提高了吸附-光催化性能.
2.3 光催化降解紫外-可见光谱
在100 W高压汞灯作用下, 研究复合催化剂(用量0.40 g)在光照作用下对甲基橙(200 mL, 200.0 mg/L)的降解过程.不同光照时间的紫外-可见光谱如图3所示.由图3可见, 在200 nm和465 nm 处出现较大强度的吸收峰, 其中200 nm处的峰主要归属于芳烃的环结构[25]; 465 nm处的峰主要归属为偶氮双键[26].光照时间越长, 两个吸收峰越弱, 表明甲基橙含量逐渐减少.465 nm处的偶氮双键特征峰减弱速度较快, 表明反应开始后偶氮双键先被破坏.当反应6 h时, 465 nm处的吸收峰几乎消失, 此时溶液接近无色, 甲基橙的偶氮双键几乎完全被破坏.273 nm处的吸收峰由芳烃与生色基团间相互作用产生[27].200 nm和273 nm处的吸收峰也随光照时间的增加而降低, 且峰宽变大, 表明在甲基橙降解过程中可能产生了新的中间产物.当反应6 h时, 除部分芳环外, 其他生色基团均被降解.
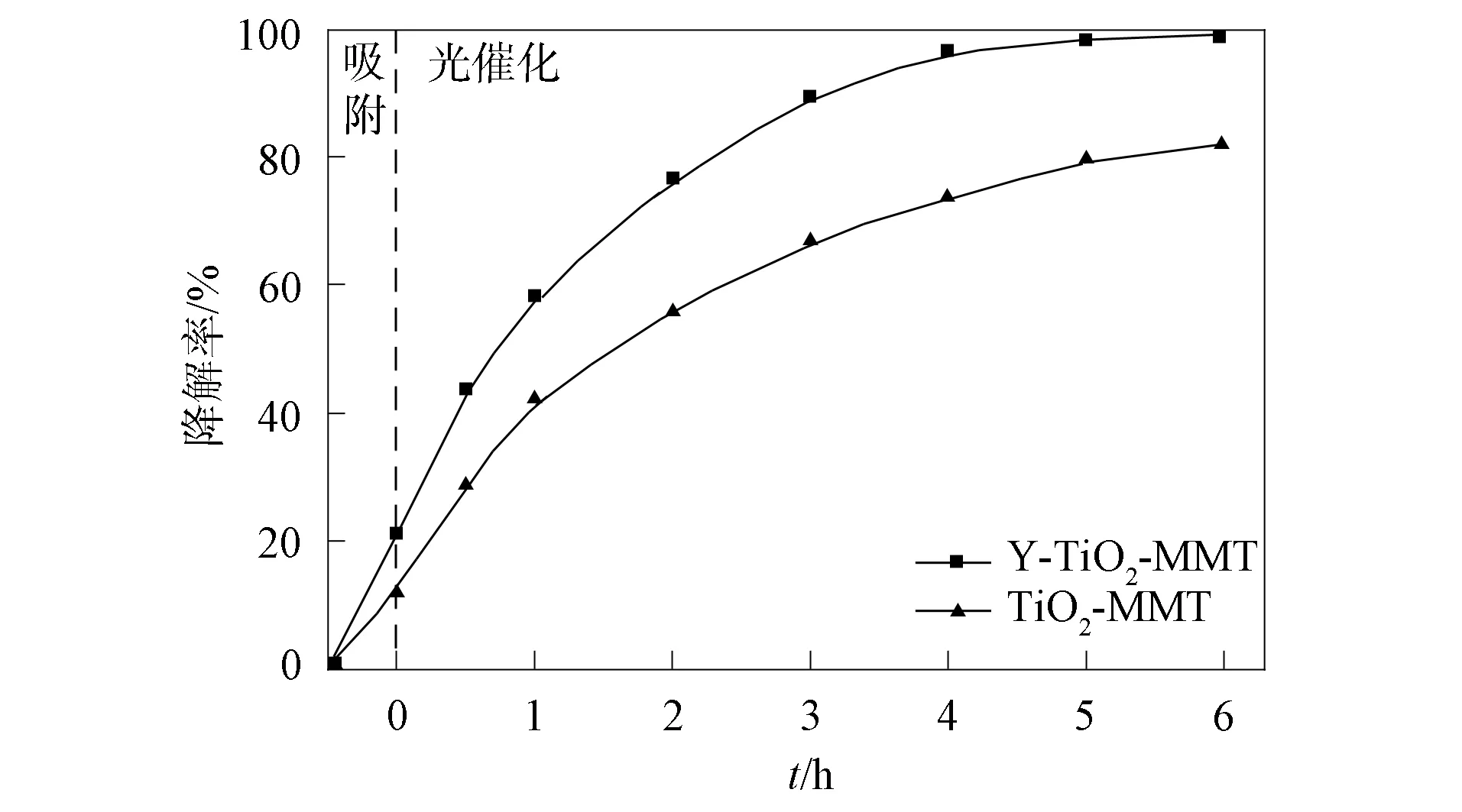
图2 Y-TiO2-MMT和TiO2-MMT对 甲基橙溶液降解率的对比Fig.2 Comparison of degradation rate of Y-TiO2-MMT and TiO2-MMT on methyl orange solution

a~h: 0,0.5,1,2,3,4,5,6 h.图3 甲基橙溶液光催化降解的紫外-可见光谱Fig.3 Ultraviolet-visible spectra of photocatalytic degradation of methyl orange solution
2.4 降解过程的溶液pH值和电导率变化
降解过程的溶液pH值和电导率变化如图4所示.由图4可见, 在反应的前3 h, 溶液的pH值降低, 这是由于反应在催化剂表面发生, 在光催化过程中MO降解生成以甲苯磺酸为主的中间产物小分子酸所致.在反应3 h后, 中间产物进一步分解, 生成无机离子, 最终矿化为矿化产物CO2和H2O, pH值增加.
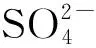
2.5 体系COD值的变化
COD可用于观察污水中有机污染物降解的程度.图5为光催化过程中体系的COD值随光照时间的变化.由图5可见: 随着反应的进行, 体系的COD值下降, 上清液的COD值由80.20 mg/L降至12.20 mg/L; 悬浊液的COD值由201.20 mg/L降至102.90 mg/L, 表明溶液中有机物的含量随光催化反应的进行而减少.在同一时刻, 悬浊液比上清液的COD值高, 这是由于上清液中有机物含量少, 有机物多数附着在催化剂上所致.
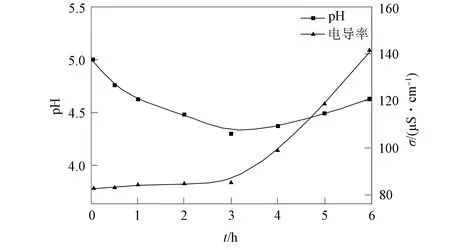
图4 降解过程的溶液pH值和电导率变化Fig.4 Changes of pH values and conductivities of solution during degradation

图5 光照时间对甲基橙体系上清液和悬浊液COD值的影响Fig.5 Effect of illumination time on COD values of supernatant and suspension of methyl orange system
2.6 体系TOC值的变化
TOC可用于观察有机物的矿化程度.光照时间对溶液和催化剂TOC值的影响如图6所示.由图6可见, 在同一时刻, 催化剂比溶液中的TOC值高, 这是由于溶液中的有机物附着在催化剂上所致.溶液和催化剂的TOC初始值分别测定为30.20,76.80 mg/L.在反应初期, 由于MO在降解过程中不断产生易降解的小分子有机物, 因此有机物的总量变化较小, TOC值基本不变; 在反应3 h后, TOC值降低, 表明有机物开始矿化, 在反应结束后, 溶液TOC值降至13.10 mg/L, 催化剂TOC值降至43.10 mg/L, 此时甲基橙溶液基本完全矿化.

图6 光照时间对溶液和催化剂TOC值的影响Fig.6 Effect of illumination time on TOC values of solution and catalyst
2.7 溶液中间产物的生成及变化
图7为溶液光催化过程中的高效液相色谱, 其中: 图7(A)为未进行光照的甲基橙溶液色谱; 图7(B),(C),(D)分别为光照1,3,5 h溶液的色谱.由图7(A)可见, 峰1出现在23.3 min处; 由图7(B)可见, 峰1的强度减弱, 表明甲基橙分子被分解, 在19.6 min处出现新的尖峰2, 表明在光催化过程中产生了新物质, 质谱显示其归属为对苯二酚(C6H6O2), 在17.3 min和20.6 min处分别出现较弱的峰3和峰4, 质谱显示峰3归属为甲苯磺酸(C6H6OS), 峰4归属为苯胺(C6H7N); 由图7(C)可见, 光照时间越长, 峰1的强度越弱, 甲基橙分子继续降解, 峰2、峰3和峰4的强度快速减弱, 峰4几乎完全消失, 表明苯胺、对苯二酚及甲苯磺酸均为光催化过程的中间产物, 易被进一步催化降解; 由图7(D)可见, 峰1、峰2和峰3的强度均减弱并趋于消失, 峰4的强度几乎完全消失.

图7 甲基橙及其降解中间产物的高效液相色谱Fig.7 High performance liquid chromatograms of methyl orange and its degradation intermediates
甲基橙染料可能的降解途径如图8所示.根据高效液相色谱和质谱分析结果, 可推测染料分子在紫外灯作用下可能的降解途径为: 首先, 染料分子吸附到催化剂的表面, 然后发生光催化, 生成强氧化物质, 如超氧自由基和羟基自由基[28]等.根据甲基橙的结构特征, 甲基橙分子通过破坏偶氮双键降解, 在降解过程中产生的中间产物(如苯胺、对苯二酚及甲苯磺酸等)均会进一步降解, 并最终矿化.

图8 甲基橙的光催化降解途径Fig.8 Photocatalytic degradation pathway of methyl orange
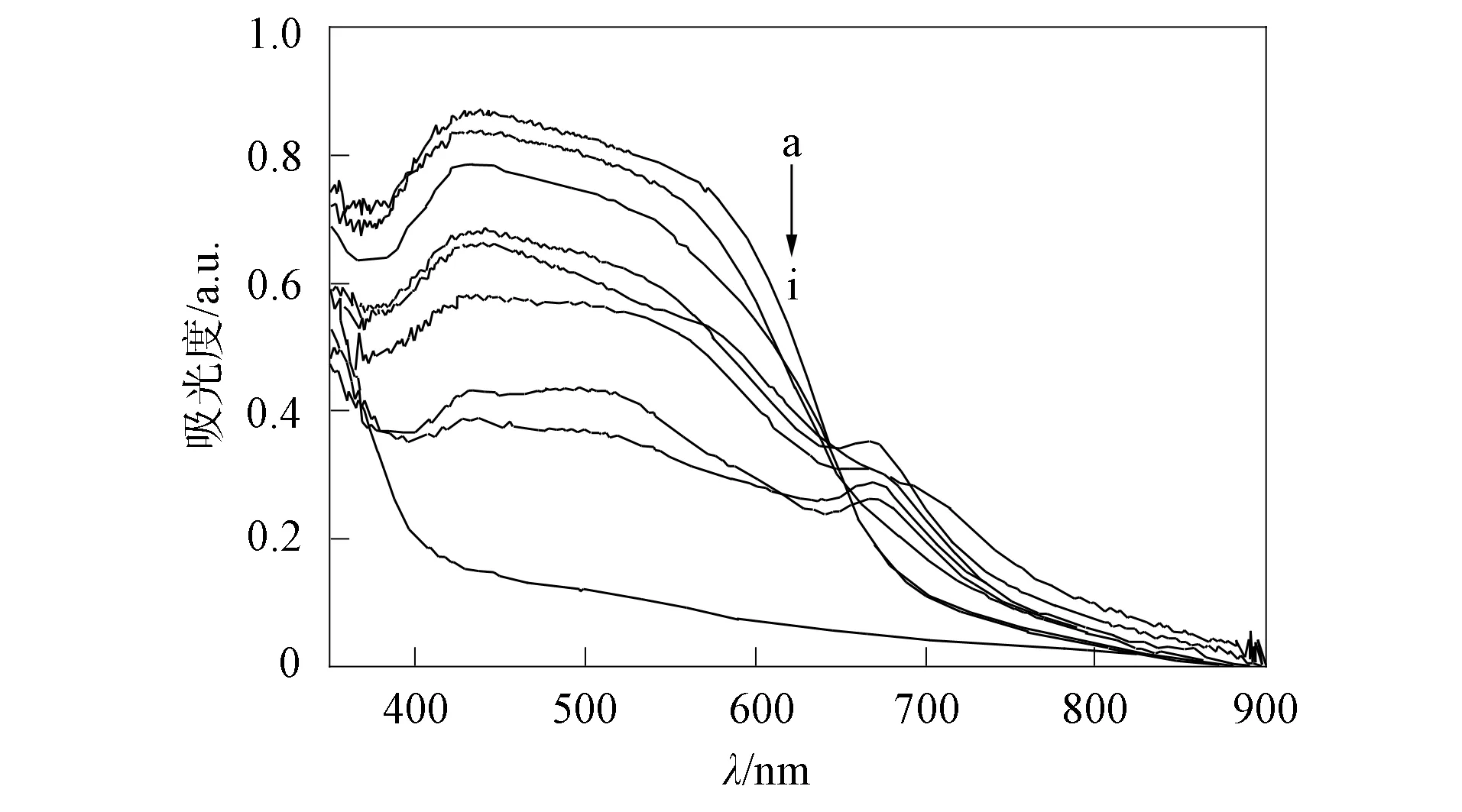
a: 吸附0.5 h; b~h: 光催化0.5,1,2,3,4,5,6 h; i: 对照.图9 吸附和光催化降解甲基橙后 Y-TiO2-MMT的漫反射光谱Fig.9 UV-Vis DRS of Y-TiO2-MMT after adsorption and photocatalytic degradation of methyl orange
光催化性能随催化剂的吸附性增强而增强, 表明催化剂的吸附与光催化性能间存在一定的相关性.吸附和光催化降解甲基橙后Y-TiO2-MMT的漫反射光谱如图9所示.由图9可见, 在可见光吸收范围内, 催化剂有较强的吸收峰, 表明催化剂表面已附着了大量的甲基橙, 催化剂的吸附作用有利于将有机污染物聚集在催化剂表面并将其光催化降解.经过0.5 h的充分吸附后进行光照, 吸附在催化剂表面上的染料分子被持续分解, 有机物质不断减少, 吸收峰逐渐降低.经过1 h光照后, 在 670 nm处出现一个新的吸收峰(对苯二酚), 表明在光催化过程中出现了新的有机物吸附在催化剂上, 该处的吸收峰逐渐降低, 表明新出现的中间产物逐渐降解.由于吸附是在催化剂表面进行, 有机分子在催化剂表面即被降解, 降解产物溶于溶液中, 同时新的分子继续吸附在催化剂表面并被降解.因此吸附和光催化性能间有一定的协同性, 对染料分子的降解也是按吸附-光催化协同机制进行的.染料分子的吸附-光催化降解反应模型如图10所示.
综上所述, 本文用酸性溶胶法制备了掺杂Y3+的TiO2柱撑膨润土, 该膨润土具有较强的吸附作用和降解作用, 吸附0.5 h即可使MO溶液降解21.2%, 光照6 h后可使MO溶液降解99.6%.光催化过程中, 溶液的pH值从5.0降至4.6, 电导率增加了58.9 μS/cm, 上清液和悬浊液COD值分别减少了68.00,98.30 mg/L, 溶液和催化剂的TOC值分别减少了17.10,33.70 mg/L.因此, 甲基橙分子的降解发生在催化剂表面.根据甲基橙的结构特征, 甲基橙分子通过破坏偶氮双键降解, 降解产生的中间产物(苯胺、对苯二酚及甲苯磺酸等)均会进一步降解, 并最终矿化.其降解过程按吸附-光催化协同机制进行.

图10 染料分子的吸附-光催化降解反应模型Fig.10 Adsorption and photocatalytic degradation model of dye molecules
