MnO2/Gh的制备及对亚甲基蓝的降解研究
2020-05-25张程蕾韩恩山滕厚开谢陈鑫聂荣健任春燕
张程蕾 ,韩恩山 ,滕厚开 ,,谢陈鑫 ,聂荣健 ,任春燕
(1.河北工业大学,天津300130;2.中海油天津化工研究设计院有限公司,天津300131)
目前,我国的环境问题日趋严重,制药、化工、石油和印染等行业产生的废水对生态系统存在巨大的威胁。这些废水成分复杂,生物可降解性差,亟需一种耗能小、清洁无污染的方法处理。Fenton法是处理废水的常用技术,该技术通过催化H2O2产生·OH来降解污染物,但在处理过程中需要对水体进行预酸化,反应后会产生大量的铁泥,增加了处理成本,限制了其在污水处理中的应用〔1〕。
石墨烯具有sp2杂化的六方晶格二维碳原子层,可以通过缠绕闭合、卷曲成环和堆叠形成零维富勒烯、一维碳纳米管和三维石墨〔2〕。氧化还原法得到的石墨烯材料存在大量结构缺陷和褶皱,具有较多的吸附位点和活性中心。通过对石墨烯进行表面修饰,不仅能够解决石墨烯团聚的问题,还能提高材料的催化活性和电化学性能。在过渡金属氧化物中,低毒性、低成本的纳米MnO2具有催化活性高、比表面积大等特点,近年来,其作为类Fenton试剂中催化剂受到研究者的广泛关注〔3-4〕。MnO2的结构是由MnO6八面体单元组成,制备方法和条件决定了其晶型和形貌,进而决定了其性能〔4〕。
本研究以KMnO4为锰源,采用氧化还原法制备MnO2/石墨烯(MnO2/Gh)纳米复合材料。研究KMnO4的初始浓度对MnO2晶型的影响。将MnO2/Gh作为非均相电-Fenton催化剂,应用于电催化降解亚甲基蓝体系,研究电流密度、初始pH等对亚甲基蓝降解效果的影响。实验通过曝气的方式改变水中的含氧量,利用阴极的还原作用原位生成H2O2〔5〕。曝气可以使材料始终处于悬浮运动状态,既能够增大传质速率,还可以提高电流效率〔6〕。
1 实验部分
1.1 实验原料及仪器
实验原料:自制石墨烯,亚甲基蓝、无水硫酸钠、KMnO4、浓硫酸,天津市风船化学试剂科技有限公司,以上试剂均为分析纯。
实验仪器:KXN-3020D型直流稳压电源,深圳市欧瑞佳科技有限公司;Hitachi S-4800型扫描电子显微镜,株式会社日立制作所;UItimaⅣ型X射线衍射仪,株式会社理学;TGA/DSC 1/1100 TGA热重分析仪,梅特勒托利多国际贸易(上海)有限公司;Thermo Fisher ICAP-7200电感耦合等离子发射光谱仪,深圳市瑞盛科技有限公司;ASAP 2000型全自动物理吸附分析仪,厦门名大科技有限公司。
1.2 MnO2/Gh的制备
取100 mg石墨烯加入到80 mL 1 mol/L H2SO4溶液中,超声使其均匀地分散在溶液中。向烧杯中加入一定量的KMnO4,并不断搅拌,在水浴80℃的条件下反应2 h,自热冷却至室温。在这个过程中,石墨烯表面的C和KMnO4发生氧化还原反应,同时伴有KMnO4的自分解反应〔7〕。之后过滤,用去离子水洗涤至中性,在60℃的条件下真空干燥。干燥至恒重后,标记为MnO2/Gh-X(X为锰源的浓度,mol/L),放入干燥器中待用。按照同样的方法分别制备了MnO2/Gh-0.2、MnO2/Gh-0.5、MnO2/Gh-0.8 和 MnO2/Gh-1。
1.3 MnO2/Gh非均相电-Fenton体系处理亚甲基蓝
实验阳极采用催化性能较好的圆筒形Ti/PbO2电极,有效面积为610 cm2,阴极为网状圆筒形Ti电极,网孔形状为边长0.2 cm的菱形,有效面积为471 cm2,网状电极有利于H2O2的生成与扩散,极板间距为1.5 cm。配制100 mg/L电导率为10 mS/cm的亚甲基蓝溶液,并向体系中加入一定量的催化剂,通入O2使其均匀悬浮并吸附饱和。实验过程中的电流电压由直流稳压电源控制。每隔10 min取样,测其吸光度、COD,以亚甲基蓝降解率和COD去除率作为研究指标,探讨MnO2的晶型、电流密度和pH对亚甲基蓝降解效果的影响。
2 结果与讨论
2.1 MnO2/Gh的表征分析
2.1.1 SEM和BET分析
用SEM对MnO2/Gh复合材料的表面形貌进行表征,结果见图1。

图1 不同形貌MnO2的SEM图
由图 1(a)可知,当 KMnO4浓度较低时,MnO2呈片状结构;由图1(b)可知,随着锰源浓度的增加,MnO2逐渐变为“三明治”结构,部分区域出现带孔球状突起;由图 1(c)可知,当 KMnO4浓度为 0.8 mol/L时,MnO2为花球状结构,较均匀地分布在石墨烯片层上且孔径较大;由图1(d)可知,当KMnO4浓度继续增加时,出现了较严重的团聚现象。这是因为石墨烯具有巨大的比表面积,为MnO2晶核的形成提供了大量的活性位点。氧化还原法制备的石墨烯表面含有部分含氧官能团,在酸性条件下,石墨烯表面的C元素与 KMnO4发生氧化还原反应〔7〕。当 KMnO4的量较少时,在石墨烯表面形成片状结构的MnO2。随着KMnO4浓度的增大,晶核过饱和,MnO2彼此团聚形成花球状结构。由于溶液中存在大量K+,花球状结构的MnO2能够稳定存在〔8〕。但是,当锰源的浓度过大时,反而会破坏石墨烯的碳骨架结构而降低材料的催化性能。催化材料的比表面积对其催化性能产生重要影响,较大的比表面积能够提供更多的反应位点,有利于催化反应的进行〔9〕。
MnO2/Gh-0.8的BET分析结果表明,MnO2/Gh-0.8具有较大的比表面积(40.75 m2/g),为亚甲基蓝的催化降解反应提供了较大的反应场所。
2.1.2 XRD和TGA分析
MnO2/Gh复合物的XRD见图2。

图2 MnO2/Gh复合物的XRD
由图2可知,MnO2/Gh-0.2中MnO2的衍射峰位置出现在 21.70°、37.13°、42.58°、56.56°,分别对应 γ-MnO2的(120)、(131)、(300)、(160)晶面〔10〕。γ-MnO2特征峰强度较弱且较宽,说明MnO2/Gh复合物结晶度较差〔11〕。石墨烯表面的MnO2是以一种无定形的非晶体状态存在,这与文献〔12〕报道的一致。MnO2/Gh-0.8、MnO2/Gh-1 中都出现了在 12.2°、24.3°、36.9°、65.9°的特征峰,与δ-MnO2相一致,分别对应MnO2的(001)、(002)、(111)、(020)晶面〔3,13〕。 而MnO2/Gh-0.5是2种晶型锰氧化物的混合物。随着锰源浓度的增加,石墨烯表面的γ-MnO2转变为δ-MnO2,并且衍射峰的强度相对增强,结晶度变好,有利于提高催化剂的催化活性。XRD图中并未出现石墨烯的衍射峰,可能是由于石墨烯的含量较低造成的,或者是石墨烯表面被 MnO2修饰〔8〕。
利用TGA研究了MnO2/Gh-0.8的热稳定性,结果表明,MnO2/Gh-0.8仅在40~200℃范围内发生了质量损失,主要是由于材料表面的物理吸附水和石墨烯表面剩余的含氧官能团的去除;在200~800℃内并没有质量损失,表明MnO2/Gh-0.8具有较高的热稳定性;过程中没有出现石墨烯燃烧而引起的质量损失,可能是因为石墨烯表面全部被MnO2覆盖,这与XRD的结果是一致的。
2.2 MnO2/Gh复合物-电Fenton体系对亚甲基蓝的处理效果分析
2.2.1 MnO2的晶型对亚甲基蓝降解的影响
实验过程中的电耗按照式(1)计算。

式中:W——电耗,kW·h/t;
I——电流值,A;
U——电压值,V;
0.9 ——交流电转换为直流电的效率;
V——处理废水的体积,L;
T——反应时间,h。
非均相电-Fenton的处理能力与材料的晶型直接相关,研究石墨烯片层上不同MnO2晶型对亚甲基蓝的降解具有重要意义,在电流密度为50 A/m2,电耗为12.8 kW·h/t时,考察MnO2晶型对亚甲基蓝降解和COD去除效果的影响,结果见图3。
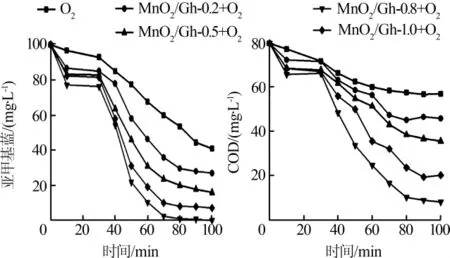
图3 MnO2晶型对亚甲基蓝降解和COD去除效果的影响
由图3可知,MnO2/Gh-0.8对亚甲基蓝的降解率高达100%,对COD的去除率为89.61%,分别比传统电催化高出40.99%和60.68%。反应前30 min为吸附阶段,亚甲基蓝的降解和COD的去除均不明显,该阶段主要取决于材料的比表面积和孔结构。而在电催化阶段,O2在阴极原位生成H2O2。当H2O2与MnO2共同存在时,H2O2参与 MnO2表面的 Mn3+和Mn4+的电子交换而分解产生了·OH,使得亚甲基蓝的降解效果变好,COD的去除率提高〔4〕。当反应70 min后,亚甲基蓝降解效果并不明显,这是因为反应时间过长会有电解水等副反应发生,因此确定反应时间为70 min。材料的晶型对其催化能力有很大的影响,δ-MnO2/Gh催化能力要优于γ-MnO2/Gh,这是因为石墨烯表面δ-MnO2的结晶度比γ-MnO2好,催化剂的结晶度会影响催化剂表面的离子空穴;δ-MnO2/Gh为花球状结构,特殊形貌使得活性位点暴露,为降解反应提供了更大的反应场所。
2.2.2 电流密度对亚甲基蓝废水COD去除效果的影响
考察电流密度对甲基蓝废水COD去除效果的影响,结果见图4。
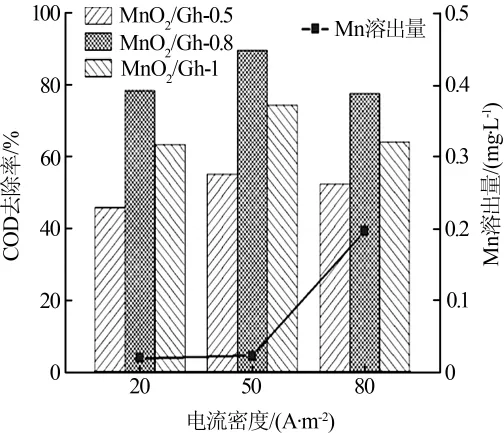
图4 电流密度对COD去除效果的影响
由图4可知,随着电流密度的增大,溶液的传质速率增大,反应强度增加,使得COD的去除率逐渐增大,当电流密度为50 A/m2时,MnO2/Gh-0.8非均相电-Fenton体系中COD的去除率达到最高。但是当电流密度过大时,降解效果反而降低,这是因为电流过大时,使得大量的锰元素溶出,导致了析氢析氧等副反应的发生,甚至在阴极附近处发生4e-的转移生成水,造成 H2O2的浓度降低〔14〕。
2.2.3 pH对亚甲基蓝废水COD去除效果的影响
pH对反应体系的影响主要体现在H2O2的稳定性和亚甲基蓝的吸附两方面。H2O2在pH为3时比较稳定,且随着pH的增大易分解为O2和H2O〔1〕。传统Fenton反应的pH控制在3左右,探究pH对亚甲基蓝降解的影响具有重要的意义。由于在不同pH条件下,溶液中的H+浓度发生变化,MnO2表面可能会发生去质子现象。而MnO2吸附主要是利用表面化学吸附水中—OH的H原子,使之与亚甲基蓝中的N原子结合,达到吸附亚甲基蓝的目的,使亚甲基蓝废水的COD降低〔15〕。此外,锰氧化物表面电荷发生变化也会对吸附产生影响。考察了pH对MnO2/Gh-0.8非均相电-Fenton体系去除COD效果的影响,结果见图5。
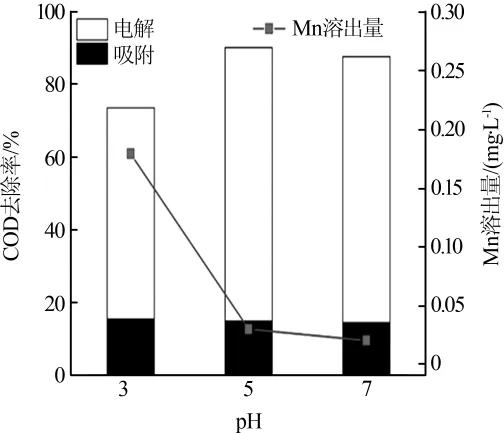
图5 初始pH对COD去除效果的影响
由图5可知,在吸附阶段,pH分别为3和5时COD的去除率仅与中性条件下相差2.95%和0.63%,可见在吸附阶段pH并非是影响去除效果的主要因素〔12〕。 在非均相电-Fenton过程中,O2在阴极还原为H2O2。在酸性条件下H2O2会比在中性条件下稳定,因而反应一段时间后,酸性水中的H2O2的累积量更高。然而体系在pH为3时,降解效果并不明显。这是由于复合材料中MnO2在该pH下表面有大量的锰溶出,使得非均相电-Fenton反应减弱造成的。由图5可见,该非均相电-Fenton反应最适pH范围为5~7。
2.3 反应机理分析
非均相电-Fenton体系的反应机理主要由表面吸附和催化氧化两部分组成,前者为后者奠定了基础。为了探究反应机理,向MnO2/Gh-0.8非均相电-Fenton体系中分别加入了叔丁醇和碘化物(I-)作为溶液和催化剂表面·OH的淬灭剂,考察其对该非均相体系去除 COD 效果的影响,结果见图 6(a)〔4〕。 另外,考察了在非均相电-Fenton体系下催化剂和气体种类对COD去除效果的影响,结果见图6(b)。
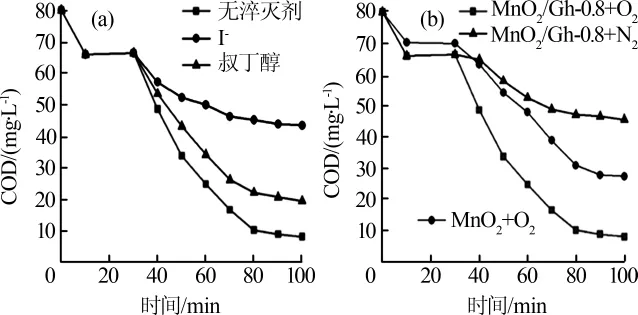
图6 淬灭剂、催化剂和气体种类对COD去除效果的影响
由图6(a)可知,加入叔丁醇的体系中,COD去除率发生轻微下降。而当体系中加入I-时,降解效果明显变差。结果表明,该反应主要是利用催化剂表面的·OH对亚甲基蓝的强氧化作用将其降解。
由图 6(b)可知,持续曝 O2时,在吸附阶段,MnO2/Gh-0.8非均相电-Fenton体系对COD的去除率比纯MnO2体系高出5.38%,这是由于MnO2/Gh-0.8具有巨大的比表面积,其吸附位点远多于纯MnO2。而电催化反应70 min后,MnO2/Gh-0.8体系对COD去除率比纯MnO2体系高出24.1%,原因可能在于石墨烯和MnO2存在协同作用;石墨烯提供了更多的活性位点能够加快界面电子的转移速率〔13〕。Fenton技术对污水的处理效果与H2O2的量是直接相关的。在电-Fenton阶段,O2体系对COD的去除率比N2体系高出45.0%,O2在阴极被还原为H2O2,MnO2/Gh-0.8具有较强催化H2O2的能力,实现了高效率的反应循环。在此体系下,TOC去除率高达72.2%,亚甲基蓝被有效矿化,彻底分解成CO2和H2O。
2.4 循环使用
为了评估复合材料MnO2/Gh-0.8的稳定性,进行了重复实验,结果见表1。

表1 MnO2/Gh-0.8的稳定性
由表1可知,第5次使用后COD去除率比第1次仅降低了6.37%,该催化剂仍具有较高的催化活性。MnO2的溶出量随着循环次数的增加而增加,尤其在循环5次后,Mn溶出明显,但仍符合污水排放标准。结果证明,该复合材料具有良好的循环稳定性。
3 结论
(1)由氧化还原法成功合成MnO2/Gh复合材料。利用SEM和XRD等表征表明,在制备过程中,锰源初始浓度会影响复合物的晶型和形貌。当浓度较低时,石墨烯表面生成γ-MnO2,随着浓度的增加,逐渐变为δ-MnO2,并且形貌由片状转变为花球状。且花球状的MnO2/Gh-0.8复合物具有一定的热稳定性。
(2)研究了 MnO2/Gh-H2O2非均相电-Fenton体系对亚甲基蓝的降解效果,并研究了其晶型、pH和电流密度等因素对降解效果的影响。结果表明,在非均相体系中,δ-MnO2/Gh的催化效果优于γ-MnO2/Gh。中性条件下,电流密度为50 A/m2时,MnO2/Gh-0.8非均相体系反应70 min后对亚甲基蓝的去除率可达100%,COD的去除率可达89.61%,与传统的电催化体系相比分别提高了约40.99%和60.68%。该非均相电-Fenton体系最佳适用pH为5~7。该反应主要发生在催化剂的表面,在循环使用5次后催化效果仅下降了6.37%,表明该催化剂具有较高的稳定性。
