植物内生真菌Penicillium tropicum发酵产物中化学成分及其抑菌活性研究
2020-05-22贾少杰戴好富解修超曾艳波
吕 妍, 贾少杰, 戴好富, 解修超, 曾艳波
(1.陕西理工大学 生物科学与工程学院, 陕西 汉中 723000;2.海南省海洋生物资源功能性成分研究与利用重点实验室, 海南 海口 571101;3.中国热带农业科学院 热带生物技术研究所, 海南 海口 571101)
植物内生真菌是指在植物寄主中度过全部或近乎全部生活周期而不使寄主表现任何症状的一类真菌[1]。近年来人们对它的研究逐渐深入。植物内生真菌代谢产生结构新颖、生物活性较好的化合物总数远高于土壤微生物[2],这主要是因为植物内生真菌种类和数量多、生存环境多样化。它的次生代谢产物普遍具有抗菌、抗病毒、抗肿瘤以及抗心血管疾病等活性[3]。1929年,从青霉属(Penicillium)真菌中分离出对多种病原菌具有极强抑制作用的化合物青霉素开始,人们对青霉属真菌的研究从未停止。青霉属是一类主要营腐生生活的较为多样和常见的真菌[4]。目前,从青霉属真菌中已经分离出1300种不同的代谢产物[5]。本研究是从青霉属植物内生真菌Penicilliumtropicum(KU641695)中分离纯化出5个化合物,鉴定其结构,并对抑菌活性进行测试。
1 实验器材
1.1 实验仪器、试剂
核磁共振仪Bruker AV-500 (Bruker,German);柱层析硅胶(Qingdao Haiyang Chemical Co.,Ltd.);薄层层析硅胶板GF254(Qingdao Haiyang Chemical Co.,Ltd.);20~45 μm ODS(Fuji Silysia Chemical Co.,Ltd.);Sephadext LH-20(Merck Co.Ltd.);薄层层析硅胶H(Qingdao Haiyang Chemical Co.,Ltd.);马铃薯葡糖液体培养基(马铃薯200.0 g、葡萄糖20.0 g、pH自然);大米固体发酵培养基(大米100.0 g、水150.0 mL、pH自然);实验所用试剂均为市售分析纯。
1.2 实验菌株
植物内生真菌Penicilliumtropicum分离自植物Sapiumellipticum的新鲜叶片、金黄色葡萄球菌(Staphylococcusaureus)。现保藏于中国热带农业科学院热带生物技术研究所B502室。
2 实验方法
2.1 内生真菌的发酵
以大米固体培养基对目标菌种进行大规模发酵培养。待马铃薯葡萄糖肉汤培养基(PDB)中长满菌丝球时,在无菌操作台中,用5.0 mL移液枪吸取10.0 mL种子液接入大米固体培养基中(已灭菌,每瓶大米用量100.0 g),接40瓶,室温下静置培养35 d。将接有内生真菌种子液的40瓶大米固体培养基,在无菌环境中,28 ℃静置培养,期间每隔2 d观察真菌菌丝体生长情况,有无污染。35 d后菌丝体均匀分布于大米表面且长透大米培养基,发酵结束。
2.2 代谢产物的提取与分离
真菌固体发酵结束后,使用乙酸乙酯过夜浸泡发酵物(每个三角瓶中加入400.0 mL),超声30 min,过滤并收集滤液,重复3次,合并滤液并减压浓缩得到粗提物。向粗提物中加入适量蒸馏水溶解样品,随后加入等体积的乙酸乙酯,用分液漏斗连续萃取3次,合并乙酸乙酯萃取物,减压浓缩至无溶剂味,得到乙酸乙酯萃取物56.5 g。将乙酸乙酯萃取物采用减压柱(硅胶H)进行粗划段,使用氯仿-甲醇为洗脱溶剂进行梯度洗脱,得到10个馏分Fr.A—J。Fr.C馏分经葡聚糖凝胶柱色谱(甲醇)划分为4个小馏分Fr.C1—C4,其中,Fr.C1经硅胶柱色谱(氯仿-甲醇,20∶1)得到单体化合物(1);Fr.C3经硅胶柱色谱(氯仿-甲醇,10∶1)和半制备高效液相色谱分离出化合物(2);Fr.C4经半制备高效液相色谱分离出化合物(3);Fr.F经葡聚糖凝胶(氯仿-甲醇,1∶1),得到7个馏分Fr.F1—F7,Fr.F3经过(石油醚-氯仿,10∶1)分离得到化合物(4);Fr.F5经(石油醚-乙酸乙酯,10∶1)柱色谱和半制备高效液相色谱(C18色谱柱,甲醇-水,80∶20)得到化合物(5)。化合物(1)—(5)的结构如图1所示。
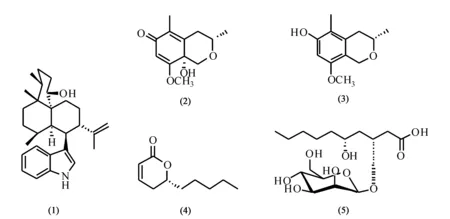
图1 化合物(1)—(5)的结构
2.3 抑菌活性测定
采用微量稀释法测定样品的抑菌活性。化合物溶于DMSO,母液浓度为2.56 mg/mL,用微量肉汤稀释法测定化合物的最低抑菌浓度(MIC)。具体步骤如下:从新鲜活化的平板上挑取单克隆菌落至新鲜TSB培养基,于摇床37 ℃、250 rpm/min培养至对数生长期;测定菌液OD值后,用MHB培养基稀释至约5×105CFU/mL;稀释好的菌液分装至96孔板中,第一列每孔190.0 μL,其余每孔加100.0 μL;加化合物10.0 μL至第一列孔中,用排枪充分混匀后进行2倍倍比稀释,使化合物浓度范围在0.125~128.0 μg/mL;稀释完成后,用封口膜封闭好96孔板,放置于37 ℃培养箱静置培养24 h;24 h后观察结果,记录MIC值(最低抑菌浓度),MIC以肉眼观察时能够完全抑制细菌生长所需的最低药物浓度为准;以盐酸万古霉素作为阳性对照,同时包括DMSO生长对照、培养基对照。
3 实验结果及活性测试
3.1 菌株的代谢产物
化合物(1):无色针状结晶,溶于氯仿;分子式C28H39NO,ESI-MSm/z:406[M+H]+;1H NMR(500 MHz,DMSO-d6)δ(ppm):7.39(1H,d,J=7.8 Hz,H-5),7.31(1H,d,J=8.0 Hz,H-8),7.08(1H,d,J=2.1 Hz,H-2),7.03(1H,t,J=7.5 Hz,H-7),6.97(1H,t,J=7.4 Hz,H-6),4.82(1H,d,J=1.8Hz,H-25),4.65(1H,brs,H-19),4.59(1H,brs,H-25),3.60(1H,dd,J=13.0,5.2 Hz,H-10),3.13(1H,dt,J=12.6,5.8 Hz,H-23),2.48(1H,m,H-12),2.07(1H,m,H-21),2.06(1H,m,H-16),2.01(1H,m,H-18),1.86(1H,dq,J=13.2,4.6 Hz,H-22),1.74(1H,m,H-18),1,74(H,m,H-17),1.64(1H,dt,J=13.1,4.6 Hz,H-21),1.57(1H,m,H-22),1.54(1H,m,H-13),1.49(1H,m,H-14),1.46(3H,s,H-26),1.25(1H,m,H-17),1.22(3H,d,J=7.0 Hz,H-27),1.21(1H,m,H-12),1.09(1H,d,J=13.7 Hz,H-14),0.92(3H,s,H-29),0.81(1H,d,J=13.2 Hz,H-13);13C NMR(125 MHz,DMSO-d6)δ(ppm):123.4(C-2),114.8(C-3),127.0(C-4),117.4(C-5),118.2(C-6),120.6(C-7),111.5(C-8),135.9(C-9),34.0(C-10),38.1(C-11),31.0(C-12),30.1(C-13),27.9(C-14),38.9(C-15),29.4(C-16),25.3(C-17),28.7(C-18),66.2(C-19),43.4(C-20),24.2(C-21),27.1(C-22),42.8(C-23),150.0(C-24),111.0(C-25),18.2(C-26),21.6(C-27),15.9(C-28),18.2(C-29)。
以上化合物(1)波谱数据与Petersen L M等[6]报道的数据基本一致。因此,将化合物(1)鉴定为epi-10,23-dihydro-24,25-dehydroaflavinine。
化合物(2):淡黄色固体,溶于甲醇;分子式C12H16O4,ESI-MSm/z:225[M+H]+;1H NMR(500 MHz,CD3OD)δ(ppm):5.60(1H,s,H-7),4.45(1H,m,H-3),3.98(1H,d,J=11.9 Hz,H-1),3.78(3H,s,H-13),3.54(1H,d,J=11.9 Hz,H-1),3.07(1H,dd,J=13.5,6.2 Hz,H-4),2.57(1H,brd,J=13.5 Hz,H-4),1.86(3H,d,J=1.4 Hz,H-12),1.12(3H,d,J=6.8 Hz,H-11);13C NMR(125 MHz,CD3OD)δ(ppm):188.6(C-6),176.5(C-8),149.2(C-10),131.0(C-5),101.9(C-7),72.9(C-3),70.2(C-9),70.1(C-1),56.7(C-13),33.4(C-4),16.4(C-11),10.8(C-12)。
以上化合物(2)数据与Zeng Y B等[7]报道的数据基本一致。因此,将化合物(2)鉴定为penitropone。
化合物(3):黄色结晶,溶于氯仿;分子式C12H16O4,ESI-MSm/z:209[M+H]+;1H NMR(500 MHz,CDCl3)δ(ppm):6.23(1H,s,H-7),4.89(1H,d,J=15.1 Hz,H-1β),4.57(1H,d,J=15.1 Hz,H-1α),3.74(1H,m,H-3),3.68(3H,s,H-11),2.61(1H,brd,J=16.5 Hz,H-4β),2.43(1H,dd,J=16.7,10.6 Hz,H-4α),2.04(3H,s,H-10),1.38(3H,d,J=6.2 Hz,H-9);13C NMR(125 MHz,CDCl3)δ(ppm):64.8(C-1),70.8(C-3),34.2(C-4),134.2(C-4a),113.0(C-5),152.8(C-6),96.2(C-7),154.0(C-8),115.4(C-8a),21.8(C-9),10.2(C-10),55.2(C-11)。
以上化合物(3)数据与Smetanina O F等[8]报道的数据基本一致。因此,将化合物(3)鉴定为:(3S)-3,5-dimethyl-8-methoxy-3,4-dihydro-1H-isochromen-6-ol。
化合物(4):淡黄色油状,溶于氯仿;分子式C10H16O2,ESI-MSm/z:169[M+H]+;1H NMR(500 MHz,CDCl3)δ(ppm):6.86(1H,ddd,J=9.5,5.4,3.0 Hz,H-3),6.00(1H,ddd,J=9.8,2.0,1.5 Hz,H-2),4.41(1H,m,H-5),2.32(2H,m,H-4),1.78(1H,m,H-6),1.63(1H,m,H-6),1.51(1H,m,H-7),1.40(1H,m,H-7),1.31(2H,m,H-9),1.30(2H,m,H-8),0.88(3H,t,J=6.8 Hz,H-10);13C NMR(125 MHz,CDCl3)δ(ppm):164.8(C-1),145.2(C-3),121.6(C-2),78.2(C-5),35.0(C-6),31.6(C-8),29.5(C-4),24.6(C-7),22.6(C-9),14.1(C-10)。
以上化合物(4)波谱数据与Carosi L等[9]报道的数据基本一致。因此,将化合物(4)鉴定为:
(-)-massoialactone。
化合物(5):黄色膏状,溶于甲醇;分子式C16H30O9,ESI-MSm/z:367[M+H]+;1H NMR(500 MHz,CD3OD)δ(ppm):4.69(1H,m,H-3),4.66(1H,brs,H-1′),4.41(1H,m,H-5),3.87(1H,dd,J=11.8,2.4 Hz,H-6′),3.83(1H,d,J=3.3 Hz,H-2′),3.70(1H,dd,J=11.8,6.2 Hz,H-6′),3.53(1H,t,J=9.5 Hz,H-4′),3.45(1H,dd,J=9.5,3.2 Hz,H-3′),3.23(1H,ddd,J=9.1,6.3,2.2 Hz,H-5′),2.87(1H,ddd,J=18.0,3.2,1.8 Hz,H-2),2.77(1H,dd,J=17.9,4.9 Hz,H-2),2.15(1H,m,H-6),1.75(1H,m,H-6),1.65(1H,m,H-4),1.54(1H,m,H-7),1.44(1H,m,H-7),1.35(2H,m,H-8),1.35(2H,m,H-9),0.93(2H,t,J=6.8 Hz,H-10);13C NMR(125 MHz,CD3OD)δ(ppm):173.7(C-1),37.8(C-2),78.0(C-3),36.6(C-4),70.8(C-5),33.7(C-6),25.6(C-7),32.8(C-8),23.6(C-9),14.4(C-10),100.2(C-1′),72.7(C-2′),75.2(C-3′),68.5(C-4′),78.4(C-5′),62.9(C-6′)。
以上化合物(5)波谱数据与Dang Q L等[10]报道的数据基本一致。因此,将化合物(5)鉴定为:(3R,5R)-3-O-β-D-mannosyl-3,5dihydroxydecanoic acid。
3.2 抗菌活性检测
采用微量稀释法对化合物(1)—(5)的抑菌活性进行检测,以盐酸万古霉素作为阳性对照(见表1)。化合物(1)对金黄色葡萄球菌USA300具有抑制活性,MIC为2.0 μg·mL-1,化合物(2)、(3)、(4)和(5)没有抑制活性。

表1 化合物(1)—(5)对金黄色葡萄球菌USA300的抑制活性
4 结论讨论
本研究从植物内生真菌Penicilliumtropicum的发酵产物中共分离鉴定5个化合物:epi-10,23-dihydro-24,25-dehydroaflavinine (1)、Penitropone (2)、(3S)-3,5-dimethyl-8-methoxy-3,4-dihydro-1H-isochromen-6-ol (3)、(-)-massoialactone (4)和(3R,5R)-3-O-β-D-mannosyl-3,5-dihydroxydecanoic acid (5)。并对以上5个化合物进行了抑菌活性测试,结果表明化合物(1)对金黄色葡萄球菌USA300具有抑制活性,MIC为2.0 μg·mL-1。化合物(1)为吲哚二萜类化合物,吲哚二萜类化合物具有多种生物活性,如杀虫、抗MRSA、阻断离子通道等[11]。因此,化合物(1)的生物活性值得更加深入的研究。
