响应面分析优化荧光衍生法测定硫熏党参及其饮片二氧化硫残留量的研究
2020-05-21,*
,*
(1.甘肃中医药大学药学院,甘肃兰州 730000; 2.中国科学院兰州化学物理研究所,甘肃兰州 730000)
党参为桔梗科植物党参(Codonopisispilosula(Franch.)Nannf.)、素花党参(CodonopisispilosulaNannf.var.modesta(Nannf.)L. T. Shen)或川党参(CodonopisispilosulaOliv.)的干燥根,具有健脾益肺、养血生津的功效,用于脾肺气虚、食少倦怠、咳嗽虚喘、气血不足、面色萎黄、心悸气短、津伤口渴、内热消渴等症[1]。2018年国家卫健委将党参列入药食同源目录[2],其具有增强人体免疫功能、耐疲劳、降血压、抗溃疡等保健作用,可用于开发保健产品[3]。由于其含糖量较高,在贮藏过程中易生虫和霉变,因此在产地加工中常使用硫磺熏蒸。硫熏作为一种传统的产地加工方法,在中药材的加工和贮藏中有重要的作用,但过度硫熏严重影响中药材的品质和药效[4-8]。近些年报道,中药材中的SO2残留物有神经系统、呼吸系统、心血管系统、消化系统等方面的毒性[9]。2015版药典中收载的酸碱滴定法、气相色谱法和离子色谱法分别作为SO2测定的第一法、第二法和第三法[1],但存在前处理繁琐和操作复杂等问题。亚硫酸盐可与邻苯二甲醛溶液和乙酸铵溶液反应生成荧光化合物1-磺酸基-异吲哚,其荧光强度与亚硫酸盐的浓度成正比[10-13],根据此原理Peng等[14]建立了荧光衍生法用于检测山药中SO2的残留量,此外还有荧光衍生法检测人参及浙贝母SO2残留量研究的报道[15-16],结果均表明荧光衍生法具有操作简单、灵敏度高等优点。
本实验以荧光强度为指标,用响应面法对磷酸氢二钠-磷酸二氢钾缓冲溶液pH及其用量、邻苯二甲醛用量及乙酸铵浓度四个影响荧光强度的因素进行优化,确定最佳荧光衍生条件,建立荧光衍生法检测党参SO2残留量的方法;将党参硫熏不同时间,并加工炮制为不同规格饮片,测定SO2残留量,研究硫熏时间及加工炮制对党参SO2残留量的影响。
1 材料与方法
1.1 材料与仪器
党参药材 采自甘肃省陇西县双泉镇何家沟村,经甘肃中医药大学杨扶德教授鉴定为桔梗科植物党参(Codonopisispilosula(Franch.)Nannf.);蜂蜜 桂林周氏顺发食品有限公司;亚硫酸钠 天津市科密欧化学试剂有限公司;乙酸铵 上海三友试剂厂;邻苯二甲醛 上海中秦化学试剂有限公司;磷酸氢二钠 天津市科密欧化学试剂有限公司;磷酸二氢钾 西陇化工股份有限公司;无水乙醇 天津医药化学有限公司;以上试剂 均为分析纯。
Fluorolog-3稳态/瞬态荧光光谱仪 HORIBA公司;元素型1860d超纯水机 上海摩勒科学仪器有限公司;WB-2000型恒温水浴锅 郑州长城科工贸有限公司;H1650台式高速离心机 长沙湘仪离心机仪器有限公司;FW100型高速万能粉碎机 天津市泰斯特仪器有限公司。
1.2 实验方法
1.2.1 样品处理 将党参药材硫熏后,加工炮制为节子货、厚片[17]、米炒[18]、蜜制[19]四个规格的饮片,晾干后用密封袋密封,置阴凉处保存,用时将样品粉碎,取过40目筛的粉末测定二氧化硫残留量。
1.2.1.1 硫熏党参原药材制备 将党参药材用硫磺分别熏蒸0、30、60、90 min(硫磺∶药材=1∶150)后晾干备用。
1.2.1.2 饮片样品制备 将硫熏党参原药材用少量清水闷湿后,切制成为0.2~0.4 cm的厚片和5~6 cm的节子货,晾干;蜜制党参:炼蜜:蜂蜜用量为25%,称取蜂蜜于炒制容器中,武火加热烧开后,加入蜂蜜用量三分之一的热水,小火烧开即可;闷润:将炼蜜加入党参厚片,搅拌均匀,过夜,使蜂蜜被完全吸收;炒制:将炒制容器预热后,倒入闷润后的党参片,文火加热,炒制表面黄棕色,不粘手时取出放凉,即可;米炒党参:将大米置预热的炒制容器内,用量为党参25%,用中火加热炒至冒烟时,投入党参厚片拌炒,至党参表面呈黄色,米呈焦黄时,取出,筛去米,放凉。
1.2.2 供试品溶液制备 称取硫熏党参药材或其饮片样品粉末1.0 g于100 mL锥形瓶中,加入0.7%的NaOH溶液40 mL,超声提取30 min,8000 r/min离心3 min,取上清液1.0 mL定容于25 mL容量瓶即得[15]。
1.2.3 衍生化溶液制备 参考文献[14]方法,取1 μg/mL亚硫酸钠对照品溶液或供试品溶液于10 mL容量瓶中,依次加入磷酸氢二钠-磷酸二氢钾缓冲溶液、1 mmol/L邻苯二甲醛溶液及乙酸铵溶液,用水定容至刻度,水浴反应后静置,即得衍生化溶液。
1.2.4 激发与发射波长确定 取亚硫酸钠对照品溶液,按“1.2.3”项下方法制备衍生化溶液,用Fluorolog-3稳态/瞬态荧光光谱仪扫描激发和发射波长。
1.2.5 荧光衍生条件优化单因素实验 考察磷酸氢二钠-磷酸二氢钾缓冲溶液pH与用量、邻苯二甲醛溶液用量、乙酸铵溶液浓度与用量、反应温度、反应时间及静置时间对荧光强度的影响[20-23]。
1.2.5.1 缓冲溶液pH考察 于10 mL容量瓶中加入亚硫酸钠对照品溶液0.5 mL,分别加入pH为5.8、6.0、6.2、6.3、6.4、6.5、6.6、6.7、6.8、6.9的磷酸氢二钠-磷酸二氢钾缓冲溶液2 mL、邻苯二甲醛溶液2 mL和5 mmoL/L的乙酸铵溶液2 mL,用蒸馏水定容,50 ℃水浴反应5 min,冷却后静置50 min,检测荧光其强度。
1.2.5.2 缓冲溶液用量考察 在磷酸氢二钠-磷酸二氢钾缓冲溶液pH为6.6,其它条件不变的情况下,考察磷酸氢二钠-磷酸二氢钾缓冲溶液用量分别为0.5、1.0、1.5、2.0、2.5、3.0 mL时对荧光强度的影响。
1.2.5.3 邻苯二甲醛用量考察 pH为6.6的磷酸氢二钠-磷酸二氢钾缓冲溶液用量1.5 mL,其它条件不变的情况下,考察邻苯二甲醛溶液用量分别为0.5、1.0、1.5、2.0、2.5、3.0、3.5 mL对荧光强度的影响。
1.2.5.4 乙酸铵浓度考察 pH为6.6的磷酸氢二钠-磷酸二氢钾缓冲溶液用量1.5 mL,邻苯二甲醛溶液用量2 mL,其它条件不变的情况下,考察浓度为0.5、1.0、2.5、5.0、7.5、10.0、15.0 mmoL/L的乙酸铵溶液对荧光强度的影响。
1.2.5.5 乙酸铵用量考察 pH为6.6的磷酸氢二钠-磷酸二氢钾缓冲溶液用量1.5 mL,邻苯二甲醛溶液用量2 mL,其它条件不变的情况下,考察5 mmol/L乙酸铵溶液用量分别为0.5、1.0、1.5、2.0、2.5、3.0、3.5 mL对荧光强度的影响。
1.2.5.6 反应温度对荧光强度的影响 pH为6.6的磷酸氢二钠-磷酸二氢钾缓冲溶液用量1.5 mL,邻苯二甲醛溶液用量2 mL,5 mmoL/L的乙酸铵溶液用量2 mL,其它条件不变,分别考察水浴温度为30、35、40、45、50、55、60 ℃对荧光强度的影响。
1.2.5.7 反应时间对荧光强度的影响 pH为6.6的磷酸氢二钠-磷酸二氢钾缓冲溶液用量1.5 mL,邻苯二甲醛溶液用量2 mL、5 mmoL/L的乙酸铵溶液用量2 mL,其它条件不变,分别考察50 ℃水浴反应1、3、5、7、10、13、15 min对荧光强度的影响。
1.2.5.8 静置时间对荧光强度的影响 pH为6.6的磷酸氢二钠-磷酸二氢钾缓冲溶液用量1.5 mL,邻苯二甲醛溶液2 mL,5 mmoL/L的乙酸铵溶液用量2 mL,50 ℃下水浴反应5 min,分别考察静置5、10、15、20、25、30、40、50、60、70、80、90、100、110、120 min对荧光强度的影响。
1.2.6 响应面优化试验 为得到最佳荧光衍生条件,在单因素实验的基础上,参考文献[15]采用响应面分析法研究磷酸氢二钠-磷酸二氢钾缓冲溶液pH(A)及其用量(B)、邻苯二甲醛用量(C)及乙酸铵浓度(D)四个因素对荧光强度的影响。根据Box-Behnken实验设计原理,取单因素实验最优结果为中心,上下各取一水平作为响应面设计因素水平[24-25],用Design-Expert 10.0设计实验,实验因素及水平见表1。
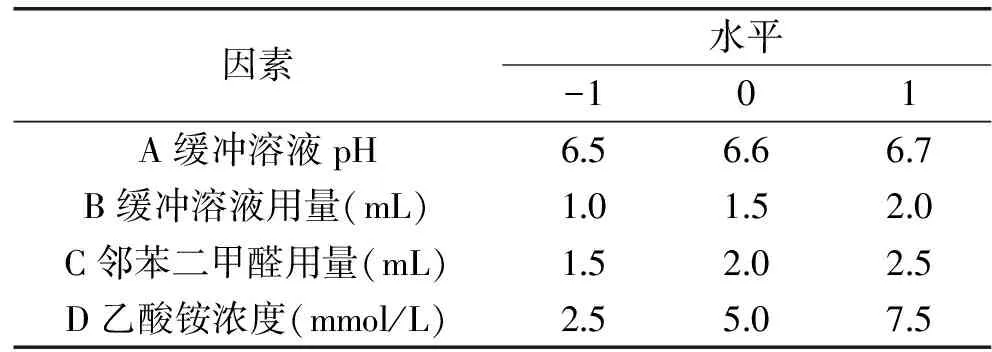
表1 Box-Behnken实验设计因素及水平Table 1 Factors and levels of the Box-Behnken design
1.2.7 方法学考察
1.2.7.1 线性关系及检测限考察 精密吸取亚硫酸钠对照品溶液0.1、0.2、0.4、0.6、0.8、1.0、1.2、1.5、2.0 mL于10 mL容量瓶中,根据优化后的衍生条件制备衍生化溶液,测定荧光强度,以亚硫酸钠浓度与荧光强度绘制标准曲线,并对其检测限进行考察(检测限=3σ/k,σ为空白测量的标准差,k为标准曲线斜率)。
1.2.7.2 精密度试验 取硫熏90 min党参样品粉末,平行制备供试品溶液3份,衍生后连续测定6次,计算SO2残留量RSD值。
1.2.7.3 重复性试验 取硫熏90 min的党参原药材粉末,平行制备供试品溶液6份,衍生化后检测SO2残留量,计算RSD值。
1.2.7.4 稳定性试验 取硫熏90 min的党参原药材粉末,按“1.2.2”项下方法平行制备供试品溶液3份,分别在0、0.5、1、1.5、2、2.5、3 h测定荧光强度,计算SO2残留量RSD值。
1.2.7.5 加样回收试验 称取硫熏30 min的党参原药材(编号1、2、3)与米炒(编号4、5、6)、蜜制(编号7、8、9)饮片粉末各3份,分别加入浓度为120 μg/mL的亚硫酸钠对照品溶液0.8、1.0与1.2 mL,按“1.2.2”项下方法制备供试品,衍生后测荧光强度,计算回收率。

1.2.8 样品测定 取硫熏党参原药材及其饮片样品粉末,按“1.2.2”项下供试品制备方法制备供试品溶液,衍生后测定荧光强度,计算SO2残留量。酸碱滴定法测定方法参照《中国药典》2015版第四部通则目次“2331项”二氧化硫检测方法[1]检测SO2残留量。其中荧光衍生法测得最终结果为亚硫酸钠的含量,将亚硫酸钠折算为SO2,计算公式:
试中:c为供试品溶液衍生化后测得的亚硫酸钠浓度,μg/mL;10为溶液体积,mL;1000为供试品稀释倍数;0.5075为每g亚硫酸钠相当的SO2的质量;m为供试品的质量,g。
1.3 数据处理
实验数据以平均值(Mean)±标准差(SD)表示,应用SPSS 22.0软件进行单因素方差分析(ANOVA),P<0.05认为具有显著差异。
2 结果与分析
2.1 激发发射波长
激发与发射波长扫描结果见图1,激发波长(λEx)为320 nm,发射波长(λEm)为385 nm,最终确定测定衍生溶液荧光强度的条件为λEx/λEm=320/385。
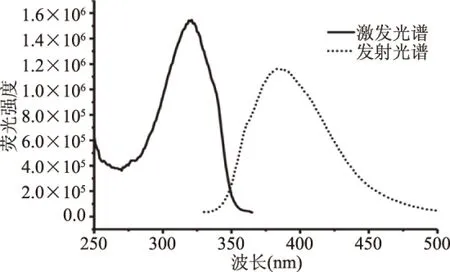
图1 激发发射图谱Fig.1 Excitation and emission spectrum
2.2 单因素实验结果
2.2.1 缓冲溶液pH对荧光强度的影响 由图2可知,随磷酸氢二钠-磷酸二氢钾缓冲溶液pH的增大,荧光强度先增大后减小,pH为6.6时荧光强度为681755.24,此时荧光强度最大。根据方差分析结果可得pH6.6与pH6.5、6.7对荧光强度的影响有显著性差异(P<0.05),因此选择磷酸氢二钠-磷酸二氢钾缓冲溶液最佳pH为6.6。

图2 磷酸氢二钠-磷酸二氢钾缓冲溶液pH对荧光强度的影响Fig.2 Effect of pH of disodium hydrogen phosphate-potassiumdihydrogen buffer solution on the fluorescence intensity注:不同小写字母代表差异显著(P<0.05);图3~9同。
2.2.2 缓冲溶液用量对荧光强度的影响 由图3可知,随磷酸氢二钠-磷酸二氢钾缓冲溶液用量的增加,荧光强度先增大后减小,磷酸氢二钠-磷酸二氢钾缓冲溶液用量为1.5 mL时,荧光强度最大,为674537.77。根据方差分析结果,磷酸氢二钠-磷酸二氢钾缓冲溶液用量1.5 mL与用量1.0和2.0 mL对荧光强度的影响有显著差异(P<0.05),因此选择磷酸氢二钠-磷酸二氢钾缓冲溶液最适用量为1.5 mL。
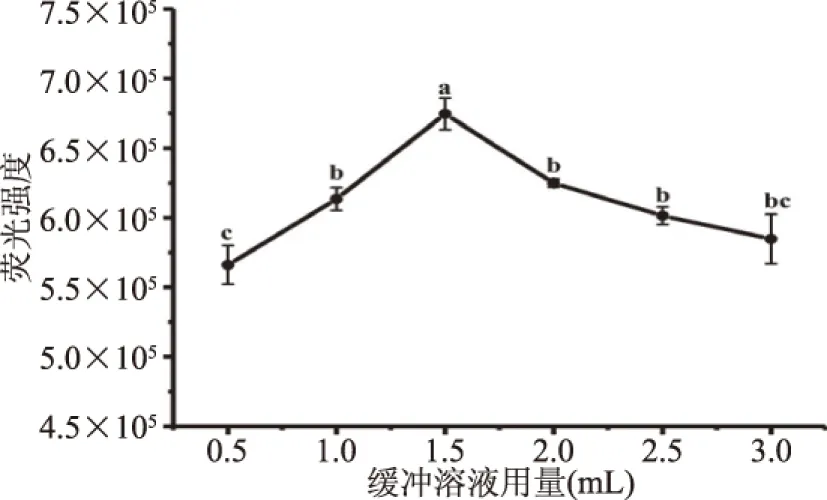
图3 磷酸氢二钠-磷酸二氢钾缓冲溶液用量对荧光强度的影响Fig.3 Effect of dosage of disodium hydrogenphosphate-potassium dihydrogen buffersolution on the fluorescence intensity
2.2.3 邻苯二甲醛用量对荧光强度的影响 由图4可得,随邻苯二甲醛用量的增加,荧光强度先增大后减小,当邻苯二甲醛溶液用量为2.0 mL时,荧光强度最大,为589218.52。邻苯二甲醛溶液用量2.0 mL与用量1.5和2.5 mL对荧光强度的影响有显著差异(P<0.05),因此选择邻苯二甲醛最适用量为2.0 mL。

图4 邻苯二甲醛用量对荧光强度的影响Fig.4 Effect of dosage of o-phthalaldehydesolution on the fluorescence intensity
2.2.4 乙酸铵浓度对荧光强度的影响 由图5可知,随乙酸铵浓度的增大,荧光强度先增大后减小,当乙酸铵浓度为5 mmol/L时,荧光强度最大,为776035.51。乙酸铵浓度为5 mmol/L与浓度为2.5和7.5 mmol/L对荧光强度的影响有显著性差异(P<0.05),因此选择乙酸铵最适浓度为5 mmol/L。

图5 乙酸铵浓度对荧光强度的影响Fig.5 Effect of ammonium acetate concentrationon the fluorescence intensity
2.2.5 乙酸铵用量对荧光强度的影响 由图6可知,随乙酸铵用量的增加,荧光强度先增大后减小,当乙酸铵用量为2.0 mL时,荧光强度最大,为616380.16,。根据方差分析,乙酸铵用量2.0、1.5 mL对荧光强度的影响无显著差异(P>0.05),根据荧光强度测定结果最终选择乙酸铵用量为2.0 mL。

图6 乙酸铵用量对荧光强度的影响 Fig.6 Effect of ammonium acetate dosageon the fluorescence intensity
2.2.6 反应温度对荧光强度的影响 由图7可知,随反应温度的升高,荧光强度先增大后减小,当反应温度为50 ℃时,荧光强度最大,为768253.66。根据方差分析,反应温度为50 ℃与45、55 ℃时的荧光强度之间无显著性差异(P>0.05),根据荧光强度测定结果选择反应温度为50 ℃。

图7 反应温度对荧光强度的影响Fig.7 Effect of reaction temperatureon the fluorescence intensity
2.2.7 反应时间对荧光强度的影响 由图8可知,随反应时间延长,荧光强度先增大后减小,反应时间为5 min时,荧光强度最大,为748425.61。反应5 min与反应3、7 min时的荧光强度之间无显著性差异(P>0.05),根据荧光强度测定结果选择反应时间为5 min。
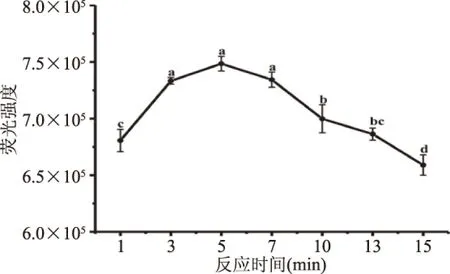
图8 反应时间对荧光强度的影响Fig.8 Effect of reaction timeon the fluorescence intensity
2.2.8 静置时间对荧光强度的影响 由图9可知,随静置时间的增长,荧光强度逐渐降低,在40~120 min之间其荧光强度降低了4.28%,变化较小。根据方差分析,静置40、50 min时荧光强度之间无显著性差异(P>0.05),从时间角度考虑选择静置时间为40 min。

图9 静置时间对荧光强度的影响Fig.9 Effect of static reaction timeon the fluorescence intensity
2.3 响应面优化试验结果
2.3.1 响应面结果及方差分析 响应面试验设计方案及结果见表2,用Design-Expert 10.0对结果分析,方差分析见表3,由表3可知回归模型极显著(P<0.01),表明该回归模型有意义;模型R2=0.9691,说明该模型可解释绝大部分实验数据,失拟项P>0.05,无显著差异,表明拟合度良好。从表3中可知,模型中一次项A不显著(P>0.05),B、D极显著(P<0.01),C显著(P<0.05),二次项中A2、B2、C2均极显著(P<0.01),D2不显著(P>0.05),交互作用均不显著(P>0.05)。得到磷酸氢二钠-磷酸二氢钾缓冲溶液pH(A)、磷酸氢二钠-磷酸二氢钾缓冲溶液用量(B)、邻苯二甲醛溶液用量(C)及乙酸铵浓度(D)与反应体系荧光之间的回归方程为:
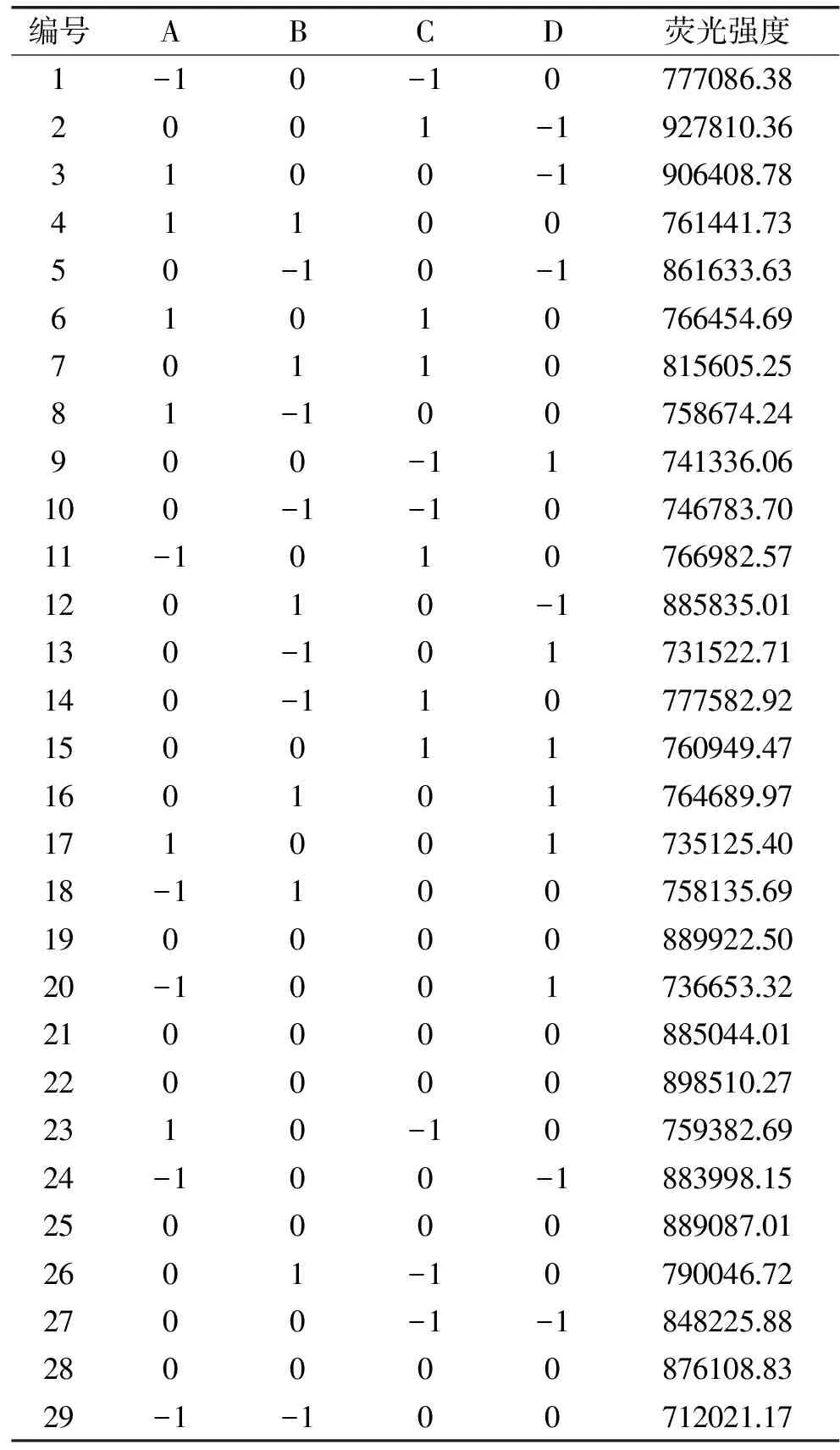
表2 响应面试验设计及结果Table 2 Design and results of response surface experiment
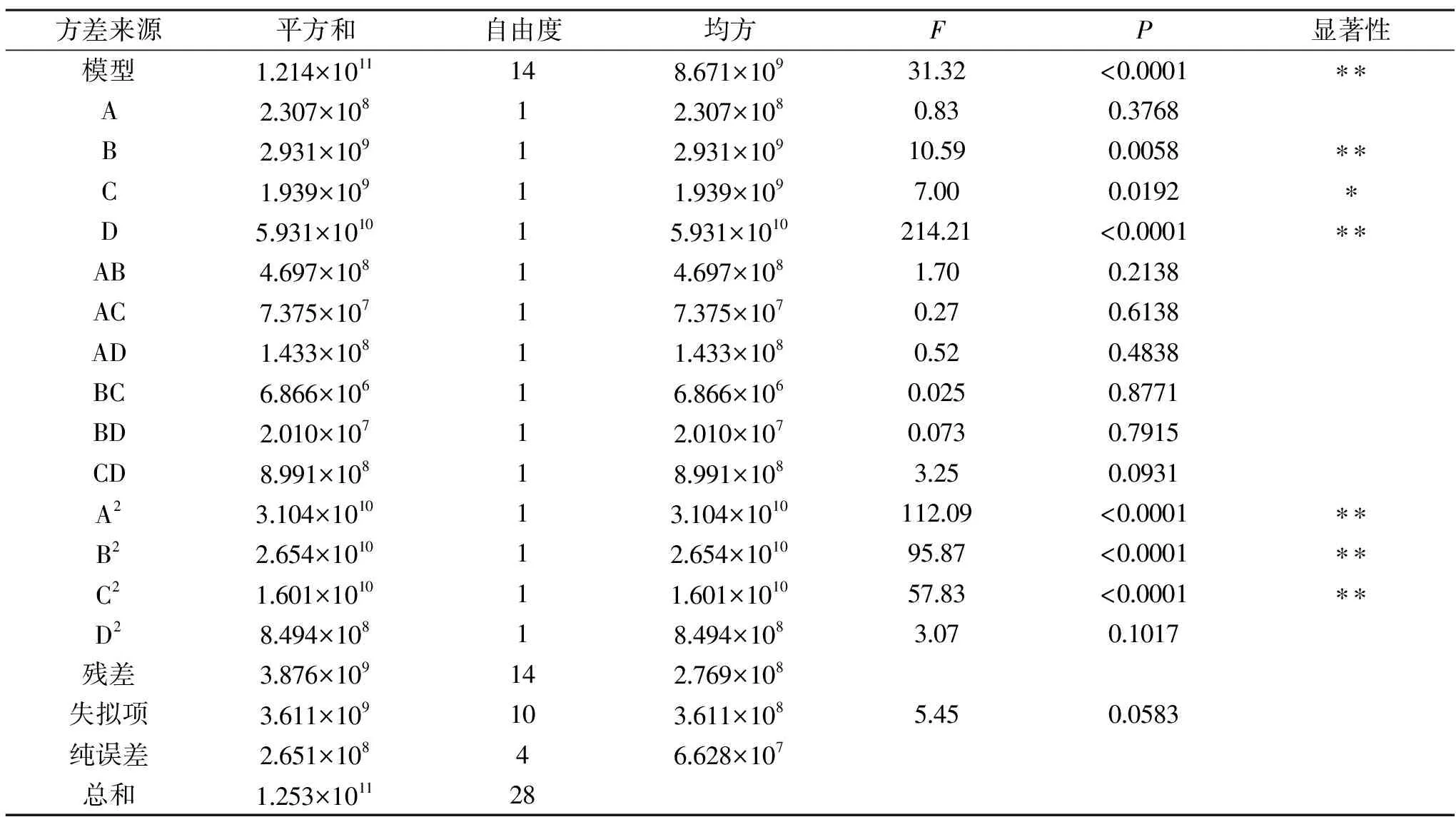
表3 方差分析结果Table 3 Results of variance analysis
R1=8.877E+005+4384.21A+15628.02B+12710.29C-70302.88D-10836.69AB+4293.95AC-5984.64AD-1310.17BC+2241.47BD-14992.68CD-69171.06A2-63970.07B2-49685.91C2-11443.15D2。
2.3.2 响应面分析 响应面的坡度越大,表明因素对响应值的影响越大;响应面坡度越小,表明因素改变对响应值的影响也越小[26]。磷酸氢二钠-磷酸二氢钾缓冲溶液pH及用量、邻苯二甲醛溶液用量及乙酸铵溶液浓度对荧光强度的影响如图10所示,结合方差分析结果可知,四个因素之间的交互作用均不显著。
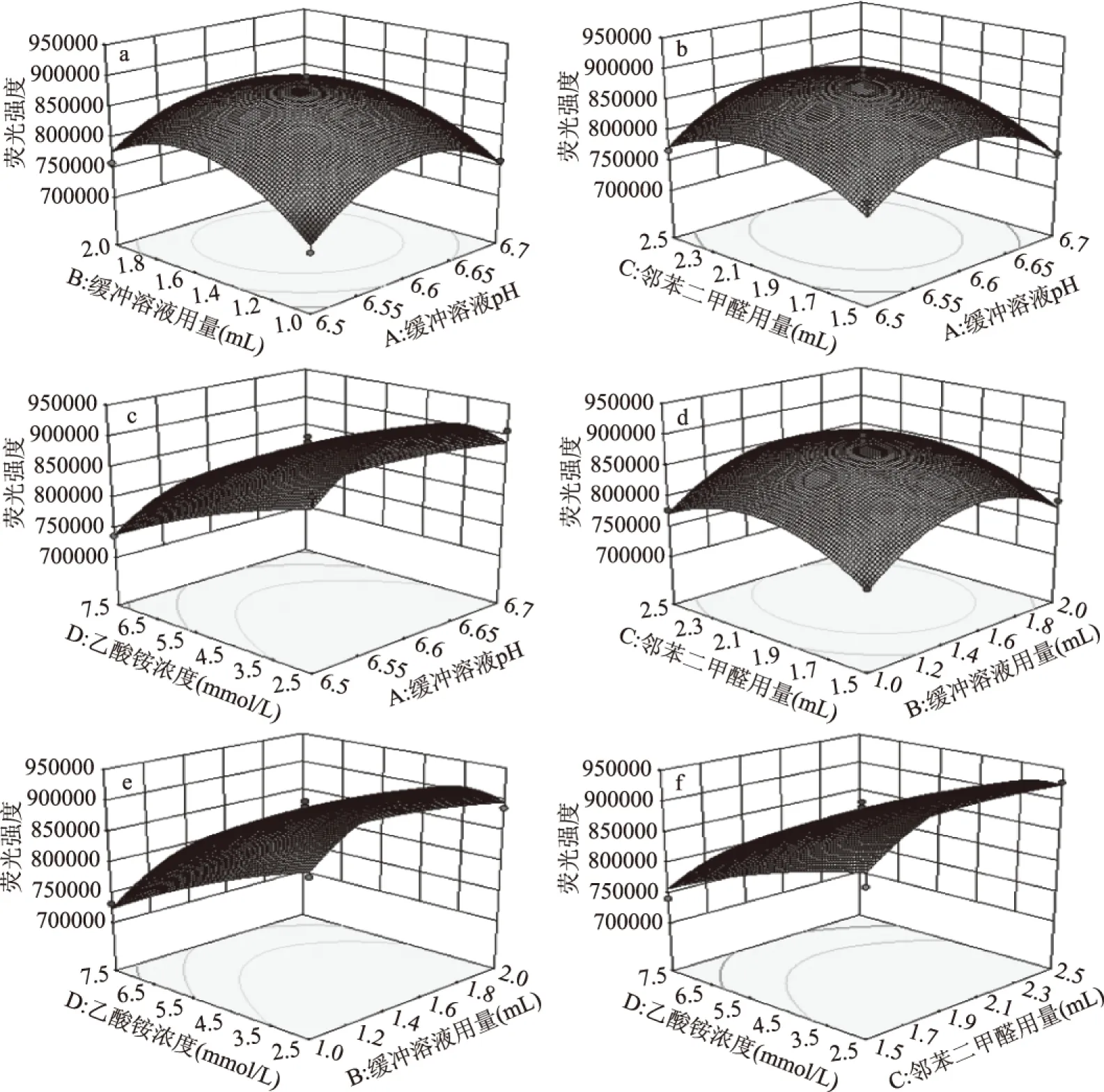
图10 各因素相互作用对荧光强度影响的响应面图Fig.10 Response surface plots of interaction of factors affecting the fluorescence intensity
2.3.3 验证试验及结果 根据Design Expert 10.0软件预测的最佳结果,确定最佳衍生条件为:pH为6.6的磷酸氢二钠-磷酸二氢钾缓冲溶液用量为1.5 mL,邻苯二甲醛溶液用量为2.1 mL,2.5 mmol/L乙酸铵用量2.0 mL,反应温度为50 ℃,反应时间为5 min,静置时间为40 min,预测结果为951516.78。根据最佳衍生条件对预测结果进行验证,实际测得平均荧光强度为955865.21,经方差分析,预测结果与实际测得结果无显著差异(P>0.05),误差为0.46%。因此,用Box-Behnken响应面优化荧光衍生法的结果可靠。
2.4 方法学考察结果
2.4.1 线性关系考察结果 以亚硫酸钠浓度与荧光强度绘制标准曲线,得方程Y=1.37064E7X+288776,R2=0.9991,表明亚硫酸钠浓度在0.01~0.2 μg/mL之间线性关系良好,见图11,检测限为1.89×10-3μg/mL。
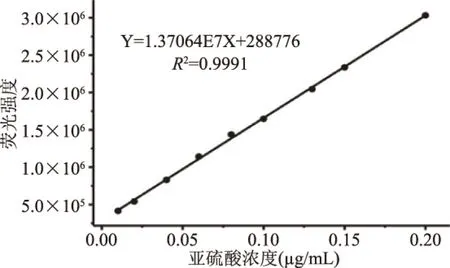
图11 亚硫酸钠线性关系Fig.11 Standard curve of sodium sulfite
2.4.2 精密度试验 荧光强度RSD为0.76%,表明仪器精密度良好,结果见表4。
2.4.3 重复性试验 二氧化硫残留量RSD为1.59%,说明该方法重复性良好,结果见表5。
2.4.4 稳定性试验 在3 h内荧光强度RSD为4.13%,在3 h内稳定性良好,结果见表6。

表6 稳定性考察结果Table 6 Stability test results of experimental methods
2.4.5 加样回收试验 平均回收率为98.61%,回收率RSD为4.89%,表明该方法回收率较好,结果见表7。

表7 加样回收考察结果Table 7 Addition standard recycling inspection results

图12 专属性考察结果Fig.12 Results of specificity inspection
2.5 样品测定结果与分析
2.5.1 不同硫熏时间对党参药材SO2残留量的影响 药典规定党参药材及饮片SO2残留量不得超过400 μg/g[27],图13~图16中荧光衍生法测定结果显示:硫熏0、30 min原药材SO2残留量未超出药典规定的400 μg/g的标准,而硫熏60、90 min原药材SO2残留量均超出药典规定的400 μg/g的标准。其中,硫熏0 min原药材也检测出SO2残留,但含量较低,可能有以下两个因素:一是在党参生长过程中从自然界中吸收的少量SO2,二是在贮藏过程中被污染而有SO2残留。SO2可以杀死虫卵,其与水结合后产生的亚硫酸可以抑制细菌滋生;党参样品在贮存两个月时,硫熏0、30、60 min原药材均出现发霉现象,贮存六个月后硫熏0、30 min原药材生虫现象严重,硫熏60 min原药材生虫现象较轻,而硫熏90 min原药材在贮存1年内未出现生虫和发霉现象。虽然党参硫熏90 min可以防止生虫发霉,但SO2残留量超出药典标准,影响用药安全。党参的产地加工中应尽量避免硫磺熏蒸,近些年有文献报道了热风干燥、红外干燥、微波干燥[28-30]等取代硫熏的加工方法,可以起到防虫、防霉的作用,为替代党参硫熏提供新的发展思路。

图13 硫熏0 min样品二氧化硫残留量变化Fig.13 Change of sulfur dioxide residualin sulfur fumigation sample for 0 min注:显著性在相同测定方法结果内比较,不同字母表示差异显著,P<0.05;图14~16同。
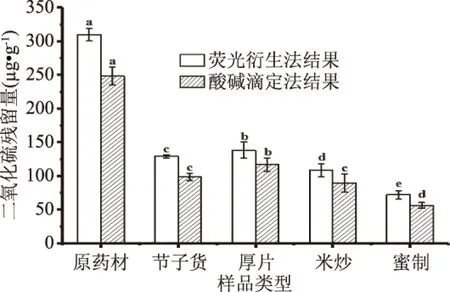
图14 硫熏30 min样品二氧化硫残留量变化Fig.14 Change of sulfur dioxide residualin sulfur fumigation sample for 30 min

图15 硫熏60 min样品二氧化硫残留量变化Fig.15 Change of sulfur dioxide residualin sulfur fumigation sample for 60 min

图16 硫熏90 min样品二氧化硫残留量变化Fig.16 Change of sulfur dioxide residualin sulfur fumigation sample for 90 min
2.5.2 加工炮制对党参SO2残留量的影响 党参经加工炮制为饮片(节子货、厚片、米炒和蜜制)后,SO2残留量测定结果见图13~图16,荧光衍生法测定结果显示:原药材与饮片之间SO2残留量均有显著差异(P<0.05),蜜制饮片与其它样品SO2残留量也均有显著差异(P<0.05),说明硫熏党参经加工炮制后,饮片较原药材SO2残留量明显降低,而蜜制饮片的SO2残留量最低;其中硫熏0、30、60 min饮片与硫熏90 min蜜制饮片SO2残留量符合药典标准,硫熏90 min节子货、厚片及米炒饮片SO2残留量均超出药典标准;与原药材相比节子货SO2残留量平均降低49.75%,厚片SO2残留量平均降低约42.73%,米炒后SO2残留量平均降低50.2%,蜜制后SO2残留量平均降低61.08%,可能是在样品处理过程中用水将党参闷湿后,再进行切片的过程中SO2残留量降低较大,其次米炒与蜜制饮片较厚片SO2残留量低,可能是因为在炒制过程中,高温加热使部分SO2挥发,且高温使SO2与党参成分发生反应,转化为含硫衍生物[31-32],从而使SO2残留量残留量降低。
2.5.3 荧光衍生法与酸碱滴定法结果比较 荧光衍生法测得结果较酸碱滴定法测得结果平均高24.87%,因为酸碱滴定法在酸性条件下测得的SO2留量仅为游离态亚硫酸盐转化为SO2的量,而可逆结合态的亚硫酸盐在酸性条件下稳定;而荧光衍生法采用NaOH溶液提取,可将可逆结合态的亚硫酸盐转化为游离的亚硫酸盐[33],其测得结果要比酸碱滴定法测得结果略高。
3 结论
本文用响应面法对荧光衍生法的衍生条件进行优化,建立回归模型,经方差分析证明该模型可靠,根据响应面分析结果确定最佳荧光衍生件为:pH为6.6的磷酸氢二钠-磷酸二氢钾缓冲溶液用量为1.5 mL,邻苯二甲醛溶液用量为2.1 mL,2.5 mmol/L乙酸铵用量2.0 mL,反应温度为50 ℃,反应时间为5 min,静置时间为40 min,在此条件下测得平均荧光强度为955865.21;方法学考察结果显示:亚硫酸钠浓度在0.01~0.2 μg/mL之间,荧光强度有较好的线性关系,检测限为1.89×10-3μg/mL,精密度、稳定性、重复性、加样回收及专属性考察结果较好;荧光衍生法可作为党参SO2残留量的测定方法,其测得结果与酸碱滴定法测定结果相比平均高24.87%。
党参硫熏0、30 min原药材SO2残留量未超出药典标准,而硫熏60、90 min原药材SO2残留量超出药典标准;加工炮制可以降低硫熏党参的SO2残留量,硫熏党参经加工炮制后,饮片较原药材SO2残留量均明显降低,蜜制饮片SO2残留量最低;硫熏0、30、60 min饮片与硫熏90 min蜜制饮片SO2残留量符合药典标准,硫熏90 min节子货、厚片及米炒饮片SO2残留量均超出药典标准。
