甘蔗Rieske Fe/S蛋白前体基因ScPetC的克隆及表达分析
2020-05-21郑清雷余陈静姚坤存阙友雄辉许莉萍
郑清雷 余陈静 姚坤存 黄 宁 阙友雄,4 凌 辉许莉萍,4,*
甘蔗Rieske Fe/S蛋白前体基因的克隆及表达分析
郑清雷1余陈静1姚坤存1黄 宁1阙友雄1,4凌 辉2,3,*许莉萍1,4,*
1福建农林大学/ 农业农村部福建甘蔗生物学与遗传育种重点实验室, 福建福州 350002;2福建农林大学生命科学学院, 福建福州 350002;3玉林师范学院农学院, 广西玉林 537000;4福建农林大学/ 教育部作物遗传育种与综合利用重点实验室, 福建福州 350002
细胞色素bf复合体还原型铁硫蛋白前体(Cytochrome bfcomplex Rieske Fe/S precursor protein, PetC)是由细胞核基因编码的蛋白, 其成熟蛋白参与构成细胞色素bf复合体, 是电子传递的重要元件。基于前期构建的受高粱花叶病毒(, SrMV)侵染的甘蔗转录组数据库, 从主栽甘蔗品种‘新台糖22号’叶片中成功克隆到该基因, 并命名为(GenBank登录号为MH333037.1)。生物信息学分析发现,基因cDNA全长824 bp, 包含了一个678 bp的开放阅读框, 编码226个氨基酸。ScPetC属于PRK13473超家族, 其C末端具有典型的Rieske保守结构域; 蛋白理论等电点为8.19, 属于稳定的、亲水性蛋白; 二级结构多为无规则卷曲, 三级结构预测其比其他植物PetC多出一段α螺旋结构。在本氏烟()叶片瞬时表达中, ScPetC定位于叶绿体、细胞质和细胞膜。尽管前人研究表明,的表达量会受SrMV侵染的影响, 不同于半夏() PetC与大豆花叶病毒(, SMV) P1蛋白之间的互作, ScPetC不能与SrMV-P1蛋白互作, 但能与甘蔗黄叶病毒(, SCYLV) P0蛋白互作。实时荧光定量PCR分析表明,基因在甘蔗不同组织中均有表达, 但在叶片中的表达量最高。甘蔗受脱落酸胁迫3 h时,表达量显著上调, 但是随着处理时间的延长, 表达受到抑制; 在茉莉酸甲酯、水杨酸、氯化铜、氯化镉和氯化钠胁迫下,表达量均显著下调。本研究通过对ScPetC生物学功能、环境外源激素与重金属等胁迫下的表达模式及其与甘蔗病原病毒蛋白互作的初步探究, 增加了对甘蔗PetC的了解, 也为深入研究其在甘蔗受黄叶病毒侵染中的作用奠定基础。
甘蔗; 细胞色素bf复合体还原型铁硫蛋白前体; 生物信息学; 亚细胞定位; 蛋白互作; 实时荧光定量PCR
甘蔗(spp. hybrids)是最重要的糖料作物和重要的能源作物[1]。甘蔗花叶病和黄叶病是甘蔗生产上最主要的2种病毒性病害, 严重影响甘蔗产量[2-4]。感染花叶病的甘蔗叶片会出现黄绿相间的嵌纹、条斑等症状, 严重时导致叶片失绿[2]。高粱花叶病毒(, SrMV)属于马铃薯Y病毒属(), 是引起甘蔗花叶的主要原因之一[5]。甘蔗黄叶病毒(, SCYLV)属马铃薯卷叶病毒属(), 甘蔗感染后也会出现失绿症状[3], 但其典型症状是叶片的中脉发黄[3]。研究这2种病毒与宿主甘蔗基因的互作机制对甘蔗抗病育种具有重要意义。
一般而言, 植物RNA病毒的基因组具有多个开放读码框(open reading frame, ORF), 它们编码的蛋白控制着病毒侵染植物过程中的不同机制, 但不同的病毒之间也存在一些功能相似的蛋白。P1和P0蛋白分别是SrMV和SCYLV基因编码的首个蛋白, 并且都参与病毒—寄主互作以及病毒抑制宿主免疫反应[6-11]。前人通过对马铃薯Y病毒属的李痘病毒(, PPV) P1蛋白进行研究, 发现此蛋白并没有直接的沉默抑制效应, 但可以通过自身剪切, 与HC-Pro配合行使沉默抑制功能[8-9]; 同属的黄瓜脉黄病毒 (, CVYV) P1蛋白中的P1a前导蛋白对控制病毒特异性识别寄主具有重要作用[8]。在对植物致病方面, 当从PPV基因组中移除编码P1蛋白的区域后, 受PPV侵染的本氏烟()叶片坏死和萎缩症状加深[9]; 相反地, 当马铃薯卷叶病毒属的甘蔗黄叶病毒P0蛋白缺失N端的15个氨基酸后, 该蛋白则会丢失对植物的致病性[10]。另外, 也有报道称其同属的甜菜西黄病毒(, BWYV) P0区域能转录出一个参与病毒和寄主相互识别作用的蛋白[11]。
叶绿体是高等植物进行光合作用的场所。一方面, 对植物的生长发育起着重要作用; 另一方面, 也成为自身健康生长的隐患[12-13]。当植物感染病毒后, 会利用叶绿体进行复制扩繁, 破坏叶绿体相关的结构原件, 影响光系统、电子传递链等过程, 最终影响植物正常生长[13]。截至目前, 已经发现多个植物叶绿体蛋白会同病毒蛋白互作并参与病毒侵染过程, 洋葱1,5-二磷酸核酮糖羧化酶/加氧酶大亚基(Rubisco large subunit, RbcL)和1,5-二磷酸核酮糖羧化酶/加氧酶小亚基(Rubisco small subunit, RbcS)都能与马铃薯Y病毒属的青葱黄条病毒 (, SYSV)、芜菁花叶病毒(, TuMV)、大豆花叶病毒(, SMV) P3蛋白互作, 参与叶片失绿症状的形成[14]。甘蔗花叶病毒(, SCMV)的VPg会和甘蔗NAD(P)H脱氢酶复合体O亚基在叶绿体内发生互作, 阻碍电子循环, 影响叶绿体的形成, 最终导致花叶病症[15]。半夏()中的细胞色素bf复合体还原型铁硫蛋白前体(Cytochrome bfcomplex Rieske Fe/S precursor protein, PetC)会和大豆花叶病毒(, SMV)P1蛋白发生互作, 引起寄主对病毒的适应性改变[16]。在马铃薯卷叶病毒属病毒蛋白的研究中, 拟南芥S-相激酶相关蛋白(S-phase kinaserelated protein 1, AtASK1)能与甜菜西黄病毒(, BWYV)、南瓜蚜传黄化病毒(, CABYV)的P0蛋白发生互作, 降低植物对病毒的抵抗能力; 敲除本氏烟草内拟南芥同源基因后, 感病本氏烟恢复对病毒的抵抗; 同时, 在突变P0氨基酸序列中最保守的F基序后, P0丢失了沉默抑制功能, 并且不再与AtASK1互作[17]。本氏烟草1,5-二磷酸核酮糖羧化酶/加氧酶大亚基装配因子2 (Rubisco Assembly Factor 2, RAF2)会与芸薹黄化病毒(, BrYV)的P0蛋白互作, 并协助病毒进行侵染[18]。
植物的光合电子链主要由PSII (光反应系统II)、质体醌(plastoquinone, PQ)、细胞色素bf复合体(cytochromebfcomplex, Cytbf)、质蓝素(plastocyanin, PC)、PSI (光反应系统I)和铁氧还原蛋白组成; 电子传递方式主要分为非环式电子传递、环式电子传递和假环式传递3种。在这3种电子传递过程中, Cytbf皆有参与[19]。Cytbf复合体包含4个大亚基 (细胞色素、细胞色素b、Fe/S蛋白和亚基IV)和4个小亚基 (PetG、PetI、PetM和PetN)[20]。自从Rieske等人在线粒体细胞色素bc中发现大量携带有[2Fe-2S]结合域的蛋白之后, 这类蛋白就被大家称为Rieske蛋白[21-22]。现已从菠菜()[23]、豌豆()[24]等植物细胞色素bf复合体中分离到Rieske Fe/S蛋白, 并且了解到该蛋白是由细胞核基因编码[25], 在细胞质基质中合成蛋白前体, 由N端信号肽引导至叶绿体基质, 后被加工成成熟蛋白, 结合到类囊体膜上[26-27], 与细胞色素、细胞色素b和亚基IV共同装配成叶绿体细胞色素bf复合体, 参与光合电子传递过程[28-30]。在转入基因的水稻()[31]和拟南芥()[32]的试验中发现, PetC成熟蛋白在叶片内富集会提高光合系统电子传递量, 从而提高产量。西瓜在强光干旱胁迫下通过转变PetC蛋白翻译后修饰模式, 稳定此蛋白的表达量, 维持电子传递量, 进而缓解胁迫对植物的危害[33]。
时至今日, 越来越多植物中编码PetC的基因被克隆出来[31-34], 并发现它会响应强光[33]、模拟干旱[34]等非生物胁迫。不仅如此, 植物在响应生物胁迫方面也有报道, 在感染了白粉病菌()的小麦()表达序列标签(Expressed Sequence Tags, EST)的表达文库中, 编码PetC的基因出现了差异表达[35]。课题组[36]前期在黑穗病菌()侵染甘蔗黑穗病易感与抗性品种后, 质谱分析结果显示, 甘蔗高感品种Ya71-374中PetC相对于高抗品种NCo376中的表达量增加。Ling等[37]利用RNA定量的方法对感染SrMV甘蔗叶片进行分析, 结果显示在抗性品种YZ01-1314中下调表达, 在易感品种ROC22、FN40中上调表达。虽然编码ScPetC成熟蛋白的序列已经被克隆出来并被命名为[34], 但与此不同的是, 本研究中克隆到的是甘蔗细胞色素bf复合体铁硫亚基蛋白前体基因。通过在本氏烟叶片进行瞬时表达, 我们观察了ScPetC亚细胞定位情况, 并利用酵母双杂交和双分子荧光互补实验, 验证该蛋白与SrMV-P1蛋白、SCYLV-P0蛋白的互作情况, 研究结果对深入了解PetC如何参与病毒引起甘蔗叶片变黄症状奠定一定的理论和实践基础。
1 材料与方法
1.1 材料和处理方法
供试甘蔗基因型为我国主栽品种新台糖22号, 由福建农林大学农业农村部福建甘蔗生物学与遗传育种重点实验室提供。
RT-PCR克隆材料: 取植株的+1叶(第1片可见肥厚带的叶片), 用锡纸包好, 液氮速冻, 保存于-80℃冰箱。
组织特异性分析材料: 参照黄宁等[38]方法, 从田间选取健康长势一致的植株9株, 清理根部泥土, 取白色幼根作为材料; 从地面以上可见完整第1节间算起, 选取第7~8节段, 用75%酒精擦拭表皮, 从侧芽、蔗皮、蔗髓取样; 叶片选取甘蔗+1叶。以上样品均选择3株混合作为一个重复, 共3个生物学重复, 用锡箔纸包好所有材料, 立刻投入液氮速冻, 保存于-80℃冰箱。
不同外源胁迫处理材料: 考虑到植物会释放内源激素来抵抗病毒的侵染[13], 因此我们用不同外源胁迫处理甘蔗的方法来模拟病毒侵染。参照苏亚春等[39]方法, 在田间随机选取长势一致的植株, 将其蔗茎砍成单芽茎段、洗净, 放在含有100 mg L-1多菌灵(福瑞得, 中国郑州)水溶液中进行52℃温浴脱毒30 min, 然后将这些茎段种在无菌土中(16 h光/ 8 h暗, 28℃)培养, 直至长出蔗苗, 切下蔗苗用于无菌苗的诱导生根。随后放入蒸馏水中培养一段时间待其生长稳定, 从中挑选一部分健壮且长势一致的蔗苗, 置于250 mmol L-1氯化钠(sodium chloride, NaCl)、100 mmol L-1氯化铜(copper chloride, CuCl2)、500 mmol L-1氯化镉(cadmium chloride, CdCl2)的水溶液中培养, 并于0、6、12、24 h取样; 取另一部分蔗苗在100 μmol L-1脱落酸(abscisic acid, ABA)、5 mmol L-1水杨酸 (salicylic acid, SA) (含0.01%吐温-20, v/v)和25 mmol L-1茉莉酸甲酯(methyl jasmine, MeJA)(含0.01%吐温-20, v/v)水溶液中培养, 并于0、3、6、12 h取样, 每个处理选择3株混合作为1个重复, 共取3个生物学重复。每个样品取样完成、液氮速冻, 保存于-80℃冰箱。
1.2 RNA提取与cDNA的合成
采用TRIzol Reagent (Invitrogen, Carlsbad, USA)试剂提取所有甘蔗样品的总RNA, 提取方法参照Liu等[40], cDNA第一链合成方法参照RevertAid First Strand cDNA Synthesis Kit (Thermo Scientific, Lithuania, Vilnius)和PrimerScript RT-PCR Kit (Takara, 中国大连)试剂盒说明书。
1.3 甘蔗ScPetC基因序列获取与RT-PCR克隆
基于课题组构建的感染SrMV叶片的甘蔗转录组uingene注释库, 挖掘得到基因unigene序列(转录本ID: T2_Unigene_BMK.38583), 并根据其序列设计克隆特异性引物-F/R (表1), 以甘蔗叶片cDNA为模板, 进行PCR扩增。PCR扩增程序为94℃ 4 min; 94℃ 30 s, 55℃ 30 s, 72℃ 60 s, 40个循环; 72℃ 10 min; 随后进行回收、纯化、测序与鉴定。
1.4 生物信息学分析
利用ExPaSy、Prabi、SWISSMODEL在线软件, 对ScPetC进行一、二、三级结构预测, 使用NCBI conserved domains、SignalP 4.1 Server、TMHMM 2.0 Server、ProtScale和WoLFPSORT, 分别进行保守结构域、信号肽、跨膜结构域、疏水性和亚细胞定位预测, 在线软件网址如表2所示。使用DNAMAN 6.0将基因编码的氨基酸序列与NCBI下载的来自其他植物的PetC的氨基酸进行多序列比对。参考Schmidt等[41]的方法, 使用MEGA 6.0软件对ScPetC、其他高等植物PetC和细胞色素bcRieske Fe/S蛋白、蓝藻细菌细胞色素bfRieske Fe/S蛋白和细菌细胞色素Rieske Fe/S蛋白进行进化树构建。通过MEME对植物氨基酸进行motif (基序)预测, 在Adobe Photoshop CS6上进行图片美化。

表1 引物序列及用途

表2 生物信息学研究的数据库和软件
1.5 酵母双杂交实验
以pMD19-、pMD19-、pMD19-(课题组前期实验获得)质粒为模板, 以-AD-F/R、-BK-F/R、-BK-F/ R (表1)为引物, 通过PCR、胶回收获得基因编码序列。随后使用ClonExpress II One Step Cloning Kit (诺唯赞, 中国南京)同源重组的方法, 将基因编码序列导入经过限制性内切酶RI和HI (Thermo Scientific, Lithuania, Vilnius)双酶切的pGADT7、pGBKT7载体中, 构建载体pGADT7-pGBKT7、pGBKT7-。测序正确的阳性质粒以共转化方式导入酵母Y2HGold感受态细胞(上海维地, 中国上海)。实验参照Matchmaker Gold酵母双杂交系统说明书, 在SDO (SD/-Trp)固体培养基上进行毒性验证, 在SDO (SD/-Trp/X-α-Gal/AbA)固体培养基上进行自激活验证, 在QDO (SD/-Ade/-His/ Leu/-Trp/X-α-Gal)和QDO/X/A (SD/-Ade/-His/Leu/- Trp/X-α-Gal/AbA)固体培养基上进行互作验证。
1.6 植物表达载体构建
以携带有、、基因的相关质粒为模板, 用引物-YN-F/R、- YC-F/R、-YC-F/R (表1)进行PCR、胶回收获得基因编码序列。随后使用ClonExpress II One Step Cloning Kit同源重组的方法, 将基因编码序列导入经过限制性内切酶I和I、I和I双酶切的pCAMBIA1300S-YN、pCAMBIA2300S- YC[42]载体中, 构建载体pCAMBIA1300S-YN-、pCAMBIA2300S-YC-、pCAMBIA2300S- YC-用于双分子荧光互补试验 (Bimolecular Fluorescent Complimentary, BiFC)。
以pMD19-T-阳性质粒为模板, 使用引物-Subloc-F/R (表1)进行PCR、胶回收获得基因编码序列。随后使用ClonExpress II One Step Cloning Kit同源重组的方法, 将基因编码序列导入经过限制性内切酶I和HI双酶切的pCAMBIA2300-YFP载体中, 构建载体pCAMBIA2300--YFP用于蛋白亚细胞定位实验。
1.7 本氏烟草叶片注射与荧光观察
将pCAMBIA1300S-YN-、pCAMBIA 2300S-YC、pCAMBIA2300S-YC-和pCAMBIA 2300--YFP转化农杆菌菌株GV3101 (上海唯地, 中国上海), 在含有35 μg mL-1利福平和50 μg mL-1卡纳霉素的YPD液体培养基中扩繁后, 收集农杆菌菌体, 用MS盐缓冲液悬浮, 并将菌体悬浮液OD600调至0.8。加入乙酰丁香酮(工作浓度200 μmol L-1), 28℃避光诱导培养2 h, 随后注射本氏烟叶片下表皮, 于48 h后在激光共聚焦显微镜(Leica TCS SP8, 曼海姆, 德国)下拍摄YFP荧光(激发光波长514 nm, 捕获波长为530~590 nm)、叶绿体自发荧光(激发光波长552 nm, 捕获波长为650~680 nm)。
1.8 实时荧光定量PCR (Quantitative real-time PCR, qRT-PCR)分析
根据基因序列设计特异性定量引物-QF/QR (表1), 以clathrin adaptor complex ()和cullin ()作为内参基因[43]。参照SYBR Green PCR Master Mix (Roche, 中国上海)试剂盒说明书配制定量反应体系, 进行定量PCR, 以检测目的基因在甘蔗的不同组织(根、芽、叶、蔗髓和蔗皮)和不同外源胁迫(SA、MeJA、ABA、NaCl、CuCl2和CdCl2)处理样品中的相对表达量。定量PCR程序为50℃ 2 min; 95℃预变性10 min, 95℃变性15 s, 60℃退火延伸1 min, 40个循环; 增加熔解曲线, 95℃ 15 s, 60℃ 1 min, 95℃ 15 s, 60℃ 15 s。每个样品设3次技术重复和3次生物学重复, 阴性对照以无菌水为模板, 定量数据采用2–DDCT法计算基因相对表达量。使用DPS 7.05对数据进行显著性分析, Original 8.0软件做柱状图。
2 结果与分析
2.1 甘蔗ScPetC基因克隆及生物信息学分析
采用基于SrMV侵染甘蔗的转录组数据库基因Unigene序列设计扩增引物, 以叶片cDNA为模板, 扩增得到一条长824 bp的片段 (图1-A)。扩增产物经过连接、转化、测序, 获得基因序列。经过ORF Finder在线分析,基因的完整开放读码框为678 bp, 编码225个氨基酸。与基因(GenBank登录号为JQ712582)进行序列比对发现, 核酸相似度达到73.87%,在5¢端比多129个碱基, 在3¢端比少了97个碱基, 但不影响蛋白编码。氨基酸比对结果显示, 2条基因编码的氨基酸序列相似度为84.44% (图1-B), 经过进一步的分析, ScPetC氨基酸链的N端比SoCYT多出33个氨基酸残基, 并且2条链中的第47个(丙氨酸A~缬氨酸V)、第70个(丝氨酸S~甘氨酸G)氨基酸不同。综上结果表明, 克隆自现代杂交种的与成熟蛋白基因的编码序列和蛋白序列高度保守, 仅存在个别位点的差异。

图1 甘蔗ScPetC基因的RT-PCR扩增及其编码氨基酸序列
(A) M: marker 100 bp; I: RT-PCR产物。(B): 甘蔗细胞色素bf复合体还原型铁硫蛋白前体序列;: 甘蔗细胞色素bf复合体铁硫亚基氨基酸序列[34]。
(A) M: DNA marker 100 bp; I: RT-PCR product. (B): Sugarcane cytochromebfcomplex reduced iron-sulfur protein precursor sequence;: Sugarcane cytochromebfcomplex iron-sulfur subunit amino acid sequence[34].
利用ExPaSy在线软件对ScPetC一级结构进行预测, 结果显示该蛋白分子式为C1054H1668N294O315S11, 相对分子量为23.85 kD, 疏水性平均值为-0.146, 蛋白不稳定系数为21.61, 等电点为8.19 (表3)。蛋白不稳定系数小于40, 等电点大于7.5, 表明该蛋白为稳定的碱性蛋白; 通过SignaIP 4.1 server、TMHMM 2.0 Server和NCBI conserved domains软件对ScPetC结构域或基序进行预测, 结果表明该蛋白无信号肽(图2-A), 为非分泌蛋白, 并且在第66个到第88个氨基酸之间存在一个跨膜区域(图2-B), 属于PRK13474超家族(图2-C)。因此推测ScPetC是一个碱性稳定亲水非分泌蛋白。

表3 ScPetC一级结构预测分析
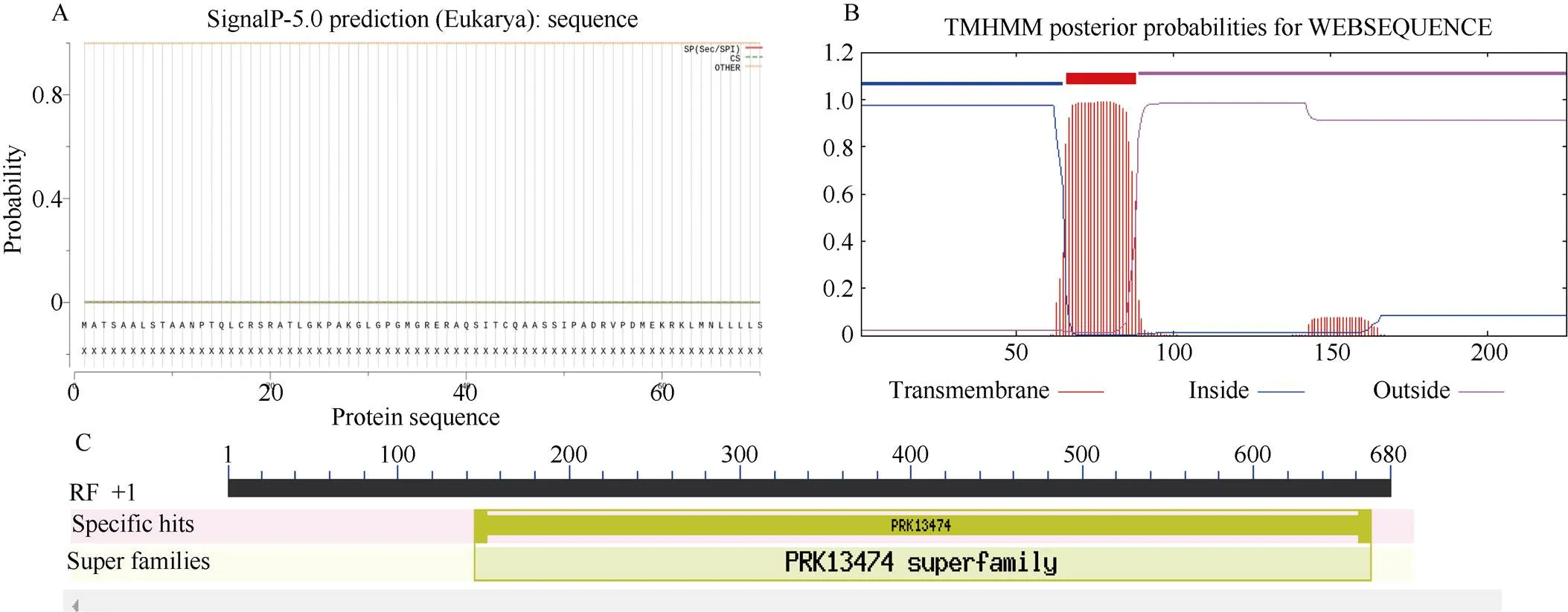
图2 甘蔗ScPetC的生物信息学软件预测结果
A: 信号肽; B: 跨膜结构域; C: 保守结构域。
A: signal peptide; B: transmembrane domain; C: conservative domain.
ScPetC的二级结构预测结果显示, α螺旋、延伸链和无规则卷曲的氨基酸残基数分别为42、49和134个, 占比分别为18.67%、21.78%和59.56%。
根据SWISSMODEL三维结构预测, 比较甘蔗与单子叶植物水稻、双子叶植物半夏和菠菜PetC三维空间结构 (图3), 甘蔗ScPetC构象与其他3种植物空间构象基本相似, 都具有N末端α螺旋结构和[2Fe-2S]结合域, 但甘蔗该蛋白的构象中多出了一个α螺旋结构(图3-A)。

图3甘蔗、水稻、半夏和菠菜的PetC成熟蛋白三级结构预测
黄色箭头处为PetC蛋白的[2Fe-2S]结合域; 蓝色和红色箭头所指位点为氨基酸链的N端和C端; 绿色箭头所指位点为α螺旋。图A中白色箭头表示ScPetC与其他植物PetC的差异α螺旋所在位置。
Yellow arrow is the conservative binding domain [2Fe-2S] of PetC; blue and red arrows represent the N-terminus and C-terminus of the amino acid chain; green arrows represent α helix. White arrow represents the α helix in sugarcane that is different from other plants of tertiary structure in figure A.
根据WoLFPSORT对ScPetC氨基酸序列的扫描结果, 了解到该蛋白定位于甘蔗细胞的亚细胞结构中的可能性由大到小, 分别为叶绿体类囊体(65.7%)、线粒体(15.38%)、细胞质(13.29%)、细胞核(11.59%)、液泡(11.01%)和叶绿体基质(8.95%)。因此, 本研究推测ScPetC最有可能定位于叶绿体类囊体。
2.2 甘蔗ScPetC的保守结构域及系统进化
对比甘蔗与其他植物PetC氨基酸序列(图4), 发现甘蔗与高粱()、水稻、半夏、本氏烟、菠菜和豌豆的PetC序列相似度分别是97.35%、84.14%、70.74%、68.87%、66.95%和64.38%。这7种植物的PetC序列中均含有N末端的转移多肽区域、跨膜α螺旋区域、结合[2Fe-2S]的Rieske区域和靠近C末端的脯氨酸环区域(图4)。
将甘蔗与27个其他物种PetC的氨基酸序列构建系统进化树(图5)。结果显示, 所有物种的PetC可以被划分为细胞色素bc复合体和细胞色素bf复合体2个亚类。在细胞色素bf复合体亚类中, 不同物种的PetC可以被分为5组(I、II、III、IV、V), 其中甘蔗与高粱的PetC聚为一个分支, 表明其亲缘关系较近。细胞色素bc复合体亚类中, 不同物种的PetC可以被分为2组(VI、VII)。MEME软件预测结果显示, ScPetC和其他高等植物细胞色素bf复合体PetC一样具有6个motif。综上, 本研究推测ScPetC也可能与其他植物PetC具有相似的功能。

图4 甘蔗ScPetC与其他植物PetC氨基酸序列对比
红色方框表示ScPetC内为已报道保守氨基酸基序。CAM57108: 半夏; XP_015647138: 水稻; XP_002441121: 高粱; P08980: 菠菜; P26291: 豌豆; CAA45705: 本氏烟。
Red squares indicate the reported conserved motif of amino acid regions within the ScPetC. CAM57108:; XP_015647138:; XP_002441121:; P08980:; P26291:; CAA45705:.
2.3 甘蔗ScPetC的亚细胞定位
由图6可知, 对照组中YFP黄色荧光信号在本氏烟叶表皮细胞的细胞膜、细胞核和细胞质均有分布; ScPetC-YFP融合蛋白的黄色荧光信号既定位于质膜、细胞质, 又与叶绿体的自荧光信号重合, 显示出橙色, 表明ScPetC定位于叶绿体(图6)。
2.4 甘蔗ScPetC与病毒蛋白的互作
酵母双杂交互作实验中, 分别导入以下质粒组合pGADT7-T+pGBKT7-Lam、pGADT7-T+pGBKT7- 53、pGADT7-+pGBKT7-、pGADT7-+ pGBKT7-、pGADT7-+pGBKT7、pGADT7+ pGBKT7-、pGADT7+pGBKT7-到Y2Hgolden菌株中, 它们均能在DDO (SD/-Leu/-Trp)固体培养基上正常生长, 说明质粒组合成功转入酵母感受细胞。同时, 在QDO (SD/-Ade/-His/-Leu/-Trp/X-α-Gal)和QDO/X/A (SD/-Ade/-His/-Leu/-Trp/X-α-Gal/AbA)固体培养基上, 阳性对照能正常生长并在加入X-α-Gal后表现出蓝色, 阴性对照不能正常生长, pGADT7+pGBKT7-不能在酵母缺陷培养基上生长(图7-A), 而pGADT7-+pGBKT7-能在缺陷培养基上生长并且在加入X-α-Gal后成功显色, 说明ScPetC与SrMV-P1蛋白不存在互作, 与SCYLV-P0蛋白存在互作(图7-B)。
为进一步验证互作结果, 本研究将基因构入pCAMBIA1300S-YN载体, 形成YN-ScPetC; SCYLV-P0基因构入pCAMBIA2300S-YC载体, 形成YC-P0; 结果在注射YN-ScPetC和YC-P0的本氏烟叶片细胞内出现了黄色荧光(图7-C)。酵母互作和双分子荧光互补实验的结果一致, 说明ScPetC和SCYLV-P0确实存在互作。
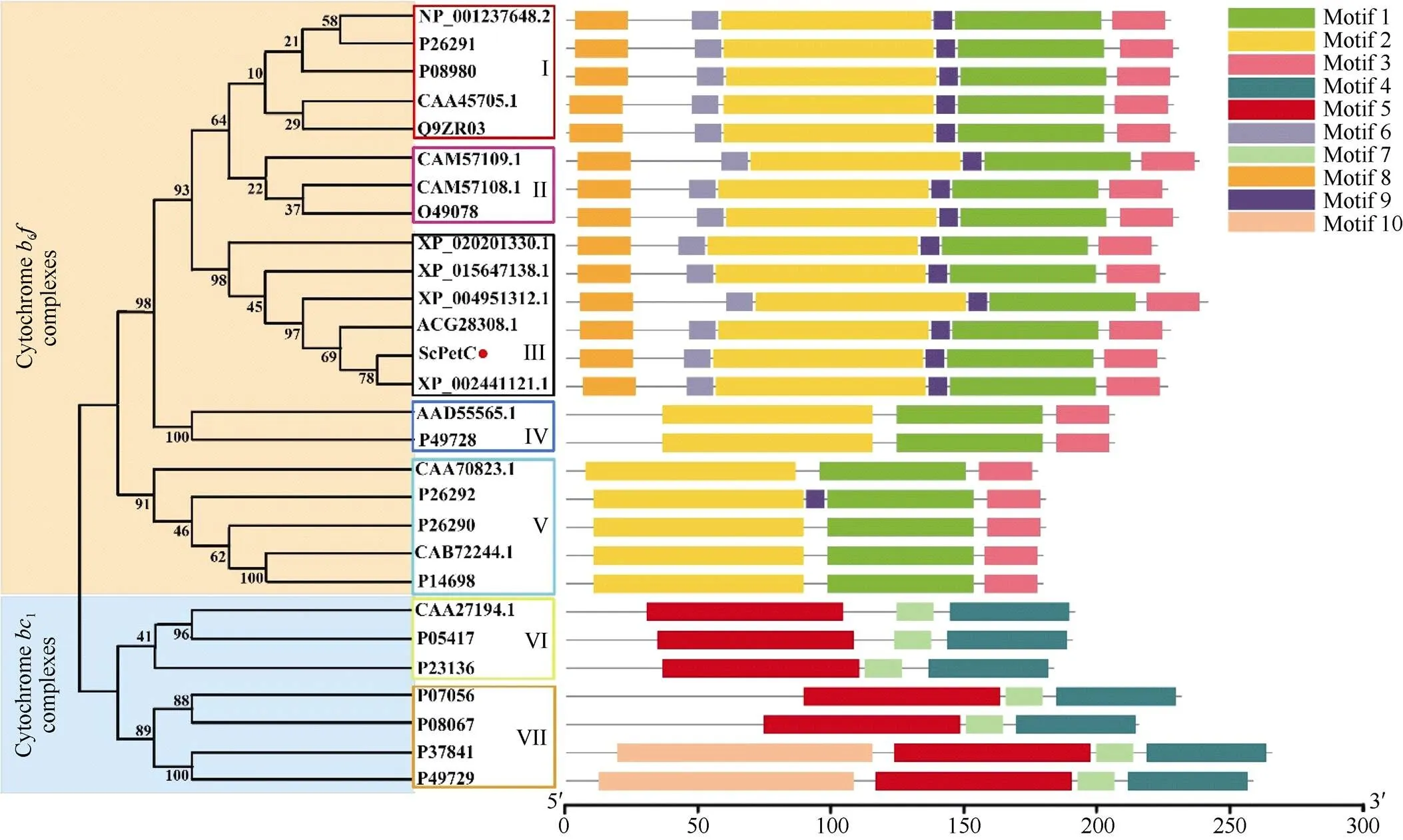
图5 甘蔗ScPetC与其他物种PetC的系统进化树分析与motif预测
图中进化树橘色部分代表细胞色素bf复合体类, 蓝色部分代表细胞色素bc复合体类; III组中的红色圆圈标记为ScPetC; 不同颜色的方框代表不同的组(I、II、III、IV、V、VI、VII)。NP_001237648.2: 大豆; XP_015647138.1: 水稻; XP_0202013301.1: 小麦; Q9ZR03.1: 拟南芥; P26291: 豌豆; AAD55565.1: 团藻; CAA27194: 类红球细菌; CAA45705: 本氏烟; CAA70823: 席藻; CAB72244: 鱼腥藻; CAM57108.1: 半夏; CAM57109.1: 马蹄莲; O49078: 贝母; P05417: 脱氮副球菌; P08067: 酿酒酵母; P08980: 菠菜; P14698: 蓝藻; P23136: 深红红螺菌; P26290: 集胞藻; P26291: 豌豆; P26292: 聚球藻; P37841: 马铃薯; P49728: 衣藻; Q9ZR03: 拟南芥; XP_002441121: 高粱; ACG28308: 玉米; XP_004951312: 小米。
The orange part of the phylogenetic tree represents the cytochromebfcomplex cluster, the blue part represents the cytochrome bccomplex cluster; the red cycle is labeled as ScPetC; the different color boxes in the figure represent different groups (I, II, III, IV, V, VI, VII). NP_001237648.2:; XP_015647138.1:; XP_0202013301.1:; Q9ZR03.1:; P26291:; AAD55565.1:; CAA27194:; CAA45705:; CAA70823:; CAB72244:; CAM57108.1:; CAM57109.1:; O49078:; P05417:; P08067:; P08980:; P14698:spPCC; P23136:; P26290:sp.PCC; P26291:; P26292:sp. PCC; P37841:; P49728:; Q9ZR03:; XP_002441121:; ACG28308:; XP_004951312:. motif 1: X6NAXCTHLGCVVPX3ENKFXCPCHGSX10GPAP; motif 2: NLX11PDX3RX3NLX22PX3GX3GXXAKGXXGNDX6LX7LXXGLKGDPTYX2V; motif 3: X7WXETDFRTX3PWW; motif 4: XGDX3GWFCPCHGSHYDX2GRIRXGPAPXNLX15; motif 5: X7MX4DX2AX5VX7GX6WXGKPVFXRXRX4IX5VX4LXDX10; motif 6: X2AXSIX ADXV; motif 7: XWLX3GXCTHLGCX; motif 8: X9QLX10; motif 9: LVVEXDXT; motif 10: FX5FX3DDSSX2RSXSPSLXSXFLX3RGFS SNSVSPAHX2GLVXDLPXTVAAIKNPXSKIVYDX2NHERYPPGDPSKRAFAYFVLTGGRFVY.
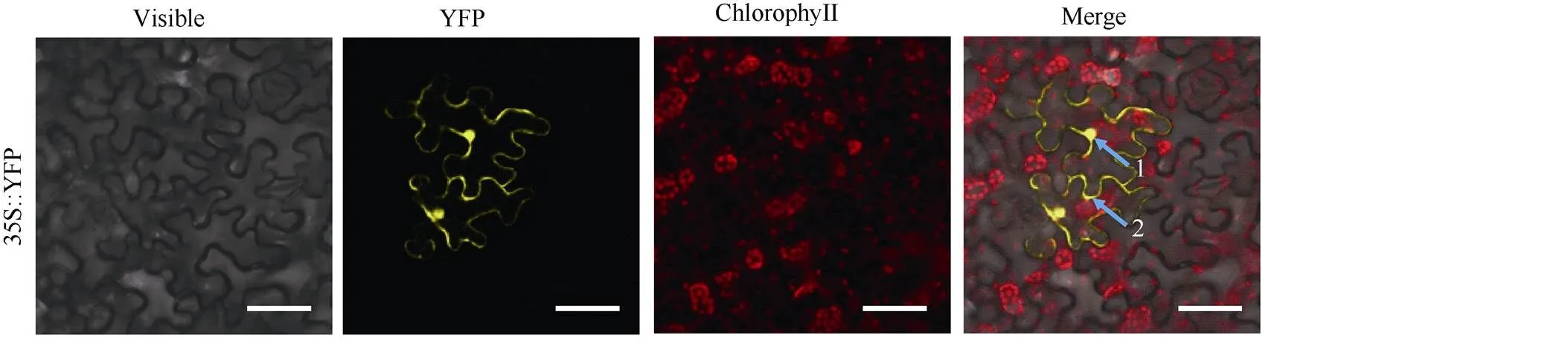
(图6)
农杆菌介导及空载体在本氏烟叶片瞬时表达48 h后的亚细胞定位结果; 本氏烟叶片表皮细胞被用于明场、黄色荧光、叶绿体自发荧光、明场和黄色及红色荧光叠加后的图像分析; 蓝色箭头1、2分别表示细胞核、质膜; 红色虚线框表示被放大区域; 比例尺=50 μm; 35S::YFP: 携带空载pCAMBIA2300-YFP的农杆菌菌株; 35S:: ScPetC::YFP: 携带重组载体pCAMBIA2300--YFP的农杆菌菌株。
Subcellular localizations of themediated transformation ofand empty vector inleaves after 48 h infiltration; the epidermal cells ofwere used for taking images of visible light, yellow fluorescence, chloroplast autofluorescence, and merged visible light. Blue arrows 1 and 2 indicate nucleus and plasma membrane. The area in the red rectangle is magnified. Bar=50mm; 35S::YFP: thestrain carrying the empty vector pCAMBIA2300-YFP; 35S:: ScPetC::YFP: thestrain carrying the recombinant vector pCAMBIA2300--YFP.

图7 甘蔗ScPetC与高粱花叶病毒和甘蔗黄叶病毒蛋白的互作实验验证
A: 甘蔗ScPetC与SrMV-P1蛋白的酵母双杂交互作验证。B: 甘蔗ScPetC与SCYLV-P0蛋白的酵母双杂交互作验证; SD/-Ade/-His/Leu/-Trp: 腺嘌呤、组氨酸、亮氨酸和色氨酸营养缺陷型平板培养基; SD/-Ade/-His/Leu/-Trp/X-α-Gal: 腺嘌呤、组氨酸、亮氨酸和色氨酸营养缺陷型平板培养基(添加5-溴-4-氯-3-吲哚-α-D-半乳糖苷); SD/-Ade/-His/Leu/-Trp/X-α-Gal/AbA: 腺嘌呤、组氨酸、亮氨酸和色氨酸营养缺陷型平板培养基(添加5-溴-4-氯-3-吲哚-α-D-半乳糖苷和金担子素A)。C: ScPetC与SCYLV-P0蛋白的双分子荧光互补实验; YC、YN、YN-ScPetC和YC-P0分别代表质粒pCAMBIA2300S-YC、pCAMBIA2300S-YN、pCAMBIA2300S-YN-和pCAMBIA2300S-YC-[42]。
A: ScPetC was verified by yeast double-hybrid interaction with SrMV-P1 protein. B: ScPetC was verified by yeast double-hybrid interaction with SCYLV-P0 protein; SD/-Ade/-His/Leu/-Trp: synthetic dropout medium plate without adenine, histidine, leucine, tryptophan; SD/-Ade/-His/Leu/-Trp/X-α-Gal: synthetic dropout medium plate without adenine, histidine, leucine, tryptophan (plus 5-bromo-4-chloro-3- indoxyl-α-D-galactopyranoside); SD/-Ade/-His/Leu/-Trp/X-α-Gal/AbA: synthetic dropout medium plate without adenine, histidine, leucine, tryptophan (plus 5-bromo-4-chloro-3-indoxyl-α-D-galactopyranoside and aureobasidin A). C: the bimolecular fluorescence complementation (BiFC) assay of the interaction between ScPetC andSCYLV-P0 protein; YC, YN, YN-ScPetC, YC-P0 represent the plasmids pCAMBIA2300S-YC, pCAMBIA2300S-YN, pCAMBIA2300S-YN-, pCAMBIA2300S-YC-, respectively[42].
2.5 甘蔗ScPetC基因的转录表达模式分析
由图8-A可知,基因在甘蔗叶片中的表达量最高, 其次是蔗皮、蔗芽和蔗髓, 在根中几乎不表达。分析结果显示, 该基因在叶片中的表达量分别是蔗髓、蔗芽、蔗皮和根部表达量的15、15、4和174倍, 说明该基因在叶绿体和线粒体丰富的细胞中均有表达。
分析基因在不同外源胁迫下的表达特性, 结果表明在对甘蔗施以CuCl2、CdCl2和NaCl处理后,的表达量下降并显著低于对照(图8-B); 用SA、MeJA处理甘蔗后,表达量随着施用时间延长, 持续下降; 甘蔗在受ABA处理3 h后,的表达量显著提高并达到峰值, 为对照组的1.3倍, 当处理时间达到6 h时, 表达量下降但仍高于对照, 处理达到12 h时, 表达量下降并显著低于对照(图8-C)。我们推测该基因可以在短时间内积极响应ABA的胁迫。
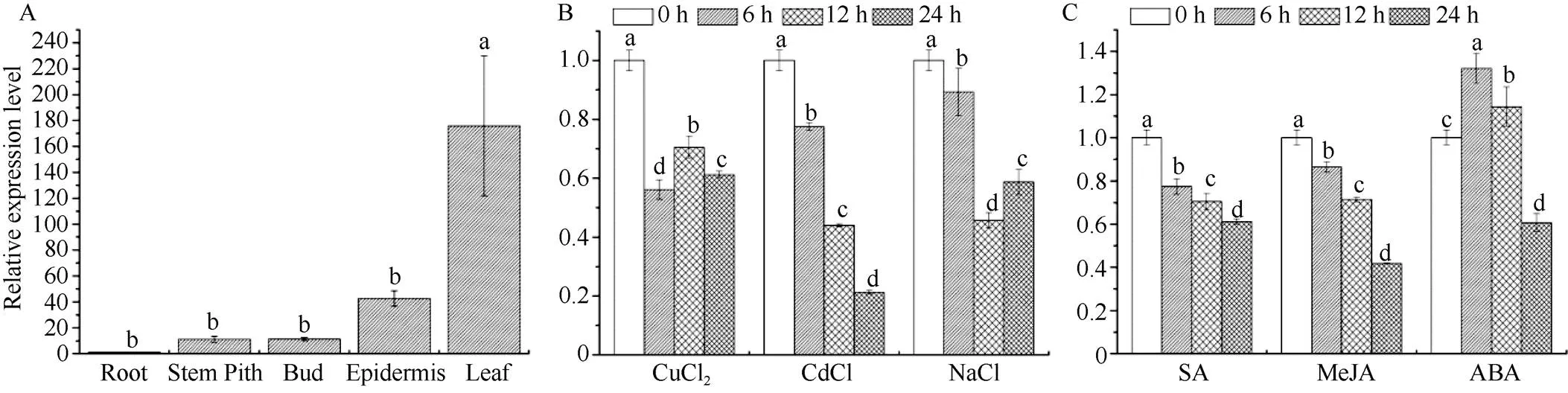
图8 甘蔗ScPetC基因的转录表达模式分析
A: 甘蔗基因在甘蔗不同组织中的表达情况; B和C: 甘蔗基因在不同外源胁迫下的相对表达情况。不同的小写字母(a、b、c、d)表示差异显著性(≤ 0.05); 误差线为每组处理的标准误差(= 3)。
A: the tissure-specific expression analysis ofgene in sugarcane; B and C: relative expression ofin sugarcane under different exogenous stresses. Bars with different superscripts (a, b, c, d) represent differ significantly (≤ 0.05) and error bars represent the standard error of each treating group (= 3).
3 讨论
植物受到病毒侵染时, 会通过改变体内相关基因的表达量来抵抗病毒侵染。叶绿体作为植物重要的细胞器, 其中的基因与蛋白也会参与到病毒抵御过程[13]。到目前为止, 已经发现多个叶绿体蛋白能参与到病毒的复制、移动、致病等过程中[13]。ScPetC成熟蛋白是植物细胞色素bf复合体的元件之一, 在叶绿体光合电子转运过程中起重要的作用[20], 但是关于植物ScPetC与病毒蛋白互作研究仍比较少见, 截至目前只有两例, 一例是半夏PetC与马铃薯Y病毒属SMV-P1蛋白互作[16]; 另一例是拟南芥PetC与马铃薯Y病毒属TuMV-HC-Pro蛋白互作[44]。本研究是首次报道ScPetC与马铃薯卷叶病毒属SCYLV- P0蛋白互作。
ScPetC属于PRK13474超家族, 包含由半胱氨酸和组氨酸组成的(CTHXXC, CPCHXX) Rieske结构域 (图4)。这个结构域位于氨基酸链的C端附近, 是Rieske家族蛋白主要特征[41]。高等植物Rieske蛋白主要被分为两类, 分别是细胞色素bf复合体类和细胞色素bc复合体类。本研究中ScPetC属于细胞色素bf复合体类, 其N端存在一个由33个氨基酸组成的区域, 在梁潘霞等[34]克隆到的基因编码氨基酸链中并不存在。通过与其他植物PetC氨基酸序列比对后, 认识到这段氨基酸是转移多肽区域, 其中的保守序列与前人研究结果相一致[23-24], 因此我们确定克隆到的是甘蔗叶绿体细胞色素bf复合体Rieske Fe/S蛋白前体基因。生物信息学分析显示, ScPetC为碱性蛋白, 不同于基因所编码蛋白质pI值小于7的结果[34], 其主要原因是N端转移多肽区内存在多个碱性氨基酸引起ScPetC整体平均pI值大于7。使用SWISSMODEL对ScPetC进行三级结构预测, 其结果表明其与拟南芥PetC成熟蛋白在三维结构上极为相似[44], 说明植物PetC蛋白在结构上极为保守, 极可能行使高度保守的生物学功能。经过仔细比对观察, 发现ScPetC三级结构组成是从第55个缬氨酸V开始, N端转移多肽不在ScPetC成熟蛋白的三维构象中。另外, 在甘蔗与其他植物PetC蛋白三级结构的对比结果中, 我们发现ScPetC多出一段α螺旋结构(图3-A), 这或许是ScPetC和SrMV-P1蛋白之间不存在互作的原因, 这与半夏PetC蛋白和SMV-P1蛋白互作的结果有所不同[16]。从所构建的系统进化树中, 我们发现甘蔗和高粱的PetC蛋白被聚为一簇, 表明其亲缘关系最近, 这和前人研究结果一致[34]。有研究表明, 植物PetC一共有5个外显子保守区域[25], 本研究结果显示, ScPetC有6个motif, 包含了上述的5个保守区域。因此, 可以推测ScPetC与其他植物PetC具有相似的功能。
蛋白质的生物学功能与其在细胞中的定位密切相关。本研究对ScPetC亚细胞定位进行预测, 结果显示, 此蛋白定位在叶绿体类囊体的概率最大为65.70%, 细胞质的概率为13.29%, 叶绿体基质的概率为8.95%。在本氏烟叶片中的亚细胞定位分析表明, ScPetC定位在细胞质、细胞膜和叶绿体, 这与拟南芥PetC融合GFP荧光标签在本氏烟叶片细胞内的亚细胞定位结果相似[44]。课题组前期在SrMV侵染甘蔗的转录组研究中, 发现基因发生了差异表达, 且在抗感品种中表现出不同的表达模式[37]。前人研究表明半夏PetC和马铃薯Y病毒属SMV-P1蛋白存在互作[16]。但酵母双杂交实验结果显示, SrMV-P1蛋白和ScPetC不存在互作, 因此, 我们比对了SrMV和SMV的P1蛋白氨基酸序列, 发现相似性只有9.25%; 半夏和甘蔗的PetC蛋白之间相似率为70.74% (图1-B), 我们推测是序列上的差异导致马铃薯Y病毒属病毒的P1蛋白不能与其寄主PetC蛋白互作, 这种互作可能只存在某些物种之中, 因而基因在宿主受到SrMV侵染时所发生的差异表达可能是其他未知机制引起的。与此同时, 酵母双杂交和BiFC实验结果显示, ScPetC与SCYLV-P0蛋白互作发生在细胞膜周和细胞质内, 这和拟南芥PetC蛋白与TuMV-HC-Pro蛋白存在互作的结果相一致[44]。PetC蛋白是由核基因编码的, 在细胞质中形成蛋白前体, 然后被引导到叶绿体内, 经过加工后的成熟蛋白铆在类囊体膜上, 参与Cyt bf的形成。因此, 推测SCYLV-P0与ScPetC在细胞质中发生互作, 可能阻断了ScPetC由细胞质向叶绿体运输的过程, 影响了Cyt bf正常组装, 破坏光合电子传递过程, 从而引起了甘蔗叶片变黄等症状。另外, SCYLV-P0蛋白和马铃薯Y病毒属病毒HC-Pro蛋白都具有沉默抑制的功能[10, 44], 但ScPetC是否参与P0蛋白沉默抑制作用仍需进一步验证。
在转基因融合GUS标签的拟南芥中,基因在叶片、茎、花、荚均有表达, 在根中却没有表达[25]。甘蔗组织表达定量结果显示,在根中的表达量相对于蔗芽、蔗髓、蔗皮、叶片表现很低; 相反地, 其在叶中表达量最高。该基因之所以会在蔗芽、蔗髓、蔗皮等组织中有少量表达, 可能因为是细胞核基因, 普遍存在于植物不同组织细胞中。课题组前期对感染SrMV的甘蔗易感和抗性品种进行了RNA-seq和qRT-PCR定量相关实验, 结果表明基因在SrMV易感品种ROC22和FN40中上调表达, 在抗性品种YZ01-1413中下调表达[37]。由于没有找到SCYLV侵染甘蔗的中间载体, 也无法通过人工对甘蔗实现该病毒的接种, 因此并没有相关材料。但相关研究表明, SA或MeJa信号通路与病毒侵染相关[13], 因此我们用SA或MeJa模拟病毒等生物胁迫侵染。截至目前, 植物中的基因在ABA、MeJA、SA等激素处理条件的定量表达分析尚无人报道。ABA是响应干旱、盐胁迫等非生物的关键调控因子[45]。在本研究中, 发现短时间的ABA处理可以引起基因上调表达。推测其原因是: 在施加ABA后, 甘蔗叶片缺水、细胞渗透压变化, 引起光合效率降低, 植物为了补偿光合作用而上调表达光合组分基因, 但长时间的高表达对植物造成负担, 于是降低基因表达量以适应低光合作用。SA、JA作为植物系统获得抗性(systemic acquired resistance, SAR)和诱导系统抗性(induced systemic resistance, ISP)的重要信号分子[46]。SA、MeJA处理甘蔗后,基因下调表达, 说明在植物受生物胁迫过程中, 植物可能通过抑制的表达, 降低光合作用。用CuCl2、CdCl2溶液处理后, 甘蔗因受到重金属离子的毒害作用,下调表达。NaCl处理条件下,基因的表达量下降, 这与黄瓜幼苗在NaCl胁迫下, 叶片中的基因的下调表达结果相似, 这同样可能是由于高盐环境的刺激引起了甘蔗叶片气孔闭合, CO2吸收量下降, 光合电子传递速率降低[47]。
4 结论
从甘蔗主栽品种新台糖22号叶片中成功分离到基因, 该基因长824 bp, 包含一个678 bp的ORF, 编码226个氨基酸, 含有半胱氨酸和组氨酸[2Fe-2S]结合域, 属于PRK13474超家族。ScPetC为碱性稳定亲水非分泌蛋白, 其二级结构只有α螺旋、延伸链、无规则卷曲; 从ScPetC的序列、三维结构推测, PetC蛋白在植物中高度保守, 具有相似的生物学功能。ScPetC定位于细胞质、叶绿体和细胞膜, 与SrMV-P1蛋白不存在互作, 但与SCYLV-P0蛋白存在互作。基因在甘蔗叶片中的表达量最高, 在蔗肉、蔗芽、蔗皮表达量较低, 在根中几乎不表达。在外源激素SA和MeJA、重金属 (CuCl2、CdCl2)和高盐(NaCl)溶液处理下, 均呈现下调表达; 但短时间ABA处理, 可以引起基因的上调表达。
[1] Yadav R L, Solomon S. Potential of developing sugarcane by product based industries in India., 2006, 8: 104–111.
[2] 何炎森, 李瑞美. 甘蔗花叶病研究现状. 中国糖料, 2006, (1): 47–49. He Y S, Li R M. Research status ofdisease in China., 2006, (1): 47–49 (in Chinese with English abstract).
[3] Diaz O D L C A, Hechavarra M D L L O, Izaguirre Y P, Navarro M D L A Z, Lopez J M M L, Lissbrant S, Arencibia A. Genotyping ofin commercial cultivars and the Cuban germplasm collection., 2016, 19: 102–108.
[4] 王伯辉. 我国甘蔗病害的发生现状与研究进展. 中国糖料, 2007, (3): 261–265. Wang B H. The occurrence status and research progress of surgarcane disease in China., 2007, (3): 261–265 (in Chinese with English abstract).
[5] Shukla D D, Frenkel J M, McKern M N, Ward C W, Jilka J, Tosic M, Ford R E. Present status of the sugarcane mosaic subgroup of potyviruses., 1992, 5: 363–373.
[6] Elsayed A I, Komor E. Investigation of ORF0 as a sensitive alternative diagnostic segment to detect., 2012, 78: 207–216.
[7] Mirkov T E, Ingelbrecht I, Castillon A, Hernandez J C. Identification of sugarcane proteins involved in posttranscriptional gene silencing., 2001, 24: 327–330.
[8] Shan H Y, Pasin F, Valli A, Castillo C, Rajulu C, Carbonell A, Mateo S C, García J A, Rodamilans B. TheP1a leader protease contributes to host range specificity., 2015, 476: 264–270.
[9] Fabio P, Carmen S M, Antonio G J. The hypervariable amino terminus of P1 protease modulates potyviral replication and host defense responses., 2014, 10: e1003985. doi 10.1371/journal.ppat.1003985.
[10] Mangwende T, Wang M L, Borth W, Hu J, Moore P H, Mirkov T E, Albert H H. The P0 gene ofencodes an RNA silencing suppressor with unique activities., 2009, 384: 38–50.
[11] Veidt I, Bouzoubaa S E, Leiser R M, Zieglergraff V A, Guilley H, Richards K, Jonard G. Synthesis of full-length transcripts ofRNA messenger properties and biological activity in protoplasts.,1992, 186: 192–200.
[12] 燕照玲, 段俊枝, 冯丽丽, 陈海燕, 齐红志, 杨翠苹, 施艳, 张会芳. 马铃薯Y病毒属病毒编码蛋白与寄主植物叶绿体蛋白互作研究进展. 河南农业科学, 2017, 46(11): 1–5. Yan Z L, Duan J Z, Feng L L, Chen H Y, Qi Z H, Yang C P, Shi Y, Zhang H F. Progress on interaction between potyviruses coded proteins and chloroplast proteins of host plants., 2017, 46(11): 1–5 (in Chinese with English abstract).
[13] Zhao J P, Zhang X, Hong Y G, Liu Y L. Chloroplast in plant virus interaction., 2016, 7: 1565. doi: 10.3389/ fmicb.2016.01565.
[14] Lin L, Luo Z P, Yan F, Lu Y W. Interaction between potyvirus P3 and ribulose-1,5-bisphosphate carboxylase/oxygenase (RubisCO) of host plants., 2011, 43: 90–92.
[15] 翟玉山, 赵贺, 张海, 邓宇晴, 程光远, 杨宗桃, 王彤, 彭磊, 徐倩, 董萌, 徐景升. 甘蔗NAD(P)H脱氢酶复合体O亚基基因克隆及其与甘蔗花叶病毒VPg互作研究, 作物学报, 2019, 45: 1478–1487. Zhai Y S, Zhao H, Zhang H, Deng Y Q, Cheng G Y, Yang Z T, Wang T, Peng L, Xu Q, Dong M, Xu J S. Cloning of NAD(P)H complex O subunit gene and its interaction with VPg of., 2019, 45: 1478–1487 (in Chinese with English abstract).
[16] Shi Y, Chen J, Hong X, Chen J, Adams M J. A potyvirus P1 protein interacts with the Rieske Fe/S protein of its host., 2010, 8: 785–790.
[17] Pazhouhandeh M, Dieterle M, Marrocco K, Lechner E, Berry B, Brault V, Hemmer O, Kretsch T, Richards K E, Genschik P, Graff V Z. F-box-like domain in the polerovirus protein P0 is required for silencing suppressor function., 2006, 103: 1994–1999.
[18] Sun Q Q, Li Y Y, Wang Y, Zhao H H, Zhao T Y, Zhang Z Y, Li D W, Yu J L, Wang X B, Zhang Y L, Han C G.BrYV P0 protein impairs the antiviral activity of NbRAF2 in, 2018, 69: 3127–3139.
[19] 李合生. 现代植物生理学(第3版). 北京: 高等教育出版社, 2012. pp 114–118. Li H S. Modern Plant Physiology, 3rd edn. Beijing: Higher Education Press, 2012. pp 114–118 (in Chinese).
[20] Schottler M A, Tóth S Z, Boulouis A. Photosynthetic complex stoichiometry dynamics in higher plants: biogenesis, function, and turnover of ATP synthase and the cytochrome bfcomplex., 2015, 66: 2373–2400.
[21] Rieske J S, Zaugg W S, Hansen R E. Studies on the electron transfer system., 1964, 242: 2051–2061.
[22] Rieske J S. Composition, structure, and function of complex III of the respiratory chain., 1976, 456: 195–247.
[23] Steppuhn J, Rother C, Hermans J, Jansen T. The complete amino acid sequence of the Rieske Fe/S precursor protein from spinach chloroplasts deduced from cDNA analysis., 1987, 210: 171–177.
[24] Salter A H, Newman B J, Napier J, Gray J C. Import of the precursor of the chloroplast Rieske iron-sulfur protein by pea chloroplasts., 1992, 20: 569–574.
[25] Knight J S, Duckett C M, Sullivan J A, Walker A R, Gray J C. Tissue-specific, light-regulated and plastid-regulated expression of the single-copy nuclear gene encoding the chloroplast Rieske Fe/S protein of., 2002, 43: 522–531.
[26] Madueno F, Bradshaw S A, Gray J C. The thylakoid-targeting domain of the chloroplast Rieske iron-sulfur protein is located in the N-terminal hydrophobic region of the mature protein., 1994, 26: 17458–17463.
[27] Vitry C D. Characterization of the gene of the chloroplast Rieske iron-sulfur protein inindications for an uncleaved lumen targeting sequence., 1994, 269: 7603–7609.
[28] Carrell C J, Zhang H, Cramer W A, Smith J L. Biological identity and diversity in photosynthesis and respiration: structure of the lumen side domain of the chloroplast Rieske protein., 1997, 5: 1613–1625.
[29] Hasan S S, Yamashita E, Cramer W A. Transmembrane signaling and assembly of the cytochromebf-lipidic charge transfer complex., 2013, 1827: 1295–1308.
[30] Cramer W A, Hasan S S, Yamashita E, Kahlau S. The Q cycle of cytochromebccomplexes: a structure perspective., 2011, 1807: 788–802.
[31] Yamori W, Kondo E, Sugiura D, Terashima I, Suzuki Y, Makino A. Enhanced leaf photosynthesis as a target to increase grain yield: insights from transgenic rice lines with variable Rieske Fe/S protein content in the cytochromebf complex., 2016, 39: 80–87.
[32] Simkin A J, Lorna M, Lawson T, Raines C A. Over-expression of the Rieske Fe/S protein increases electron transport rates and biomass yield., 2017, 175: 134–145.
[33] Sanda S, Munekage Y N, Yoshida K, Akashi K, Yokota A. Excess light-induced molecular responses of chloroplast Rieske Fe/S protein., 2008, 14: 941–944.
[34] 梁潘霞, 李杨瑞. 甘蔗细胞色素bf复合体铁硫亚基()基因的克隆和表达分析. 西南农业学报, 2016, 29: 1032–1037. Liang P X, Li L R. Cloning of cytochromecomplex iron-sulfur subunit () from sugarcane and analysis of its expression under PEG stress., 2016, 29: 1032–1037 (in Chinese with English abstract).
[35] Luo M, Kong X Y, Jiang T, Jia C, Zhou R H, Jia J Z. Analysis of resistance toin wheat based on Expressed Sequence Tags (EST) technique., 2002, 44: 567–572.
[36] 阙友雄, 林剑伟, 徐景升, 阮秒鸿, 许莉萍, 张木清, 陈由强, 陈如凯. 甘蔗与黑穗病菌互作的叶片差异蛋白分析. 热带作物学报, 2008, 29: 136–140. Que Y X, Lin W J, Xu J S, Ruan M H, Xu L P, Zhang M Q, Chen Y Q, Chen R K. Analysis of protein expression patterns of leaves from interaction between sugarcane and., 2008, 29: 136–140 (in Chinese with English abstract).
[37] Ling H, Huang N, Wu Q B, Su Y C, Peng Q, Ahmed W, Gao S W, Su W H, Que Y X, Xu L P. Transcriptional insights into the sugarcane-interaction., 2018, 11: 163–176.
[38] 黄宁, 张玉叶, 凌辉, 罗俊, 吴期滨, 阙友雄. 甘蔗二氨基庚二酸异构酶基因的克隆与表达分析. 热带作物学报, 2013, 34: 2200–2208. Huang N, Zhang Y Y, Ling H, Luo J, Wu Q B, Que Y X. Cloning and expression analysis of a diaminopimelate epimerase gene in sugarcane., 2013, 34: 2200–2208 (in Chinese with English abstract).
[39] 苏亚春, 黄珑, 凌辉, 王竹青, 刘峰, 苏炜华, 黄宁, 吴期滨, 高世武, 阙友雄. 甘蔗基因的cDNA全长克隆与表达分析. 作物学报, 2017, 43: 42–50. Su Y C, Huang L, Ling H, Wang Z Q, Liu F, Su W H, Huang N, Wu Q B, Gao S W, Que Y X. Cloning and expression analysis ofGene in sugarcane.2017, 43: 42–50 (in Chinese with English abstract).
[40] Liu F, Huang N, Wang L, Ling H, Sun T T, Ahmad W, Muhammad K, Guo J X, Xu L P, Gao S W, Que Y X, Su Y C. A novel L-ascorbate peroxidase 6 gene,, plays an important role in the regulation of response to biotic and abiotic stresses in sugarcane., 2017, 8: 2262. doi: 10.3389/fpls.2017. 02262.
[41] Schmidt C L, Shaw L. A comprehensive phylogenetic analysis of Rieske and Rieske-type iron-sulfur proteins., 2001, 33: 9–26.
[42] Schütze K, Harter K, Chaban C. Bimolecular fluorescence complementation (BiFC) to study protein-protein interactions in living plant cells., 2009, 479: 189–202.
[43] Guo J L, Ling H, Wu Q B, Xu L P, Que Y X. The choice of reference genes for assessing gene expression in sugarcane under salinity and drought stresses., 2014, 4: 7042. doi: 10.1038/srep07042.
[44] 郑红英. TuMV HC-Pro蛋白自身互作及其与拟南芥编码Rieske Fe/S蛋白的互作研究. 华中农业大学博士学位论文, 湖北武汉, 2011. Zheng H Y. The Self Interaction of TuMV HC-Pro and Its Interaction with Rieske Fe/S Protein Encoded by. PhD Dissertation of Huazhong Agricultural University, Wuhan, Hubei, China, 2011 (in Chinese with English abstract).
[45] Dashevskaya S, Horn R, Chudobova I, Schillberg S, Velez S M R, Capell T. Abscisic acid and the herbicide safener cyprosulfamide cooperatively enhance abiotic stress tolerance in rice., 2013, 32: 463–484.
[46] Liu B, Xue X D, Cui S P, Zhang X Y, Han Q M, Zhu L, Liang X F, Wang X J, Huang L L, Chen X M, Kang Z S. Cloning and characterization of a wheat β-1,3-glucanase gene induced by the stripe rust pathogenf. sp.., 2010, 37: 1045–1052.
[47] 严蓓. 钙缓解黄瓜幼苗NaCl胁迫伤害的蛋白质组学及光合碳代谢研究. 南京农业大学硕士学位论文, 江苏南京, 2013. Yan P. Proteomics and Photosynthetic Carbon Metabolism Research on Calcium Alleviating Salt Stress of Cucumber Seedlings. MS Thesis of Nanjing Agricultural University, Nanjing, Jiangsu, China, 2013 (in Chinese with English abstract).
Cloning and expression analysis of sugarcane Fe/S precursor protein gene
ZHENG Qing-Lei1, YU Chen-Jing1, YAO Kun-Cun1, HUANG Ning1, QUE You-Xiong1,4, LING Hui2,3,*, and XU Li-Ping1,4,*
1Key Laboratory of Sugarcane Biology and Genetic Breeding (Fujian), Ministry of Agriculture and Rural Area / Fujian Agriculture and Forestry University, Fuzhou 350002, Fujian, China;2College of Life Science, Fujian Agriculture and Forestry University, Fuzhou 350002, Fujian, China;3College of Crop Science, Yulin Normal University, Yulin 537000, Guangxi, China;4Key Laboratory of Crop Genetics and Breeding and Comprehensive Utilization, Ministry of Education / Fujian Agriculture and Forestry University, Fuzhou 350002, Fujian, China
Cytochrome bf complex Rieske Fe/S precursor protein (PetC) is encoded by the nucleargene, and its mature protein involved in the formation of the cytochromebfcomplex, which is important for electron transfer. Based on our previous transcriptome data of sugarcane (spp. hybrids) infectedby(SrMV), a cytochrome bf complex reduced iron-sulfur precursor protein gene was cloned from leaves of sugarcane superior elite cultivar ‘ROC22’, and named as(GenBank accession number: MH333037.1). Bioinformatics analysis showed that thegene was 824 bp in length, containing a 678 bp open reading frame (ORF), and encoding a peptide of 226 amino acids. ScPetC belongs to the PRK13473 superfamily and has a typical Rieske domain at its C-terminus of the amino acid chain. ScPetC is a stable and hydrophilic protein with pI 8.19. Most of the secondary structural elements in ScPetC were random coil. Compared to the PetC from the other plants, ScPetC contained one more fragment of helix in its third dimensional structure. The transient expression of YFP-fused protein inleaves showed that ScPetC was located in the chloroplast, cytoplasm and cell membrane. Although the previous study indicated that the expression ofwas affected by SrMVinfection in sugarcane, different to the interaction betweenPetC and SMV-P1, without interaction between ScPetC and the SrMV-P1, it did interact with SCYLV-P0, i.e. the P0 protein of(SCYLV). Real-time quantitative PCR analysis showed thatgene was expressed constitutively in different tissues of sugarcane, and the highest level of its expression was found in leaves. When sugarcane plant was exposed to abscisic acid stress for 3 h, the expression ofwas significantly up-regulated, but the expression level was then inhibited with longer treatment time. Under the stress of methyl jasmine, salicylic acid, copper chloride, cadmium chloride and sodium chloride, the expression ofwas significantly down-regulated. The study on biological function, expression pattern and interaction of ScPetC with the proteins of sugarcane pathogenic virus will improve the understanding of the happening of yellow leaf symptom, which caused by SCYLV.
sugarcane; cytochrome bf complex Rieske Fe/S precursor protein; bioinformatics; subcellular location; protein interaction; real-time flourescent quantitative PCR
10.3724/SP.J.1006.2020.94171
本研究由国家自然科学基金项目(31801424)和国家现代农业产业技术体系建设专项(CARS-17)资助。
This study was supported by the National Natural Science Foundation of China (31801424) and the China Agriculture Research System (CARS-17).
许莉萍, E-mail:xlpmail@126.com; 凌辉, E-mail: linghuich@163.com
E-mail: zhengqinglei1666@163.com.
2019-11-10;
2020-01-15;
(网络出版日期): 2020-02-17.
URL: http://kns.cnki.net/kcms/detail/11.1809.S.20200215.1522.002.html
