制备工艺对重晶石-硼硅酸盐玻璃陶瓷结构及性能的影响
2020-05-19杨远波张海洋
雷 杰,吴 浪,江 枫,杨远波,张海洋,康 泽
(西南科技大学材料科学与工程学院,绵阳 621010)
0 引 言
高放废液(High Level Liquid Waste,HLLW)主要来自乏燃料后处理过程中铀钚共去污循环产生的萃余液[1],具有放射性强、半衰期长、释热量高等特点,对生物圈造成了极大的威胁。因此,HLLW的安全处理和处置受到世界各国的高度关注。硼硅酸盐玻璃因具有良好的抗辐照、化学稳定性和耐水性等,是包括中国在内的很多国家固化高放废液的首选玻璃固化材料[2-4]。
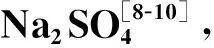
在含硫的矿物中,重晶石(BaSO4)矿物的化学稳定性和热稳定性最高[11-14]。课题组前期研究结果表明[15],在模拟废液中加入Ba(NO3)2溶液,模拟废液中的Na2SO4会与Ba(NO3)2反应生成BaSO4。因此,实验中采用BaSO4代替Na2SO4引入硫。当BaSO4掺量较高(SO3≥5wt%)时,玻璃陶瓷体内存在未完全溶解的BaSO4晶体,对硫酸盐具有较高的包容量。值得注意的是,该研究中是将基础玻璃原料与模拟废物氧化物直接混合熔制获得玻璃陶瓷固化体。而工业生产中是先制得硼硅酸盐玻璃球,再与模拟废液混合熔制获得硼硅酸盐玻璃固化体。王孝强等[6]的研究表明,玻璃固化体样品的准备方式对玻璃包容硫的能力有显著影响。
由于共存物相和实验条件对硫酸盐的分解温度影响较大[16],因此,本文拟采用工艺A(将基础玻璃原料与BaSO4直接混合熔制)、工艺B(将基础玻璃原料煅烧后再与BaSO4混合熔制)和工艺C(先制得玻璃再与BaSO4混合熔制)分别制备玻璃陶瓷固化体,根据固化体的物相组成、显微结构、硫含量以及抗浸出性能等实验数据对比,筛选出较佳的熔制工艺,为含硫高放废液的固化提供技术参考和实验数据支撑。
1 实 验
1.1 样品制备
用分析纯的化学试剂SiO2、H3BO3、Na2CO3、Li2CO3、Al2O3、CaCO3、TiO2、MgO、BaSO4为原料,采用熔融法制备重晶石-玻璃陶瓷固化体。根据文献[15]选择硫酸盐包容硫含量较高(~2.17wt%,以SO3计)的玻璃配方作为本实验的研究配方,玻璃中各氧化物含量分别为:SiO2,56.21wt%;B2O3,20.68wt%;Na2O,4.7wt%;Li2O,2.16wt%;Al2O3,3.29wt%;CaO,5.08wt%;TiO2,0.94wt%;MgO,0.94wt%;SO3,6wt%。SO3以BaSO4的形式引入。根据配比称取原料,在玛瑙研钵中充分混合均匀。将混合物利用不同工艺在高温下熔融制得重晶石-玻璃陶瓷固化体,随后在马弗炉中退火1 h。不同工艺的制备条件为:
(1)工艺A:将基础玻璃原料直接与BaSO4混合,在750 ℃下煅烧2 h,然后在1 200 ℃下熔融3 h,所得样品称为样品A;
(2)工艺B:将基础玻璃原料在750 ℃下煅烧2 h,再与BaSO4混合,在1 200 ℃熔融3 h,所得样品称为样品B;
(3)工艺C:先将基础玻璃原料在750 ℃下煅烧2 h,再升到1 200 ℃熔融3 h,熔制成玻璃,再与BaSO4混合,1 200 ℃下熔融3 h,所得样品称为样品C。
1.2 样品表征
用DMAX1400型X射线衍射仪(X-ray Diffractometer,XRD)分析样品的物相组成。将样品打磨、抛光、超声清洗后,用EVO 18型扫描电子显微镜(Scanning Electron Microscope,SEM)以及Oxford IE450X-Max80能谱仪(Energy Disperse Spectroscopy,EDS)分析样品断面的微观形貌及成分。采用STA449F5同步热分析仪(Synchronous Thermal Analyzer,TG-DSC),以20 ℃/min的升温速率在N2气氛下从室温升到1 200 ℃,分析不同样品的质量损失情况。用Axios型X射线荧光光谱仪(X-ray Fluorescence Spectrometer,XRF)分析样品中SO3的含量。采用阿基米德排水法测定玻璃陶瓷的体积密度。用Nicolet-5700傅里叶红外吸收光谱仪(Infrared Absorption Spectrometer,FTIR)进行红外光谱测试。
1.3 抗浸出性能测试
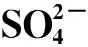
(1)
式中:LRi为固化体中元素i的归一化浸出率,g·m-2·d-1;Ci为浸出液中元素i的质量浓度,g/m3;S为固体颗粒表面积之和;V为浸出液的体积,按标准S/V取为2 000 m-1;fi为样品中元素i所占的质量分数;Δt为间隔时间,d。
2 结果与讨论
2.1 样品的物相组成和显微结构
图1是不同工艺制备样品的外观照片。由图1可知,样品中均存在白色晶体,其中样品A和样品B中晶体较少,与文献[15]获得的样品相似,白色晶体主要分布在玻璃基体表面,样品C表面和内部均存在较多的白色晶体。图2是不同工艺制备样品的XRD谱。由图2可知,样品中均检测到了BaSO4晶相(PDF No.76-0213),其中样品A和样品B的衍射峰强度较弱,样品C的衍射峰强度较强,表明工艺C制得的样品中BaSO4晶体含量较高,与图1样品外观照片分析结果一致。

图1 不同工艺制备样品的外观照片Fig.1 Appearance of different process samples
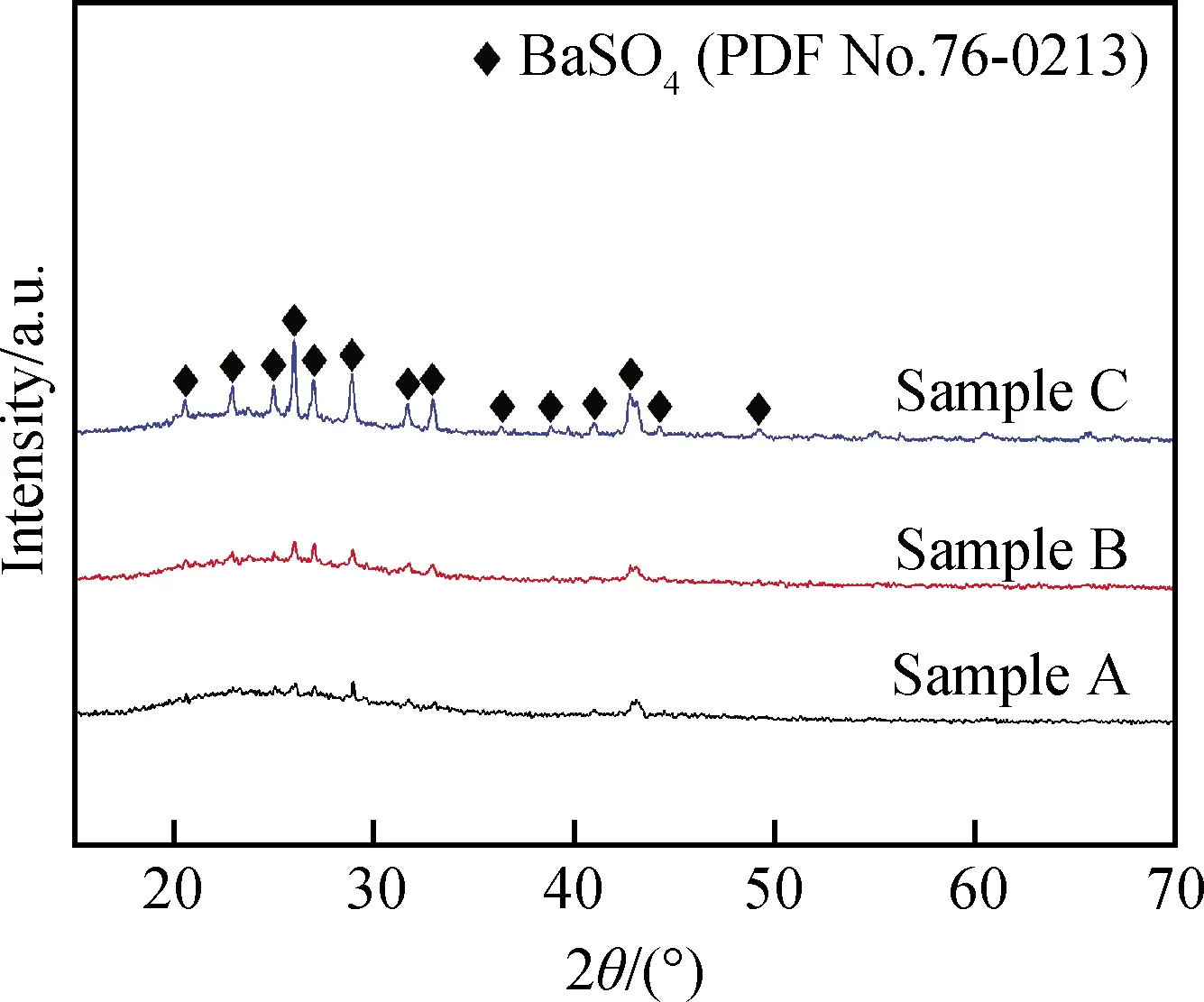
图2 不同工艺制备样品的XRD谱Fig.2 XRD patterns of different process samples
图3(a)~(c)分别是样品A、样品B和样品C断面的背散射(BSE)照片(200倍),图3(d)显示了样品C的局部放大BSE照片(2 000倍)。由图3(a)~(c)可知,样品A与样品B的晶体含量接近,分布较少。而样品C中晶体含量明显增多,分布密集。从图3(d)可以看出,样品C中晶体上有很多微孔,晶体与玻璃的界面附近存在明显的孔隙。图3(e)和图3(f)分别是样品C中的A点晶相和B点玻璃相的EDS谱。由图3(e)可知,A点主要由Ba、S和O元素组成,原子比例分别为19.10%、18.42%、62.48%,比值约为1.04∶1∶3.39。结合XRD分析结果可知,该白色晶体为BaSO4。图3(f)显示B点主要由Si、Na、Al、Ca和Ti元素组成,还含有少量Ba元素,表明部分BaSO4可能在高温下分解生成了BaO,成为网络修饰体进入了玻璃基体。
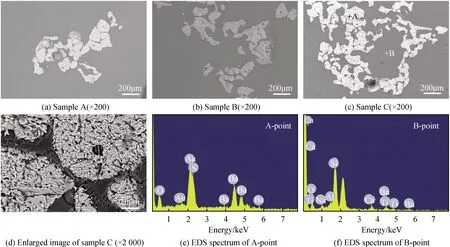
图3 不同工艺制备样品断面的BSE照片和EDS谱Fig.3 BSE images and EDS spectra of sample sections prepared by different processes
图4是不同工艺制备样品的红外吸收光谱。由图4可知,红外光谱中主要有4个特征峰,波数为466 cm-1附近处的吸收峰为[SiO4]中Si-O-Si的弯曲振动峰,611 cm-1处为[BO4]中B-O-B的振动吸收峰,1 086 cm-1附近处为[SiO4]中Si-O-Si反对称伸缩振动峰和[BO4]中B-O-B的反对称伸缩振动峰的合峰,1 385 cm-1处为[BO3]中B-O-B的反对称伸缩振动峰[17-19]。相对于样品C,样品A与样品B的红外曲线相似,611 cm-1处[BO4]中B-O-B的振动吸收峰显著减弱,说明[BO4]含量减少。
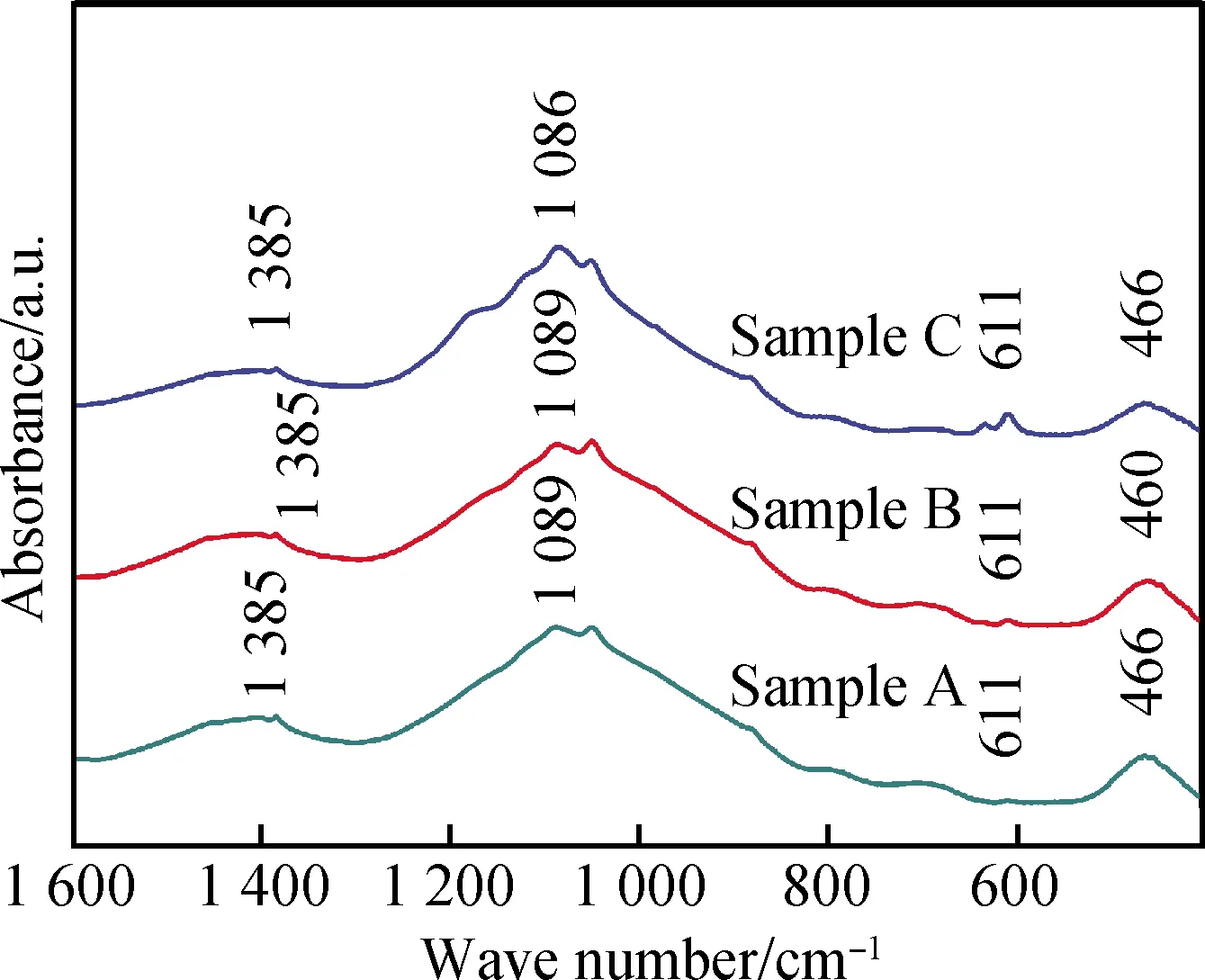
图4 不同工艺制备样品的红外吸收光谱Fig.4 FTIR spectra of different process samples
图5是不同工艺制备样品在800~1 300 cm-1波段的分峰图。可以看到相对于样品C,样品A和样品B在波数为1 100 cm-1附近对应[BO4]中B-O-B的反对称伸缩振动峰有所减弱,也说明[BO4]含量减少。这可能是由于样品A与样品B在熔制过程中BaSO4分解相对较多,生成的BaO作为网络修饰体进入玻璃基体,非桥氧的增加导致[BO4]出现部分解体,使[BO4]含量减少,[BO3]相应增加[20-22]。上述结果表明,样品A和样品B的[BO4]/[BO3]比值较低,玻璃网络结构疏松,密度较小[23-24]。另一方面,样品C中BaSO4晶体较多,BaSO4的密度较高(~4.5 g/cm3),应具有较高的密度;而通过阿基米德排水法测得样品A、样品B和样品C的体积密度基本相同,分别为2.55 g/cm3、2.53 g/cm3和2.54 g/cm3,表明样品C不够致密,这与BSE分析结果一致。
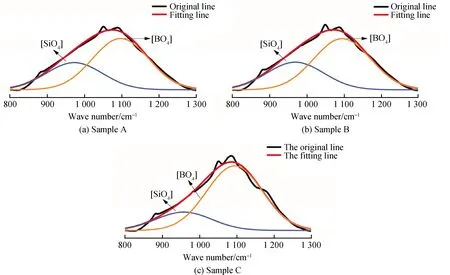
图5 不同工艺制备样品在800~1 300 cm-1波段处红外分峰光谱Fig.5 Infrared peak splitting spectra of different process samples at of 800-1 300 cm-1 band
2.2 样品的硫含量及差热分析
样品A中硫含量为2.04wt%(以SO3计),样品B为2.19wt%,样品C为4.45wt%。样品A与样品B的硫含量相差不大,而样品C中的硫含量达4.45wt%,这是因为样品C中BaSO4较多,而S元素基本保留在BaSO4中。此外,在不同工艺制备的样品中的硫含量都低于原始硫的加入量,说明在熔融过程中部分BaSO4发生了分解,导致硫含量降低,这与图3的BSE-EDS分析结果一致。
图6为不同工艺制备样品的TG曲线。由图可知,样品A的TG曲线在100~200 ℃之间下降,主要为硼酸的分解,500~730 ℃之间主要为碳酸盐的分解,730 ℃以后TG曲线基本平稳,说明碳酸盐已经分解完全。在860~1 200 ℃的温度范围内,样品A、样品B和样品C的质量损失率分别为1.876%、1.610% 和1.434%。在此温度范围内的质量损失可认为主要是样品中Na、B、Li等元素的挥发以及BaSO4的分解,其中样品C的质量损失率最小,可能是因为样品C中BaSO4分解最少,从而导致玻璃陶瓷体内BaSO4含量最高,这与XRF分析结果一致。
2.3 样品的抗浸出性能
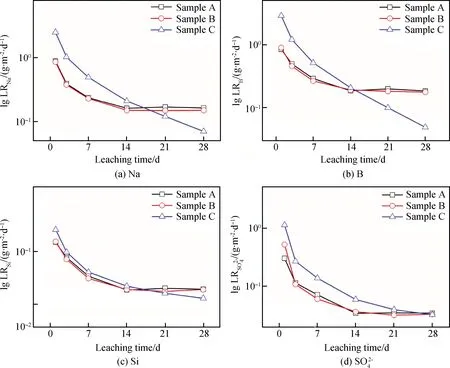
图7 不同工艺制备样品中Na、B、Si元素和的归一化浸出率Fig.7 Normalized leaching rates of Na, B, Si and of different process samples
3 结 论
(1)工艺A和工艺B对玻璃陶瓷结构和性能影响不大,工艺C制得的样品体内BaSO4含量较高,包容硫含量高达4.45wt%(以SO3计)。
(2)样品中未溶解的BaSO4晶体存在大量微孔,样品C致密度较低。
(3)样品C的Na、B、Si元素初始浸出速率较高,在28 d后归一化浸出率较低(~10-2g·m-2·d-1),抗浸出性能较好。
