基于网络药理学的桂枝甘草汤抗失眠作用的潜在机制研究
2020-05-15黄强汪亚楠韩飞刘明
黄强 汪亚楠 韩飞 刘明


〔摘要〕 目的 利用網络药理学技术对桂枝甘草汤抗失眠的潜在作用机制进行探讨研究。方法 首先,利用TCMSP、Swiss、SuperPred和Stitch数据库寻找与桂枝甘草汤方中2味中药材有关的化学成分及其可能的作用靶点,并设定OB≥30%、DL≥0.18为阈值对化学成分进行筛选,再利用文献检索加以补充;同时,通过OMIM、TTD、Gene Card、 Pharm Gkb等数据库获取与失眠症相关的靶标,并进一步建立桂枝甘草汤抗失眠作用的靶点;然后,利用DAVID数据库对失眠症相关的作用靶点进行GO及KEGG富集分析;最后,采用Cytoscape软件构建“单味药-活性成分-作用靶点”相互作用网络并进行度值和介数值分析,确认关键靶点和关键通路。结果 在桂枝甘草汤中,共筛选出101个与失眠相关的潜在活性成分,主要涉及MAPT、ESR1、CYP19A1等85个潜在作用靶点;GO 生物功能分析共包含293条富集结果,主要涉及蛋白结合、质膜等;KEGG富集分析得到18条代谢通路,主要包括神经活性配体-受体相互作用通路、钙信号通路、5-羟色胺能突触通路等。结论 本研究揭示了桂枝甘草汤治疗失眠症的“多成分-多靶点-多途径”的作用特点,并预测了其可能的活性成分、关键靶点和作用通路,为其药效物质基础和作用机制研究提供了理论基础。
〔关键词〕 失眠;桂枝甘草汤;网络药理学;靶点;作用机制
〔中图分类号〕R256.23 〔文献标志码〕A 〔文章编号〕doi:10.3969/j.issn.1674-070X.2020.04.013
Potential Mechanism of Anti-insomnia Effect of Guizhi Gancao Decoction Based on
Network Pharmacology
HUANG Qiang1, WANG Yanan2, HAN Fei2, LIU Ming1*
(1. Patent Examination Cooperation Jiangsu Center of the Patent Office, State Intellectual Property Office, Suzhou, Jiangsu 215163, China; 2. Shenyang Pharmaceutical University, Shenyang, Liaoning 110016, China)
〔Abstract〕 Objective To study the potential mechanism of the anti-insomnia effect of Guizhi Gancao Decoction (GGD) by using network pharmacological technology. Methods Firstly, TCMSP, Swiss, SuperPred and Stitch databases were used to search for the chemical compounds and the possible targets related to the 2 herbs in GGD. OB ≥ 30%, DL ≥ 0.18 were set as screening conditions to screen for chemical compounds. Literatures were searched for supplement. Meanwhile, the targets related to insomnia were screened through OMIM, TTD, Gene Card and Pharm Gkb databases. Moreover, the interactive targets of GGD and insomnia were further constructed. Then, GO analysis and KEGG enrichment analysis of insomnia related targets were performed using DAVID database. Finally, degree and betweenness analysis were performed to find key targets and key pathways after the “single herb-active compounds-acting targets” interaction network was constructed by Cytoscape software. Results A total of 101 potential active compounds related to insomnia were screened in GGD, which mainly involved 85 potential targets such as MAPT, ESR1 and CYP19A1. A total of 293 enrichment results were obtained by GO analysis, mainly involving protein binding, plasma membrane, etc. 18 metabolic pathways were obtained through KEGG analysis, mainly including neuroactive ligand-receptor interaction pathway, calcium signaling pathway, serotonergic synapse and etc. Conclusion This study revealed the action characteristics of GGD with “multi-compounds, multi-targets and multi-pathways” in the treatment of insomnia and predicted its possible active ingredients, key targets and action pathways, which provided a theoretical basis for the study of its pharmacodynamic material basis and action mechanism.
〔Keywords〕 insomnia; Guizhi Gancao Decoction; network pharmacology; targets; action mechanism
失眠通常是指患者对睡眠时间和(或)质量不满足而影响日间社会功能的一种主观体验,临床表现为入睡困难、睡眠维持障碍、早醒、睡眠质量下降、总睡眠时间减少并同时伴有日间功能障碍等[1-2]。近年来,随着经济的发展,人们的生活压力越来越大,我国失眠群体正趋于年轻化。2018年中国睡眠研究会数据显示,我国超过60%的重度失眠患者为90后[3]。而且已有多项研究表明,失眠往往与人体多个系统的生理功能紊乱和多种疾病的发生发展具有密切的关系[4-5]。然而,失眠的形成原因多样、发生机制复杂、临床研究尚不充分,针对其治疗的药物也多以镇静催眠类西药为主,且这些药物普遍具有成瘾性,患者长期服用易产生药物依赖性,在治疗过程中往往难以取得理想的疗效[6-7]。因此,研究开发可有效防治失眠且毒副作用小的药物具有重大意义。
传统中医认为人的睡眠是营卫之气正常循行,阴阳之气规律转化的结果,当这种规律性遭到破坏时,人体就会出现睡眠障碍,而中医药可通过辨证论治补其不足,泻其有余,调其虚实,使气血调和,阴阳平衡,从根本上对机体进行调节达到痊愈的目的[8]。而且,中医药治疗失眠既不会产生成瘾性、依赖性和耐药性,且不良反应少,毒副作用小,故用中医药辨证治疗失眠具有很大的优势。中药桂枝甘草汤出自汉代张仲景名著《伤寒论》,是由桂枝和甘草两味中药组成,具有温补心阳、生阳化气之功效,是治疗心阳虚之祖方[9]。近期,我们通过研究桂枝甘草汤对腹腔注射氯苯丙氨酸所致失眠模型大鼠的影响发现,桂枝甘草汤可通过调控大鼠血浆和脑组织内神经递质5-HT、NE、DA的平衡而达到抗失眠的药理作用。由此可见,桂枝甘草汤具有潜在的抗失眠作用。
英国药理学家Hopkins[10]于2007年在系统生物学与多向药理学的基础上首次提出了网络药理学的概念。该技术是利用生物分子网络分析方法,通过网络中节点的连接和节点之间的相互作用关系来分析网络的特征,从多维度视角探索药物干预疾病的分子机制,特别适用于多成分、多靶点、多途径的中药药效物质基础和作用机制的研究[11-13]。因此,本研究尝试采用网络药理学的方法和思维,通过构建“单味药-活性成分-作用靶点”网络模型系统地预测桂枝甘草汤抗失眠症“多成分-多靶点-多途径”的作用特点,以期为进一步研究其抗失眠的药效物质和作用机制提供理论依据。
1 材料与方法
1.1 软件与数据库
TCMSP数据库(http://lsp.nwu.edu.cn/);ChemBioDraw软件;Swiss数据库(http://www.swisstargetprediction.ch/);SuperPred数据库(http://prediction.charite.de/);Stitch数据库(http://stitch.embl.de/); String数据库(https://string-db.org/);OMIM数据库(http://www.omim.org/);TTD数据库(http://bidd.nus.edu.sg/BIDD-Databases/TTD/);PharmGkb数据库(https://www.pharmgkb.org/);Gene Card数据库(https://www.genecards.org/);Uniprot数 据 库(http://www.unipr?鄄ot.org/);DAVID 6.8数据库(https://david. ncifcrf.gov/);Cytoscape软件(Version 3.4.0);OriginPro软件(Version 8.0);Omicshare平台(http://www.omicshare.com/tools/index.php/)。
1.2 方法
1.2.1 桂枝甘草汤化学成分信息的归纳和整理 利用TCMSP数据库并结合文献检索收集与桂枝甘草汤中的2味药材相关的化学成分信息并保存其化学结构,然后采用ChemBioDraw软件得到化学成分结构的Smiles格式。
1.2.2 活性成分的筛选 收集的化学成分中,以同时满足OB≥30%、DL≥0.18为条件进行化合物筛选,得到桂枝甘草汤的潜在活性成分。同时,通过结合文献挖掘和整理,对筛选结果进行补充,尽可能全面地获得桂枝甘草汤的主要活性成分。
1.2.3 靶点的预测 在Swiss、SuperPred、Stitch数据库中上传桂枝甘草汤潜在活性成分的Smiles结构进行靶点预测,将所得靶点去重后即得活性成分相关靶点信息。以“insomnia”为关键词在OMIM、TTD、Gene Card、PharmGkb数据库中进行检索获取相关靶点信息,将得到的靶点利用Uniprot矫正并去除假阳性基因,合并去重后即得疾病相关靶点信息。最后,将活性成分相关靶点与疾病靶点进行对比分析,得交互靶标,即桂枝甘草汤抗失眠的潜在作用靶点。
1.2.4 靶点相互作用网络构建 通过String数据库获得交互靶标的靶点相互作用关系,并保存為TSV格式[14]。然后,将该文件中的node1、node2和combined score信息导入到Cytoscape软件中,构建靶点相互作用网络。
1.2.5 网络构建 利用Cytoscape 3.4.0软件对“1.2.4”数据进行可视化处理,即构建桂枝甘草汤抗失眠的“单味药-活性成分-作用靶点”网络模型,再利用度值、介数值等参数对上述模型进行分析。节点的度值和介数值越大,在网络中的重要性就越强[15]。
1.2.6 GO生物功能富集分析 将上述潜在作用靶点输入到DAVID 6.8数据库中,获得GO生物功能富集分析,然后限定P<0.05,使用OriginPro软件将结果绘制条形图展示。
1.2.7 KEGG代谢通路富集分析 利用DAVID 6.8数据库对潜在作用靶点进行KEGG代谢通路富集分析。将基因物种和背景限定为人,并设定P<0.05,得富集结果,再通过Omicshare平台进行可视化处理。
2 结果
2.1 桂枝甘草汤潜在活性成分筛选
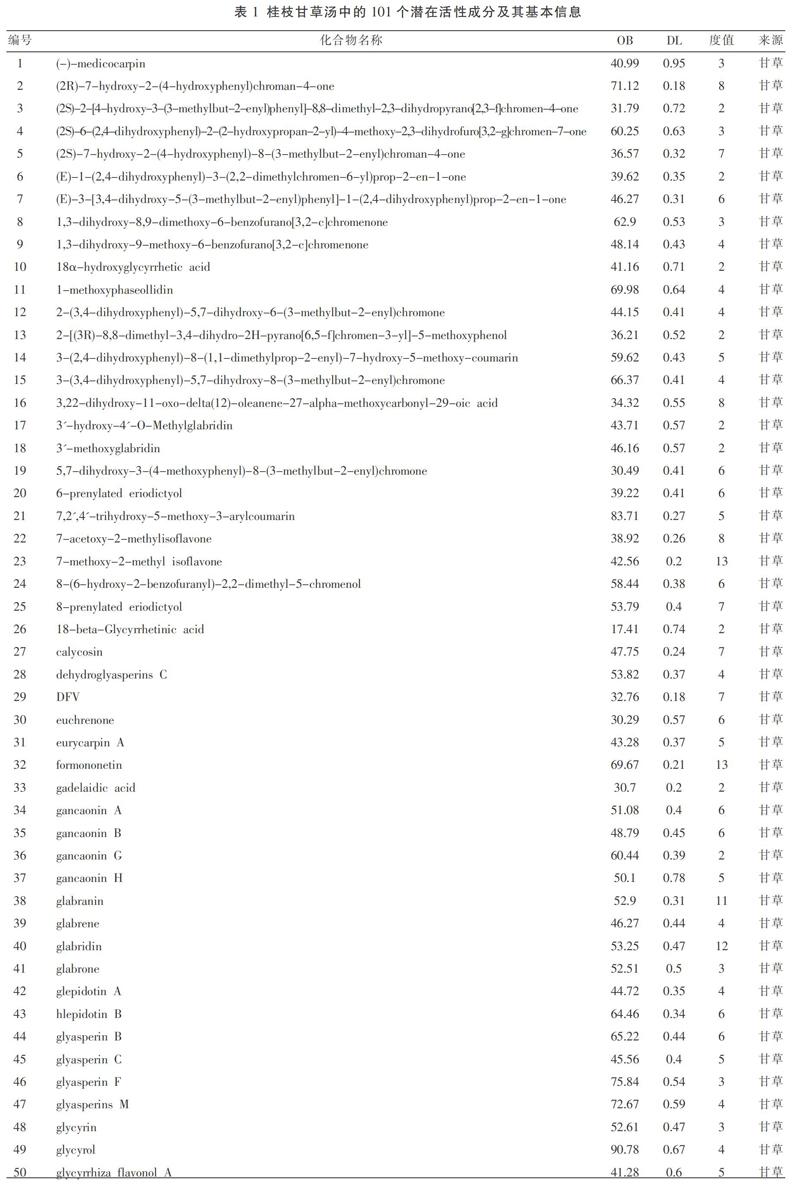
通过TCMSP数据库收集桂枝甘草汤中2味药材的化合物,再根据OB和DL值共筛选得到99个成分,但因甘草中glycyroside与疾病靶点无关联性而被剔除。因此,共得到98个潜在活性成分,其中甘草中包含91个,桂枝中包含7个。另外,通过文献挖掘和整理发现,在桂枝和甘草中仍可能含有一些其它的活性成分,因其不满足OB、DL值而被删除。比如,桂枝中桂皮醛具有降压、降糖、抗炎、抗抑郁、神经保护等药理作用[16];甘草中甘草甜素可能通过调控cyclin D1和P21蛋白表达以及PI3K/AKT信号通路激活来抑制前列腺癌细胞株PC3的生长[17];而18β-甘草次酸可通过抑制炎症反应及氧化应激,从而减轻脑组织细胞凋亡及脑损伤[18]。故将上述3个活性成分纳入,最终获得101个潜在活性成分,其基本信息见表1。
2.2 桂枝甘草汤抗失眠的靶点预测
通过Swiss、SuperPred、Stitch数据库对101个潜在活性成分进行靶点预测,得甘草潜在作用靶点452个、桂枝201个;将靶点进行合并去重得活性成分相关靶点491个。然后,利用OMIM、TTD、GAD、PharmGkb数据库以“insomnia”为关键词进行检索,筛选得疾病相关靶点668个。最后,将潜在活性成分靶点与疾病靶点进行对比匹配,最终获得与桂枝甘草汤抗失眠症相关的潜在作用靶点85个。
2.3 靶点相互作用网络分析
利用String数据库获得85个潜在作用靶点的相互作用关系。该网络中包含84个节点和567条边,平均局部聚类系数为0.557,平均节点度值为13.3。(SLC28A2因与其它靶点没有相联性而未体现在该网络中)从图1可以直观的看出,度值较大的靶点是ALB、BDNF、SLC6A4、HTR3A、ACHE,分别为48、40、27、27、27,说明这些靶点在整个网络中发挥重要作用。提示这些靶点可能是桂枝甘草汤治疗失眠症的关键靶点。
2.4 桂枝甘草汤单味药-活性成分-作用靶点相互作用网络分析
利用Cytoscape软件构建桂枝甘草汤中2味药材、101个潜在活性成分、85个潜在作用靶点的“单味药-活性成分-作用靶点”相互作用网络(图2)。在该网络中,共包含188个节点和616条边。表1中列出了101个潜在活性成分的度值。据表1可知,化合物cinnamaldehyde(桂皮醛)度值最大,与40个靶点相连,介数值为0.105 8;其次是glycyrrhizin(甘草甜素),与38个靶点相连,介数值为0.122 6;然后是quercetin(槲皮素),与37个靶点相连,介数值为0.160 3。这些拥有较高度值和介数值的潜在活性成分可能在桂枝甘草汤抗失眠的功效中发挥着重要的作用。此外,靶点MAPT、ESR1、CYP19A1也拥有较高的度值(79、42、39)和介数值(0.239 3、0.064 8、0.034 3)。由此推断,这些靶点可能与桂枝甘草汤抗失眠的药理作用密切相关。对网络进行系统分析可知,整个网络的平均度值为6.54,其中每个化合物平均与6.09个靶点相互作用,每个靶点平均与6.05个化合物相互作用,说明在桂枝甘草汤中存在着不同活性成分作用于不同靶点或作用于同一靶点的现象,充分体现出桂枝甘草汤以“多成分、多靶点”协同治疗失眠症的作用机制。
2.5 GO生物功能富集分析
采用DAVID 6.8数据库对85个潜在作用靶点进行GO基因本体富集分析,确定了293个GO条目。其中,相关条目最多的是生物学过程(BP)211个,主要涉及氧化还原过程、信号转导、G蛋白偶联受体信号通路等;其次是分子功能(MF)相关条目53个,主要涉及蛋白结合、酶结合、氧化还原酶活性等;最后是細胞组成(CC)相关条目29个,主要涉及质膜、膜的组成、内质网等;然后限定P<0.05,利用OriginPro8.0绘制条形图展示前20条富集结果(图3)。显然,与桂枝甘草汤抗失眠相关的关键靶标主要与氧化还原过程、蛋白结合、质膜等生物功能有关。
2.6 KEGG代谢通路富集分析
利用DAVID 6.8数据库对85个潜在作用靶点进行KEGG代谢通路富集分析,限定P<0.05,共获得18条KEGG代谢通路及其相关信息,再通过Omicshare平台对富集分析结果进行可视化处理,得气泡图(图4)。从图中可以看出,涉及基因数较多的代谢通路主要包括:神经活性配体-受体相互作用通路(neuroactive ligand-receptor interaction)、钙信号通路(calcium signaling pathway)、5-羟色胺能突触通路(serotonergic synapse)、cAMP信号通路(cAMP signaling pathway)等。以上数据表明,桂枝甘草汤的潜在活性成分可能主要通过作用于上述代谢通路发挥治疗失眠症的疗效。
3 讨论
本研究采用网络药理学研究策略,构建了桂枝甘草汤“单味药-活性成分-作用靶点”交互网络模型,最终共筛选出101个潜在活性成分,85个作用靶点,18条与失眠症相关的KEGG代谢通路,基本阐明了桂枝甘草汤治疗失眠症的“多成分-多靶点-多通路”的可能作用机制。
从桂枝甘草汤“单味药-活性成分-作用靶点”相互作用网络中分析可知,桂皮醛是与失眠症相关靶点作用最多的化学成分。郑芳昊等[19]采用行为药理学实验方法,通过高架十字迷宫和旷场实验证明了桂皮醛可使大鼠睡眠潜伏期缩短,睡眠持续时间增加。肖刚等[20]通过研究甘草甜素对大鼠蛛网膜下腔出血后血脑屏障损伤的影响发现,甘草甜素可降低脑组织中的IL-6细胞因子。而IL-6是一种与睡眠/剥夺关系密切的细胞因子,IL-6能够抑制IL-1的合成,降低IL-6细胞因子,则IL-1合成增多,进而增强患者非快眼动睡眠的时间[21]。可见,以上化学成分极有可能是桂枝甘草汤抗失眠的药效物质。
靶点分析结果表明,靶点MAPT其度值最大,可能是重要的关键靶点。相关研究[22-23]表明,MAPT基因主要负责编码神经元微管相关蛋白tau,当MAPT基因突变时则会加剧tau蛋白的聚集,引起神经元细胞功能障碍和神经元数目减少,导致γ-氨基丁酸(GABA)、多巴胺(DA)等神经递质释放异常,进而引发睡眠障碍。因此,靶点MAPT可能是桂枝甘草汤治疗失眠症的关键作用靶点。靶点ESR1也在“单味药-活性成分-作用靶点”相互作用网络中显示出突出的地位。Helen等[24]认为雌激素可以通过作用于表达ER的GABA能中间神经元,促进邻近神经元脑源性神经营养因子(brain derived neur?鄄otrophic factor,BDNF)的表达,或者通过与位于BDNF基因上的雌激素反应元件相互作用,诱导BDNF的表达。同时,已有多项临床研究表明BDNF的神经营养功能参与了睡眠的自我平衡调节过程[25]。
KEGG代谢通路结果显示,涉及靶点最多的代谢通路是神经活性配体-受体相互作用通路,该通路包含质膜上所有与细胞内外信号通路相关的受体和配体[26]。A类生物胺类是一种对多种行为有潜在效应的神经递质,其中包括与失眠症密切相关的DA、NE、5-HT等神经递质,当脑内5-HT升高,NE、DA降低时,将有助于失眠症的治疗。其次,在桂枝甘草汤发挥抗失眠的药理过程中钙信号通路可能也发挥着重要的作用。众所周知,神经递质的释放离不开钙离子通道,而N型和P/Q型钙离子通道则主要存在于神经元内,影响中枢神经系统DA、NE、Glu、GABA等神经递质的释放和传递,临床上治疗失眠症的西药多是GABA复合受体拮抗剂,其作用机制就是通过促进中枢抑制性神经递质GABA的释放或突触的传递而发挥抗失眠的药理作用[27]。所以,桂枝甘草汤可能通过调节上述这些代谢通路而影响中枢神经系统中神经递质的释放及突触传递,最终达到良好的治疗效果。
综上所述,本研究通过网络药理学方法剖析了桂枝甘草汤治疗失眠症的潜在药效物质和可能的作用机制,构建了“单味药-活性成分-作用靶点”和靶点相互作用网络,并进行了生物功能和代谢通路富集分析。结果表明,桂枝甘草汤中的101个潜在活性成分可能主要是通过作用于MAPT、ESR1、CYP19A1等85个与失眠症相关的潜在作用靶点,富集于蛋白结合、质膜、神经活性配体-受体相互作用通路、钙信号通路等多种生物功能和代谢通路中,以缓解神经元损伤、调控神经递质释放、调节突触传递等多种途径来增加不同时期的睡眠时间,发挥良好的抗失眠药理作用。该研究体现出桂枝甘草汤“多成分、多靶点、多途径”协同治疗失眠症的复杂机制,为后续更精准的研究其药效物质基础和作用机制提供了理论基础。
参考文献
[1] 贾 玉,贾跃进,郑晓琳.中医对失眠认识的探讨及展望[J].中华中医药杂志2015, 30(1):163-166.
[2] 李 娜,樊 旭.基于肝“体阴用阳”理论论治失眠[J].辽宁中医药大学学报,2019,21(5):136-138.
[3] 赵克娜,张锦文,吴增强,等.失眠症状与青少年学校表现的相关性研究[J].中国儿童保健杂志,2018,26(2):141-144,157.
[4] EMILY F L P, SEE W T M, RACHEL V A P, et al. Hybrid Cognitive-Behavioral Therapy Intervention for Adolescents With Co-Occurring Migraine and Insomnia: A Single-Arm Pilot Trial[J]. Headache: The Journal of Head and Face Pain, 2018,58(7):1060-1073.
[5] 杜玉梅.失眠(中醫不寐)症的中医辨证治疗探讨[J].心理医生,2017,23(17):133-134.
[6] 张石革,孙定人.镇静助眠药[J].中国药房,2001(2):61-62.
[7] 刘仲玮.黄连复方治疗原发性失眠研究进展[J].中国处方药,2019,17(4):32-34.
[8] 盛亚男.交泰丸镇静催眠的有效成分研究[D].广州:广州中医药大学,2010:1-48.
[9] 钟相根.大国医系列之张仲景传世名方:伤寒论卷[M].北京:中国医药科技出版社,2013:75.
[10] HOPKINS A L. Network pharmacology: The next paradigmindrug discovery[J]. Nature Chemical Biology, 2008,4(11):682-690.
[11] 韩 森,吕爱平,李 健,等.网络药理学在中药药性理论研究中的应用概述[J].中国中医基础医学杂志,2019,25(1):127-130.
[12] 吴 丹,高 耀,向 欢,等.基于网络药理学的栀子豉汤抗抑郁作用机制研究[J].中草药,2018,49(7):1594-1602.
[13] ZHANG Y Q, MAO X, GUO Q Y, et al. Network Pharmacology-based Approaches Capture Essence of Chinese Herbal Medicines[J]. Chinese Herbal Medicines, 2016,8(2):107-116.
[14] SZKLARCZYK D, FRANCESCHINI A, WYDER S, et al. STRING v10: Protein-protein interaction networks, integrated over the tree of life[J]. Nucleic Acids Research, 2014,43(D1):D447-D452.
[15] 王 强,刘敏莹,韩隆胤,等.基于网络药理学探讨断藤益母汤治疗类风湿关节炎的作用机制[J].中国实验方剂学杂志,2019,25(24):150-158.
[16] 张利青,张占刚,付 岩,等.桂皮醛药理作用的研究进展[J].中国中药杂志,2015,40(23):4568-4572.
[17] 王雪峰,赵 琪.甘草甜素抑制人前列腺癌PC3细胞生长及其机制[J].临床与病理杂志,2018,38(11):2308-2313.
[18] 王志国,吴椋冰,关 雷,等.18β-甘草次酸对局灶性脑缺血再灌注损伤的保护作用[J].中国新药杂志,2017,26(11):1315-1321.
[19] 郑芳昊,罗佳波.桂枝对大鼠中枢神经系统作用的研究[J].中药药理与临床,2014,30(4):76-79.
[20] 肖 刚,罗 超,彭 形,等.甘草甜素通过抑制炎症反应和氧化应激改善大鼠蛛网膜下腔出血后血脑屏障损伤[J].中国免疫学杂志,2019,35(7):811-818.
[21] 王春燕,赵忠新.细胞因子与睡眠/剥夺的研究进展[J].脑与神经疾病杂志,2004(2):154-156,122.
[22] 李明月,王 群.额颞叶痴呆MAPT基因的研究进展[J].中华临床医师杂志(电子版),2015,9(9):1679-1684.
[23] ROBERSON E D. Mouse models of frontotemporal dementia[J].Annals of Neurology,2012,72(6):837-849.
[24] SCHARFMAN H E, MACLUSKY N J.Estrogen and brain-derived neurotrophic factor (BDNF) in hippocampus: Complexity of steroid hormone-growth factor interactions in the adult CNS[J]. Frontiers in Neuroendocrinology,2006,27(4):415-435.
[25] 劉欣欣,王亚博,王晓雪,等.认知行为疗法联合药物治疗对原发性失眠患者疗效及血液相关指标的影响[J].中国实用神经疾病杂志,2019,22(4):358-364.
[26] 潘玲珍,闫智勇,左长英,等.长期使用地西泮对神经活性配体受体相互作用信号通路的影响[J].中国药科大学学报,2011,42(5):443-446.
[27] 吴 杲,瞿发林,吴汉斌.失眠症的药物治疗进展[J].现代中西医结合杂志,2004(6):835-837.
〔收稿日期〕2019-08-28
〔作者简介〕黄 强,男,副研究员,研究方向:医药领域的专利申请审查。
〔通讯作者〕*刘 明,男,助理研究员,E-mail:liuming_2@cnipa.gov.cn。
