改性活性炭对Cr(Ⅵ)的吸附性能研究
2020-05-13刘瑞森杨怡心井海融
刘瑞森, 杨怡心, 井海融, 骆 欣
(1. 华北科技学院 安全工程学院,北京 东燕郊 065201; 2. 华北科技学院 环境工程学院,北京 东燕郊 065201)
0 引 言
铬在水中的存在形式主要有Cr (Ⅲ)和Cr (Ⅵ),而Cr(Ⅵ)作为毒性最强的重金属离子之一[1],其毒性远大于Cr (Ⅲ),且Cr(Ⅵ)更易迁移,容易被人体吸收并在体内蓄积,对人体及水生生物具有致癌、致畸、致突变效应[2]。采矿、印染、电镀等行业产生大量含铬废水。含铬废水的处理方法主要有化学沉淀法、膜分离法、吸附法和离子交换法等[3],相对于其他方法,吸附法在操作、处理费用、吸附剂种类和处理效果上有一定优势,被广泛使用。
活性炭具有较高的比表面积,常用作吸附剂。通过对活性炭进行表面改性,可提高其吸附速度和吸附量。本研究利用Al2(SO4)3对活性炭进行表面改性处理,探究不同因素对改性活性炭对Cr (Ⅵ)的吸附的影响。通过吸附动力学方程、吸附等温方程等,研究改性活性炭的吸附机理和吸附性能。
1 实验部分
1.1 材料、试剂和仪器
实验所用活性炭为粉末活性炭,模拟废水由K2Cr2O7(优级纯)溶于去离子水制成。
UV752N紫外可见分光光度计:上海奥析科学仪器有限公司;THZ-82A水域恒温振荡器:常州荣华仪器制造有限公司;MFL-3664智能一体化马弗炉:长春乐镤科技有限公司;雷磁PHS-3C pH计:上海仪电科学仪器股份有限公司;DHG-9070A型电热鼓风干燥箱:上海一恒科学仪器有限公司。
1.2 实验方法
1.2.1 改性活性炭的制备
将活性炭用去离子水反复清洗后,在105℃条件下干燥至恒重,记为PAC。将5 g经预处理的活性炭置于100 mL浓度为0.1 mol/L的Al2(SO4)3溶液中,室温条件下震荡4小时(转速150 r/min),静置24 h,抽滤,水洗,置于马弗炉中,在360℃条件下烘培、活化2.5 h。铝盐改性活性炭制备完成,记为Al-PAC。
1.2.2 初始pH值的影响
Al-PAC和PAC的投加量均为2 g/L,溶液的初始Cr (Ⅵ)质量浓度为10 mg/L,溶液的初始pH值范围为3~7。在30℃、150 r/min的振荡速度下振荡4 h,测定滤液的Cr (Ⅵ)质量浓度。
1.2.3 吸附时间的影响
Al-PAC投加量为2 g/L,pH值为3,溶液的初始Cr (Ⅵ)质量浓度为10 mg/L、20 mg/L、30 mg/L,在30℃、150 r/min的振荡速度振荡,时间在5~180 min之间变化,考察吸附效果与吸附时间的关系。
1.2.4 初始Cr (Ⅵ)浓度的影响
温度为20℃、30℃和40℃,Al-PAC投加量为2 g/L,pH值为3,溶液的初始Cr (Ⅵ)质量浓度在10~150 mg/L之间变化,在恒温条件下以150 r/min的振荡速度振荡4 h,分析初始Cr (Ⅵ)浓度对吸附量和吸附率的影响。
1.2.5 干扰离子的影响
溶液的初始Cr (Ⅵ)质量浓度为10 mg/L,pH值为3,向溶液中分别加入同等质量浓度的NaCl、Na2SO4、Na3PO4,并设置空白对照组,Al-PAC的投加量均为2 g/L,在30℃、150 r/min条件下振荡4 h,测定滤液的Cr (Ⅵ)质量浓度。
1.3 分析方法
Cr (Ⅵ)的浓度由二苯碳酰二肼分光光度法测定[4],本实验通过吸附量和吸附率两个指标来分析Al-PAC和PAC对废水中Cr (Ⅵ)的吸附效果,吸附率和吸附量的计算式如下:
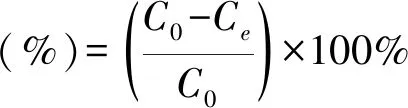
(1)
(2)
式中,φ为Cr(Ⅵ)的吸附率,%;C0为溶液初始Cr(Ⅵ) 浓度,mg/L;Ce为吸附后溶液的Cr(Ⅵ)浓度,mg/L;q为吸附剂的吸附量,mg/g;V为溶液的体积,L;m为投加的吸附剂质量,g。
In thispaper,thefollowing initialassumptionsare considered.
2 实验结果分析
2.1 溶液初始pH值对吸附的影响
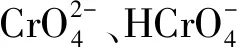
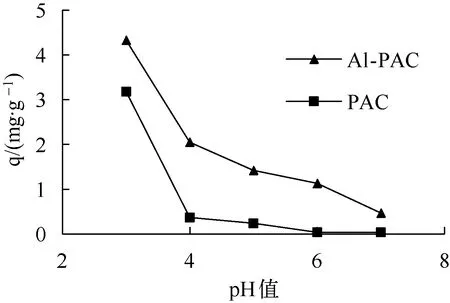
图1 pH对Cr(Ⅵ)吸附的影响
2.2 吸附时间对吸附的影响
从图2可以看出,对于不同初始溶液Cr(Ⅵ)浓度,Al-PAC的吸附量随吸附时间的延长均呈现增加的趋势。吸附初期,吸附过程较快,在30 min后吸附量增长缓慢,在90 min时吸附接近平衡。吸附速率减慢是因为溶质由吸附剂颗粒表面向颗粒内部扩散,内扩散过程也是吸附速率的主要限制因素[6]。
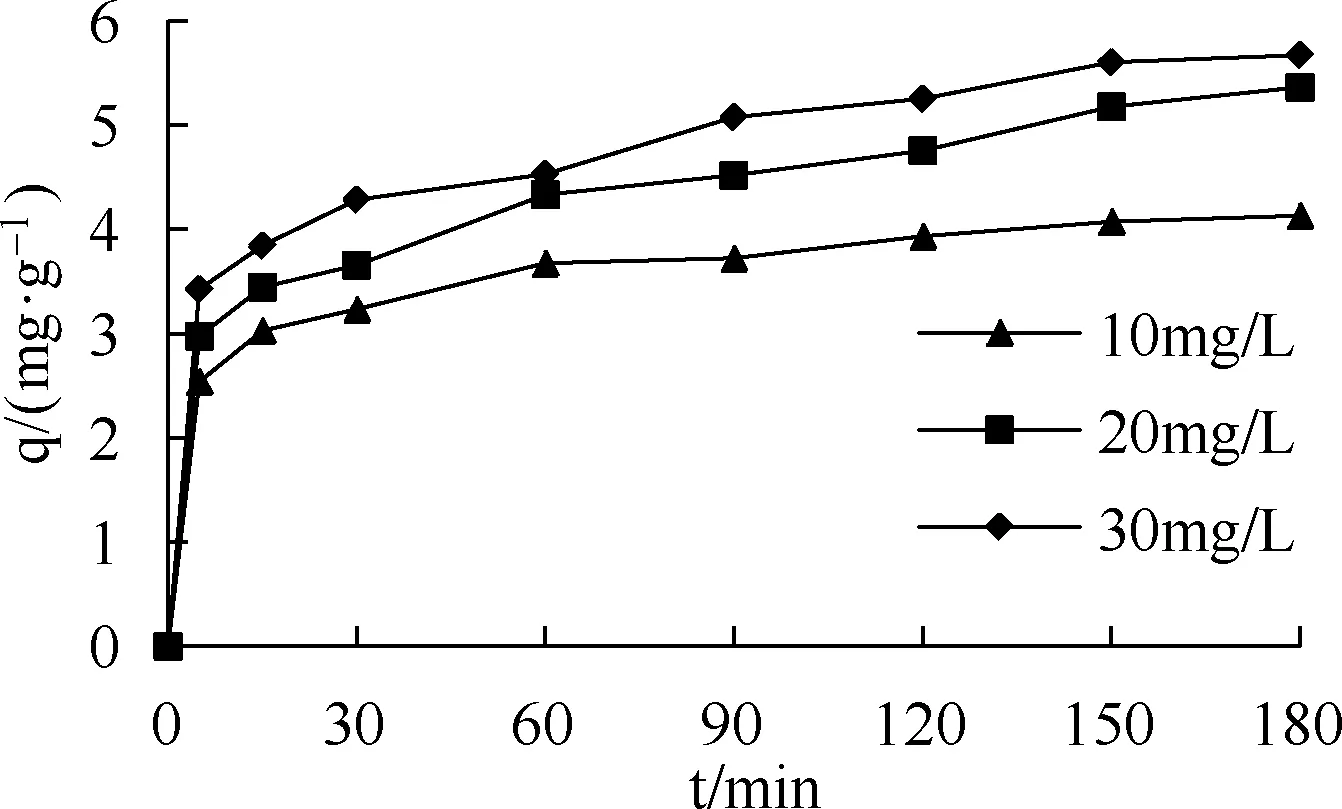
图2 时间对Cr(Ⅵ)吸附的影响
2.3 初始Cr(Ⅵ)浓度对吸附的影响
从图3可以看出,当初始Cr (Ⅵ)浓度由10 mg/L逐渐升高至150 mg/L时,Al-PAC的吸附率由89.75%降至12.54%,吸附量由4.49 mg/g升至9.41 mg/g。由于吸附剂用量一定时其表面吸附位点有限,随着溶液初始Cr(Ⅵ)浓度的上升,过多的Cr(Ⅵ)不能够被吸附,导致吸附率下降;而吸附量逐渐上升的原因是随着溶液初始Cr(Ⅵ)的浓度增大,吸附动力梯度不断增大[7],Cr(Ⅵ)可以和吸附点位有更多的接触。
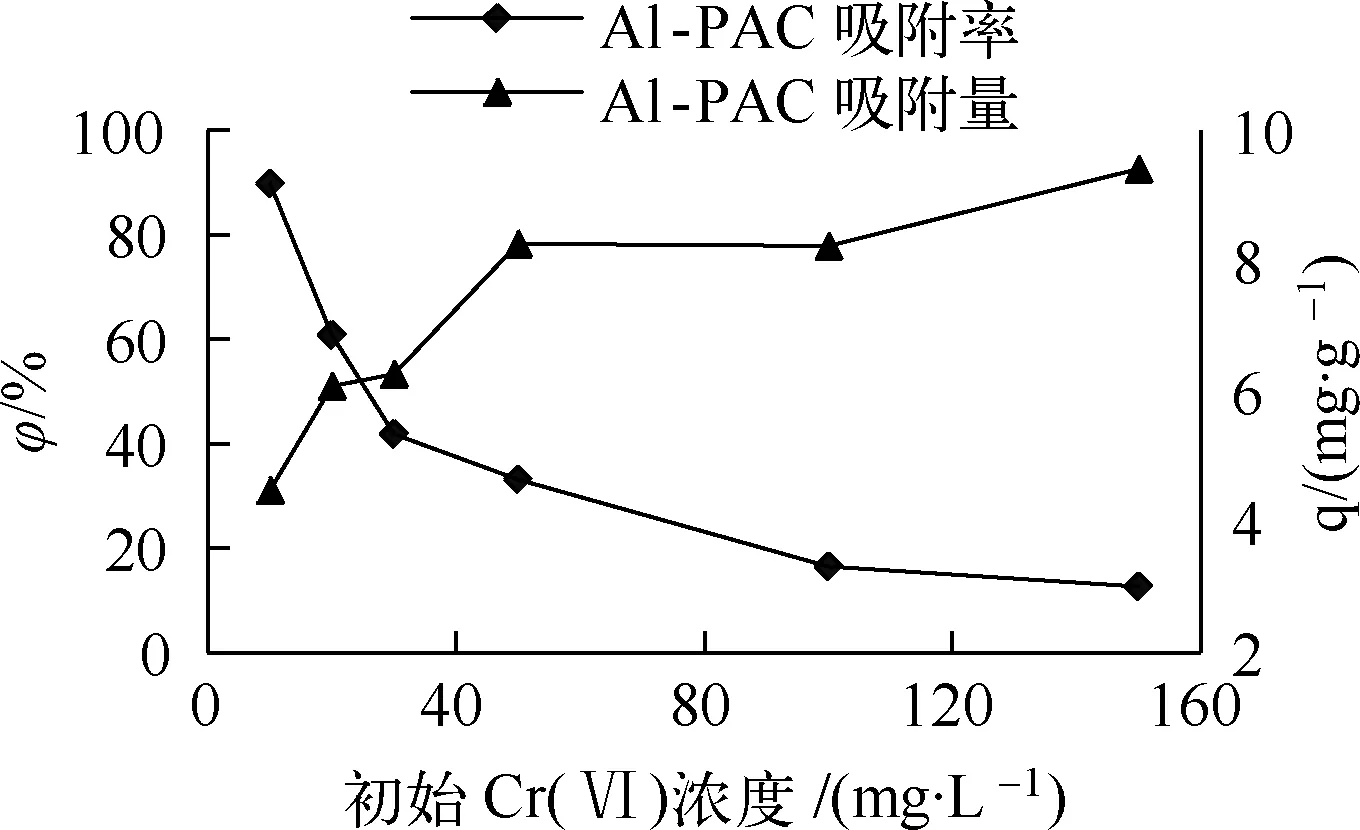
图3 溶液初始Cr(Ⅵ)浓度对吸附的影响
2.4 干扰因子对吸附的影响
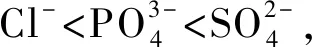
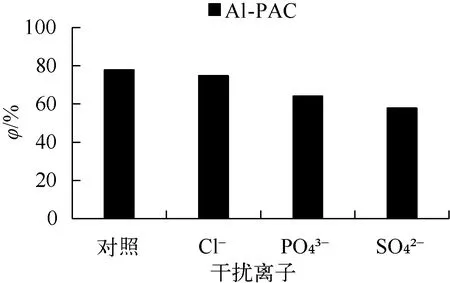
图4 干扰离子对Cr(Ⅵ)吸附的影响
2.5 吸附机理分析
2.5.1 吸附动力学分析
采用准一级、准二级动力学方程拟合Al-PAC对Cr(Ⅵ)的吸附数据,并用相关系数R2表征模型的拟合效果,拟合结果见图5、图6,拟合参数见表1。由表1可知,准二级动力学方程拟合的相关系数更接近1,且准二级动力学方程的平衡吸附量与实验吸附量相差不大,因此准二级动力学方程更加符合Al-PAC对Cr(Ⅵ)的吸附过程。这表明液膜扩散不是控制吸附的唯一模式[8],Al-PAC对Cr(Ⅵ)的吸附主要是化学吸附,而不是物理吸附[9,10]。Cr(Ⅵ)的吸附量取决于活性炭表面的活性点位,而不是溶液中吸附剂和吸附质的含量[11]。由图7和表1可见,qt与t0.5呈线性相关,且相关性较好,表明颗粒内扩散过程是限速步骤。图7中直线均不过原点,说明吸附速率由多个过程控制。
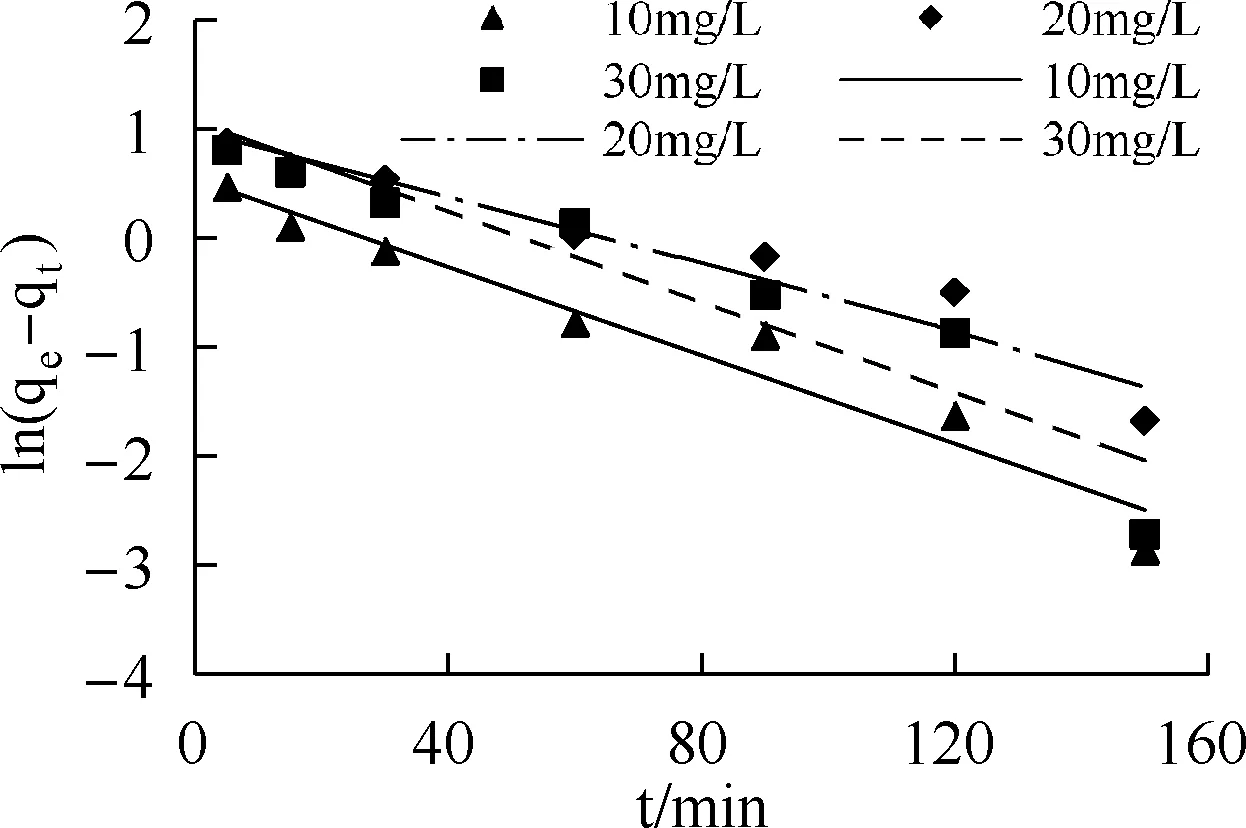
图5 Al-PAC吸附Cr(Ⅵ)的准一级动力学拟合
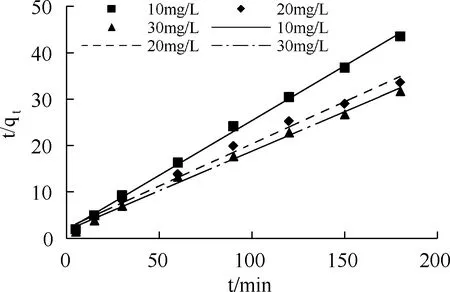
图6 Al-PAC吸附Cr(Ⅵ)的准二级动力学拟合
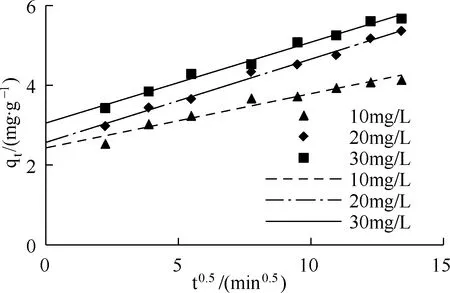
图7 Al-PAC吸附Cr(Ⅵ)的颗粒内扩散拟合
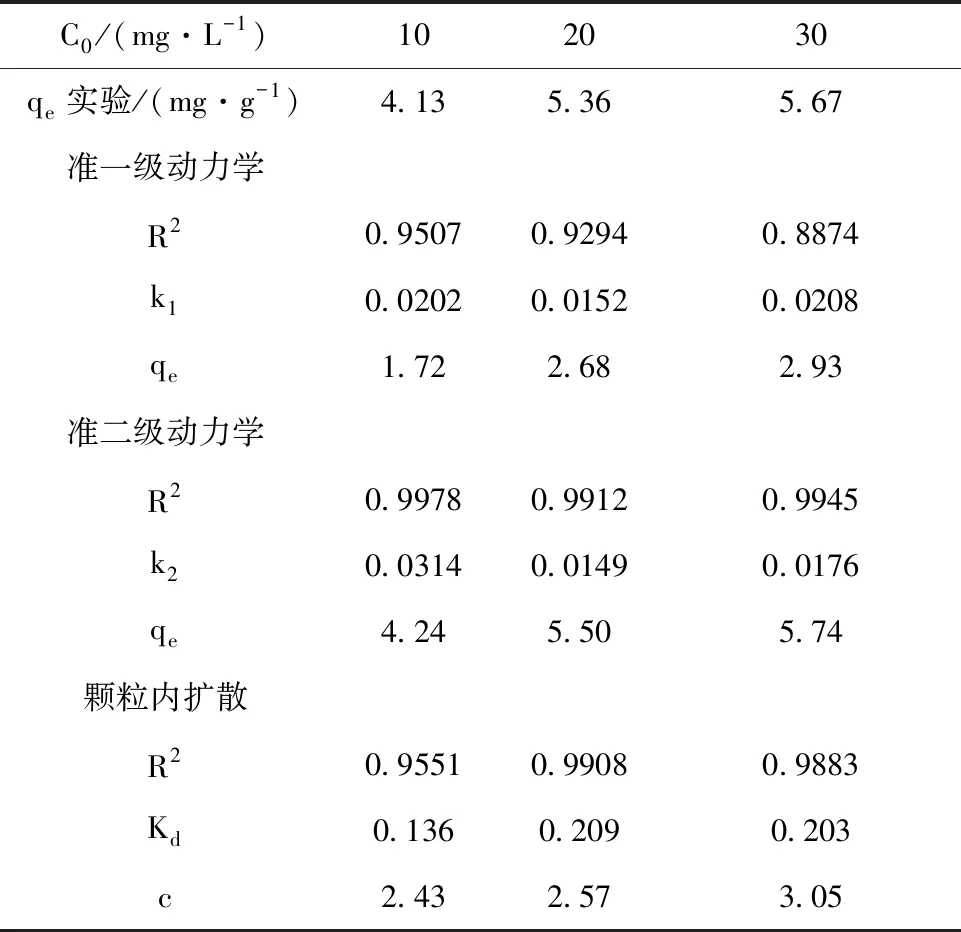
C0/(mg·L-1)102030qe实验/(mg·g-1)4.135.365.67准一级动力学R20.95070.92940.8874k10.02020.01520.0208qe1.722.682.93准二级动力学R20.99780.99120.9945k20.03140.01490.0176qe4.245.505.74颗粒内扩散R20.95510.99080.9883Kd0.1360.2090.203c2.432.573.05
2.5.2 吸附等温线分析
采用Langmuir和Freundlich吸附等温方程,对吸附等温线进行拟合,拟合结果见图8、图9,拟合参数见表2。由表2可知Langmuir方程相关系数更接近1,可以更好地拟合Al-PAC对Cr(Ⅵ)的吸附过程,吸附为单层吸附[12]。由表2可知,随温度上升,平衡吸附量增大,表明Al-PAC对Cr(Ⅵ)的吸附是吸热反应。在Freundlich等温线拟合中,n值为6.23~6.66,吸附易于进行[13-15]。
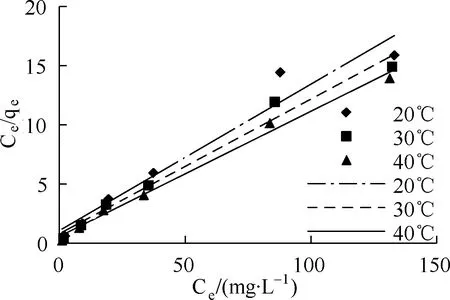
图8 Al-PAC吸附Cr(Ⅵ)的Langmuir等温方程拟合
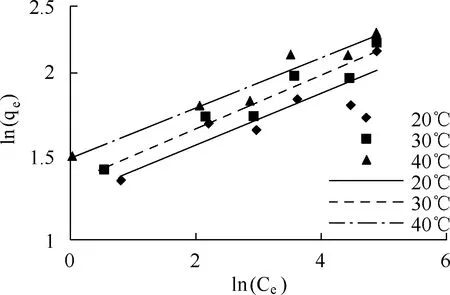
图9 Al-PAC吸附Cr(Ⅵ)的Freundlich等温方程拟合
2.5.3 吸附热力学分析
通过标准熵变ΔS、标准焓变ΔH和吉布斯自由能ΔG来分析吸附热力学的性质,计算式如下:
(3)
ΔG=-RTln(KD)
(4)
(5)
式中,KD为固液分配系数,mL/g;qe为平衡时吸附量,mg/g;Ce为吸附平衡溶液的Cr(Ⅵ)浓度,mg/L;R为气体摩尔常数,kJ/(mol·K);T为绝对温度,K。
取初始Cr(Ⅵ)浓度为50 mg/L,根据公式(5),以lnKD对1/T作图,见图10,热力学参数见表3。由表3可知,ΔG<0,表明Al-PAC对Cr(Ⅵ)的吸附过程是自发的。ΔH>0说明吸附过程是吸热的,升高温度利于吸附进行。ΔS>0,表明Al-PAC吸附Cr(Ⅵ)的过程是熵增的,固液界面的自由度因吸附行为增大。
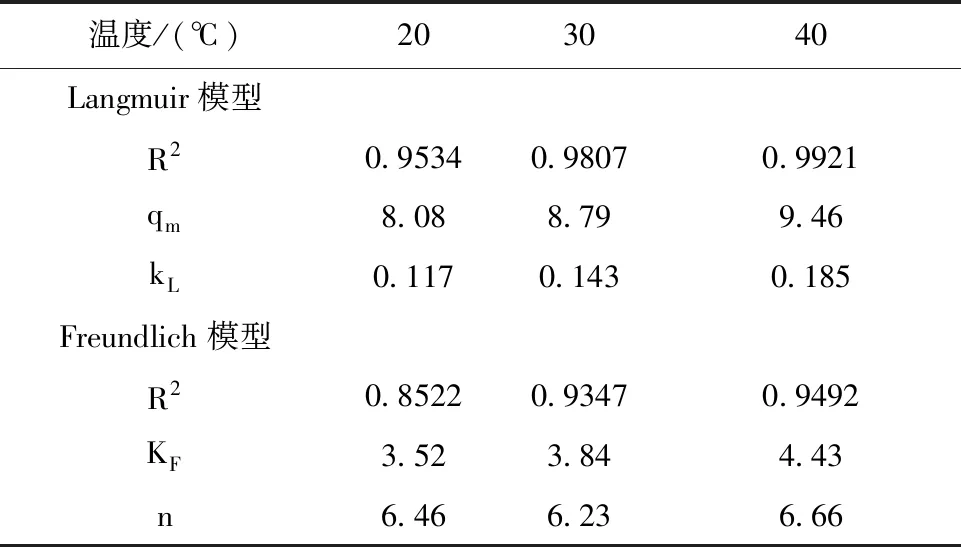
表2 Al-PAC对Cr(Ⅵ)的吸附等温线参数
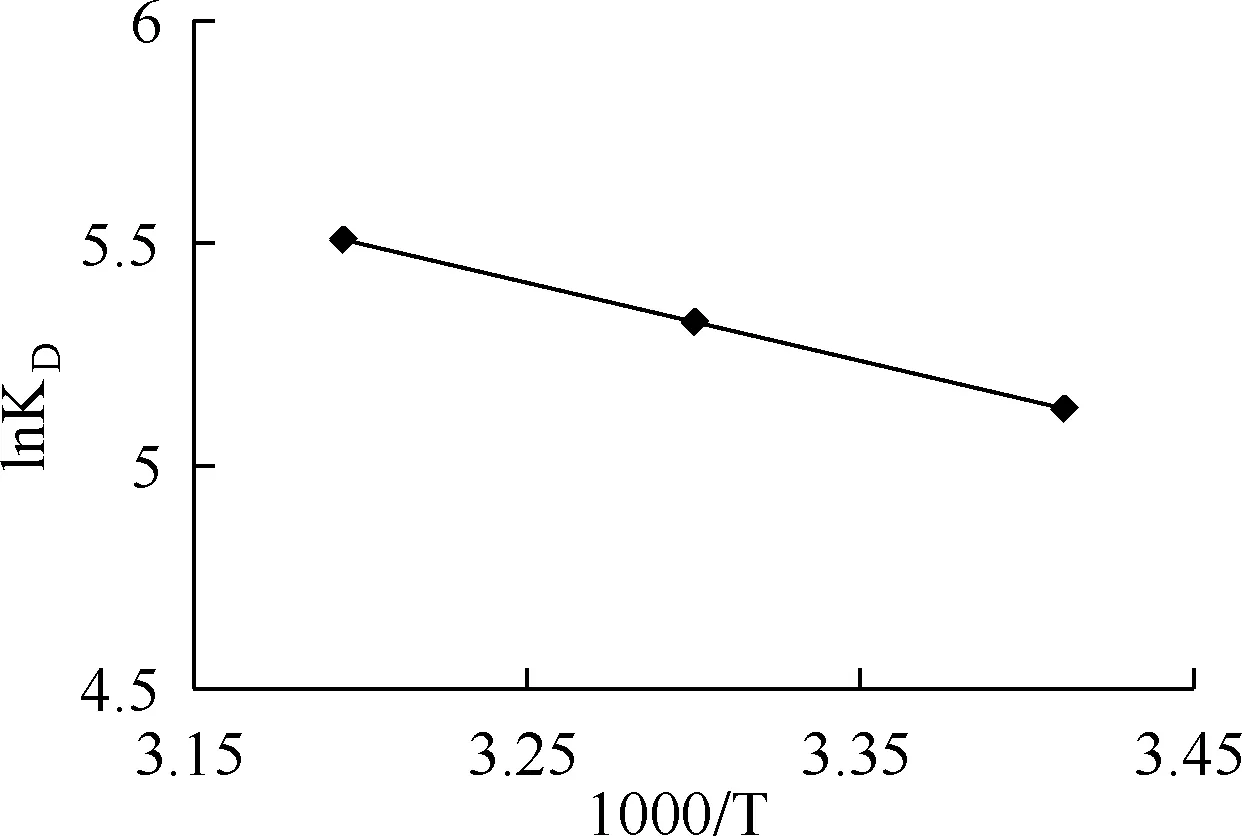
图10 lnKD与1/T的关系曲线

表3 不同初始Cr(Ⅵ)浓度下的热力学参数
3 结论
(1) 通过0.1 mol/L的Al2(SO4)3溶液浸渍法改性得到的Al-PAC,吸附溶液中Cr(Ⅵ),浓度由10 mg/L降至1.33 mg/L,与PAC相比吸附量由3.18 mg/g增加至4.33 mg/g,对Cr(Ⅵ)的吸附效果有一定提升。通过实验,时间、温度和废液初始Cr(Ⅵ)浓度与Al-PAC对Cr(Ⅵ)的吸附量呈正相关,改性活性炭对Cr(Ⅵ)的吸附主要受pH影响。
(2) 当pH为3~7时,与未改性活性炭相比,改性活性炭对Cr(Ⅵ)的吸附量均有所增加。
(3) Al-PAC对Cr(Ⅵ)的吸附等温线符合Langmuir方程,吸附动力学符合准二级动力学方程,吸附主要为单分子层化学吸附。吸附速率受颗粒内扩散控制,但不是唯一控制因素。
ΔG为负值,ΔH为正值,表明Al-PAC对Cr(Ⅵ)的吸附属于自发的吸热过程。
