不同剂量阿司匹林对大鼠钛合金种植体早期骨整合的影响
2020-05-08温丹丹吕亚林
温丹丹, 吕亚林
首都医科大学附属北京安贞医院口腔医疗中心,北京(100029)
近年来,心脑血管疾病的发病率逐年上升[1],阿司匹林,又称为乙酰水杨酸,作为典型的抗血小板药物被广泛用于预防和治疗心脑血管疾病[2]。在生活水平提高的同时,多数牙齿缺失的患者选择种植修复。相关研究表明口服抗血小板药物患者不停药进行种植手术是安全的[3]。种植成功的关键是形成良好的骨整合,既往相关研究多探索阿司匹林与骨密度间的关系。通过对916 名服用阿司匹林患者2008~2012 年骨密度变化的观察发现,长期服用低剂量的阿司匹林与患者的骨密度减低无关,且不会增加骨折风险[4];在研究阿司匹林、鲑鱼降钙素对去势大鼠影响的实验中发现,与对照组相比,给予阿司匹林的大鼠骨密度增加,骨硬度及抗折性增加[5]。然而阿司匹林对种植体周围骨形成的影响研究甚少。本实验对种植术后的大鼠持续给予不同剂量的阿司匹林,通过观察不同时期种植体周围的成骨情况,分析阿司匹林对于大鼠种植后早期骨形成的影响,为临床上服用阿司匹林患者的牙种植提供参考。
1 材料和方法
1.1 主要设备与材料
6 周龄雄性SD 大鼠[斯贝福(北京)生物技术有限公司],动物合格证号:SCXK(京)2016-0002;7%的水合氯醛(中国医药集团化学试剂有限公司);阿司匹林(索莱宝,中国);阿莫西林(索莱宝,中国);Ti-6Al-4V 种植钉[奥齿泰(北京)商贸有限公司];正置光学显微镜(Nikon Eclipse CI,日本尼康);成像系统(Nikon DS-U3,日本尼康);显微镜(Nikon E100,日本尼康);苏木素-伊红染液(武汉谷歌生物科技);Masson 染色试剂盒(武汉谷歌生物);Anti-BMP2-Rabbit pAb(赛维尔生物,中国);山羊抗兔二抗(赛维尔生物,中国);BSA(赛维尔生物,中国);苏木素染液(赛维尔生物,中国);苏木素分化液(赛维尔生物,中国);苏木素返蓝液(赛维尔生物,中国);免疫组织化学试组化试剂盒DAB 显色剂(赛维尔生物,中国);TRAP 染液套装(赛维尔生物,中国)。
1.2 动物及分组
48 只6 周龄清洁级雄性SD(Sprague-Dawley,SD)大鼠,饲养于北京安贞医院动物实验中心SPF级实验动物房,动物饲养许可证件编号:1118052100279,室温控制(22 ± 2)℃,相对湿度(55±10)%,人工照明模拟昼夜变化,自由饮水进食,适应性喂养两周。随机分为对照组与实验组A、B、C 4 组。实验获得首都医科大学附属北京安贞医院伦理委员会批准。
1.3 种植手术
取48 只SD 雄性大鼠,用7%的水合氯醛0.5 mL/100 g 腹腔注射行全身麻醉。大鼠膝关节处脱毛,消毒,无菌操作下于右侧下肢膝关节内侧作一长1 cm 纵行切口,切开皮肤及皮下组织,分离肌层,显露髌骨及股骨远端,用低速牙科手机(800 rpm/min,穿透骨皮质)和种植钉专用钻针预备种植窝,将直径1.4 mm,长度6 mm 的Ti-6Al-4V 种植钉,稍加压旋入预备好的种植窝内,分层拉拢缝合手术切口。
1.4 术后处理及给药
种植术后的大鼠均放置于干净通风的鼠笼内单笼饲养,维持笼内温度25 ℃左右,观察大鼠呼吸等一般情况,直至麻醉苏醒。术后给予3 d 阿莫西林67 mg/kg 每次(依据成人1 次0.75 g,3 次/d 给药剂量换算),3 次/d。于大鼠麻醉苏醒当日A、B、C组给予阿司匹林,根据药理实验人鼠剂量换算标准,按照临床上心脑血管疾病预防及治疗时成年人常用剂量即患者每天口服100、200、300 mg计算,体重为200 g 的大鼠A、B、C 组每天需给予阿司匹林的剂量分别为8.93 mg/kg、17.86 mg/kg、26.79 mg/kg,即每天需灌胃给药量为1.786、3.572、5.358 mg,将100、200、300 mg 阿司匹林粉末分别溶于56.0、28.0、18.7 mL 的0.9%氯化钠注射液中,混合液均为当日使用前现配制。对照组给予等剂量的0.9%氯化钠注射液灌胃。
大鼠于SPF 级实验动物房中饲养,自由进食饮水,每周称1 次体重,根据大鼠体重变化调整给药量,给药至2周、4周各组大鼠行安乐死。
1.5 骨组织标本采集
分别于2 周、4 周时,每组大鼠各随机抽取6 只腹腔注入480 mg/kg 水合氯醛行安乐死,收集大鼠右侧含种植体在内的1.5 cm 长的股骨骨块,在PBS 中剔除周围筋膜、肌肉及关节处韧带,所有骨组织标本均放于4%多聚甲醛溶液中进行内外双重固定,在4 ℃条件下固定7 d。
1.6 标本处理及检测
1.6.1 组织脱钙及石蜡包埋切片 将组织从固定液取出行脱钙处理,EDTA 液(0.5 mol/L,pH 7.4)脱钙4 周,每天更换新鲜脱钙液,直到骨组织能被细针轻松插入则脱钙完成。小心去除种植钉,冲洗,梯度酒精进行脱水,石蜡包埋,切片机沿种植体长轴作矢状连续切片,切片厚度4.0 μm,烤片,待水烤干蜡烤化后取出常温保存备用。
1.6.2 HE 染色 石蜡切片脱蜡至水,Harris 苏木素染,自来水洗,1%的盐酸酒精分化,自来水冲洗,0.6%氨水返蓝,流水冲洗,伊红染液染色,脱水封片。 Caseviewer2.0 扫描仪获取切片影像,200 × 视野下观察种植体周围新生骨组织情况并进行分析。
1.6.3 Masson 染色 石蜡切片脱蜡至水,Weigert氏铁苏木素染,自来水洗,1%的盐酸酒精分化,自来水冲洗,流水冲洗返蓝,丽春红酸性品红液染,蒸馏水快速漂洗,磷钼酸水溶液处理,苯胺蓝液复染,1%冰醋酸处理,脱水封片。200 × 视野下观察种植体周围新生骨组织中I 型胶成熟情况。
1.6.4 BMP-2 免疫组织化学染色 石蜡切片脱蜡至水,修复盒中在微波炉内行抗原修复,自然冷却后置于PBS(PH 7.4)中在脱色摇床上晃动洗涤3次,每次5 min;后于3%双氧水溶液中室温避光孵育25 min,脱色摇床上晃动洗涤;在组化圈内滴加3%BSA 均匀覆盖组织,室温封闭30 min。加兔抗鼠一抗,切片平放于湿盒内4 ℃孵育过夜,加山羊抗兔二抗,脱色摇床上晃动洗涤;切片稍甩干后在圈内滴加二抗(HRP标记)覆盖组织,室温孵育50 min,脱色摇床上晃动洗涤。切片稍甩干后在圈内滴加新鲜配制的DAB 显色液,显微镜下控制显色时间,自来水冲洗切片终止显色。苏木素复染,自来水洗,苏木素分化液分化,自来水冲洗,苏木素返蓝液返蓝,流水冲洗。脱水封片。Image Pro Plus 6.0 图像分析软件观察种植周围500 μm×500 μm 范围内新生骨组织中BMP-2 的平均光密度值(mean optical density,MOD)表达情况并进行统计学分析。
1.6.5 破骨细胞染色 石蜡切片脱蜡至水,配制TRAP 孵育液:TRAP 染液A 18 mL+B 液1 mL+C 液1 mL 混匀,再加TRAP 染液F 0.282 g,充分溶解过滤后备用。将切片用组化画笔画圈后放在湿盒中,用蒸馏水37 ℃孵育2 h 后,将切片重新放置在湿盒中,滴加过滤好的现配的TRAP 孵育液放于37 ℃烤箱孵育20 min。倾去染液,水洗后,苏木素染液复染核15 s,分化液分化,返蓝液返蓝。脱水封片。
每张切片植体周围500 μm × 500 μm 范围作为感兴趣区(region of interest,ROI),随机选取6 个不重叠ROI,测量破骨细胞单位面积计数,重复测量3 次后取平均值。
1.7 统计学方法
采用SPSS 22.0 统计软件分析数据,数据用x±s表示,Shapiro-Wilk 法检验数据是否符合正态分布,Levene′s 法验证数据方差齐性。对实验组和对照组间,方差齐的组别行Tukey-Kramer 检验,方差不齐的组别行Games-Howell 检验,P <0.05 为差异有统计学意义。
2 结 果
2.1 一般情况观察
种植术后当天,各组大鼠均表现为身体蜷缩、毛发光泽度降低、嗜睡、活动减少、进食和饮水略减少。术后7 d,毛发光泽度恢复,活动恢复正常,各组大鼠均表现为一级愈合创口,未发生感染现象,进食、饮水恢复正常。
2.2 HE 染色
植体周围500 μm 范围内,各组松质骨及髓腔区域种植体周围均有新生骨组织形成,但各组的种植体周骨板厚薄不一。对照组与A 组中种植体周骨板稍厚,连续性尚可,骨小梁少量,骨髓腔较小;B、C 两组种植体周骨板较对照组纤细,局部可见不连续,植体周的骨板外围髓腔相对增大,骨小梁相对减少且变细,且C 组更明显(图1、图2)。
2.3 Masson 染色
Masson 染色结果中,骨组织中成熟I 型胶原红染,而骨组织中未成熟的胶原为蓝染。种植体植入2 周和4 周时,在植体周围500 μm 范围内,对照组与A 组的种植体周围骨组织中红染部分未见明显差异,B、C 两组较对照组红染区域相对减少,且C 组减少更明显(图1、图2)。
2.4 BMP-2 在各组大鼠骨组织中的表达
2 周时,C 组MOD 数值最低,与对照组、A、B 组间比较差异具有统计学意义(P <0.05),对照组较B 组MOD 值略高,差异有统计学意义(P <0.05),其余组间差异无统计学意义(P >0.05);4 周时,C组MOD 数值最低,与对照组、A、B 组间比较差异具有统计学意义(P <0.05),其余组间差异无统计学意义(P >0.05)(图1~图3)。
2.5 破骨细胞染色
2 周和4 周时,对照组与A、B、C 组的单位面积TRAP 阳性染色细胞数依次降低,差异具有统计学意义(P <0.05),表明阿司匹林对于破骨细胞有抑制作用,且随着剂量增大抑制作用增强(图1、图2、图4)。
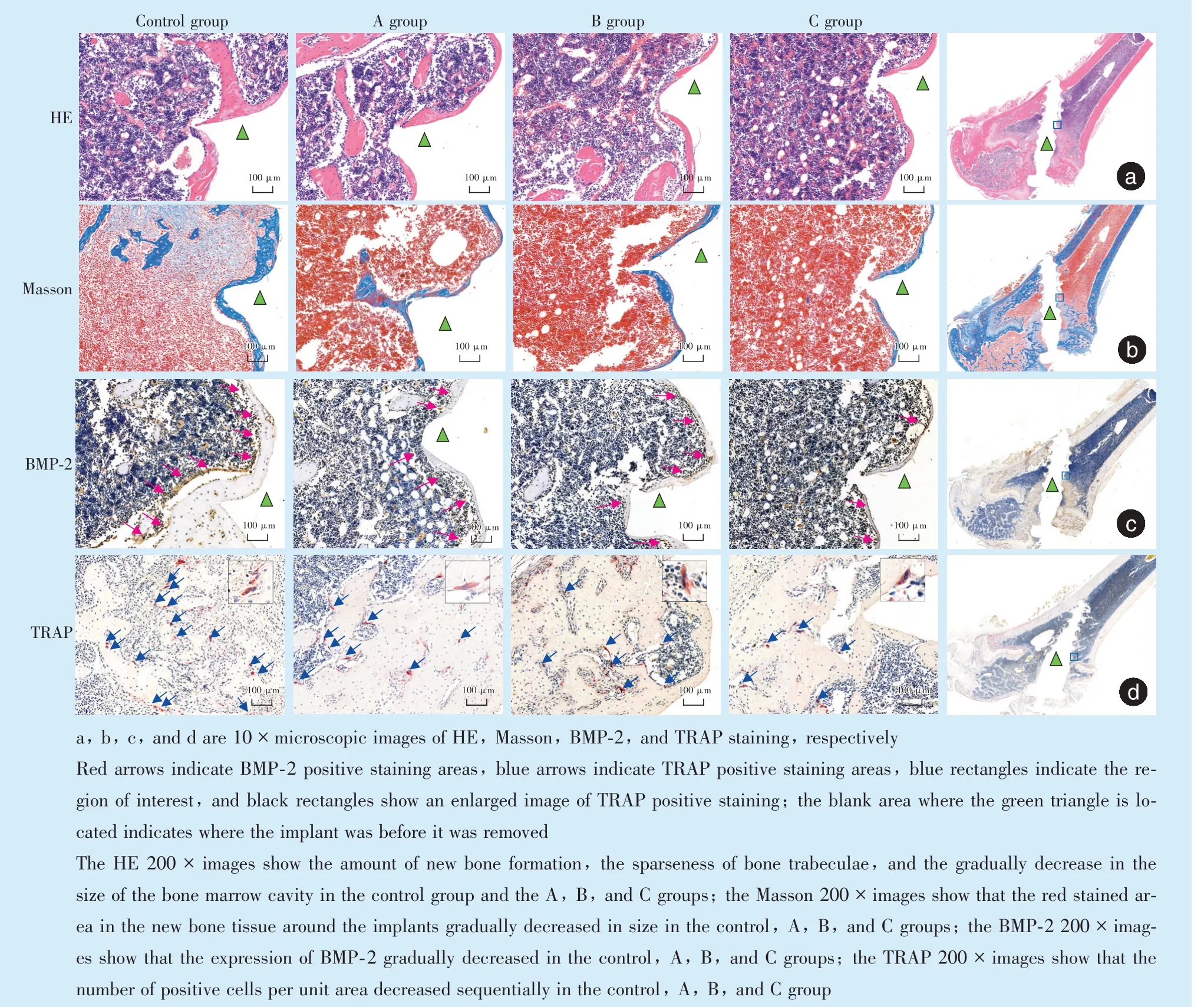
Figure 1 Results of HE,Masson,BMP-2 and TRAP staining in each group in the 2nd week图1 2 周时各组HE、Masson、BMP-2 及TRAP 染色结果
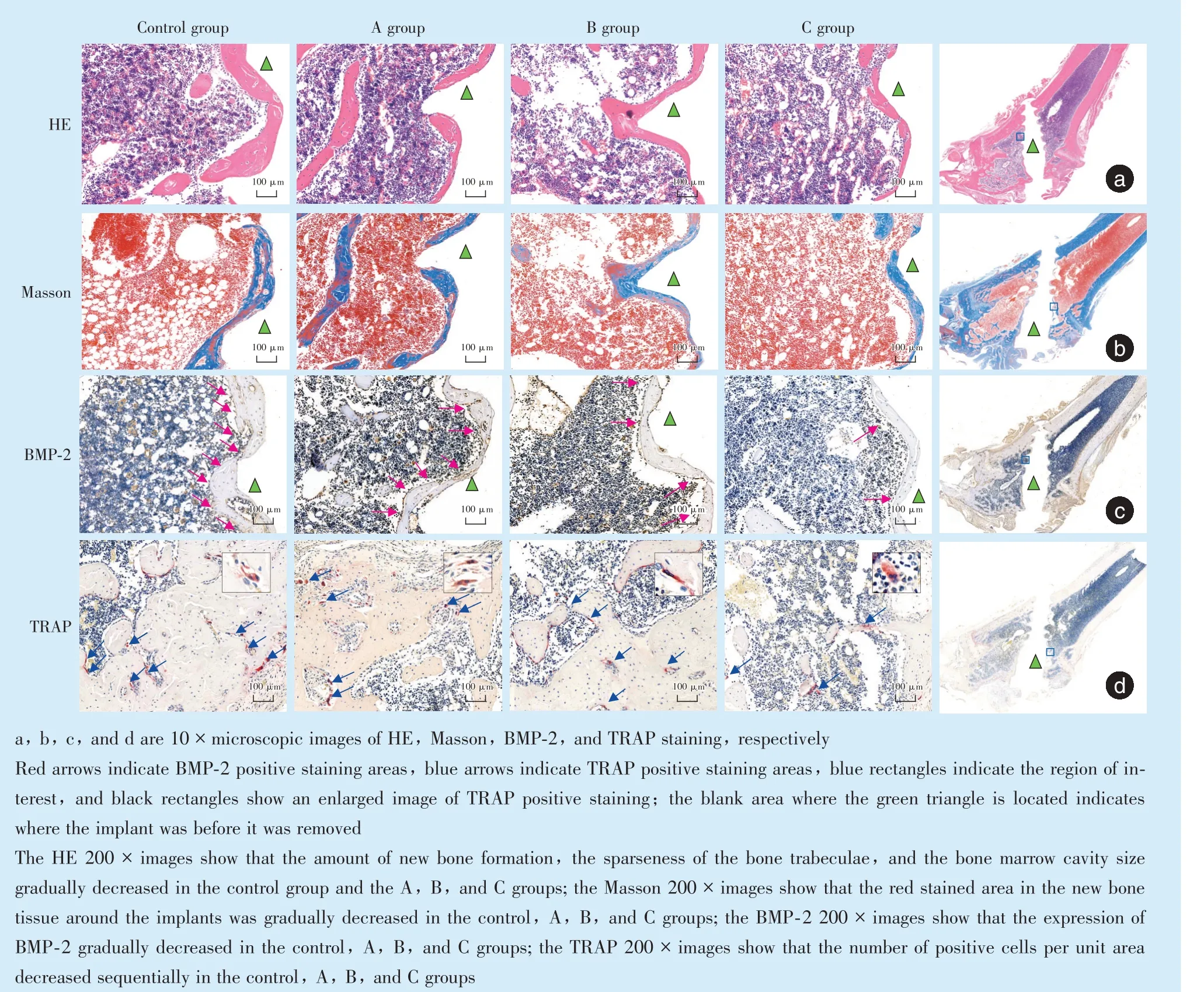
Figure 2 Results of HE,Masson,BMP-2 and TRAP staining in each group in the 4th week图2 4 周时各组HE、Masson、BMP-2 及TRAP 染色结果
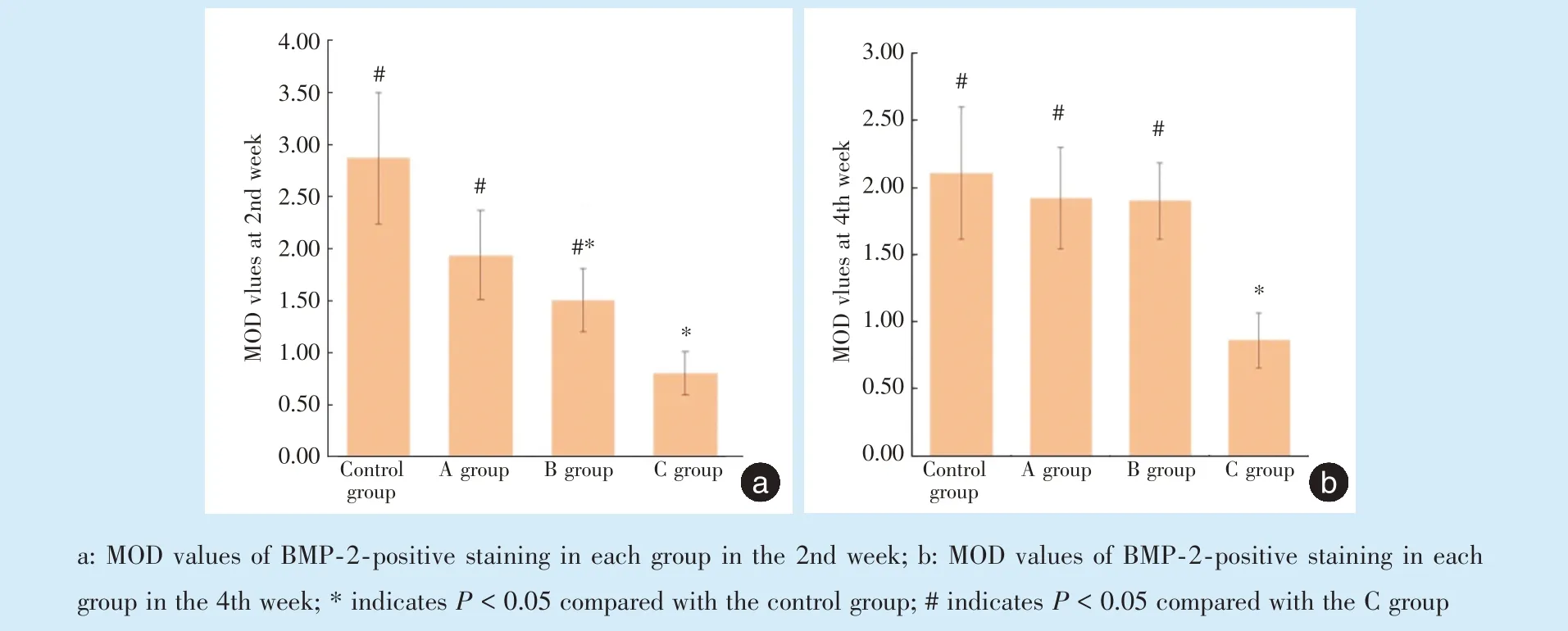
Figure 3 MOD values of BMP-2-positive staining in each group in the 2nd and 4th week图3 2、4 周时各组BMP-2 阳性染色的MOD 值
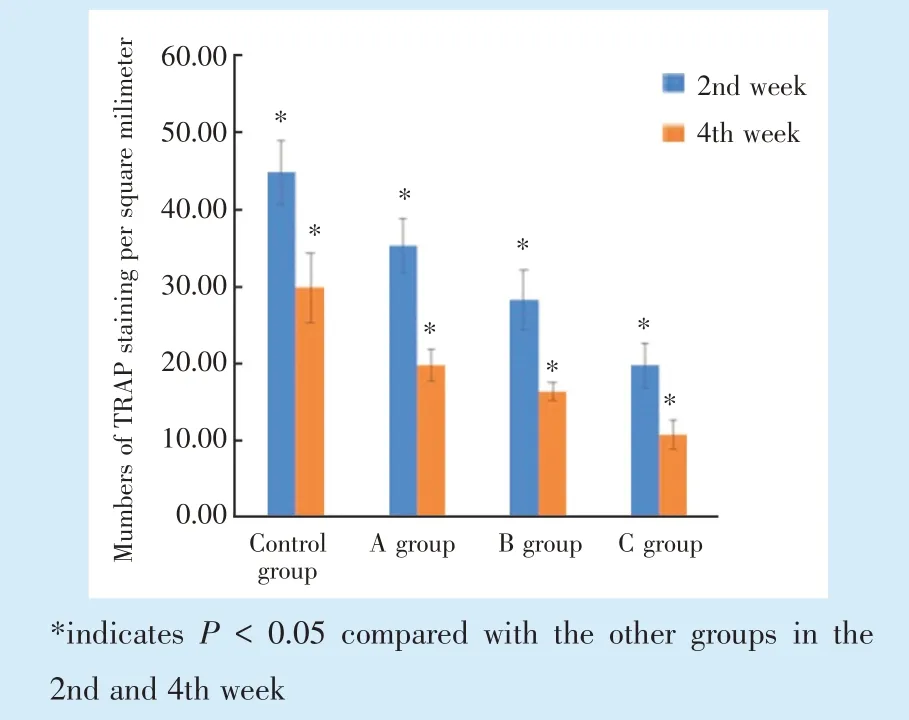
Figure 4 Amount of TRAP-positive staining per unit area in the 2nd and 4th week图4 2、4 周时单位面积TRAP 阳性染色个数
3 讨 论
阿司匹林为非选择性环氧合酶(cyclooxygenase,COX)抑制药,通过使COX 乙酰化失活,阻断花生四烯酸(arachidonic acid,AA)转化为血栓烷A2(thromboxane,TXA2);同时也减少前列腺素(prostaglandin,PG)的合成。前列腺素E2(prostaglandin E2,PGE2)为PG 家族中的一种,PGE2 参与骨细胞间的信号转导,对于成骨细胞的分化及骨组织的形成至关重要,同时也影响着破骨细胞的形成和表达[6]。种植成功的关键是形成良好的骨整合,成骨细胞与破骨细胞在骨组织的形成与改建中发挥重要作用[7],阿司匹林降低PGE2 的生成,而PGE2又促进成骨细胞及破骨细胞的成骨过程,因而阿司匹林可能抑制种植体周围骨形成[8]。
阿司匹林可能对种植体周围骨形成有抑制作用,且该作用与阿司匹林剂量呈相关性。在阿司匹林对于兔尺骨骨折影响的实验中发现,阿司匹林给药量而非给药频率在骨折端骨延迟愈合中发挥作用,且延迟程度呈剂量依赖性[9]。在去势大鼠骨缺损模型中也发现,单独使用阿司匹林未明显改变骨形成及代谢相关指标[10]。本研究HE 染色结果显示,B、C 组较对照组种植体周围新生骨板厚度薄、连续性差、骨小梁数量少、骨髓腔大,随着给药量的增加新骨形成量逐渐降低,且C组最明显,但A组与对照组比较差异却不明显,推测高剂量阿司匹林可能减少种植体周围新骨形成量,且减少程度与阿司匹林剂量相关,这与上述高剂量阿司匹林对于骨形成的抑制作用相符合。
阿司匹林可能通过抑制成骨细胞的分泌、增殖及分化功能进而抑制种植体周围的骨形成过程。用50、100、200 μg/mL 的阿司匹林作用于人骨髓基质细胞(bone marrow stromal cells,BMSCs),结果显示阿司匹林直接抑制BMSCs 的增殖并减慢细胞外间质的矿化,且该作用呈剂量依赖性[11]。通过将不同剂量的阿司匹林等非甾体类抗炎药(nonsteroidal anti-inflammatory drugs ,NSAIDs)作用于MG63 细胞,发现高剂量组增加了MG63 细胞的坏死和凋亡,而在低剂量组中此现象不明显[12-13]。骨基质的主要有机成分是Ⅰ型胶原,I 型胶原由成骨细胞分泌,与成骨细胞的增殖与分化、骨基质的形成与矿化密切相关。本研究Masson 染色结果显示随着药物浓度的增加,实验组红染区域较对照组逐渐减小,且C 组减小最明显,但A 组较对照组差异不明显。骨形成蛋白2(bone morphogenetic protein-2,BMP-2)由成骨细胞产生,能够促进成骨细胞分化增殖并诱导成骨,在新骨形成活跃阶段表达增高[14]。研究表明,通过COX-2 途径生成的PGE2 能够与EP4 受体结合促进BMP-2 及核因子κB 受体活化因子(receptor activator of nuclear factor kappa B,RANKL)的表达进而促进骨再生及愈合[15-16]。本研究免疫组织化学染色结果显示骨组织中BMP-2 的表达随着药物浓度的增加依次减小,但对照组与A 组差异不明显,C 组与其余组间差异具有统计学意义。由Masson 及BMP-2 染色结果可以推测:阿司匹林通过失活COX 降低PGE2 生成,PGE2 的减少可能又降低了成骨细胞的分泌、增殖及分化的能力,进而抑制种植体周围骨形成,且与阿司匹林剂量有关,这与上述阿司匹林对成骨细胞的抑制作用相符合。
阿司匹林可能通过抑制破骨细胞的生成进而抑制种植体周围骨改建过程。在骨组织吸收和重建中,破骨细胞至关重要[17],且与成骨细胞间存在相互作用影响成骨细胞的生成及生理功能[18-19]。研究发现破骨细胞能够促进人间充质干细胞(human mesenchymal stem cell,hMSC)迁移及分化为成骨细胞,破骨细胞通过1-磷酸神经鞘氨醇(sphingosine 1-phosphate,S1P)和骨形成蛋白-6 来募集骨损伤区成骨前体细胞,并通过Wnt/BMP 通路促进骨的形成[20]。动物研究发现,因c-fos 基因缺乏不能形成破骨细胞的鼠,骨的形成也相对减少[21]。通过比较富破骨细胞骨硬化症鼠与乏破骨细胞骨硬化症鼠的骨形成情况,发现前者的骨形成量、骨组织体积及骨小梁强度均高于后者[22]。抗酒石酸酸性磷酸酶(tartrateresistant acid phosphatase,TRAP)是破骨细胞中高度表达的关键酶,参与破骨细胞介导的骨转换过程。对去势大鼠给予小剂量阿司匹林6 个月,经TRAP 染色发现大鼠胫骨组织中破骨细胞的数量较对照组减少[23]。在C57BL/6J 小鼠种植体相关感染的实验中,TRAP 染色显示15、30、60 mg的阿司匹林明显降低破骨细胞的表达,且该抑制作用呈剂量依赖性[24]。本研究发现破骨细胞的数量随着阿司匹林给药量的增加而减少,呈剂量依赖性。破骨细胞的减少反映了骨形成与重塑活动的减弱,进而减弱种植体周围新骨的形成与改建。此结果也验证了阿司匹林对于破骨细胞的抑制作用。
综上所述,阿司匹林可能通过抑制成骨细胞的生成及破骨细胞的表达来减少种植体周围骨组织的产生,该影响可能与阿司匹林使COX失活进而减少PGE2 形成有关。阿司匹林对种植体周围骨形成的抑制作用呈剂量依赖性,高剂量阿司匹林抑制作用更明显。本实验结果为临床上服用阿司匹林患者的牙种植早期骨形成情况提供参考,而阿司匹林在骨形成中的具体作用机制及远期影响还有待进一步的实验加以探究。
