原发性高血压患者血浆可溶性ST2浓度与左室肥厚的关系
2020-04-29杨树涵陈红伟刘艳宾邢永生王志方
杨树涵 陈红伟 刘艳宾 邢永生 王志方
(新乡市中心医院心血管内科,河南 新乡 453000)
左室肥厚(LVH)是一种心室壁增厚、心肌重量增加和心肌重塑的心肌变化现象,进一步发展可造成心脏泵功能下降,继而出现心力衰竭症状,是长期高血压对心脏靶器官造成的器质性结构损害,是心血管疾病不良预后的独立危险因素〔1〕。可溶性ST2是白细胞介素(IL)-1受体家族的成员之一,可作为“诱饵受体”与ST2L竞争性结合IL-33,阻断ST2L/IL-33系统的抗心肌肥大和纤维化的心血管保护作用,与心肌重塑和心血管事件有关〔2〕。已经证实可溶性ST2是心力衰竭、急性心肌梗死不良预后的独立危险因素〔3〕。但目前可溶性ST2在原发性高血压(EH)患者中的研究较少。本研究拟通过测定EH患者中血浆可溶性ST2的浓度探讨其在EH患者中与LVH的关系。
1 对象与方法
1.1研究对象 本研究为单中心横断面研究。选择2017年6~12月在新乡市中心医院心血管内科门诊就诊的260例EH患者,其中男144例,女116例,年龄30~72岁,平均(54.2±8.5)岁,根据超声心动图结果分为EH组(132例)、EH+LVH组(128例),同期来院进行健康体检者为对照组(140例)。LVH 诊断标准:左室质量指数(LVMI)男≥115 g/m2,女≥95 g/m2。入选标准:(1)符合EH诊断标准;(2)年龄30~80岁。排除标准:(1)继发性高血压;(2)缺血性心脏病;(3)风湿性心脏病;(4)合并急、慢性严重感染;(5)合并严重肝、肾功能损害者;(6)合并恶性肿瘤者;(7)合并糖尿病。本研究经新乡市中心医院伦理委员会批准,所有患者同意参与并签署知情同意书。
1.2方法 每个患者进行常规病史询问,体格检查,测量血压,心率,抽血送化验室进行生化检测并测量N末端B型利钠肽(NT-proBNP)水平。
1.3心脏超声检查 采用荷兰飞利浦ie33型超声心动仪,探头频率为3.5 MHz,采用标准胸骨旁左室长轴切面,测量5个连续心动周期,取平均值。测量指标包括室间隔厚度(IVST)、左心室后壁厚度(LVPWT)和左室舒张末期内径(LVEDD)。左心室质量(LVM)=0.8×1.04〔(IVST+LVEDD+LVPWT)3-LVEDD3〕+0.6,LVMI=LVM/体表面积(m2)。体表面积(m2)=0.005 7×身高+0.012 1×体重(kg)+0.088 2(男性)。体表面积(m2)=0.007 3×身高+0.012 7×体重(kg)-2.106(女性)。
1.4可溶性ST2浓度测定 常规取肘静脉血2 ml,注入肝素抗凝管内,4 000 r/min离心10 min,取上层血清标本置于-80℃ 冰箱保存,待标本收集完成后统一检测。采用酶联免疫吸附试验应用商品化试剂盒(美国C&D公司)检测可溶性ST2浓度,试剂配制和操作步骤严格按说明书进行。
1.5统计学方法 采用SPSS22.0 软件和MedCalc进行方差分析、q检验、非参数秩和检验、χ2检验、Pearson 直线相关分析;采用受试者工作特征(ROC)曲线判断可溶性ST2和预测LVH的能力;采用Logistic回归分析多变量与LVH的关系。
2 结 果
2.13组一般情况比较 3组性别、体重指数(BMI)、空腹血糖、肌酐、心率比较差异无统计学意义(P>0.05),EH组和EH+LVH组年龄、收缩压、舒张压、平均动脉压、IVST、LVPWT、LVEDD、LVMI、NT-proBNP、可溶性ST2比较差异均有统计学意义(均P<0.05),见表1。
2.2EH患者可溶性ST2和收缩压、LVMI、NT-proBNP相关性 可溶性ST2 与收缩压、LVMI、NT-proBNP呈正相关(r=0.481,P=0.02;r=0.512,P=0.01;r=0.346,P=0.02)。
2.3ROC分析可溶性ST2和NT-proBNP对EH患者出现LVH鉴别诊断价值 可溶性ST2对鉴别EH患者出现LVH的ROC曲线下最大面积(AUC)为0.816,取得敏感性为70.2%,特异性为82.3%,切点值为28.8 ng/ml,P<0.05。NT-proBNP鉴别诊断的AUC为0.702,取得敏感性为76.2%,特异性为83.4%,切点值为280.6 ng/L,P<0.05,两者相比有明显差异(P<0.05)。
2.4EH患者发生LVH的相关危险因素Logistic回归分析 以EH患者LVH为因变量,将年龄、舒张压、收缩压、NT-proBNP、可溶性ST2纳入Logistic回归模型,结果显示可溶性ST2、收缩压是EH患者发生LVH的独立预测因素(P<0.05),见表2。

表1 3组基线资料比较
与EH+LVH组相比:1)P<0.05;与对照组相比:2)P<0.05
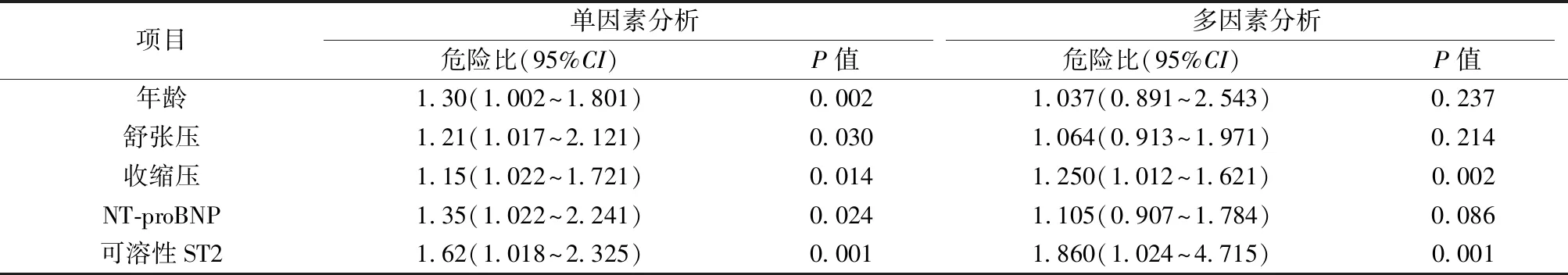
表2 Logistic回归分析EH患者发生LVH的相关危险因素
3 讨 论
可溶性ST2参与免疫炎症的调节,与包含高血压在内的许多心血管疾病预后相关。有研究〔4〕显示,缺氧诱导内皮细胞表达IL-33/ST2,激活下游炎症介质导致肺血管重构,进而导致肺动脉高压。高血压的病理表现是动脉血管内皮功能障碍导致的一种慢性炎症反应,进而引起小动脉血管重构。Coglianese等〔5〕分析发现可溶性ST2浓度与收缩压相关。Ho等〔6〕研究显示,较高的基线可溶性ST2浓度和以后发生高血压相关,基线可溶性ST2浓度在最高四分位数的人群比最低四分位数人群3年后收缩压增加2.6 mmHg,而脉压增加1.8 mmHg,舒张压没有明显变化,患高血压的风险增加了1.8倍。Wu等〔7〕研究表明可溶性ST2基因多态性与高血压易感性有相关性,基因变异可能通过调节可溶性ST2的表达促进EH发生发展。本研究结果和既往研究〔5~7〕相一致。有研究〔8〕显示循环中的可溶性ST2和IL-33主要来源于血管内皮细胞,高血压引起的左室壁张力的增加调节ST2和IL-33的分泌,进而影响下游炎症分子的表达,参与高血压发生发展的过程。LVH是EH患者进展为心力衰竭的关键中间环节,也是包括EH等广泛心血管疾病的不良因素。临床上已有多种药物能够延缓和预防心力衰竭,因此,如何及早检出LVH患者对EH患者的危险分层及防止或延缓心力衰竭的发生至关重要。最早采用12导联心电图检测LVH,虽然简便易行,重复性好,但由于敏感性问题,临床上通常作为超声检查前的一项筛查方法。心脏超声敏感性特异性均较高,已成为目前诊断LVH最常用的检查手段。但由于心脏超声的准确性受到操作者技术水平的影响较大及肥胖病人或合并慢性阻塞性肺疾病患者受到自身声窗条件的限制,诊断的准确性和可重复性受到很大制约。心脏磁共振虽然克服了以上缺点,但由于成本、方便性等原因,目前不常用于诊断目的〔9〕,仅用于鉴别诊断。因此,临床上需要一种准确性高、方便性强、重复性高的监测技术。
综上,EH患者中基线可溶性ST2浓度和LVMI呈正相关,可能是LVH的一种很好的生物标志物。
