硫酸盐对土壤铁矿物还原转化及砷释放的影响
2020-04-28张翅鹏郝瑶玲邱丽娟黄臣臣
刘 涛,张翅鹏,郝瑶玲,邱丽娟,黄臣臣
(贵州大学 资源与环境工程学院,贵州 贵阳 550025)
砷(As)是土壤中的污染物之一。人类活动和自然来源产生的As在土壤环境中不断累积。在砷污染土壤上生长的水稻能大量吸收土壤中的As,进而通过食物链传递严重威胁人类健康[1]。在氧化环境下,As在土壤中主要以As(Ⅴ)存在,通常能与铁氧化物结合,生物可利用度较低;但在厌氧环境下,氧化还原电位降低导致铁氧化物还原溶解并将吸附的As释放到土壤孔隙水中,其生物活性增强[2-3]。此外,在厌氧微生物的还原作用下,生成的硫化物还能与液相中的Fe(Ⅱ)离子相互作用,从而改变As在土壤中的迁移性[4]。
通常,土壤环境中的硫(S)和As具有相似的微生物氧化还原特征[5]。水稻土中S的还原作用是以硫酸盐还原菌(SBR)为主的微生物介导过程,硫酸盐的含量直接影响SBR的数量,并进一步影响硫酸盐还原过程,及Fe的形态转化。在厌氧还原环境下,与Fe、As迁移转化有关的微生物的群落水平、代谢和基因表达会发生改变,从而影响As的生物化学过程[6]。Fe具有高氧化还原敏感性[7],硫酸盐还原作用驱动Fe还原也会影响土壤中As的固定和释放[8]。当氧化还原条件达到硫酸盐还原范围时,SO2-4还原为S2-,与As形成金属硫化物沉淀,对As起到固持作用[9];而当硫酸盐不足时,微生物的还原作用可导致As被还原、活化和释放,此时外加硫酸盐可使As处于较为稳定的状态[10]。由此可知,硫酸盐是影响土壤环境中As形态与环境行为的关键因素之一。
目前,国内外学者针对土壤环境中S-Fe-As相互作用的研究已经取得不少进展,但关于高砷煤矿区As污染稻田中S-Fe-As相互作用的认识还有待进一步加深[11-12]。为此,本研究以受酸性矿山废水(AMD)污染的水稻土为供试土壤,通过室内土壤泥浆厌氧培养实验,旨在揭示外源硫酸盐加入下S和Fe相互作用对土壤中As释放的影响,以期为As污染水稻土的修复提供科学依据和理论指导。
1 材料与方法
1.1 供试土壤
供试土壤系贵州省黔西南兴仁县交乐村高As煤矿区受AMD污染的稻田耕作层土壤(黄壤),该稻田离污染源较近,当地居民长期使用受AMD影响的水体进行农田灌溉。土壤总As含量为132.26 mg·kg-1,总Fe含量为16.05 g·kg-1,总S含量为2.45 g·kg-1,有机质含量为66.01 g·kg-1。土壤微生物种群主要包括脱硫芽孢弯曲菌属(Desulfosporosinus)、脱亚硫酸菌属(Desulfitobacterium)、厌氧黏细菌属(Anaeromyxobacter)、硫还原地杆菌属(Geobacter)[13-14]。
1.2 实验设计
采用室内土壤泥浆厌氧恒温培养的方法,研究硫酸盐对土壤中砷形态转化的影响。称取若干份水稻土样品,每份3 g,置于30 mL的已灭菌血清瓶中。设置3个处理组:①灭菌组(SG),用高压灭菌锅对水稻土进行高压灭菌处理,121 ℃灭菌20 min后,添加灭菌水1 mL;②非灭菌组(N-SG),向含有未灭菌水稻土的血清瓶内直接添加灭菌水1 mL;③加硫非灭菌组(S-N-SG),向含有未灭菌水稻土的血清瓶内添加浓度为100 mmoL·L-1的Na2SO4溶液1 mL。向所有处理组血清瓶中添加同体积的灭菌水,定容至20 mL。向所有处理组的血清瓶充氮气5 min,除去培养瓶内氧气后,加橡胶帽和铝盖密封,置于气浴恒温振荡器中,30 ℃恒温振荡5 min,然后置于(30±2)℃的恒温培养箱中避光静置培养,定期培养0、5、10、15、20、25、30 d。培养完成后将样品取出,并迅速置于恒温振荡箱中30 ℃恒温振荡5 min,然后全部放入厌氧手套箱(温度30 ℃,湿度70%)中静置,待澄清后倒出一小部分上清液于100 mL离心管中,分别测定溶液的pH值和氧化还原电位(Eh)。上清液经0.22 μm滤膜过滤后置于4 ℃保存,用于测定液相中Fe(Ⅱ)、As(Ⅲ)浓度。所有的取样、测定,以及上清液过滤等步骤均在厌氧手套箱内进行。
称取过滤后的沉积物于离心管中,按照固液质量体积比3∶20的比例加入1 mol·L-1的盐酸,随后在气浴恒温振荡箱中30 ℃恒温振荡浸提24 h,3 000 r·min-1离心分离,上清液过滤后置于4 ℃保存,测定As、Fe(Ⅱ)含量,分析土壤中铁矿物的还原与As的活化。
1.3 样品测定
pH和Eh用酸度计测定(PHSJ-3F,上海雷磁仪器厂);总As含量采用水浴消解法消解,用原子荧光光谱仪(AFS-9700,北京海光仪器有限公司)测定;液相中As(Ⅲ)的含量采用高效液相色谱原子荧光联用仪(HPLC-AFS9700,美国赛默飞世尔)测定;总Fe含量采用高压密闭消解法消解,用原子吸收光谱仪(ICE3500,美国赛默飞世尔)测定;总S含量采用艾式卡熔融BaSO4质量法测定[15];液相中Fe(Ⅱ)的浓度用邻菲罗啉光度法测定。
1.4 数据分析
运用Microsoft Excel 2013进行数据统计与分析,用Origin 2018和SPSS 21.0进行图表绘制和相关性分析。
2 结果与分析
2.1 厌氧条件下硫酸盐对土壤溶液pH和Eh的影响

图1 不同培养时间土壤溶液中pH(a)和Eh(b)的变化Fig.1 Variation of pH (a) and Eh (b) in soil solution at different incubation time
在实验条件下,3组土壤悬液的初始pH相近,后均先降低又逐渐升高(图1-a)。有研究表明,还原菌(如硫酸盐还原菌)在厌氧条件下分解有机质会产酸、产氢,使体系pH降低[16],在此过程中,氧化还原电位也逐渐降低,介于-243~60 mV,土壤中的铁氧化物可作为电子受体参与反应[17]。随着氧化还原电位的持续降低(图1-b),硫酸盐可被还原菌利用生成OH-,致使pH迅速升高,这是S-N-SG组pH持续高于其他实验组的主要原因。此外,SG组氧化还原电位最低值为-118 mV,还原性相对较弱,10~30 d该组pH低于N-SG组;S-N-SG组氧化还原电位相对较低,最低值为-243 mV。总之,在厌氧环境条件下,微生物可使得土壤体系的pH升高,氧化还原电位降低,硫酸盐的添加会进一步增强这一作用。
借助Fe和As的pH-Eh图判断,土壤中的Fe会以亚铁态[Fe(Ⅱ)]溶出,随着实验的进行,Fe2+易于形成羟基氧化铁(FeO·OH),伴随释放出的As的稳定态为亚砷酸(H3AsO3)(图2)。当也有H2S释放时,会与Fe2+反应生成FeS,或同时发生如下反应[18]:


图2 pH-Eh影响下溶液中As、Fe的不同存在形式相图(25 ℃,101.3 kPa)Fig.2 pH-Eh phase diagram for iron and arsenic at 25 ℃ and 101.3 kPa
2.2 厌氧条件下硫酸盐对土壤中Fe还原的影响
土壤厌氧微生物对铁矿物的还原转化起着重要作用。SG组土壤在实验过程中盐酸提取态Fe(Ⅱ)含量增加相对缓慢,且在第10天后持续降低(图3-a);N-SG和S-N-SG组土壤Fe(Ⅱ)含量在0~5 d迅速增加,平均增速分别为0.22、0.27 g·kg-1·d-1,5 d后增速放缓,平均为0.01、0.03 g·kg-1·d-1,至实验结束时,土壤Fe(Ⅱ)含量分别为SG组的2.18和2.71倍,表明在微生物的作用下,硫酸盐的添加有助于增强土壤铁矿物的还原累积。
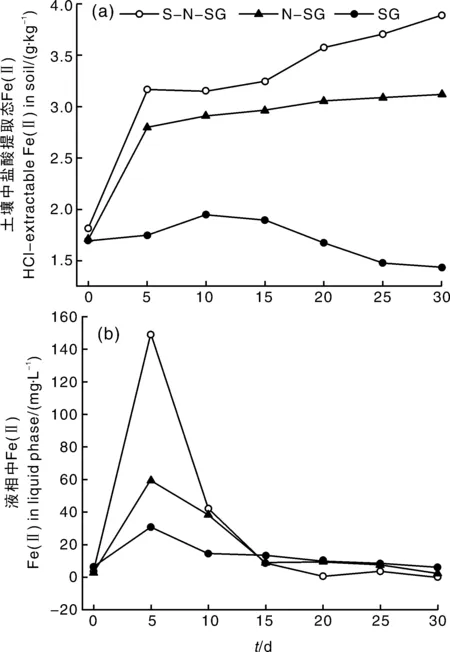
图3 不同培养时间土壤盐酸提取态Fe(Ⅱ)(a)和液相中Fe(Ⅱ)(b)含量的变化Fig.3 Variation of HCl-extractable Fe(Ⅱ) in the solid phase (a) and Fe(Ⅱ) content in liquid phase (b) at different incubation time
随着土壤铁矿物的还原转化,液相中的Fe(Ⅱ)含量也不断变化,3个实验组的变化趋势相同,均在第5天达到最大值,其中S-N-SG组为149 mg·L-1,分别为N-SG和SG组的2.50倍和4.78倍(图3-b),表明硫酸盐的添加会显著增强土壤厌氧微生物对铁矿物的还原释放。之后,5~10 d液相中的Fe(Ⅱ)含量均降低,分别降低71.56%(S-N-SG)、35.68%(N-SG)和53.11%(SG)。至15 d时,3个实验组液相中的Fe(Ⅱ)含量相当,直至实验结束都相差较小。实验过程中观察发现,2个非灭菌组在第5天后血清瓶开始变黑。有研究证明,土壤在还原作用下生成H2S,并与Fe2+反应生成FeS,致使显现黑色[19]。这表明,在初始阶段,受还原条件的限制,硫酸盐并未参与还原进程,因而促使Fe(Ⅱ)浓度在液相中升高。当硫酸盐被还原后,S2-与累积的Fe2+迅速反应,液相中的Fe(Ⅱ)浓度快速降低。此外,15 d后随pH值和氧化还原电位的升高,Fe(Ⅱ)更易于生成FeO·OH(s),液相中的Fe(Ⅱ)浓度受FeS和FeO·OH低溶解性的控制,因此均能被控制在较低水平,直至实验结束,而土壤中盐酸提取态Fe(Ⅱ)呈不断累积趋势(图3-a)。总之,在还原菌的作用下,土壤硫酸盐的增多会促进土壤中Fe(Ⅱ)矿物的还原累积,但在不同还原阶段,对铁矿物还原释放Fe(Ⅱ)的作用不同。

图4 不同培养时间土壤盐酸提取态As(a)和液相中As(Ⅲ)(b)含量的变化Fig.4 Variation of HCl-extractable As(a) in soil and As(Ⅲ) (b) content in liquid phase at different incubation time
2.3 厌氧条件下硫酸盐对土壤中As释放的影响
相关研究表明,随土壤中铁矿物还原As的活化程度,盐酸可提取态As越多,As被活化量越大[20]。在实验初始阶段(0~5 d),铁氧化物为主要还原反应物,3个实验组土壤中盐酸可提取态As均增加,但变化差异明显(图4-a),增加速率分别为3 μg·kg-1·d-1(SG)、114 μg·kg-1·d-1(N-SG)和338 μg·kg-1·d-1(S-N-SG),表明微生物在土壤As的活化中起关键作用,且添加硫酸盐后微生物的活化作用进一步增强,活化速率提高。当进入硫酸盐还原阶段后,铁氧化物还原减弱,土壤中盐酸可提取态As含量降低,微生物作用越强,降低越明显,至第15天降至最低值。当液相中的Fe(Ⅱ)含量降低时,FeS沉淀作用减弱,在铁氧化物还原,及FeS与As共沉淀的作用下,土壤中盐酸可提取态As含量持续增加,微生物作用越强,增加越明显。
在实验初始阶段(0~5 d),土壤向液相释放As和Fe的特征相似,均在第5天达到最大值,微生物作用越强,释放量越大,3个实验组中As和Fe的释放比例关系分别为0.14 μg·mg-1(SG)、0.10 μg·mg-1(N-SG)和0.07 μg·mg-1(S-N-SG),表明在该阶段随微生物作用增强,单位质量Fe释放的As含量降低(图4-b)。当进入硫酸盐还原阶段后,液相中的As含量迅速降低,印证了As与FeS会发生共沉淀[21],微生物作用越强,沉淀效果也越明显,至第15天,液相中的As含量降至最低。然而,进一步的研究发现,随着实验的进行,液相中的As含量并未因Fe含量的持续相对稳定而保持不变,反而不断增加。分析推测,土壤铁氧化物不断还原释放的As含量要大于被FeO·OH和FeS吸附共沉淀的量,因为高价铁氧化物被还原生成亚铁矿物后对As的吸附能力减弱[22]。此外,硫酸盐的添加会保持土壤中微生物的强还原能力,至实验结束时,S-N-SG组在液相中的As浓度要高于其他2个实验组。
2.4 厌氧条件下土壤中Fe和As转化、释放的相关性分析
综合3个实验组的数据进行相关性分析(表1):土壤中盐酸提取态Fe(Ⅱ)含量与氧化还原电位呈极显著(P<0.01)负相关关系,表明土壤铁矿物的还原转化主要受氧化还原条件的控制,还原性越强,转化量越大;液相中Fe(Ⅱ)的释放量与土壤中的盐酸提取态Fe(Ⅱ)含量无显著相关关系,但与液相pH呈极显著(P<0.01)负相关关系,表明土壤铁矿物经还原转化后释放量受液相酸碱度的控制,酸性越强,释放量越大;土壤中盐酸提取态As含量与液相中Fe(Ⅱ)浓度呈极显著(P<0.01)正相关关系,表明土壤还原释放的Fe(Ⅱ)量越多,被活化的As含量越大;土壤中盐酸提取态的As含量与液相中As浓度呈极显著(P<0.01)正相关关系,表明土壤中As活化量越大,释放量越多。
表1 土壤中Fe和As转化、释放的相关性
Table 1 Correlations of transformation and release of iron and arsenic in soil

指标IndexpHEhAs-HClAs-lFe(Ⅱ)-HClEh-0.243As-HCl-0.3740.086As-l-0.200-0.3570.786∗∗Fe(Ⅱ)-HCl0.342-0.639∗∗0.3220.569∗∗Fe(Ⅱ)-l-0.594∗∗-0.1490.814∗∗0.730∗∗0.153
As-HCl,土壤中的盐酸提取态As;As-l,液相中的As(Ⅲ);Fe(Ⅱ)-HCl,土壤中的盐酸提取态Fe(Ⅱ);Fe(Ⅱ)-l,液相中的Fe(Ⅱ)。**表示在P<0.01水平(双侧)极显著相关。
As-HCl, HCl-extractable As in soil; As-l, As(Ⅲ) in the liquid phase; Fe(Ⅱ)-HCl, HCl-extractable Fe(Ⅱ) in soil; Fe(Ⅱ)-l, Fe(Ⅱ) in the liquid phase. ** indicated significant correlation atP<0.01 level (both sides).
在实验初始阶段(0~5 d),向液相中释放的As和Fe量呈极显著(P<0.01)正相关关系,表明As是伴随Fe的释放而释放的,这与Bennett等[23]的研究结果一致,但进入硫酸盐还原阶段后,由于体系反应的复杂性,以及As和Fe的性质差异,二者之间不存在正相关关系。
3 结论
本实验显示,在厌氧条件下添加硫酸盐会促进微生物对土壤体系pH和氧化还原条件的调控,实验初始阶段,在微生物的作用下,土壤悬液pH升高、Eh降低,硫酸盐的添加会增强这一趋势。随实验进行,亚铁易于形成羟基氧化铁(FeO·OH),且伴随释放出As,释放出的As以亚砷酸(H3AsO3)形态为主。
还原转化的初始阶段,外源硫酸盐添加会显著增大Fe、As的活化释放量,随还原性增强,硫酸盐大量还原后与Fe反应生成硫化物矿物,土壤中的铁矿物还原速率随之降低,Fe和As的释放亦得到抑制。随着实验的进行,溶液中的Fe浓度受铁矿物沉淀作用持续控制在较低水平,而As浓度不断增加。加入硫酸盐会使As的释放量更高。
