基于Mn3+浓度和形貌控制的高性能LiNi0.5Mn1.5O4正极材料
2020-04-27郭满毅薛志民晏莉琴解晶莹闵凡奇
罗 英,王 勇,郭满毅,3,薛志民,4,刘 雯,晏莉琴,解晶莹,闵凡奇
(1.上海空间电源研究所空间电源技术国家重点实验室,上海 200245;2.上海动力储能电池系统工程技术有限公司,上海 200241;3.西北工业大学 材料学院,陕西 西安 710072;4.燕山大学环境与化学工程学院,河北 秦皇岛 066004)
0 引言
发展高比能、高比功率以及高可靠储能技术是空间电源发展的永恒主题[1-2]。锂离子电池以其自身高比能量、高电压平台、无记忆效应、长循环寿命等独特优势,在空间电源领域应用广泛。而提高锂离子电池比能量的途径主要有两种:一是提高正负极材料的比容量;二是提高正极材料的脱锂电位。近年来,众多研究者对5 V高电压正极材料开展了大量研究。其中,具有4.7 V电位平台的高电压尖晶石镍锰酸锂材料兼具高的能量密度以及功率密度,成为高电压材料研究的热点[3]。同时,相比传统的钴酸锂电池,镍锰酸锂电池的输出电压从3.8 V提高到了4.6 V。在满足高压锂离子电池系统需求的情况下,提高单体电池输出电压可以有效减少电池串联数量,将进一步改善电池组的可靠性。因此,高电压LiNi0.5Mn1.5O4材料在空间电源系统中具有良好的应用前景。
LiNi0.5Mn1.5O4材料是通过使用0.5 mol的Ni取代尖晶石锰酸锂(LiMn2O4)中的Mn得到的。其Mn元素理论上为+4价。目前,已报道了多种LiNi0.5Mn1.5O4材料的合成方法,如高温固相法[4]、共沉淀法[5-7]和溶胶凝胶法[8]等。大部分报道的LiNi0.5Mn1.5O4材料由于高温煅烧过程而表现为无序Fd3m空间结构[9]。这是因为镍锰酸锂材料在高温条件下由于失氧反应导致Mn4+部分还原为Mn3+,并有LixNi1-yO杂相产生。尽管Mn3+具有电化学活性,但是部分Mn3+可以通过歧化反应形成Mn2+和Mn4+。其中,Mn2+易溶于电解液,特别是在高温下,从而造成严重的容量衰减。
许多研究团队对材料中Ni或者Mn进行阳离子掺杂取代开展了大量的研究工作,如Ti、Fe、Gr和Ru等[10-13],以抑制杂相的生成,提高材料的电化学性能。Manthiram等[14]研究表明Cr、Fe、Ga等离子掺杂可以有效减小立方相之间的晶胞参数差异。另外,表面涂层也是一种改善材料性能的有效手段。截至目前,氧化物(Al2O3、ZnO、ZrO2)、磷酸盐(AlPO4、ZrP2O7)以及锂离子导体固体电解质(Li7La3Zr2O12)等[15-18]表面修饰材料已应用在高压材料上。
制备具有优良电化学性能的镍锰酸锂材料,其关键因素是对合成方法的优化。然而即使是相同的合成方法,不同团队报道的材料性能仍有明显差异。这是因为控制材料性能的关键参数,如Mn3+含量、形貌等,仍然具有一定争议。Mn3+的存在有利于提高材料的电子电导率和离子电导率,从而改善其倍率特性。但是为了减少Mn2+溶解,需要减少材料中Mn3+含量。相比于微米级颗粒,纳米级的镍锰酸锂由于缩短了锂扩散路径,降低了电化学极化而表现出高的倍率性能,但高的比表面积将加剧界面副反应,使得循环稳定性变差。因此,为了改善材料的电性能,需要调节LiNi0.5Mn1.5O4材料的形貌和Mn3+含量。
本文通过控制高温退火时间制备了不同Mn3+含量和形貌的LiNi0.5Mn1.5O4材料,对其电化学性能进行了评估,并详细讨论了Mn3+含量和形貌对材料电化学性能的作用机制。
1 实验部分
采用高分子辅助共沉淀-高温煅烧法合成LiNi0.5Mn1.5O4材料。首先,按化学计量比配置2 mol·L-1的MnSO4·H2O、NiSO4·6H2O混合溶液。其次,将聚丙烯酰胺(PAAM)溶于去离子水,配置成质量分数为0.8%的分散剂溶液,之后将Na2CO3沉淀剂按照化学计量比过量20%的用量加入并充分混合,形成混合溶液。通过蠕动泵传输两种混合溶液,使其在带搅拌的反应釜中反应生成镍锰碳酸盐沉淀。控制溶液pH值为8,反应时间为20 h。沉淀过滤干燥后在600 ℃煅烧5 h得到M2O3(M=Mn,Ni)氧化物。将氧化物与Li2CO3按比例充分混合均匀后,在空气气氛下400 ℃煅烧6 h,再在900 ℃保温20 h后,随炉冷却至室温,制得未退火的LiNi0.5Mn1.5O4材料,标记为T-0。另外三种退火的样品在900 ℃保温20 h后快速降温至700 ℃分别保温5、15和25 h,最后随炉冷却至室温,分别标记为T-5、T-15和T-25。
2 测试表征
样品的颗粒尺寸和形貌采用扫描电子显微镜(Hitachi S-4800,日本)进行表征。XRD谱图采用日本Rigaku公司的粉末X射线衍射仪采集。仪器参数为CuKα 辐射源,电压40 kV,电流150 mA。测试条件为5(°)/min的扫描速度,10°~80°的扫描范围。通过MDI Jade 5.0软件计算晶格常数。样品的拉曼谱图通过英国雷尼绍inVia显微拉曼光谱仪进行采集。波长设置为780 nm。XPS测试采用美国PHI公司的PHI 5000C ESCA System仪器,实验条件为Mg靶,高压14.0 kV,功率250 W,通能93.9 eV,以C1s(284.6 eV)为基准进行结合能校正。
将合成的活性物LiNi0.5Mn1.5O4与导电剂(SP)、粘结剂(PVDF)按照质量比8∶1∶1称量,用N-甲基吡咯烷酮(NMP)溶剂将其制成均匀浆料。将其在铝箔上涂布形成的极片在120 ℃真空烘箱中干燥形成正极片。将极片称重后转移至充满惰性气体的手套箱中,以锂片为负极,Cellgard 2400聚丙烯多孔膜为隔膜,电解液采用1 mol·L-1LiPF6/V(EC)∶V(EMC)=3∶7,组装成CR-2016扣式电池。充电测试以恒流/恒压方式进行,镍锰酸锂扣式电池电压限制在3.5~4.9 V范围内。对扣式电池进行循环伏安测试,其中锂片作为辅助电极和参比电极。电压限制在3.5~5.0 V范围内,扫速为0.1 mV·s-1。
3 结果与讨论
3.1 形貌分析
对不同退火时间合成的LiNi0.5Mn1.5O4材料形貌进行分析,如图1所示。由图1可见,未退火(T-0)材料由纳米级一次颗粒团聚形成微米级二次颗粒。随着退火时间增加,LiNi0.5Mn1.5O4材料为微米级多面体形貌。这主要是由于在700 ℃下,材料的一次颗粒逐渐长大,从而形成结晶性更好的微米级颗粒。然而,当退火时间增加至25 h时,形成的多面体颗粒进一步发生团聚,形成大尺度的微米级团聚体。

图1 不同退火时间合成的LiNi0.5Mn1.5O4材料的SEM图Fig.1 SEM images of LiNi0.5Mn1.5O4 materials synthesized at different annealing time
3.2 结构分析
不同退火时间合成的LiNi0.5Mn1.5O4材料的XRD图谱如图2所示。由图2可见,未进行退火热处理的材料在43°附近出现岩盐相LixNi1-xO杂相峰。同时,43°附近的杂相峰消失。而经历不同退火时间热处理的材料XRD图谱均为立方尖晶石结构。研究表明,LiNi0.5Mn1.5O4在高温下发生失氧反应,形成氧缺陷,部分Mn4+转化为Mn3+,并伴随杂相生成[19]。该反应为可逆反应,通过低温退火发生吸氧反应,使得部分Mn3+又重新氧化成Mn4+,减少杂相生成。不同退火时间下合成的LiNi0.5Mn1.5O4材料的晶格参数见表1。可以看到,随着退火时间增加,晶格参数逐渐减小。因为Mn4+的半径比Mn3+小,由此证明,随着退火时间增加,材料中Mn3+含量逐渐减少。

图2 不同退火时间合成的LiNi0.5Mn1.5O4材料的XRD谱图Fig.2 XRD patterns of LiNi0.5Mn1.5O4 materials synthesized at different annealing time

表1 不同退火时间合成的LiNi0.5Mn1.5O4材料的晶格参数Tab.1 Lattice parameters of LiNi0.5Mn1.5O4 materials synthesized at different annealing time
对不同退火时间合成的LiNi0.5Mn1.5O4材料进行Raman分析,如图3所示。

图3 不同退火时间合成的LiNi0.5Mn1.5O4材料的Raman谱Fig.3 Raman spectra of LiNi0.5Mn1.5O4 materials synthesized at different annealing time
由图3可见,材料中Mn的平均价态越高,632 cm-1处代表Mn4+-O键的A1g振动的峰强度越高,588 cm-1处代表Mn4+-O键的F2g(1)振动的肩峰分裂更加明显。Ni2+-O键的Eg和F2g(2)振动强度与399 cm-1和490 cm-1处的峰强度对应。相比未退火热处理的材料,退火热处理后材料F2g(1)峰开始分裂,并在218 cm-1和240 cm-1处检测到低强度峰,A1g峰变得尖锐,表明退火过程提高了Ni2+/Mn4+的有序化程度。随着退火时间的增加,F2g(1)峰分裂更加明显,218 cm-1和240 cm-1处的峰强度逐渐增强,说明Ni2+/Mn4+的有序化程度增加。从Ni2+/Mn4+的有序化说明了退火热处理使得材料由无序Fd3m空间结构向有序P4332空间结构转变。从A1g峰逐渐尖锐可以推断出体系中等方性[Mn4+O6]八面体增加,表明体系中Mn4+含量增加。由此说明了退火过程有助于将Mn3+氧化成Mn4+,随着Mn3+含量的减少,材料空间结构的有序程度逐渐增加。
对Mn2p3/2峰进行图谱拟合,其结果见表2。不同退火时间合成的LiNi0.5Mn1.5O4材料的Mn2p3/2图谱如图4所示。

表2 不同退火时间合成的LiNi0.5Mn1.5O4 材料Mn2p3/2 XPS图谱拟合结果Tab.2 Fitting results of Mn2p3/2 XPS spectra of LiNi0.5Mn1.5-O4 materials synthesized at different annealing time
Chowdari等[20]报道了Mn3+和Mn4+的Mn2p3/2结合能分别为641.9 eV和643.2 eV。由图4可见,T-0、T-5、T-15和T-25 4种材料的Mn2p3/2结合能分别为642.4、642.8、643.0和643.1 eV。表明4种材料中Mn元素均为混合价态。相对于未退火热处理的材料,退火后材料中Mn4+/Mn3+相对含量明显增加,表明体系中Mn3+含量减少。这是由于退火热处理过程使得材料中失去的部分氧又重新被吸回来,使得Mn3+被氧化成Mn4+。由此表明,通过控制退火热处理时间可以调节材料中Mn3+含量和有序度。Pasero等[21]研究认为:当LiNi0.5Mn1.5O4-δ(δ代表氧缺陷)材料中0≤δ≤0.05时,材料表现为P4332空间结构;当0.05≤δ≤0.18时,材料表现为Fd3m空间结构。由此可以推断,尽管退火热处理后材料表现为有序的P4332空间结构,当退火热处理时间较短时,体系中仍具有氧缺陷,并伴随Mn3+存在。同时也发现,退火热处理时间从15 h增加到25 h时,Mn4+/Mn3+相对含量并没有大幅度增加,表明当退火时间持续增加时,Mn3+向Mn4+转化将越来越困难。

图4 不同退火时间合成的LiNi0.5Mn1.5O4材料的Mn2p3/2 XPS图谱Fig.4 Mn2p3/2 XPS spectra of LiNi0.5Mn1.5O4 materials synthesized at different annealing time
3.3 电性能分析
不同退火时间合成的LiNi0.5Mn1.5O4材料的循环伏安曲线如图5所示。在4.7 V附近氧化还原峰对应于Ni2+和Ni3+、Ni3+和Ni4+的两个氧化还原反应,因此,4.7 V附近有两对氧化还原峰。4.0 V附近的氧化还原峰对应于Mn3+的氧化还原。研究发现,经过退火热处理的材料在4.7 V附近表现为一对氧化还原峰。这是由于P4332结构的LiNi0.5Mn1.5O4材料在4.7 V氧化还原峰对的电位差小于Fd3m结构[22]。而在一定扫速下两对氧化还原峰由于电位差小,容易重叠而表现出一对氧化还原峰。对比4.0 V附近的氧化还原峰可知,随着退火热处理时间增加,4.0 V峰强逐渐降低,这与材料中Mn3+含量趋势保持一致。
对不同退火时间合成的材料进行0.2 C/0.2 C常温充放电测试,如图6所示。由图6可见,由于Mn3+含量随着退火热处理时间逐渐减小,相应的4.0 V附近平台容量逐渐降低。未退火热处理的材料在4.7 V附近出现两个相差约50 mV的电压平台,而经过退火热处理后的材料,4.7 V附近均表现为一个连续的电压平台,这与P4332空间结构具有的电压平台现象一致。进一步证明了退火热处理使得材料由无序Fd3m空间结构向有序P4332空间结构转变。T-0、T-5、T-15和T-25材料在0.2 C下放电比容量分别为133、140、141和139 mAh·g-1。有序空间结构的材料其放电比容量明显高于无序结构的材料。
不同退火时间合成的LiNi0.5Mn1.5O4材料在0.5 C、1 C、3 C、5 C、10 C和20 C下的倍率放电性能如图7所示。由图7可见,T-0材料在低倍率下放电比容量无明显差异,甚至在0.5 C/20 C下放电比容量仍达到120 mAh·g-1,表明无序结构材料具有良好的倍率特性。而T-5、T-15材料在低倍率下表现出更高的放电比容量,但在高倍率下,材料放电比容量迅速降低。尽管T-15材料在20 C下放电比容量比T-0材料略低,但是其放电电压平台明显提高。这是由于退火处理后材料形成了微米级的多面体形貌,其晶型更加完整,结晶性提高,从而表现出较好的倍率性能。由此证明了通过调控材料Mn3+含量和形貌可以使有序结构材料具有优良的倍率特性。而T-25材料在相同倍率下放电比容量较低,这可能由于长的退火热处理时间使得微米级多面体颗粒进一步团聚形成大尺度团聚体,增加了锂扩散路径,导致其倍率性能降低。
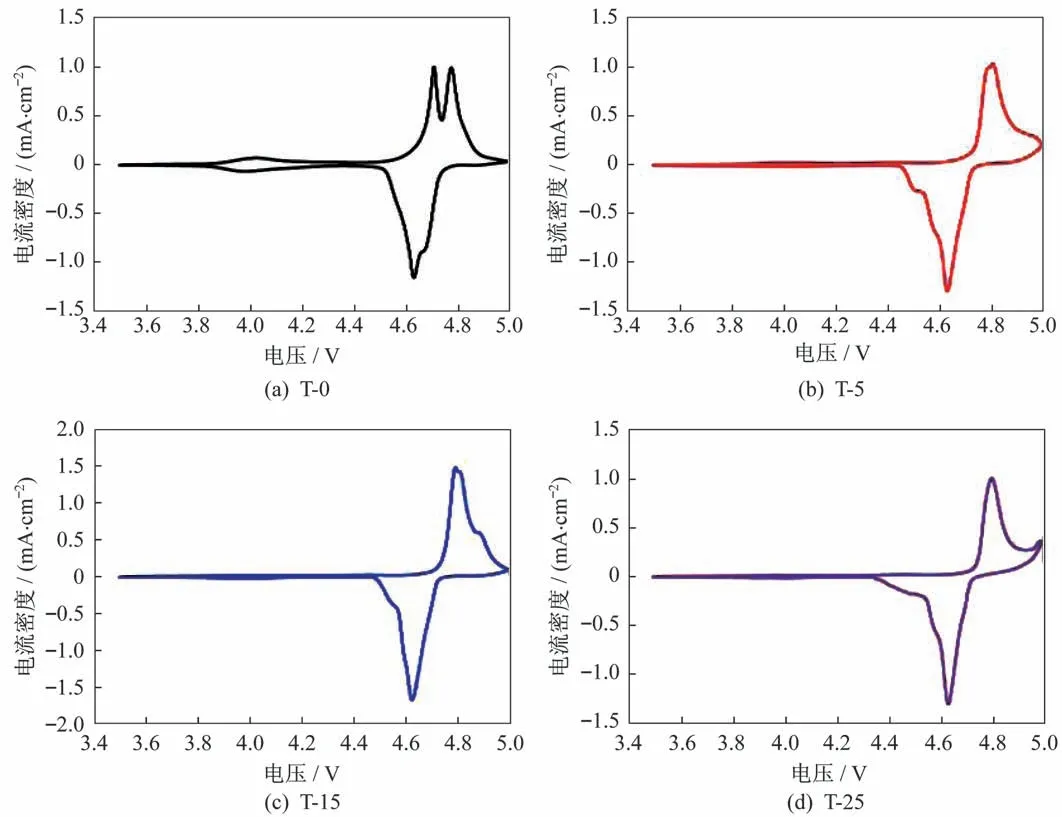
图5 不同退火时间合成的LiNi0.5Mn1.5O4材料的循环伏安曲线Fig.5 Cylic current-voltage curves of LiNi0.5Mn1.5O4 materials synthesized at different annealing time

图6 不同退火时间合成的LiNi0.5Mn1.5O4材料的0.2 C充放电曲线Fig.6 0.2 C charge-discharge curves of LiNi0.5Mn1.5O4 materials synthesized at different annealing time
进一步考察了不同退火时间合成的LiNi0.5Mn1.5O4材料分别在0.2 C/0.2 C和0.5 C/20 C常温循环性能,如图8所示。以0.2 C/0.2 C常温循环50次后,T-0、T-5、T-15和T-25材料的容量保持率相差较小,分别为95.1%、97.5%、98.8% 和98.4%。而在0.5 C/20 C常温循环100次后,T-15样品仍具有92.8%的容量保持率。T-0样品的容量保持率只有85%。这主要是由于尽管T-0样品中Mn3+含量多,有利于高倍率下容量的发挥,但是Mn3+溶解会造成容量衰减,降低材料结构稳定性,同时纳米级的一次颗粒增大了材料的比表面积,导致电解液与界面副反应加剧,从而表现出较低的循环稳定性。由此证明,通过调控材料中Mn3+含量和形貌制备的镍锰酸锂材料具有优异的循环性能。
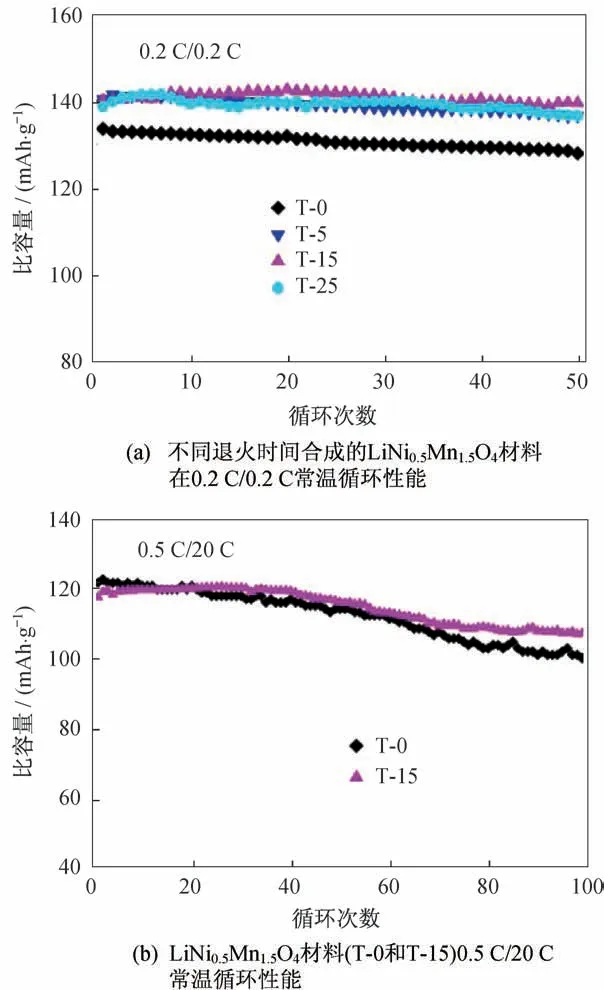
图8 不同退火时间合成的LiNi0.5Mn1.5O4 材料的常温循环性能Fig.8 Cyclic performance of LiNi0.5Mn1.5O4 materials synthesized at different annealing time under room temperature
4 结束语
本文采用高分子辅助共沉淀-高温煅烧法,通过调控Mn3+含量和材料形貌制备了高电压LiNi0.5Mn1.5O4材料。LiNi0.5Mn1.5O4材料的电性能与材料的结构、形貌等影响因素密切相关。合成条件的选择对LiNi0.5Mn1.5O4结构和形貌影响显著。Mn3+含量直接影响材料的电化学性能,特别是在高倍率条件下。因此,为了使材料具有优异的倍率放电性能,应该使Mn3+的含量保持在合适的水平,这样既有利于材料容量的发挥,又具有较高的循环稳定性。实验结果表明:退火热处理15 h合成的材料不仅具有较高的倍率放电容量,同时也具有较高的倍率循环性能。
