新型冠状病毒肺炎的免疫失衡及干预策略
2020-04-26杨晨茜刘怡彤孟思伟王冰琳冯美卿
杨晨茜,瞿 娇,刘怡彤,孟思伟,王冰琳,冯美卿,孙 洋
(1. 南京大学生命科学学院生物技术与药学系,医药生物技术国家重点实验室,江苏 南京 210023;2. 复旦大学药学院,上海 201203)
1 引言
在过去的几十年里,冠状病毒(coronaviruses,CoVs)已经上升为全球公共卫生的重大威胁[1]。自2019年12月起,由新型冠状病毒SARS-CoV-2引发的新型冠状病毒肺炎(以下简称新冠肺炎)的迅速传播加剧了人们对疫情的恐慌[2]。与先前爆发的SARS冠状病毒(SARS-CoV)及中东呼吸综合征冠状病毒(MERS-CoV)相比,新型冠状病毒除了具有相似的基因组、体内复制动力学和生物学性质外,还表现出一些独特性[3-4]。因此,全面认识新型冠状病毒对于疾病防控和药物研发十分关键。
同时,临床上观测到新冠肺炎患者,尤其是重症患者的淋巴细胞计数显著降低,中性粒细胞异常增多,同时伴随着细胞因子大量累积[5]。在SARS和MERS等病毒感染的后期,患者同样出现免疫力低下和系统性炎症[6]。这些现象提示新冠肺炎发病过程中存在免疫应答失调,通过对患者免疫状态进行动态评估,有望为新冠肺炎患者诊断、治疗效应监测及预后评估提供辅助信息。然而新冠肺炎免疫应答机制十分复杂,临床用药时机、方法及剂量亟待进一步探究。
该文通过对SARS冠状病毒、MERS冠状病毒以及新近流行的新型冠状病毒进行全面比较,以更好地深入了解宿主-病原体相互作用,希望有助于从这几次冠状病毒引起的传染病爆发中吸取教训,积累经验。通过对新冠肺炎免疫应答机制的深入研究,可为提高临床疗效及开发药物奠定坚实的理论基础。
2 冠状病毒的介绍及分类
冠状病毒(coronaviruses, CoVs)是属于巢病毒目(nidovirales)的一类在自然界中广泛存在的单链RNA病毒。冠状病毒直径约为80~120 nm,基因组全长约为27~32 kb,是目前已知的基因组最大的RNA病毒,可感染人类和多种哺乳动物,引起呼吸道、消化道以及神经系统等多种疾病,其中在人类中主要引起呼吸道的感染[3]。
冠状病毒由刺突糖蛋白(spike protein,S蛋白)、核衣壳蛋白(nucleocapsid protein, N蛋白)、小包膜糖蛋白(envelope protein,E蛋白)、膜糖蛋白(membrane protein, M蛋白)以及核糖核酸组成[7]。S蛋白(180 ku)是一种插入到病毒包膜中的I型膜蛋白,赋予冠状病毒特有的冠状形态,可利用病毒和宿主细胞特异性受体的结合介导病毒的吸附和侵入过程。S蛋白由受体结合亚基S1和膜融合亚基S2组成。在病毒入侵时,S1亚基与宿主细胞表面受体结合使病毒附着于细胞表面,然后S2亚基促使病毒与宿主细胞的膜融合使病毒基因组进入细胞中[8]。N蛋白是核衣壳中唯一的蛋白质,也是病毒感染的细胞中含量最多的蛋白,它由两个与RNA结合的N端结合域和C端结合域组成,负责与病毒基因组结合,识别基因组包装信号将包膜基因组打包成病毒颗粒[9-11]。E蛋白(8~12 ku)是仅含有76~109个氨基酸残基的完整跨膜蛋白,包括一个N端胞外域和一个C端胞内域,主要参与病毒粒子的组装与释放。M蛋白(25~30 ku)是冠状病毒中含量最多的结构蛋白,含有3个跨膜结构域,它与E蛋白相互作用共同介导病毒包膜的组装[12]。在一些β冠状病毒中还存在血凝素糖蛋白(HE蛋白),该蛋白作为血凝素,与细胞表面的唾液酸结合,具有乙酰酯酶活性,促进S蛋白介导的病毒侵入过程和病毒通过粘膜的传播[13]。
冠状病毒具有高度保守的基因组结构,含有5′帽端结构和3′poly(A)尾,基因组中编码非结构蛋白的复制酶基因约占基因组的三分之二,约20 kb;结构基因和辅助基因只占10 kb左右。冠状病毒基因组顺序如下:5′-复制酶(replicase)-S蛋白-E蛋白-M蛋白-N蛋白-3′。冠状病毒整个感染过程包括吸附入侵、基因合成、病毒包装和释放4个步骤[14]。
根据遗传学差异,冠状病毒可分为α、β、γ、δ 四个属,目前已发现七种人类冠状病毒(HCoVs):HCoV-NL63、HCoV-229E、 HCoV-OC43、HCoV-HKU1、SARS-CoV、MERS-CoV以及2019新型冠状病毒(SARS-CoV-2)[3]。
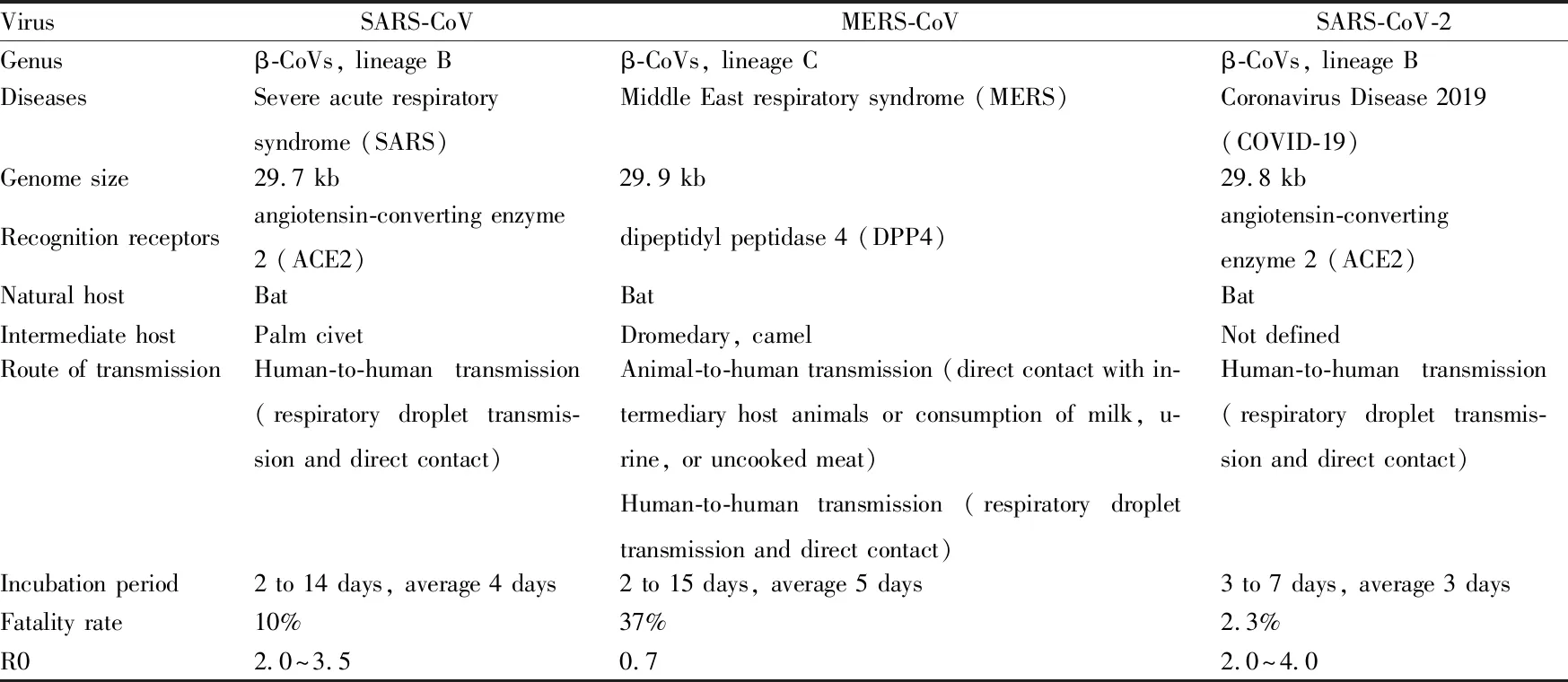
2.1 SARS冠状病毒 (SARS-CoV)2002年11月,始于中国广东省的以非典型性肺炎(非典)为主要临床表现的严重急性呼吸系统综合症(SARS)短时间内迅速在世界范围内传播,共造成全球多个国家8 437例患者感染,超过900例患者死亡[15]。几乎所有感染患者以发热、干咳、呼吸短促等呼吸道症状开始,并在随后几天迅速发展为病毒性肺炎,胸部X射线检查显示肺部炎症浸润。部分患者出现淋巴细胞减少症、白细胞减少症、血小板减少症[16-19]。通过对患者标本中分离出的病毒鉴定,发现造成此次疾病的病原体为一种冠状病毒SARS-CoV[20-22],研究人员在中国马蹄蝠中亦分离到了活性的SARS-CoV,证实蝙蝠是其自然界中的天然宿主[23-24]。SARS-CoV感染人类细胞的受体为一种金属肽酶——血管紧张素转换酶2(ACE2),它可有效地与病毒S蛋白的S1区域结合导致病毒的感染[25]。
2.2 中东呼吸综合征冠状病毒 (MERS-CoV)2012年9月,在沙特阿拉伯地区发现了一种来源于骆驼的高致病性的冠状病毒,引起人类中东呼吸综合征(MERS),这种冠状病毒被命名为MERS-CoV[26-27]。据世界卫生组织的统计数据,MERS-CoV在全球范围内造成2 066例患者感染,至少720例患者死亡,致死率远高于SARS,致病性极强[28]。与SARS感染症状相似,MERS患者首先表现为发热、寒颤和肌肉酸痛,随后急性呼吸衰竭成为主要症状,部分患者伴有消化道症状和肝肾衰竭等并发症[29]。所有患者在胸片上均有轻微到广泛的单侧和双侧异常。实验室分析显示,患者伴有乳酸脱氢酶和天冬氨酸氨基转移酶浓度升高、血小板减少症和淋巴细胞减少症的表现[30]。不同于SARS-CoV和HCoV-NL63结合ACE2,MERS-CoV是以广泛表达于肺泡上皮细胞的二肽基肽酶4(DDP4)作为感染人类细胞的表面受体[31]。这种受体分布的差异可能是引起SARS-CoV感染I型肺泡上皮细胞,而MERS-CoV感染II型肺泡上皮细胞和非纤毛支气管细胞的主要原因[32-33]。
2.3 2019新型冠状病毒 (SARS-CoV-2/2019-nCoV)2019年12月,中国湖北省武汉市爆发了一系列原因不明的与病毒性肺炎症状极为相似的肺炎病例。患者下呼吸道样本深度测序发现这是一种新型冠状病毒感染导致的肺炎,全基因组测序和系统发育分析表明这种新型冠状病毒与SARS-CoV和MERS-CoV不同,被归类为β冠状病毒的2b谱系,世界卫生组织将其命名为2019-nCoV,而后国际病毒分类委员会将其命名为SARS-CoV-2[34]。截止目前全球47个国家共造成82 294例感染,2 804例死亡[35]。当前的证据表明,蝙蝠可能是该病毒的原始宿主,而中间宿主目前尚未有定论[36]。新型冠状病毒感染导致临床最为常见的症状为发热、乏力和干咳,大多数患者出现呼吸困难和肺部双侧磨玻璃浑浊,常见并发症有急性呼吸窘迫综合征(ARDS)、急性心肌损伤、休克和继发性感染,这些症状与SARS-CoV和MERS-CoV感染存在一定相似性,但新型冠状病毒感染患者就诊时发热的比例明显低于SARS-CoV和MERS-CoV感染,且较少的出现上呼吸道和消化道症状[5,37-38]。Tab 1从多个方面对3种冠状病毒进行了比较,可以更加直观地体现3种冠状病毒的异同。
对新型冠状病毒进行结构分析发现,其与SARS冠状病毒的受体结合域具有高度相似性[36]。目前研究已证实新型冠状病毒也利用ACE2受体作为病毒感染和入侵宿主细胞的特异性受体[39-40]。2020年2月16日美国德克萨斯大学奥斯汀分校的研究团队利用冷冻电镜技术,首次解析了新型冠状病毒的S蛋白结构,他们发现新型冠状病毒是利用高度糖基化的同源三聚体S蛋白进入宿主细胞的,且ACE2蛋白与新型冠状病毒S蛋白的亲和力是SARS冠状病毒的10到20倍,这也在一定程度上解释了新冠病毒具备更强传染力的原因[41]。2月20日,西湖大学研究团队利用冷冻电镜在2.9埃全分辨率条件下全球范围内首次成功解析ACE2的完整结构,揭示了人类全长的ACE2受体与新型冠状病毒S蛋白受体结合结构域(RBD)复合体的精细化结构[42]。
Tab 1 Biological characteristics of SARS-CoV, MERS-CoV and SARS-CoV-2
在基因型-组织表达数据库(genotype-tissue expression,GTEx)中,ACE2 mRNA可广泛表达于全身各组织器官(Fig 1),其中在睾丸组织表达最高,其次是小肠末端回肠,而肺、肾脏、心脏等组织ACE2表达量相似,提示其均为新型冠状病毒的易感器官。值得注意的是,ACE2组织表达分布提示睾丸表达量很高,提示病毒很可能作用于该器官,引起病毒性睾丸炎[43],因此治愈出院的新冠肺炎年轻男性患者,更需要定期随访。
3 新冠肺炎的免疫失衡及干预策略
虽然目前临床上大部分新冠肺炎患者症状较轻,但仍存在部分患者早期病情较轻,后期突然加重的现象,最终死于多器官功能衰竭,而加重的原因可能是细胞因子风暴[5,37]。此外,新冠肺炎患者的中性粒细胞异常增多,同时伴随着淋巴细胞计数的显著降低[5,37-38]。这些现象提示新冠肺炎发病过程中存在免疫应答失调,下面将对这些现象进行逐一剖析,以进一步了解新冠肺炎发病的免疫应答机制,为制定相应的干预策略提供依据。
3.1 细胞因子风暴——新冠肺炎患者的“夺命杀手”细胞因子风暴(cytokine storm)一词首次出现在1993年一篇关于移植物抗宿主疾病的文章中[44]。从2000年开始它被广泛使用在多种感染性疾病如乙型溶血性链球菌感染、流感以及SARS中。近年来,细胞因子风暴也成为CART细胞疗法带来的最主要的副作用。那么什么是细胞因子风暴,细胞因子风暴,又称炎症风暴,是指机体在感染微生物或者其他剧烈刺激的情况下,免疫系统被过度激活,导致体液中多种细胞因子迅速大量产生的现象。细胞因子风暴引发的炎症从局部开始通过系统循环扩散到全身,从而导致多种疾病如急性呼吸窘迫综合征(ARDS)、败血症、急性胰腺炎等发生,严重威胁患者生命[45]。
在SARS冠状病毒相关的细胞因子风暴中,重症SARS患者血清中的促炎细胞因子(如IFN-γ, IL-1β, IL-6, IL-12, TGF-β)和趋化因子(如CXCL10,CXCL9, CCL2, IL-8)呈现高表达[46-49],但抗炎因子IL-10则低表达[46]。类似地,在MERS冠状病毒引起的细胞因子风暴中,重症患者血清中的促炎因子(如IFN-γ,TNF-α,IL-15,IL-17)和趋化因子(如CXCL10,CCL5,IL-8)高表达[50-52]。近来爆发的新冠肺炎重症患者血浆中的IL-2, IL-7, IL-10, G-CSF, IP10, MCP-1, MIP-1A和TNF-α显著升高[37]。值得注意的是,抗炎因子IL-10在SARS和新冠肺炎重症患者中的表达趋势完全相反。IL-10会抑制许多促炎细胞因子、趋化因子和趋化因子受体的表达,对细胞因子风暴起到抑制作用。新冠肺炎尤其是重症患者外周血抗炎因子IL-10上升的原因有待进一步研究。
对于新冠肺炎尤其是重症患者的治疗,除了一些抗病毒药物外,基于细胞因子风暴进行干预已成为减轻患者过度炎症反应的有效策略(Fig 2)。IL-6是造成细胞因子风暴的典型促炎因子,IL-6阻断策略已成功用于多种慢性炎症疾病的治疗。根据美国国家癌症研究所提出的CTCAE v4.0制定了与抗体治疗相关的细胞因子风暴的分级系统,在患者出现危及生命的症状,需要呼吸机支持或达到四级器官毒性时,可采用抗IL-6联合糖皮质激素治疗的手段[53]。第一个IL-6抑制剂托珠单抗(Tocilizumab)是一种人源化的抗IL-6受体单克隆抗体,目前广泛用于类风湿关节炎的治疗[54]。通过分析123例新冠肺炎患者外周血和细胞因子分析状况,临床研究人员发现重症患者中CD4 T和CD8 T细胞比例明显降低,而促炎因子IL-6水平明显升高,表明T细胞亚群和细胞因子可作为预测病情由轻到重转变的依据之一[55]。目前以中国科学技术大学附属第一医院牵头的托珠单抗在新型冠状病毒肺炎(COVID-19)中的有效性及安全性的多中心、随机对照临床研究(注册号:ChiCTR2000029765)正在开展中。TNF-α是急性病毒性疾病中十分关键的细胞因子,可通过过度的炎症反应加重冠状病毒的致病性。已有研究报道,使用TNF-α中和抗体或可溶性TNF-α受体融合蛋白治疗可减少流感病毒感染的小鼠肺部细胞因子产生和炎性细胞浸润[56-57]。在小鼠模型中敲除TNF-α受体可明显缓解SARS冠状病毒感染所导致的严重组织损伤[58]。临床报道新冠肺炎重症患者血浆中TNF-α水平显著上升[37],提示在重症患者上使用TNF-α中和抗体亦是阻断细胞因子风暴的有效手段。阿达木单抗为抗人肿瘤坏死因子(TNF)的人源化单克隆抗体。事实上,上海长征医院已在中国临床试验注册中心申请格乐立(阿达木单抗)治疗新型冠状病毒肺炎(COVID-19)重型和危重型患者的安全性和有效性的临床研究(注册号:ChiCTR2000030089 )。
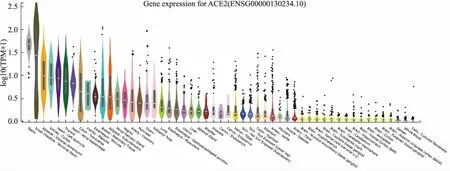
Fig 1 ACE2 mRNA expression distribution in human tissues based on GTEx database
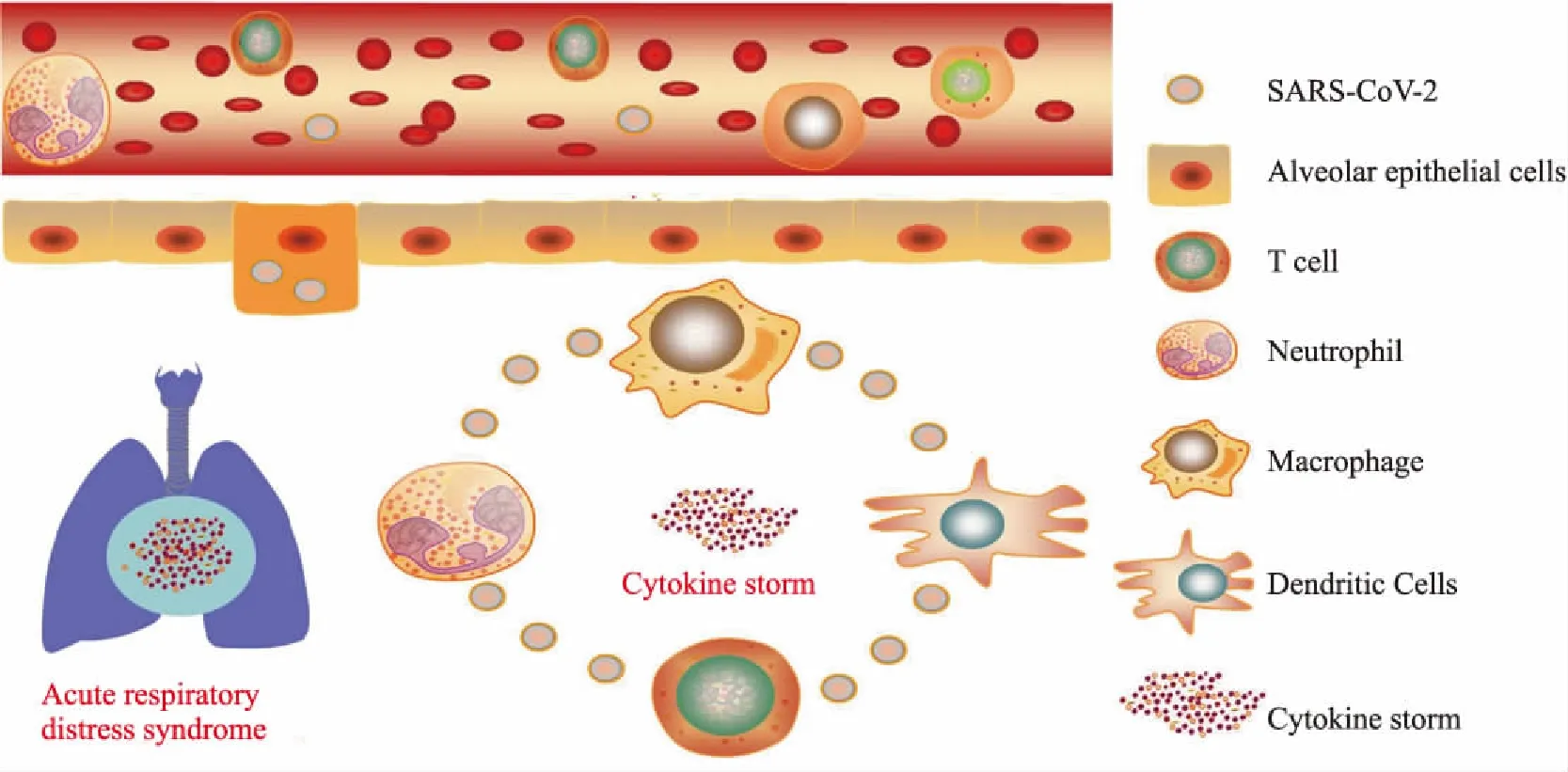
Fig 2 Cytokine storm, also termed cytokine-release syndrome, in SARS-CoV-2-induced acute respiratory distress syndrome (ARDS)
另一方面,钟南山院士团队分析了1 099新冠肺炎病例发现,只有43.1%的患者在入院时出现发热症状,即使是重症患者发热比例也只有47.4%,而在这些重症发热患者中,入院时体温大于38.0 ℃的高热只占26.3%[59]。对比1 425 例SARS患者的临床数据发现,其发热比率高达94%[60],可见新冠肺炎患者就诊时发热的比例明显低于SARS患者。南京市第二医院联合南京大学的研究团队最近发现,相比于22例非新冠病毒感染的肺炎患者,71例普通型新冠肺炎患者T细胞和B细胞更加显著地下降,而单核细胞、中性粒细胞和NK细胞数量却无显著差异[38],而这3种细胞恰恰是细胞因子风暴的主要参与者。华中科技大学同济医学院的研究团队通过对外周血细胞因子动态检测发现,与普通型新冠肺炎患者(27例)相比,重症患者(13例)的多种细胞因子如IL-6、IL-2、TNF-α、IFN-γ以及IL-10仅在某一时间段有显著性上升,而其他时间段两组无明显差异,且这些炎症因子的血清水平相对较低[61],从这13例新冠肺炎重症患者来看,细胞因子风暴的现象并不明显,可能与目前的样本数偏少有关。以上结果提示,对于新冠肺炎患者细胞因子风暴是否为病情进展的主要因素还需要进一步确证。但不可否认,失控的细胞因子风暴会进一步造成炎症弥漫,导致肺泡结构受损,进而机体肺血氧不足,最终进展为急性呼吸窘迫综合征(ARDS),危及患者生命。
3.2 中性粒细胞捕获网——新冠肺炎的免疫干预新靶点中性粒细胞是外周血白细胞中最丰富的细胞类型,是机体先天免疫的重要组成部分,在介导炎症反应和免疫应答方面发挥着十分重要的作用[62]。一方面,中性粒细胞可经过沿血管内壁运动、结合内皮细胞选择素/黏附素、迁移穿过内皮-上皮细胞层等步骤在病毒感染24小时内进入肺泡腔中[63]。在肺泡腔内,中性粒细胞被腔内炎症因子和病原体迅速激活,通过吞噬作用清除病原微生物[64]。另一方面,中性粒细胞可在炎症环境下,释放一种以DNA为骨架内含多种杀菌蛋白的网状结构,即中性粒细胞捕获网(neutrophil extracellular traps, NETs),可有效清除病原微生物,抑制其扩散[65]。
然而,越来越多的研究表明:中性粒细胞及其胞外捕获网既能杀灭入侵的病原微生物,又能加重组织器官的损伤。这主要归因于在清除病毒的过程中,中性粒细胞产生的活性氧、细胞因子、NETs均对上皮-内皮屏障具有破坏作用[66]。有研究表明NETs参与了多种病毒包括流感病毒在内感染导致的肺部炎症进程[67-72]。重症流感患者的血浆中NETs水平明显升高,同时中性粒细胞对IL-8或脂多糖刺激会释放更多的MPO-DNA复合物;另外,H7N9和H1N1感染患者体内NETs可以增加肺泡上皮细胞的通透性[67]。在甲型H1N1流感病毒PR8株侵染的小鼠模型中也观察到过多NETs的形成,进而损伤肺泡毛细血管,引发肺功能障碍[68]。补体C5a介导的NETs会加剧急性肺损伤病人对高致病性病毒的感染。在感染H1N1的小鼠模型中发现阻断C5a会抑制中性粒细胞和巨噬细胞在气道中的浸润,减少NETs的形成以及肺上皮的损伤[69]。临床研究表明[70],急性呼吸窘迫综合征患者支气管肺泡灌洗液内中性粒细胞的浓度和NETs的数量与疾病严重程度呈正相关。值得一提的是,中性粒细胞暴露于急性呼吸窘迫综合征患者支气管肺泡灌洗液后可加速NETs的产生[71],这也许归因于肺泡灌洗液中细胞因子风暴的作用。MERS患者和近来爆发的新冠肺炎患者均表现出中性粒细胞大量增多的现象[61,72]。全国首例新冠肺炎逝者的遗体解剖报告显示,新冠肺炎主要引起深部气道和肺泡损伤为特征的炎性反应,肺部纤维化及实变没有SARS导致的病变严重,但渗出性反应较SARS明显。尸体肺部切面可见大量粘稠的分泌物从肺泡内溢出[73],这或许与NETs在肺部异常聚集有关(Fig 3),但分泌物形成的具体原因仍需研究。
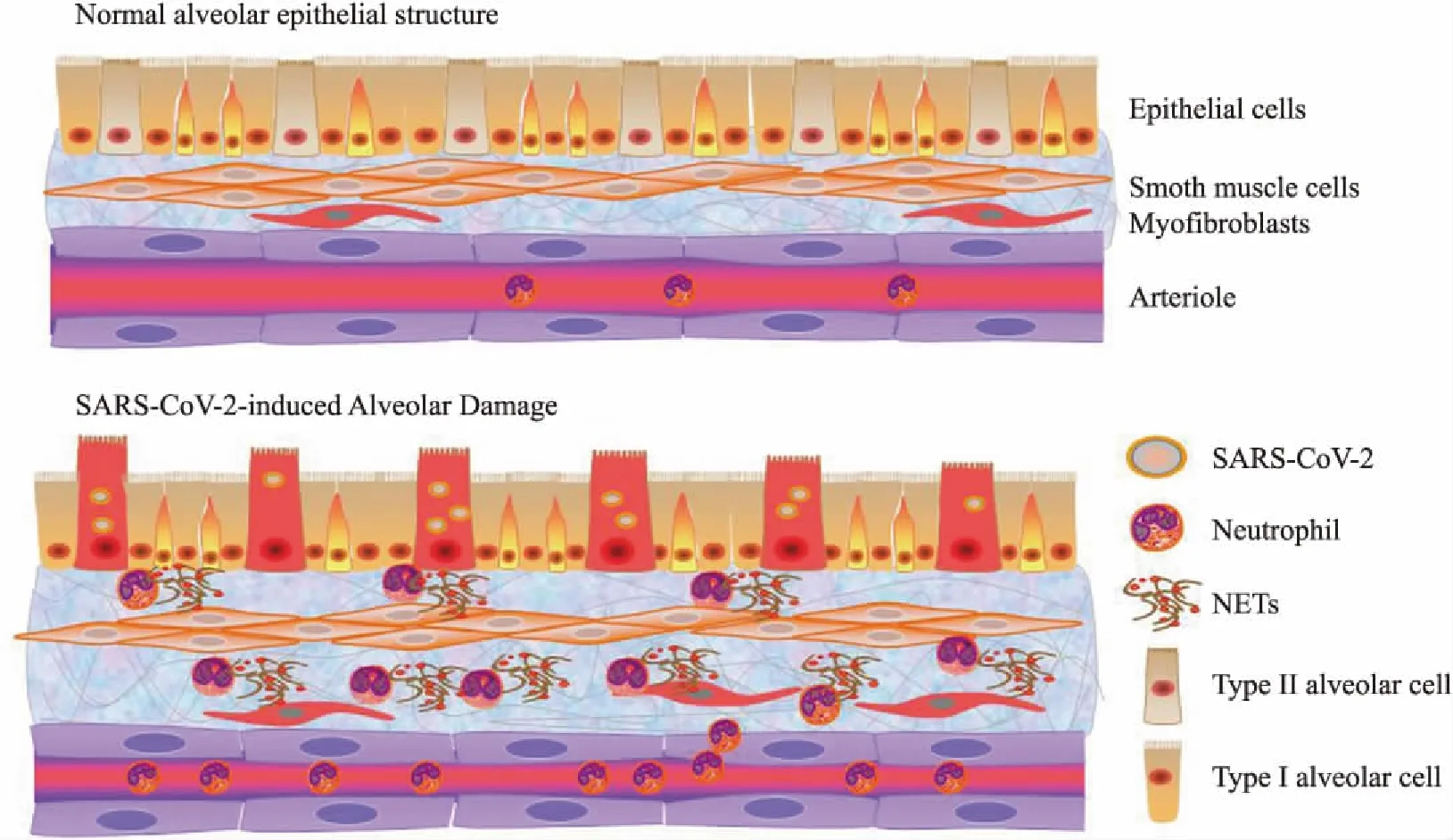
Fig 3 Neutrophil extracellular traps (NETs) is possibly invovled in SARS-CoV-2-induced lung injury
目前,进入临床试验阶段的药物也有与NETs潜在的关联。例如,利用抗IL-6受体的单克隆抗体托珠单抗(Tocilizumab)治疗新冠肺炎的临床试验(注册号:ChiCTR2000029765)已在开展之中,而IL-6是诱导NETs的重要炎症因子。此外,新冠肺炎的治疗方案中推荐了氯喹[74],而已有研究显示自噬抑制剂氯喹能抑制NETs的形成,提高胰腺炎小鼠的生存率[75]。相信随着研究的深入,针对NETs为靶点的治疗策略将为临床病毒性肺炎提供新的选择。
3.3 淋巴细胞亚群失衡——新冠肺炎临床现象带来的思考淋巴细胞(lymphocyte)可分为T淋巴细胞(T细胞)、B淋巴细胞(B细胞)和自然杀伤(NK)细胞,是免疫系统功能调节的主要执行者。在免疫应答过程中,当各淋巴细胞亚群的数量及功能出现异常时,机体可发生一系列的病理改变。因此,淋巴细胞亚群失衡是反映机体免疫应答异常的重要指标[76]。
南京市第二医院联合南京大学的团队近期研究显示,相比于非新冠病毒引起的肺炎(non-COVID-19),新冠肺炎(COVID-19)患者出现明显的T细胞和B细胞计数减少,且数量与器官损伤相关生化指标呈负相关[38]。此外,钟南山院士团队对1 099例新冠肺炎患者临床特征的回顾性研究显示,82.1%的患者出现淋巴细胞减少症状,其中重症患者占95.5%(147/154),显著高于非重症患者[59]。北京地坛医院研究团队报道,中性粒细胞与淋巴细胞比值(neutrophil-to-Lymphocyte Ratio, NLR)可作为新冠肺炎患者发展为重症的独立危险因素[72]。深圳市第三人民医院的研究团队,通过收集新冠肺炎患者支气管肺泡灌洗液中的免疫细胞,利用单细胞TCR免疫组库测序技术,发现与轻症患者相比,重症患者体内可杀伤新冠病毒的细胞毒性T淋巴细胞的克隆数目显著下降[77]。这一系列的数据提示新冠肺炎患者出现明显的淋巴细胞亚群失衡,从而造成免疫功能受损,这种情况在重症患者上更为严重[37]。此外,陆军军医大学的研究团队发现新冠肺炎患者T细胞计数明显减少以及细胞因子的累积,而存活的T细胞也呈现功能耗竭状态。随着患者病情进展,T细胞上PD-1和Tim-3表达增加,提示T细胞逐渐失能[78]。无独有偶,四川大学华西医院已经在中国临床试验注册中心申请PD-1单抗用于治疗新型冠状病毒肺炎(COVID-19)重型或危重型患者的临床对照研究(注册号:ChiCTR2000030028),利用PD-1单抗阻断PD-1/PD-L1通路,恢复T细胞功能改善免疫失衡。此外,减少的T细胞中,CD4及CD8 T细胞下降幅度更为显著,且与病情严重程度正相关[55,61,79]。另一方面,解放军总医院王福生院士团队对一例新冠肺炎死亡患者进行病理检测[80],外周血的流式分析发现CD4及CD8 T细胞数量虽然大幅降低,但T细胞的状态却被显著激活。CD4 T细胞中具有高促炎效应的Th17细胞数量增加,CD8 T细胞则呈现高颗粒酶细胞毒性,这一现象似乎可以解释患者出现的严重免疫损伤。Th17细胞作为T细胞独特的一类分支,其表达失调使患者病情更加错综复杂,同时提示淋巴细胞在新冠肺炎中的重要作用需要进一步探究。总而言之,临床治疗中密切关注T细胞,尤其是CD4及CD8 T细胞数量及功能的变化,或将直接影响后期治疗策略的选择。
针对新冠肺炎患者出现淋巴细胞数量减少的现象,临床上会使用诸如胸腺肽、丙种球蛋白等改善机体低下的免疫功能;而由细胞因子引发的免疫系统正反馈而造成的细胞因子风暴,临床上最常用的药物为糖皮质激素,然而糖皮质激素在抑制细胞因子风暴的同时会引发免疫抑制并延缓冠状病毒的清除,有继发性感染等风险[81]。最近来自Lancet的述评探讨了糖皮质激素治疗新冠肺炎的可行性,文章指出将糖皮质激素用于新冠肺炎的治疗需要符合相应的临床指征[82]。糖皮质激素使用的时机和剂量对于合理有效的免疫调节至关重要,需要更多有价值的研究为疫情诊疗提供证据,并推动相关指南的制定。
综上可知,对于新冠肺炎患者尤其是重症患者,病情的转折可能与淋巴细胞亚群失衡造成的免疫功能紊乱有关。通过结合患者基本临床特征与淋巴细胞的数量、功能以及细胞因子的种类、水平,有望挖掘出新冠肺炎诊断及预后的潜在标志物。
4 总结与展望
新冠肺炎发病是病毒与机体免疫系统“互相博弈”的过程,面对病毒的感染,机体需要启动免疫系统及时识别、清除病毒,但是失调的、过度的免疫反应又会引起患者体内炎症因子过度表达而出现细胞因子风暴。此外,临床上观察到新冠肺炎患者往往出现中性粒细胞的大量累积以及淋巴细胞数量的下降,这些都有望成为新冠肺炎免疫干预的切入环节。目前,多种已上市药物或临床前阶段的候选药物正在积极开展临床试验用于新冠肺炎的防治[83-84]。这其中的一些药物发挥疗效离不开对免疫系统的调节。未来研究人员将进一步深入探索新冠肺炎发病过程中的免疫应答机制,阐明相关的靶点及信号通路,以推动治疗药物和疫苗的研发,为临床上新冠肺炎的诊疗及预后提供可靠的科学依据。