不同方法对羊水细胞培养成功率的影响
2020-04-25胡惠彬
胡惠彬
羊水细胞培养为胎儿染色体核型检查的重要手段,适用人群包括高龄妊娠(35岁以上)、唐氏筛查高风险、夫妻一方为染色体异常携带者、产前B超检查怀疑胎儿染色体异常、近亲结婚和有异常胎儿生育史、反复流产史、先天疾患家属史(血友病、白血病)的孕妇,一般于妊娠的16~22周开展此项操作[1]。然而,该检查属于损伤性取样技术,对孕妇及胎儿均会带来一定的潜在风险,甚至引发流产,并且对操作人员技术要求高、影响因素多,培养失败后难以再次进行,所以降低羊水细胞培养的失败率成为当务之急。本研究对羊水细胞培养的成功率和染色体分裂相的质量予以分析,现报告如下。
1 资料与方法
1.1 研究对象 选择2019年1 —10月在本院进行胎儿染色体核型检查的404例孕妇作为研究对象,年龄18~46岁,平均(34.44±1.06)岁;孕周16~24周,平均(20.20±0.25)周。
1.1.1 纳入标准 ① 体温正常,无发热者;② 检查前无胎盘早期剥离、腹部感染化脓者。
1.1.2 排除标准 ① 妊娠时间<16周或>24周者;② 具有先兆流产征象者。
1.1.3 伦理学 本研究符合医学伦理学标准,经本单位伦理审批(审批号:永伦评〔2019〕8号),所有对患者的检测均获得过患者或家属的知情同意。
1.2 检查方法
1.2.1 样本采集 嘱所有孕妇排空膀胱之后取仰卧位,使用碘伏对其腹部皮肤组织进行消毒,消毒范围以穿刺点为中心,消毒半径≥15 cm。常规消毒铺巾后,以7号无菌腰穿针沿垂直方向刺入腹部,进入羊膜腔后若突然感到抵抗组织消失,形成落空感后停止刺入,拔出针芯并利用注射器抽取30 mL羊水,分别置于2支离心试管中。
1.2.2 细胞培养 将采集的细胞样本以1 500 r/min(离心半径为9 cm)离心10 min,弃除上清液之后,采集1 mL羊水和沉淀细胞,加入5 mL pH 5.0~6.8的羊水培养基(广州白云山试剂公司提供),轻轻吹打以促使二者充分混匀并形成细胞悬液,转移至25 mL无菌培养瓶,于37 ℃温箱中培养7~10 d,发现有大量成纤维样或上皮样细胞生长后更换培养液,1支试管采用原代培养法,另1支采用传代培养法[2]。原代培养试管适时收获,而传代培养试管经过吹打促使沉淀细胞与培养液充分混匀后再次置于温箱中培养72 h,待羊水细胞克隆后收获。
1.2.3 细胞收获及染色观察 收获时采用秋水仙碱处理并利用1:1的柠檬酸钠与氯化钾进行低渗处理,5 min后加入固定液,预固定1 min,以1 500 r/min(离心半径为9 cm)离心10 min,去除上清液并固定0.5 h后原转速离心,重复2次后进行滴片烤片处理[3]。将滴片置于电热干燥箱中烘烤3 h,温度设定为75 ℃。取出后利用胰酶消化1.5 min左右,进行吉姆萨染色,持续10 min后阅片核对,通过细胞计数分析,若制作羊水细胞标本玻片中的染色体可供分析的核型数量能够达到国家细胞遗传学产前诊断技术标准所要求的分析数量,即达到100个可计数核型以上,可确定为羊水细胞培养成功[4]。
1.3 观察指标 选取羊水细胞培养的成功率、失败率、羊水染色体分裂相质量作为观察指标。
1.4 统计学方法 采用SPSS 17.0软件处理数据,计量资料以均数±标准差表示,组间比较采用t检验,计数资料以例(率)表示,组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 两种羊水细胞培养法成功率和失败率比较 采用传代培养法的羊水细胞培养成功率明显高于原代培养法,而失败率明显低于后者,差异均有统计学意义(均P<0.05)。见表1。

表1 两种羊水细胞培养法成功率和失败率比较
2.2 两种羊水细胞培养法所得羊水染色体分裂相比较 采用传代培养法获得的羊水染色体分裂相出现数、可计数、可分析数均明显高于原代培养法,差异均有统计学意义(均P<0.05)。见表2。
表2 两种羊水细胞培养法羊水染色体分裂相比较(
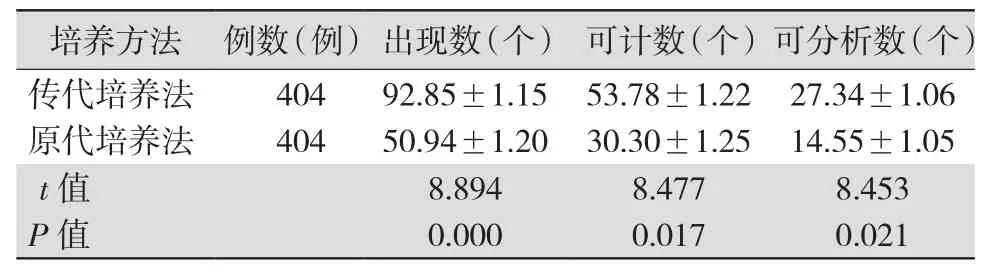
表2 两种羊水细胞培养法羊水染色体分裂相比较(
培养方法 例数(例)出现数(个) 可计数(个)可分析数(个)传代培养法 404 92.85±1.15 53.78±1.22 27.34±1.06原代培养法 404 50.94±1.20 30.30±1.25 14.55±1.05 t值 8.894 8.477 8.453 P值 0.000 0.017 0.021
3 讨论
受有害化学物质、X线照射、环境、高龄妊娠等因素的影响,妊娠时染色体变异所引发的疾病(如唐氏综合征、爱德华氏综合征、帕陶综合征、先天性睾丸发育不全综合征、克氏综合征、特纳综合征、超雌综合征和超雄综合征等)发病率随之提高[5]。而染色体变异会给胎儿发育带来严重影响,所以产前诊断并及时予以干预尤为重要。羊水细胞培养是检查染色体异常最有效的手段,也是产前诊断的重要组成部分。由于羊水细胞为胎儿发育过程中衰老及固缩的脱落细胞,相较于其他细胞而言培养难度更高,使得羊水细胞培养失败率高,一旦失败难以进行二次检查,所以提高羊水细胞培养成功率成为困扰临床的一个棘手问题。
目前羊水细胞培养多采用原代培养法,尽管其操作简便、操作所致的污染也能得到有效控制,但受限于羊水细胞生长状况的影响,往往需要数个批次收获才能够完成检查,且失败率相对较高,逐渐无法满足此项检查的需求。传代培养法则是在原有羊水细胞培养基础上作出的改良,通过细胞传代来获得更多的分裂相,便于观察和计数,能达到细胞遗传学产前诊断技术标准要求的必须计数2个以上独立培养的培养甁中平均分布的20个细胞数,分析5个细胞的量,而且还能达到出现嵌合体时需要计数细胞的高强度额外工作的数量,对于提高羊水细胞培养成功率而言具有重要意义。
本研究采用传代培养法的羊水细胞培养成功率为100.00%,明显高于原代培养法的96.04%,而失败率为0,明显低于后者的3.96%,差异均有统计学意义。在获得的羊水染色体分裂相比较中传代培养法无论是出现数、可计数还是可分析数均高于原代培养法,差异均有统计学意义,此结果提示,在羊水细胞培养中传代培养法可提高成功率以及羊水染色体分裂相检测效果,降低失败率。此外,本研究亦对失败的羊水细胞培养标本进行了分析并总结经验如下:染色体分裂相数量直接决定了羊水细胞培养的成功与失败。传代培养法通过更换培养液以促使羊水细胞重新贴壁并更有利于生长,大幅提高了分裂相的数量及质量,而原代培养法虽然省去了传代步骤,但因各种原因导致细胞贴壁生长数少,如:① 正常抽取羊水的时间为孕周16~22周,孕周太少或太大都会引起培养贴壁细胞少;② 高龄妊娠导致培养细胞少,可能跟自身抗体对外界感染产生变应原增多有关;③ 血性羊水也会影响细胞贴壁生长等。这些因素都会导致收获细胞数过少,不利于核型分析,又因原代培养羊水细胞成熟时间存在不同程度的滞后性,使得其活性存在明显差异,影响了分裂相数量,从而增加了羊水细胞培养的失败率[6]。
综上所述,采用传代培养法的羊水细胞培养成功率更高,且能收获到更多可供分析的羊水染色体核型,值得在临床检验工作中推广使用。
利益冲突 作者声明不存在利益冲突
