紫草炭制前后萘醌类化合物含量变化及止血作用研究*
2020-04-19陈永福白文明苏日娜
牧 丹,陈永福,布 仁,白文明,苏日娜*
(1. 内蒙古医科大学 呼和浩特 010010;2. 内蒙古农业大学 呼和浩特 010010)
紫草为常用药材,最早见于《神农本草经》,历代本草均有收载。2015版中国人民共和国药典[1]收载了紫草科植物新疆紫草Arnebia euchroma(Royle)Johnst.和内蒙紫草Arnebia guttata Bunge 的干燥根。有着清热凉血,活血解毒,透疹消斑的功能,用于血热毒盛,斑疹紫黑,麻疹不透,疮疡,湿疹,水火烫伤的治疗。
从报道中已知紫草中含有紫草萘醌类、生物碱类、单帖苯醌类及苯酚类、黄酮类、酚酸类等脂溶性化学成分及紫草多糖等水溶性化学成分。从新疆紫草根中分离获得30 余种萘醌类化合物,其母核多为5,8-二羟基萘醌,具有异己烯边链。因其旋光性差异而将此萘醌类化合物分为2 种光学异构体:R-型(命名为紫草素类,shikon)和S-型( 命名为阿卡宁类,alkannin)[2]。针对紫草中萘醌类化合物的含量研究有一些报道:郝鹤等[3]采用梯度洗脱HPLC 法测定了新疆紫草中的 7 种萘醌类成分;Min Cheng 等[4,5]采用 HPLC 法测定了新疆紫草和内蒙紫草中的左旋紫草素和β,β′- 二甲基丙烯酰阿卡宁的含量;昝珂等[6,7]采用HPLC 法测定了新疆紫草的特征图谱和紫草类药材中六种萘醌成分的含量。
在中医临床应用中紫草主要以油、膏的形式入药,紫草油、膏常用于治疗轻度水火烫伤,但其作用绝不仅限于此[8]。而主要药效成分紫草素可直接抑制人角质形成细胞增殖,诱导凋亡。谢欣然等通过实验证实,紫草素主要通过IL-17 细胞因子对角质形成细胞进行调控,同时还可抑制角质形成细胞内趋化因子缓解炎性反应,治疗银屑病[9,10]。由于紫草良好的抗炎和免疫调节作用[11],也经常用于各类湿疹、皮炎的治疗[12-14]。
传统的蒙药中,紫草用于治疗肺热、咳嗽、肺脓肿以及各种出血症状[15],蒙医理论[16]上,除了原药材直接入药外,还经常以炮制品入药。蒙药的炮制学认为,紫草经炒制后的炭制品更有利于各种出血症的治疗,而牛奶炮制后入药其治疗肺热的疗效加强。在前期研究中我们主要其奶炮制的工艺及萘醌类成分的变化采用HPLC 方法进行了定量的分析[17],并对其药理作用进行了一定的研究。但是蒙医的紫草的传统炭制方法的研究仅限于古籍记载,对其炭制工艺及药理作用及机制的研究仍是空白。
本研究以传统蒙药炮制理论为基础,将紫草原药材经炭制后,确定其最佳炭制工艺,测定萘醌类化合物的含量,计算炭制前后的变化,为紫草炭制品的质量标准及今后药理实验提供一定的理论指导和实验基础。
1 材料
1.1 仪器
KH5200DE 型数控超声波清洗器(昆山禾创超声仪器有限公司);万用电炉(北京科伟永兴仪器有限公司);GM1651 高温系列红外测温仪(深圳市聚茂源科技有限公司);HHS-4S 电子恒温不锈钢水浴锅(上海宜昌仪器纱筛厂);电鼓风干燥箱(上海一恒科学仪器有限公司);JA5003N 电子天平(上海菁海仪器有限公司);AL204 电子天平(梅特勒-托利多仪器(上海)有限公司);TU-1901 双光束紫外可见分光光度计(北京普析通用仪器有限责任公司);Thermo U3000 高效液相色谱仪(赛默飞世尔科技有限公司)。
1.2 试药
试剂:石油醚(60~90℃)(分析纯)、无水乙醇(分析纯)、乙腈(色谱纯)、甲酸(色谱纯)、超纯水
对照品:β,β′-二甲基丙烯酰阿卡宁(中国食品药品检定研究院,批号111689-201504)
动物:小鼠,内蒙古医科大学动物中心提供。
药材:全部批次的药材经内蒙古医科大学渠弼教授鉴定为紫草科植物新疆紫草(Arnebiaeuchroma(Royle)Johnst.)的干燥根。药材来源见下表1。

表1 药材来源
2 方法与结果
2.1 紫草炭制工艺流程
称取新疆紫草约30 g,加热电炉和铁锅,使用红外测温仪测温度,待锅底达到指定温度,放入紫草,在指定温度5 个炭制温度(200-300 ℃、350-450 ℃、400-450 ℃、450-500 ℃、500-600 ℃)下均匀翻炒一定时间(5 min、10 min、15 min、20 min),记录温度、时间、紫草颜色及形状变化见表2,放凉后,放入自封袋,备用。
2.2 紫草炭制前后颜色及形状变化比较
2.1 将批号为160301的药材经不同温度下炭制不同时间后,颜色及形状的变化如下图1。
经5个批次的药材不同温度和时间炭制后比较发现,350-400 ℃15 min 的炭制工艺,使药材外部炭化、内部保留固有性能(存性),因此将此条件定为紫草最佳炭制工艺。
3 含量测定
3.1 羟基萘醌总色素含量测定
取本品适量,在50 °C 干燥3 h,粉碎(过40 目筛),取约0.5 g,精密称定,置100 mL 量瓶中,加无水乙醇至刻度,4h 内时时振摇,滤过。精密量取续滤液5 mL,置25 mL 量瓶中,加乙醇至刻度,摇匀。照紫外-可见分光光度法(通则0401),在516 nm 波长处测定吸光度,按左旋紫草素(C16H16O5)的吸收系数(E)为242 计算,即得。本品含羟基萘醌总色素以左旋紫草素(C16H16O5)计。

表2 160301批次不同炭制工艺紫草颜色变化

图1 不同炮制温度和时间下紫草药材的变化A:紫草原药材B:200-300℃20min C:350-400℃15min D:400-450℃10min E:450-500℃10min F:500-600℃5min
经炭制后的紫草与紫草原药材相比较,羟基萘醌总色素含量不同程度的降低。炮制工艺101B(200-300 ℃20 min)和 101C(350-400 ℃15 min)时,药材中羟基萘醌总色素含量分别为3.464%、2.754%,比原药材降低了20.50%和33.28%结果见表3。而当炮制温度达到400 ℃以上的情况下,药材中羟基萘醌总色素含量减低到70%以上,500-600 ℃左右基本检测不到其成分。其他批次的紫草炭制品的情况基本相同,数据未列出。从以上测定发现,炮制温度对紫草药材中羟基萘醌总色素含量影响较大,高温的炮制导致其成分的挥发,导致含量的降低。紫草炭制品中羟基萘醌总色素含量结果与我们的最佳炮制工艺的预期结果符合。

表3 160301批次药材不同炭制工艺下羟基萘醌总色素含量
3.2 β,β′-二甲基丙烯酰阿卡宁含量测定
3.2.1 色谱条件
色谱柱:SinoChrom ODS-BP(4.6 mm×250 mm,5 μm),流动相:乙腈-0.15%甲酸水溶液(70:30),流速:1 mL·min-1,检测波长:275 nm,柱温:30 ℃。
0.15%甲酸溶液的配置:精密移取色谱级甲酸溶液1.50 mL,转移至1000 mL 的容量瓶中,加水(超纯水)稀释到刻度,摇匀,即得。
3.2.2 溶液制备
3.2.2.1 供试品溶液制备:取紫草粉末(过40 目筛)0.5g,精密称定,置具塞锥形瓶中,精密加入石油醚(60-90 ℃)25 mL,称定重量,超声处理(温度30 ℃ 功率250 W 频率33 kHz)30 min,放冷,再称定重量,用石油醚(60-90 ℃)补足减失重量,摇匀,滤过。精密量取续滤液10 mL 于试管中,蒸干,残渣加约5 mL 流动相溶解,超声处理(温度30 ℃功率250 W 频率33 kHz)10 min,转移至10 mL 容量瓶中,加流动相至刻度,摇匀,滤过,取续滤液,即得。
3.2.2.2 标准品溶液制备:取β,β′-二甲基丙烯酰阿卡宁2.01 mg,精密称定,置于10 mL 容量瓶中,加乙腈定容至刻度,摇匀,即得浓度为201.00 μg·mL-1的标准溶液。
3.2.2.3 标准品溶液的稀释:精密量取上述201.00 μg·mL-1标准溶液 1 mL,置于 25 mL 容量瓶,加乙腈定容至刻度,摇匀,即得浓度为8.04 μg·mL-1的标准溶液。
3.2.3 专属性考察
图2、图3、图4 为对照品、紫草原药材及炭制紫草的HPLC 色谱图,结果表明丙烯酰阿卡宁保留时间一致,分离度良好,HPLC测定方法专属性良好。
3.2.4 线性关系考察
精密量取按“3.2.2.2、3.2.2.3 标准品溶液制备”项下制备的标准品溶液,
用乙腈稀释配制成浓度为301.5 μg·mL-1、201 μg·mL-1、120.6 μg·mL-1、80.4 μg·mL-1、40.2 μg·mL-1、4.02 μg·mL-1的一系列标准品溶液。滤头过滤,按上述色谱条件测定,记录色谱图以峰面积积分值(Y)为纵坐标,标准品溶液浓度(X)为横坐标,进行线性回归,得线性方程为Y = 0.1742X - 0.5616(R² = 0.9996),线性范围4.02-301.50 μg·mL-1。

图2 HPLC图谱A:β,β′-二甲基丙烯酰阿卡宁B:紫草原药材

图3 同一批次药材不同炭制工艺下各组分峰面积比较
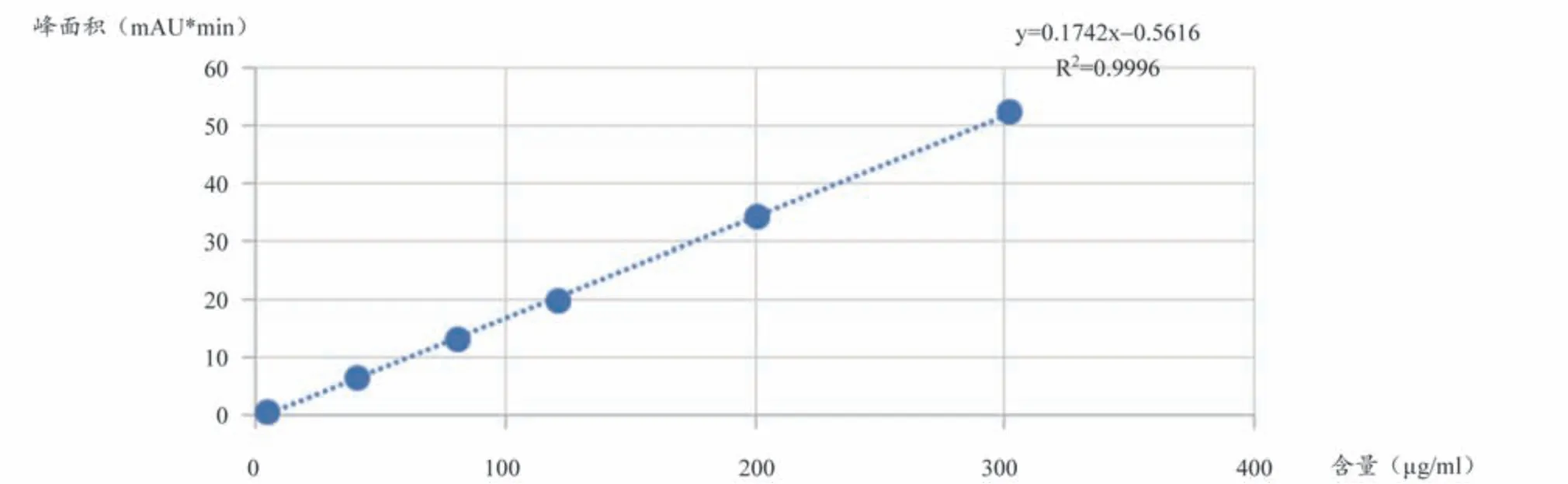
图4 β,β′-二甲基丙烯酰阿卡宁标准曲线
3.2.5 方法学考察
3.2.5.1 重复性试验 取同一批紫草炭制样品粉末(批号:160101,炭制工艺:350-400 ℃ 15 min)6 份,按“3.2.2.1 供试品溶液制备”方法平行制备供试品溶液,自动进样10.00 μL,按“3.2.1色谱条件”项下条件测定,记录色谱图,计算含量,结果如表4。
结果RSD为2.04%,表明仪器重现性良好。
3.2.5.2 精密度试验 精密吸取同一紫草供试品溶液(批号:160101,炭制工艺:350-400 ℃ 15 min)10.00 μL,按“3.2.1 色谱条件”项下条件重复测定6 次,记录色谱图,结果见表5。
计算其RSD 值为0.52%,结果表明该方法的精密度良好,符合要求。
3.2.5.3 稳定性试验 精密吸取同一紫草供试品溶液(批号:160101,炭制工艺:350-400 ℃ 15 min)10.00 μL,分别于 0、1、2、4、8、10 h 后注入色谱仪,按“3.2.1 色谱条件”项下条件测定,记录色谱图,记录峰面积,计算平均值,结果见表6。
计算其RSD 值为0.53%,结果表明供试品溶液在10 h内基本稳定。
3.2.5.4 加样回收率试验 取已知含量的炭制紫草粉末(批号:160101,炭制工艺:350-400 ℃ 15 min)约0.25g,共6份,精密称定,置50 mL具塞锥形瓶中,加入一定量的对照品,使供试品中待测定组份含有量与对照品的加入量比在1:0.5,1:1,1:1.5 左右,按“3.2.2.1供试品溶液制备”平行制备供试品溶液,自动进样10.00 μL,分别进行测定,记录色谱图,计算含量,结果下表7。

表4 重复性试验

表5 精密度试验

表6 稳定性试验
结果回收率为100.5%-104.2%,平均值为102.5%,RSD为1.37%,表明此法回收率良好。
3.2.6 样品含量测定
取各批次炭制紫草,按“3.2.2.1 供试品溶液制备”平行制备供试品溶液,自动进样10.00 μL,按“3.2.1 色谱条件”项下条件测定,记录色谱图,计算含量,批号为160101、907样品含量测定结果如下表8。
由于产地、药材形状差异,5 个不同批次产地紫草原药材中β,β′-二甲基丙烯酰阿卡宁含量有较大差异。表1 中列出两个原药材中β,β′-二甲基丙烯酰阿卡宁含量差别比较大的批次的炮制品的含量变化,发现含量降低百分比基本相同。最佳炭制工艺(350-400 ℃15 min)时,各批次炭制紫草中β,β′-二甲基丙烯酰阿卡宁含量均有降低趋势,但与原药材相比,降低率不同,故炭制工艺的稳定性有待提高。
4 不同紫草炭制品的萘醌类成分变化研究
我们通过HPLC-MS 分析及文献[18,19]对比研究,从紫草原药材和炮制品中共鉴定出7 个萘醌类成分,分别为β-羟基异戊酰紫草素、乙酰紫草素、β-乙酰氧基-异戊酰紫草素、丁酰紫草素、β,β′-二甲基丙烯酰阿卡宁、异戊酰紫草素,其中保留时间8.2min 出峰的组分为未知组分。通过色谱图的峰面积初步比较了各组分的含量变化。各组分的含量随着炮制温度的增加,都有所减少。
5 止血作用研究
5.1 小鼠全血凝血时间(CT)的测定(毛细管法)
小鼠 60 只,随机分组,每组 10 只,雌雄各半,ig 给予25 mg·kg-1(干药材量/动物体重,下同)的生理盐水空白对照组、160101A(紫草原药材)、160101C(350-400 ℃15 min)、160101E(450-500 ℃10 min)的混悬液,以及0.5 mg·kg-1的云南白药混悬液作为阳性对照组,连续给药3 天,末次给药1 h 时每鼠眼后静脉丛取血,以毛细管法测定凝血时间[20]。结果见表9,发现云南白药阳性对照组及给药三组均与与空白对照组比较具有显著差异(P<0.01),延长全血凝血时间效果明显,且160101C炮制组的凝血时间最短,但是给药组之间均没有太明显的差异。
5.2 小鼠出血时间的测定
取小鼠60 只,雌雄各半, 随机分成6 组,分别灌胃各制品溶液、云南白药和生理盐水,给药体积为20 mL·kg-1,每天 1 次,连续灌胃 5 天,末次给药 1 h 后用解剖剪距小鼠尾尖3 mm 处横向剪断,待血液自行溢出计时,每30 s 用滤纸吸血1 次,直至血液自然停止,所需的时间即为出血时间[20]。结果见表9,发现云南白药阳性对照组及给药三组均与与空白对照组比较具有显著差异(P<0.01),延长全血凝血时间效果为明显,且160101C 炮制组的凝血时间最短,但是给药组之间均没有太明显的差异。

表7 加样回收率试验

表8 样品含量测定
表9 紫草原药材及炭制品的小鼠凝血时间和出血时间的测定()

表9 紫草原药材及炭制品的小鼠凝血时间和出血时间的测定()
注:*P<0.05,**P<0.01,***P<0.001 于空白对照组比较
?
6 结果与讨论
本实验通过不同温度和时间,对5 个批次的新疆紫草进行炭制,发现350-400 ℃15 min 的炭制工艺,使药材外部炭化、内部保留固有性能(存性),因此将此条件定为紫草最佳炭制工艺。通过与原药材和不同炭制品中羟基萘醌总色素和β,β′-二甲基丙烯酰阿卡宁含量测定发现,炮制品中的含量随着炮制温度的提高逐渐下降,当温度达到500-600 ℃高温时,萘醌类成分的含量均减低到90%以上。小鼠凝血实验表明,炭制后的药材均有一定的止血作用,且160101C 炮制组的凝血时间和出血时间最短,但是紫草原药材和炭制品之间没有出现显著性差异。本研究为紫草炭制品的利用和开发提供了一定的实验数据和理论基础。
