阿帕替尼治疗耐铂型卵巢癌短期疗效与安全性观察
2020-04-17史惠蓉
张 锦,史惠蓉
卵巢恶性肿瘤是女性生殖器最常见的三大恶性肿瘤之一,由于卵巢癌位于盆腔深部,早期病变不易被发现,大部分发现时已为晚期,因此卵巢恶性肿瘤致死率居妇科恶性肿瘤首位,严重威胁妇女生命和健康[1]。目前上皮性卵巢癌的标准治疗方案为手术联合铂类化疗,虽然患者取得了明显的生存获益,但仍有70%以上的患者会复发,影响患者生存率。复发有多种形式,最常见的是影像学检查发现肿块和实验室检查发现肿瘤标志物的改变等,约70%的卵巢癌患者肿瘤标志物在复发的临床证据出现前4~6个月即有升高[2]。这些患者一旦复发预后极差,尤其是耐铂型卵巢癌,因此亟须探索出更有效地治疗方法使患者获益。
阿帕替尼是新一代小分子血管内皮生长因子受体2(VEGFR-2)酪氨酸激酶抑制剂,可竞争性拮抗ABC转运蛋白上的三磷酸腺苷(ATP)催化位点,抑制ABC转运蛋白的外排作用,增加肿瘤细胞内抗瘤药物活性成分,逆转肿瘤细胞的多重耐药[3]。本研究旨在探索阿帕替尼治疗耐铂型复发性卵巢癌的短期疗效及安全性。
1 资料与方法
1.1 临床资料收集2015年7月—2019年1月在郑州大学第一附属医院(我院)治疗的耐铂型复发性卵巢癌患者。纳入标准:①年龄18~70岁,完成满意肿瘤细胞减灭术及铂类药物化疗后无瘤生存时间<6个月或经铂类药物化疗未达完全缓解者;②组织病理学为原发性上皮性卵巢癌,手术病理分期为Ⅲ~Ⅳ期;③腹部计算机断层扫描(CT)提示至少有1个≥10 mm的可测量病灶;④肝肾功能正常,骨髓造血功能正常,心功能Ⅰ~Ⅱ级。排除标准:①铂敏感复发患者,完成铂类药物化疗后,无瘤生存时间>6个月;②组织病理学为非上皮性卵巢癌或手术病理分期为Ⅰ~Ⅱ期的原发性上皮性卵巢癌;③6个月内使用过抗血管生成药物治疗;④有严重肝肾功能损害、严重心脏疾病、骨髓造血功能异常。本研究经我院伦理委员会批准。患者均被告知研究的相关利弊及风险,并签署知情同意书。
1.2 治疗方案及治疗后的评估共46例患者纳入本研究,根据治疗方案分为2组:单纯化疗组(n=25),即吉西他滨+奥沙利铂,其中吉西他滨按照1 000 mg/m2的剂量于第1日、第8日静脉滴注,奥沙利铂按照130 mg/m2的剂量于第2日静脉滴注,28 d为1个疗程,化疗2~6个疗程。阿帕替尼联合化疗组(n=21),即阿帕替尼(500 mg,1次/d,口服)+吉西他滨+奥沙利铂,其中吉西他滨和奥沙利铂的使用方法同单纯化疗组。评价指标[依据实体瘤疗效评价标准(RECIST)及CA125水平]:治疗后肿块消失,肿瘤标志物CA125降至正常,则为完全缓解(CR);肿瘤标志物CA125降低明显(>50%),基线病灶长径之和缩小≥30%,则为部分缓解(PR);基线病灶长径之和缩小<30%,肿瘤标志物CA125降低>25%,则为稳定(SD);基线病灶长径之和较前增长或出现新病灶,肿瘤标志物CA125升高,则为进展(PD)。客观缓解率(ORR)=(CR+PR)/例数×100%,疾病控制率(DCR)=(CR+PR+SD)/例数×100%。
1.3 统计学方法采用SPSS 22.0软件对数据进行统计分析。符合正态分布的定量资料用均数±标准差(±s)表示,组间比较采用t检验;定性资料用例数(百分比)表示,组间比较采用卡方检验或Fisher确切概率法;等级资料用例数(百分比)表示,组间比较采用秩和检验。P<0.05为差异具有统计学意义。
2 结果
2.1 2组患者临床特征和疗效比较2组患者年龄、病理类型、国际妇产科联盟(FIGO)分期、肿块复发大小、肿瘤分级、转移部位数目和治疗前血清CA125水平比较,差异均无统计学意义(P>0.05)。阿帕替尼联合化疗组的ORR(52.4%vs.24.0%)及DCR(61.9%vs.32.0%)均优于单纯化疗组,差异有统计学意义(P<0.05)。见表1。
2.2 治疗后肿瘤标志物CA125水平比较在疗效达到CR和PR的患者中,单纯化疗组(CR 0例,PR 6例)及阿帕替尼联合化疗组(CR 0例,PR 11例)的CA125 水平分别为 (72.37±23.33)U/mL、(49.59±18.61)U/mL,差异有统计学意义(t=2.210,P=0.043)。
2.3 2组患者不良反应比较化疗结束后,阿帕替尼联合化疗组手足皮肤反应、高血压的发生率高于单纯化疗组,差异有统计学意义(P<0.05);2组患者消化道反应、白细胞减少、血小板减少、贫血、蛋白尿和肝功能损害的发生率比较,差异均无统计学意义(P>0.05)。患者的不良反应行对症支持治疗及药物减量等处理后均缓解。见表2。
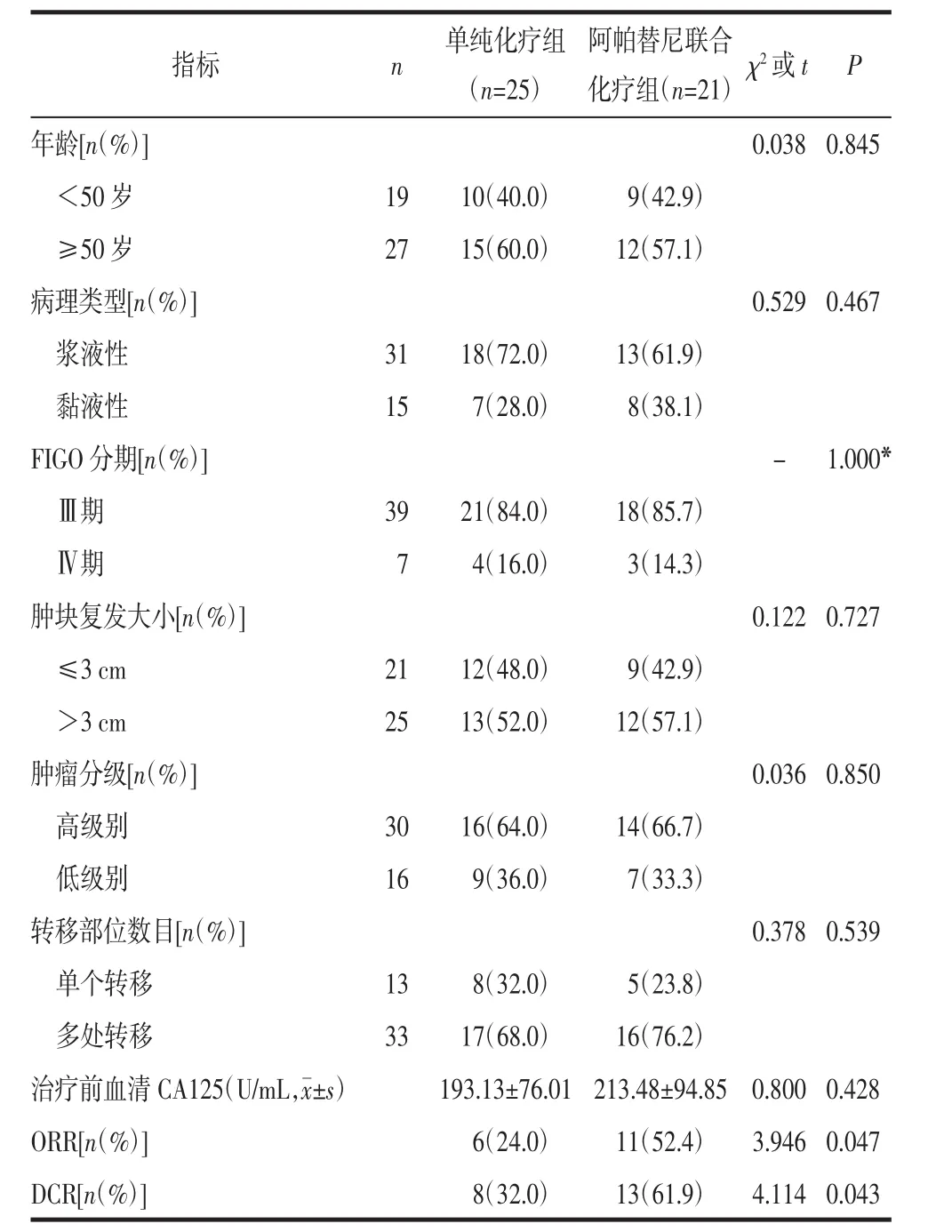
表1 2组患者临床特征和疗效比较
3 讨论
卵巢癌经治疗后约有70%复发,一旦复发,预后极差,特别是耐铂型卵巢癌,目前尚无成熟的化疗方案,一般选用二线药物治疗,如吉西他滨、脂质体阿霉素、依托泊苷、拓扑替康等。近年分子靶向药物在癌症治疗中的重要性日益显著,根据作用靶点及作用机制不同大致可分为抗血管生成抑制剂、表皮生长因子受体抑制剂、二磷酸腺苷核多糖抑制剂及其他。研究表明,VEGFR-2是血管形成的关键介导因子。其中阿帕替尼在抗VEGFR-2的特异性中较其他抗血管生成药物具有较高的精准性。有研究表明,抗VEGFR-2治疗不仅仅靶向血管,同时还作用于免疫逃逸的肿瘤细胞[4-7]。其在胃癌、乳腺癌等多种实体瘤中展现了令人满意的抗癌效果[8]。而阿帕替尼在卵巢癌中的研究较少,所以本研究旨在探讨阿帕替尼在耐铂型复发性卵巢癌中的治疗效果。
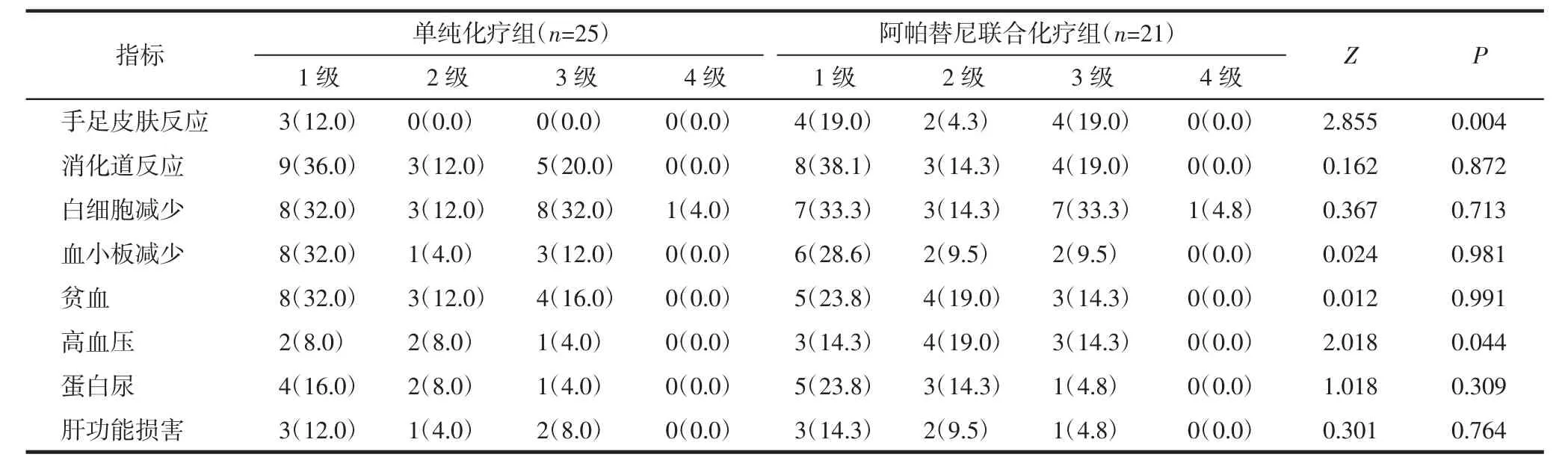
表2 2组患者不良反应比较 [n(%)]
本研究比较单纯化疗组(吉西他滨+奥沙利铂)与阿帕替尼联合化疗组之间的疗效,因奥沙利铂为第三代铂类衍生物,与顺铂及卡铂交叉耐药较少[9],且国外多篇文献显示吉西他滨联合奥沙利铂治疗耐铂型卵巢癌患者的ORR为21.9%~37%[10-13]。2019年美国国立综合癌症网络(NCCN)卵巢癌指南中提及对铂耐药患者可能有效的药物中包含奥沙利铂,因此这种联合化疗方案在临床上是被许可的。本研究结果显示,单纯化疗组ORR为24.0%,与其他研究结果类似。另外,阿帕替尼联合化疗组的ORR(52.4%)及DCR(61.9%)均优于单纯化疗组(分别为24.0%和32.0%),差异具有统计学意义(P<0.05),说明阿帕替尼联合化疗可能会提高肿瘤细胞对化疗药物的敏感性,降低耐药程度,增加对肿瘤细胞的杀伤力,能够较快达到治疗效果。
血清CA125是目前诊断复发性卵巢癌最常用的肿瘤标志物,对卵巢癌的预后也有很好的反映。妇科肿瘤研究组建议,对于复发性卵巢癌除了使用RECIST外,还应结合血清CA125来评估治疗效果[14]。本研究结果显示阿帕替尼联合化疗能明显降低血清CA125水平(P<0.05)。
本研究从手足皮肤反应、消化道反应、骨髓抑制、肝功能损害、高血压、蛋白尿等不良反应指标来看,阿帕替尼联合化疗组高血压、手足皮肤反应发生率较单纯化疗组高,但均处于1~3级,对症支持治疗后尚可缓解(手足皮肤反应可预防性给予维生素B6及塞来昔布[15])。本研究中2组均出现白细胞减少4级不良反应,在给予药物减量及对症支持治疗后均缓解。提示阿帕替尼治疗复发性卵巢癌具有安全性。
综上所述,阿帕替尼联合化疗治疗耐铂型卵巢癌安全,具有一定的疗效,为耐铂型卵巢癌患者的治疗起到了积极的作用。
