不同光照度对金线莲生长、生理特性和药用成分的影响
2020-04-16韦坤华李明杰1b王建明张重义1b
牛 欢, 韦坤华, 徐 倩, 李明杰,1b, 古 力, 王建明, 张重义,1b,①
(1. 福建农林大学: a. 农学院, b. 作物遗传育种与综合利用省部共建教育部重点实验室, 福建 福州 350002;2. 广西壮族自治区药用植物园, 广西 南宁 530023)
金线莲〔Anoectochilusroxburghii(Wall.) Lindl.〕为典型的阴生植物,在福建各县(市)均有分布,主产于福建武平、明溪、永安和永春等地,这些产地均为福建金线莲药材的道地产区[1]。金线莲全株入药,具有抗衰老和提高机体免疫等功效[2];其体内含多糖、黄酮类化合物和生物碱等多种成分,其中多糖和总黄酮含量是金线莲质量技术规范指标[3]。由于金线莲对生长环境要求严格,种子无胚乳且自然条件下发芽率极低,加之人为过度采收,导致目前金线莲野生资源严重匮乏,为此,研究者对其组织培养和栽培技术进行了研究,且目前金线莲离体保存、炼苗和移栽等全套技术体系已基本建立[4-5]。但金线莲不同品种、品系及不同类型资源的适宜生境因子尚不明确,相应的配套栽培管理技术尚待进一步完善。
阴生植物的生长对光照变化较为敏感,不同光照强度对金线莲的生长和产量有不同的影响[4]。陈裕等[5]的研究结果显示:在金线莲的栽培过程中,若光照过强则叶小、茎短,若光照过弱则根短、茎细长;何碧珠等[6]发现,在3 000 lx光照条件下,金线莲的叶面积、茎粗和纤维含量均达到最大,有机物积累量显著增加。目前,有关光照度对金线莲药用活性成分及产量的影响缺乏明确的认识;在金线莲人工栽培中光照强度的调配常依据经验设置,缺乏定性和定量的科学标准。因此,结合形态指标和药用成分含量,明确金线莲栽培过程中适宜的光照条件对于提高金线莲的品质和产量均具有重要意义。
虽然研究者在金线莲光照强度优化方面已经做了大量的研究工作,但由于实际生产中所用的金线莲品种不同以及栽培管理措施和栽培生境条件各异,因此,对金线莲最适光照强度配置没有适宜的参考阈值。此外,对金线莲光照优选是在田间或大棚环境下进行研究[7],获得的光照参数并不能真实反映金线莲在季节和气候等多重环境因子影响下的最适光照需求,且多数研究仅以金线莲表型性状变化作为筛选其光照强度的依据[5-6,8],没有综合考虑药用成分和抗逆性等综合指标,获得的金线莲光照参数具有一定的局限性。
鉴于此,作者以福建广泛种植的金线莲品种‘泰宁一号’(Anoectochilusroxburghii‘Taining No. 1’)为实验材料,在受控条件下设置不同的光照度,分析光照对金线莲生长状况、生理指标和药用成分含量的影响,以期获取适宜金线莲生产的光照参数,为提高金线莲的产量和品质提供基础研究数据。
1 材料和方法
1.1 材料
供试金线莲品种‘泰宁一号’无菌繁殖苗由福建泰宁县古农堂生物科技有限公司提供。于2017年9月6日,选取生长周期为6个月、形态基本一致的组培苗100瓶,每瓶约20株;培养基为MS基本培养基,含有7 g·L-1琼脂、25 g·L-1蔗糖、0.2 mg·L-1NAA和1.5 g·L-1活性炭,pH 5.4。在古农堂泰宁县种植基地大棚内闭瓶炼苗15 d,之后开瓶炼苗3 d,使组培苗逐渐适应外界环境。将组培苗取出,用清水洗净根部以去除残存培养基,并用质量分数0.5%KMnO4溶液对根部进行消毒处理,供试。
在福建农林大学中药材GAP研究所受控光照室内,挑选长势基本一致、根系无损伤的金线莲幼苗种植于托盘(长35.5 cm、宽28.0 cm、高7.8 cm)中,每个托盘种植120株(12列、10行,株间距3 cm),栽培土为林下腐殖土(弱酸性),常规水肥管理。
1.2 方法
1.2.1 光照设置和处理 设置5个处理组T1、T2、T3、T4和T5,光照度分别为500、1 500、3 000、4 500和6 000 lx,每处理3个托盘(视为3个重复);并依据文献[9]设置培养条件,培养温度(24±2) ℃,土壤含水量60%~86%,空气相对湿度75%~85%。
于2017年9月27日开始,采用可控制光照度的LED灯对幼苗进行持续180 d的光照处理,处理开始后每隔30 d取样1次,共取6次,用于生长指标、生理指标和药用成分测定。
1.2.2 生长指标测定 每次取样时,采取随机取样法在各处理中挑取10株样株,供生长指标测定。
统计各单株的根数、叶片数和茎节数;利用直尺(精度 1 mm)测量株高以及各单株所有根的长度以及所有叶片的长度和宽度;利用游标卡尺(精度0.1 mm)测量各单株所有根的直径以及距地面2 cm处的茎直径。上述结果均取平均值。
利用电子分析天平〔艾德姆衡器(武汉)有限公司,精度0.1 mg〕分别称量各单株的鲜质量以及地上部和地下部的鲜质量。将样株置于电热鼓风干燥箱(上海精宏实验设备有限公司)中,于105 ℃杀青30 min,之后于80 ℃继续干燥8 h,期间每隔30 min称量1次,直至达到恒质量;用电子分析天平称量各单株的干质量以及地上部和地下部的干质量。
1.2.3 生理指标测定 每次取样时,采取随机取样法在各处理中挑取3株样株,供生理指标测定。
称取完整无损伤叶片0.5 g,采用比色法[10]218-219测定超氧化物歧化酶(SOD)活性;采用愈创木酚比色法[10]100-101测定过氧化物酶(POD)活性;采用分光光度法[11]测定过氧化氢酶(CAT)活性。
称取完整无损伤叶片0.5 g,采用考马斯蓝染料结合法[10]125-126测定可溶性蛋白质含量;采用丙酮提取法提取叶绿素,并使用分光光度计比色法[10]58-59测定叶绿素a、叶绿素b和总叶绿素含量;采用蒽酮-硫酸比色法[10]103-104测定可溶性总糖含量。
1.2.4 药用成分测定 每次取样时,采取随机取样法在各处理中挑取10株样株,将样株放入电热鼓风干燥箱中,于105 ℃杀青30 min,之后于80 ℃烘干至恒质量,冷却后研磨成粉并过60目筛,供试。
称取样品粉末0.05 g,采用苯酚-硫酸法[12]测定多糖含量;采用超声法[13]提取总黄酮,并用T6紫外可见分光光度计(北京普析通用仪器有限公司)测定总黄酮含量;采用超声波法[14]提取生物碱(45 kHz、80 ℃),并用T6紫外可见分光光度计测定生物碱含量。
1.3 数据计算和分析
根据公式“根冠比=单株地下部鲜质量/单株地上部鲜质量”计算根冠比;根据公式“折干率=单株干质量/单株鲜质量”计算折干率。
采用EXCEL 2003软件对数据进行初步整理,采用DPS 7.0.5.8软件进行单因素方差分析。
2 结果和分析
2.1 不同光照度对金线莲生长的影响
2.1.1 根系生长指标的变化 经不同光照度处理30~180 d金线莲的单株根数、根长和根直径变化见表1。结果表明:在不同光照度处理下,金线莲的单株根数、根长和根直径均呈波动的变化趋势,其中,根长和根直径总体随处理时间的延长而增加,而单株根数的变化幅度总体较小。
从不同处理时间单株根数的变化看,T2(光照度1 500 lx)处理组的单株根数较多,其次为T4(光照度4 500 lx)处理组。其中,在处理30、150和180 d时,T2处理组的单株根数显著(P<0.05)多于其他处理组,且在处理60~120 d时其单株根数也较多;在处理90和120 d时,T4处理组的单株根数均最多。T1(光照度500 lx)处理组的单株根数在处理结束(180 d)时显著少于其他处理组。
从不同处理时间根长的变化看,T5(光照度6 000 lx)处理组的根长总体最高,其次为T4处理组。其中,在处理90~180 d时,T5处理组的根长显著高于其他处理组;在处理60 d时,T4处理组的根长显著高于其他处理组;而在处理30 d时,T4和T5处理组的根长显著高于另3个处理组。T1处理组的根长总体低于其他处理组。



处理组Treatment group光照度/lxIlluminance不同处理时间的单株根数 Root number per plant at different treatment times30 d60 d90 d120 d150 d180 dT15004.4±0.8b4.2±0.2ab4.3±0.3b3.5±0.2c4.3±0.6c3.8±0.3dT21 5004.9±0.9a4.3±0.7ab4.3±0.6b4.8±0.3ab5.2±0.3a6.1±0.6aT33 0003.5±0.9d3.7±0.3c4.2±0.3b3.8±0.2bc4.8±0.3b4.6±0.3cT44 5004.1±0.7bc4.2±0.1a5.0±0.6a5.0±0.3a3.8±0.1d5.6±0.4bT56 0004.0±0.6c4.0±0.7b4.3±0.2b4.0±0.1b4.0±0.3cd4.9±0.2c处理组Treatment group光照度/lxIlluminance不同处理时间的根长/cm Root length at different treatment times30 d60 d90 d120 d150 d180 dT15002.5±0.3b2.6±0.4c2.6±0.3d2.9±0.3c3.3±0.6c3.0±0.3cT21 5002.6±0.3b2.9±0.4b2.9±0.3c3.0±0.4c3.4±0.6c3.0±0.4cT33 0002.6±0.3b2.7±0.4c3.1±0.4b3.2±0.4b3.4±0.6c3.2±0.4cT44 5002.9±0.4a3.2±0.7a3.2±0.4b3.3±0.6b4.0±0.4b3.7±0.4bT56 0002.9±0.4a3.0±0.7b3.6±0.5a4.3±0.5a4.3±0.2a4.0±0.5a处理组Treatment group光照度/lxIlluminance不同处理时间的根直径/mm Root diameter at different treatment times30 d60 d90 d120 d150 d180 dT15001.1±0.4a2.1±0.4a2.5±0.4ab1.8±0.2b2.2±0.4b2.4±0.3aT21 5000.9±0.1a2.1±0.4a2.4±0.5ab2.2±0.4ab2.2±0.3b2.4±0.1aT33 0001.0±0.3a2.0±0.4a2.3±0.4b2.2±0.4ab2.3±0.4b2.3±0.3aT44 5001.1±0.3a1.9±0.5a2.6±0.4a2.3±0.3a2.3±0.4b2.2±0.3aT56 0001.0±0.4a1.8±0.5a2.4±0.4ab2.2±0.4ab2.6±0.3a2.3±0.3a
1)同列中不同的小写字母表示差异显著(P<0.05)Different lowercases in the same column indicate the significant (P<0.05) difference.
从不同处理时间根直径的变化看,各处理组的根直径总体无显著差异。其中,在处理90 d 时,仅T4处理组的根直径显著高于T3(光照度3 000 lx)处理组;在处理120 d 时,仅T4处理组的根直径显著高于T1处理组;在处理150 d时,T5处理组的根直径显著高于其他处理组。
与处理30 d时相比,处理结束时各处理组金线莲的根长和根直径分别增加15.4%~37.9%和100.0%~166.7%,而单株根数最高增加36.6%、最低则减少13.6%,因而,较长时间的光照对金线莲根数和根长的影响总体较小,但有利于根直径的增大。此外,处理结束时T4和T5处理组的根长分别较处理30 d时增加27.6%和37.9%,T3和T4处理组的单株根数分别较处理30 d时增加31.4%和36.6%,说明较高的光照有利于金线莲根的伸长,而适度的光照则有利于金线莲根数的增加。
2.1.2 株高和茎生长指标的变化 经不同光照度处理30~180 d金线莲的株高、茎直径和单株茎节数变化见表2。结果显示:在不同光照度处理下,金线莲的株高、茎直径和单株茎节数均呈波动的变化趋势,其中,株高和茎直径总体随处理时间的延长而增加,而单株茎节数的变化幅度总体较小。
从不同处理时间株高的变化看,T1处理组的株高均最高,且与其他处理组差异显著。从不同处理时间茎直径的变化看,在处理60和90 d时,各处理组的茎直径无显著差异;在处理30、150和180 d时,多数处理组间茎直径无显著差异。其中,在处理30 d时,T1处理组的茎直径显著低于T4和T5处理组;在处理120 d时,T5处理组的茎直径显著高于其他处理组;在处理150 d时,T5处理组的茎直径显著高于T2和T4处理组;在处理180 d时,T5处理组的茎直径显著高于T1和T4处理组。从不同处理时间单株茎节数的变化看,多数处理组间单株茎节数无显著差异,但在处理30 d时,T2处理组的单株茎节数显著高于T3、T4和T5处理组;在处理60和90 d时,T1处理组的单株茎节数均显著高于T3和T5处理组;在处理120 d时,T2处理组的单株茎节数显著高于T4和T5处理组;在处理150 d时,T5处理组的单株茎节数显著低于其他处理组;在处理180 d时,T5处理组的单株茎节数显著高于其他处理组。



处理组Treating group光照度/lxIlluminance不同处理时间的株高/cm Height at different treatment times30 d60 d90 d120 d150 d180 dT150014.9±0.2a16.8±0.4a16.5±0.3a18.2±0.1a18.6±0.2a19.2±0.4aT21 50012.3±0.4d16.0±0.4b13.4±0.4c16.2±0.2b16.2±0.3c16.4±0.2cT33 00012.5±0.4cd15.2±0.4d14.6±0.4b16.1±0.5b16.8±0.1b15.2±0.2dT44 50012.7±0.2c15.5±0.2c14.4±0.2b16.3±0.2b16.6±0.2b16.2±0.3cT56 00013.2±0.4b15.1±0.3d12.1±0.2d15.1±0.2c15.5±0.2d17.6±0.3b处理组Treatment group光照度/lxIlluminance不同处理时间的茎直径/mm Stem diameter at different treatment times30 d60 d90 d120 d150 d180 dT15002.1±0.2b2.4±0.3a2.3±0.1a2.2±0.3c2.6±0.1ab2.4±0.2cT21 5002.3±0.2ab2.6±0.3a2.3±0.2a2.5±0.3b2.4±0.2b2.8±0.1abT33 0002.3±0.3ab2.4±0.3a2.5±0.2a2.5±0.2b2.6±0.4ab2.6±0.2abcT44 5002.5±0.1a2.5±0.2a2.6±0.3a2.5±0.3b2.4±0.3b2.6±0.1bcT56 0002.5±0.3a2.4±0.2a2.4±0.2a3.0±0.2a2.8±0.1a2.9±0.2a处理组Treatment group光照度/lxIlluminance不同处理时间的单株茎节数 Number of stem node per plant at different treatment times30 d60 d90 d120 d150 d180 dT15006.3±0.2ab6.5±0.3a6.2±0.3a5.9±0.4ab6.6±0.1a6.8±0.2bT21 5006.6±0.2a5.9±0.2ab5.0±0.1ab6.1±0.2a6.9±0.1a6.8±0.2bT33 0005.0±0.5c5.5±0.4b4.4±0.2b5.8±0.2ab6.7±0.2a6.3±0.3cT44 5005.5±0.4bc5.9±0.2ab5.8±0.3ab5.6±0.3b6.9±0.1a6.4±0.3cT56 0005.4±0.5bc5.5±0.2b4.6±0.2b5.7±0.3b6.2±0.2b7.3±0.4a
1)同列中不同的小写字母表示差异显著(P<0.05)Different lowercases in the same column indicate the significant (P<0.05) difference.
与处理30 d时相比,处理结束时各处理组金线莲的株高、茎直径和单株茎节数分别增加21.6%~33.3%、4.0%~21.7%和3.0%~35.2%,因而,较长时间的光照对金线莲株高的影响总体较大。此外,在处理结束时,T5处理组的单株茎节数较处理30 d时增加35.2%,说明较高和较长时间的光照有利于金线莲茎节数的增加。
2.1.3 叶生长指标的变化 经不同光照度处理30~180 d金线莲的单株叶片数、叶长和叶宽变化见表3。结果显示:在不同光照度处理下,金线莲的单株叶片数、叶长和叶宽均呈波动的变化趋势,且总体随处理时间的延长而增加。
从不同处理时间单株叶片数、叶长和叶宽的变化看,各处理组间单株叶片数均无显著差异;除T4处理组的叶长在处理150 d时显著高于T3处理组外,各处理组间叶长均无显著差异;各处理组间叶宽总体也无显著差异,仅T3和T5处理组的叶宽在处理60 d时显著高于T4处理组,T5处理组的叶宽在处理120 d时显著高于T1处理组。
与处理30 d时相比,处理结束时各处理组金线莲的单株叶片数、叶长和叶宽分别增加3.3%~25.9%、27.3%~52.6%和12.5%~50.0%,因而,较长时间的光照对金线莲叶长和叶宽的影响总体较大。此外,在处理结束时,T3处理组的单株叶片数较处理30 d时增加25.9%,说明适度的光照有利于金线莲叶片数的增加。
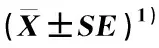


处理组Treatment group光照度/lxIlluminance不同处理时间的单株叶片数 Leaf number per plant at different treatment times30 d60 d90 d120 d150 d180 dT15006.1±0.5a5.9±0.4a6.4±0.6a6.3±0.6a6.7±0.5a6.3±0.3aT21 5006.2±0.6a6.5±0.4a6.6±0.2a6.8±0.2a6.9±0.5a6.9±0.5aT33 0005.8±0.3a6.1±0.6a6.3±0.7a7.0±0.2a7.2±0.5a7.3±0.5aT44 5006.6±0.3a6.5±0.2a7.2±0.2a6.7±0.2a7.4±0.2a7.2±0.6aT56 0006.0±0.5a6.3±0.3a7.3±0.2a7.3±0.3a6.6±0.6a7.4±0.3a处理组Treatment group光照度/lxIlluminance不同处理时间的叶长/cm Leaf length at different treatment times30 d60 d90 d120 d150 d180 dT15001.9±0.3a2.3±0.3a2.8±0.4a2.5±0.5a2.5±0.3ab2.9±0.3aT21 5002.1±0.3a2.2±0.3a2.7±0.6a2.6±0.6a2.5±0.3ab3.1±0.6aT33 0002.2±0.5a2.2±0.5a2.5±0.6a2.5±0.4a2.2±0.5b2.8±0.5aT44 5002.1±0.4a2.1±0.4a2.4±0.2a2.6±0.5a2.8±0.5a2.9±0.5aT56 0002.1±0.6a2.3±0.6a2.5±0.5a2.4±0.4a2.5±0.4ab2.8±0.3a处理组Treatment group光照度/lxIlluminance不同处理时间的叶宽/cm Leaf width at different treatment times30 d60 d90 d120 d150 d180 dT15001.4±0.2a1.7±0.3ab1.8±0.2a1.8±0.3b1.8±0.2a2.0±0.4aT21 5001.4±0.3a1.7±0.2ab1.9±0.3a1.9±0.4ab2.0±0.3a2.1±0.3aT33 0001.4±0.3a1.8±0.3a1.8±0.2a1.9±0.3ab1.8±0.3a2.1±0.3aT44 5001.6±0.2a1.5±0.2b1.9±0.3a1.9±0.2ab2.0±0.3a1.8±0.2aT56 0001.6±0.3a1.8±0.4a1.8±0.3a2.1±0.3a1.9±0.2a2.1±0.3a
1)同列中不同的小写字母表示差异显著(P<0.05)Different lowercases in the same column indicate the significant (P<0.05) difference.
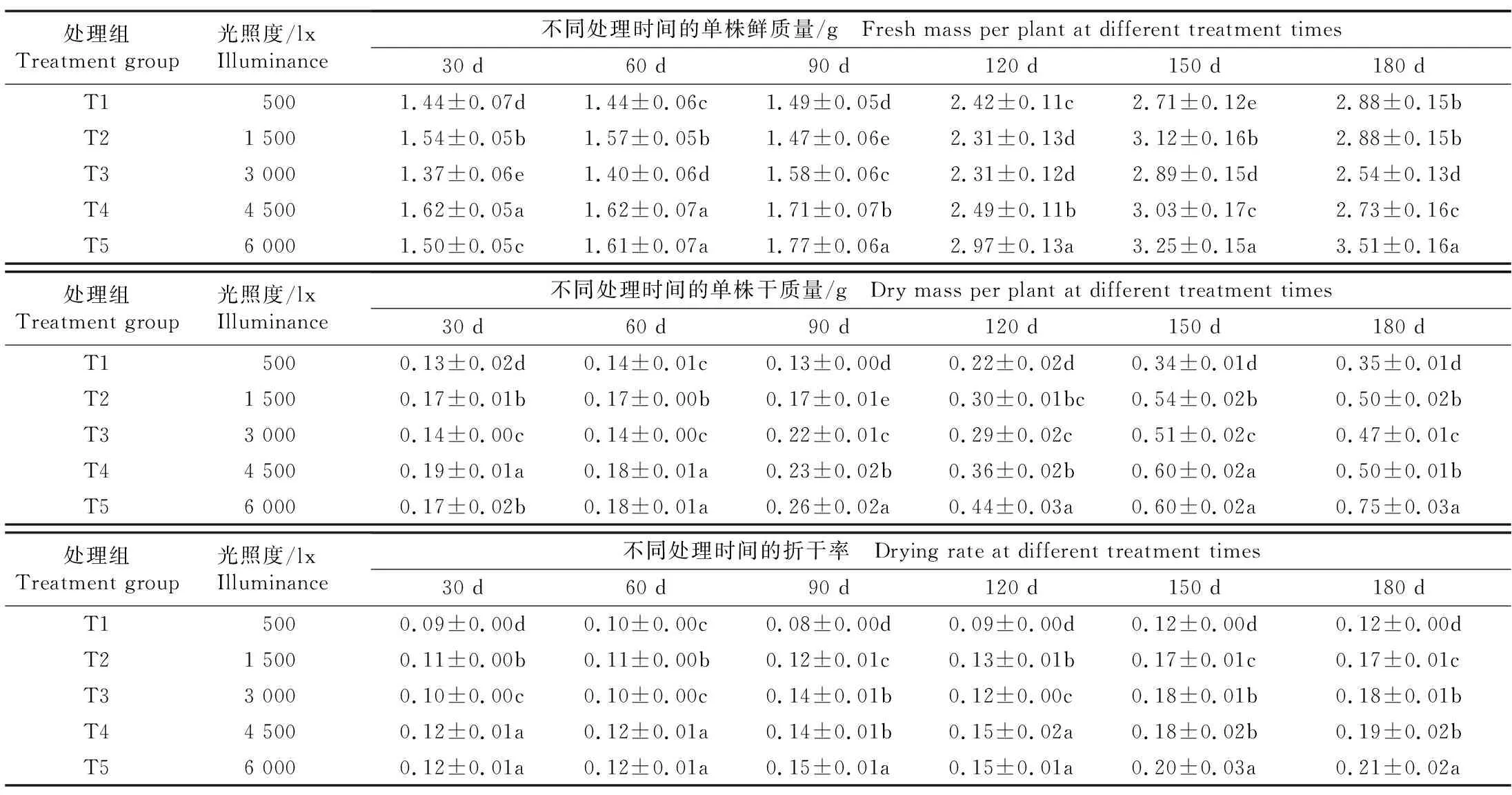
2.1.4 植株质量和折干率的变化 经不同光照度处理30~180 d金线莲的单株鲜质量、单株干质量和折干率变化见表4。结果显示:在不同光照度处理下,金线莲的单株鲜质量、单株干质量和折干率总体随处理时间的延长而增加,且各处理组间这3项指标总体差异显著,其中,单株鲜质量和单株干质量在处理90 d后增幅加大。
从不同处理时间单株鲜质量和单株干质量的变化看,在处理60~180 d时,T5处理组的这2项指标总体最高且均与T1、T2和T3处理组差异显著,在多数时间与T4处理组也差异显著。从不同处理时间折干率的变化看,T5处理组的折干率总体最高且均与T1、T2和T3处理组差异显著,在处理90、150和180 d时与T4处理组也差异显著。
与处理30 d时相比,处理结束时各处理组金线莲的单株鲜质量、单株干质量和折干率分别增加68.5%~134.0%、163.2%~341.2%和33.3%~80.0%,说明较长时间的光照有利于金线莲单株鲜质量和单株干质量的增加,其中单株干质量的增幅更大,并因此使其折干率增加。此外,在处理结束时T5处理组的单株鲜质量、单株干质量和折干率的增幅较其他处理组大,说明较高的光照有利于金线莲的物质积累。
2.2 不同光照度对金线莲叶片生理指标的影响
2.2.1 抗氧化酶活性的变化 经不同光照度处理30~180 d金线莲叶片中超氧化物歧化酶(SOD)、过氧化物酶(POD)和过氧化氢酶(CAT)活性的变化见表5。结果显示:在不同光照度处理下,金线莲叶片中SOD、POD和CAT活性均呈波动的变化趋势,其中,随处理时间的延长,SOD活性总体升高,POD活性总体降低,CAT活性总体呈“单峰型”变化趋势。
从不同处理时间SOD活性的变化看,在处理60 d时,各处理组的SOD活性开始急速升高,其中,T1(光照度500 lx)和T3(光照度3 000 lx)处理组的SOD活性分别在处理120和180 d时最高,其他处理组的SOD活性均在处理150 d时最高;总体上看,多数处理组间SOD活性无显著差异。
从不同处理时间POD活性的变化看,在处理30~90 d时,各处理组的POD活性总体较高,之后则总体下降。其中,T2(光照度1 500 lx)和T4(光照度4 500 lx)处理组的POD活性在处理30 d时最高,T3和T5(光照度6 000 lx)处理组的POD活性在处理90 d时最高,T1处理组的POD活性在处理150 d时最高;总体上看,多数处理组间POD活性差异显著。


处理组Treatment group光照度/lxIlluminance不同处理时间的单株鲜质量/g Fresh mass per plant at different treatment times30 d60 d90 d120 d150 d 180 dT15001.44±0.07d1.44±0.06c1.49±0.05d2.42±0.11c2.71±0.12e2.88±0.15bT21 5001.54±0.05b1.57±0.05b1.47±0.06e2.31±0.13d3.12±0.16b2.88±0.15bT33 0001.37±0.06e1.40±0.06d1.58±0.06c2.31±0.12d2.89±0.15d2.54±0.13dT44 5001.62±0.05a1.62±0.07a1.71±0.07b2.49±0.11b3.03±0.17c2.73±0.16cT56 0001.50±0.05c1.61±0.07a1.77±0.06a2.97±0.13a3.25±0.15a3.51±0.16a处理组Treatment group光照度/lxIlluminance不同处理时间的单株干质量/g Dry mass per plant at different treatment times30 d60 d90 d120 d150 d180 dT15000.13±0.02d0.14±0.01c0.13±0.00d0.22±0.02d0.34±0.01d0.35±0.01dT21 5000.17±0.01b0.17±0.00b0.17±0.01e0.30±0.01bc0.54±0.02b0.50±0.02bT33 0000.14±0.00c0.14±0.00c0.22±0.01c0.29±0.02c0.51±0.02c0.47±0.01cT44 5000.19±0.01a0.18±0.01a0.23±0.02b0.36±0.02b0.60±0.02a0.50±0.01bT56 0000.17±0.02b0.18±0.01a0.26±0.02a0.44±0.03a0.60±0.02a0.75±0.03a处理组Treatment group光照度/lxIlluminance不同处理时间的折干率 Drying rate at different treatment times30 d60 d90 d120 d150 d180 dT15000.09±0.00d0.10±0.00c0.08±0.00d0.09±0.00d0.12±0.00d0.12±0.00dT21 5000.11±0.00b0.11±0.00b0.12±0.01c0.13±0.01b0.17±0.01c0.17±0.01cT33 0000.10±0.00c0.10±0.00c0.14±0.01b0.12±0.00c0.18±0.01b0.18±0.01bT44 5000.12±0.01a0.12±0.01a0.14±0.01b0.15±0.02a0.18±0.02b0.19±0.02bT56 0000.12±0.01a0.12±0.01a0.15±0.01a0.15±0.01a0.20±0.03a0.21±0.02a
1)同列中不同的小写字母表示差异显著(P<0.05)Different lowercases in the same column indicate the significant (P<0.05) difference.
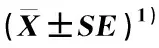


处理组Treatment group光照度/lxIlluminance不同处理时间的SOD活性/(U·mg-1) SOD activity at different treatment times30 d60 d90 d120 d150 d180 dT150066.7±8.6bc120.4±12.2c112.1±7.9ab138.0±8.4ab134.2±6.1bc133.6±11.4aT21 50054.1±7.1c128.5±14.1bc96.9±6.1b86.0±5.1c203.9±17.2ab136.6±10.1aT33 00092.3±5.9a161.5±9.1a150.3±6.3ab128.7±9.2b83.7±6.3c173.5±11.8aT44 50094.6±8.3a154.1±8.3ab171.9±9.2a150.2±8.8a204.1±18.1ab151.5±12.2aT56 00080.0±7.1ab137.6±6.2abc120.2±8.0ab143.3±8.1ab228.1±17.1a183.1±13.3a处理组Treatment group光照度/lxIlluminance不同处理时间的POD活性/(U·g-1·min-1) POD activity at different treatment times30 d60 d90 d120 d150 d180 dT1500167.3±14.2c164.9±7.5d163.2±8.5d168.0±6.4b258.1±15.9a109.4±6.4bT21 500361.8±16.0a201.2±12.9c185.5±9.8c204.4±9.1a107.4±7.2bc128.0±9.1bT33 000274.1±17.1b296.7±16.1a307.4±15.8a77.9±7.4d84.6±6.4cd251.7±12.4aT44 500335.0±14.4a207.2±14.2c198.5±8.4c100.2±7.4c145.2±4.1b233.7±13.0aT56 000256.7±11.8b258.1±12.3b265.1±15.1b159.2±5.1b49.3±7.2d39.6±5.0c处理组Treatment group光照度/lxIlluminance不同处理时间的CAT活性/(U·g-1·min-1) CAT activity at different treatment times30 d60 d90 d120 d150 d180 dT150092.2±6.9bc110.6±4.3a166.0±5.4a114.9±8.8b80.2±6.1b60.2±4.2abT21 50097.4±6.0ab92.3±8.2bc162.9±6.3a106.8±8.4c65.0±5.3d45.2±6.1cT33 00080.8±6.4cd86.2±3.0bc160.8±6.1a93.8±6.4e67.1±5.1cd45.8±4.9cT44 50068.8±6.3d99.6±8.8ab132.5±8.9a101.8±6.3d71.6±6.1c52.7±6.2bcT56 000110.3±7.4a83.0±7.1c159.8±6.1a126.1±7.8a87.1±4.3a70.3±7.0a
1)同列中不同的小写字母表示差异显著(P<0.05)Different lowercases in the same column indicate the significant (P<0.05) difference.
从不同处理时间CAT活性的变化看,T1、T2、T3、T4和T5处理组的CAT活性均在处理90 d时最高,分别较处理30 d时增加80.0%、67.2%、99.0%、92.6%和44.9%,但各处理组间CAT活性的差异不显著。在其他时间,各处理组间CAT活性总体差异显著,其中T5处理组的CAT活性在处理30、120、150和180 d时均最高,且总体与其他处理组差异显著。
与处理30 d时相比,处理结束(180 d)时T1、T2、T3、T4和T5处理组的SOD活性分别增加100.3%、152.5%、88.0%、60.1%和128.9%,POD活性分别减少34.6%、64.6%、8.2%、30.2%和84.6%,CAT活性分别减少34.7%、53.6%、43.3%、23.4%和36.3%,表明金线莲叶片内的不同抗氧化酶对光照度变化的敏感性存在一定差异。
2.2.2 可溶性蛋白质和可溶性总糖含量的变化 经不同光照度处理30~180 d金线莲叶片中可溶性蛋白质和可溶性总糖含量的变化见表6。结果显示:在不同光照度处理下,金线莲叶片中可溶性蛋白质和可溶性总糖含量均呈波动的变化趋势,其中,随处理时间的延长,可溶性蛋白质含量总体呈“单峰型”变化趋势,而可溶性总糖含量总体升高。
从不同处理时间可溶性蛋白质含量的变化看,在处理30~90 d时,各处理组的可溶性蛋白质含量总体较高,之后则总体下降;其中,T1、T2、T3和T4处理组的可溶性蛋白质含量均在处理90 d时最高,分别较处理30 d时增加58.0%、59.0%、12.4%和20.7%,但各处理组间无显著差异;而T5处理组的可溶性蛋白质含量则在处理60 d时最高,较处理30 d时增加24.2%,且显著高于T1、T2和T4处理组。
从不同处理时间可溶性总糖含量的变化看,在处理60 d时,T1处理组的可溶性总糖含量显著低于T3、T4和T5处理组;在处理90 d时,T1处理组的可溶性总糖含量显著低于T3和T4处理组;在处理150 d时,T1处理组的可溶性总糖含量显著低于T2、T3和T4处理组;在处理180 d时,T1处理组的可溶性总糖含量显著低于T3和T5处理组。总体上看,T3、T4和T5处理组的可溶性总糖含量高于T1和T2处理组。
与处理30 d时相比,处理结束时T1和T5处理组的可溶性蛋白质含量分别增加21.8%和17.1%,T2、T3和T4处理组的可溶性蛋白质含量则分别减少42.9%、5.4%和9.5%;T1、T3和T5处理组的可溶性总糖含量分别增加3.1%、18.1%和11.5%,T2和T4处理组的可溶性总糖含量则分别减少3.9%和4.1%,说明较长时间的光照对金线莲叶片可溶性蛋白质的合成和积累有较大影响。此外,处理结束时T5处理组的可溶性蛋白质和可溶性总糖含量分别较处理30 d时增加17.1%和11.5%,说明较高的光照有利于金线莲叶片中可溶性蛋白质和可溶性总糖的积累。



处理组Treatment group光照度/lxIlluminance不同处理时间的可溶性蛋白质含量/(mg·g-1) Soluble protein content at different treatment times30 d60 d90 d120 d150 d180 dT15002.38±0.21c3.10±0.36b3.76±0.43a2.37±0.12c2.87±0.12b2.90±0.17cT21 5003.10±0.12b2.94±0.56b4.93±0.30a2.69±0.30b2.62±0.16b1.77±0.18dT33 0003.70±0.10a3.40±0.21ab4.16±0.41a3.09±0.13a2.81±0.10b3.50±0.12abT44 5003.58±0.13ab2.98±0.57b4.32±0.20a2.81±0.11b3.22±0.10a3.24±0.10bcT56 0003.22±0.19bc4.00±0.12a3.86±0.27a3.12±0.30a2.68±0.10b3.77±0.11a处理组Treatment group光照度/lxIlluminance不同处理时间的可溶性总糖含量/(mg·g-1) Soluble total sugar at different treatment times30 d60 d90 d120 d150 d180 dT150018.67±0.52a12.86±0.22b17.53±0.49c15.93±0.58a18.45±0.67b19.25±0.62cT21 50019.58±0.79a14.53±0.14ab20.25±0.42abc17.15±0.31a21.14±0.52a18.81±0.70cT33 00019.45±0.54a17.41±0.12a23.83±0.60a19.45±0.66a21.89±0.34a22.98±0.54abT44 50022.44±0.41a17.39±0.23a21.75±0.34ab15.80±0.58a21.93±0.60a21.51±0.62bcT56 00022.03±0.40a18.00±0.14a18.63±0.39bc17.81±0.33a20.74±0.32ab24.56±0.71a
1)同列中不同的小写字母表示差异显著(P<0.05)Different lowercases in the same column indicate the significant (P<0.05) difference.
2.2.3 叶绿素含量的变化 经不同光照度处理30~180 d金线莲叶片中叶绿素a(Chla)、叶绿素b(Chlb)和总叶绿素(Chl)含量的变化见表7。结果显示:在不同光照度处理下,各处理组的金线莲叶片中Chla、Chlb和Chl含量均呈小幅波动的变化趋势,且随处理时间的延长总体升高,其中,除T1处理组外,其他处理组的Chla、Chlb和Chl含量在处理90 d时均最低。
从不同处理时间Chla、Chlb和Chl含量的变化看,在处理60~180 d时,T1处理组的这3项指标总体均最高,且与多数处理组间差异显著。而T5处理组的这3项指标在处理30~180 d时总体最低。T1、T2和T3处理组的这3项指标总体高于T4和T5处理组。
与处理30 d时相比,处理结束时T1、T2、T4和T5处理组的Chla含量分别增加92.1%、39.2%、73.8%和95.6%,Chlb含量分别增加70.0%、19.4%、34.6%和43.5%,Chl含量分别增加86.8%、35.3%、66.2%和84.2%,而T3处理组的Chla和Chl含量分别减少10.1%和4.0%,其Chlb含量则增加23.1%,表明较长时间的光照有利于金线莲叶片叶绿素的合成和积累,尤其对Chla含量的提升作用明显。此外,处理结束时T1处理组的Chla、Chlb和Chl含量分别较处理30 d时增加92.1%、70.0%和86.8%,增幅均较大,说明适度的光照有利于金线莲叶片中叶绿素的合成和积累。



处理组Treatment group光照度/lxIlluminance不同处理时间的叶绿素a含量/(mg·g-1) Chlorophyll a content at different treatment times30 d60 d90 d120 d150 d180 dT15001.14±0.04b1.80±0.07a1.30±0.04a1.46±0.01a1.75±0.03b2.19±0.05aT21 5001.48±0.03a1.25±0.04b0.93±0.02b1.27±0.01b1.76±0.01b2.06±0.04abT33 0001.58±0.03a1.26±0.04b0.93±0.03b1.15±0.02bc1.97±0.01a1.42±0.01dT44 5001.07±0.04bc1.14±0.04bc0.85±0.01b1.10±0.01c1.68±0.01b1.86±0.02bcT56 0000.91±0.02c1.03±0.02c0.76±0.02b0.95±0.02d1.55±0.02c1.78±0.01c处理组Treatment group光照度/lxIlluminance不同处理时间的叶绿素b含量/(mg·g-1) Chlorophyll b content at different treatment times30 d60 d90 d120 d150 d180 dT15000.30±0.01b0.46±0.03a0.36±0.02a0.54±0.03a0.55±0.02a0.51±0.02aT21 5000.36±0.01a0.36±0.02b0.27±0.02b0.51±0.02ab0.40±0.02b0.43±0.02bT33 0000.39±0.02a0.37±0.01b0.23±0.01bc0.47±0.02b0.47±0.03ab0.48±0.03abT44 5000.26±0.01bc0.32±0.02bc0.22±0.01bc0.38±0.03c0.48±0.02ab0.35±0.02cT56 0000.23±0.01c0.25±0.00c0.21±0.01c0.32±0.01d0.40±0.03b0.33±0.02c处理组Treatment group光照度/lxIlluminance不同处理时间的总叶绿素含量/(mg·g-1) Total chlorophyll content at different treatment times30 d60 d90 d120 d150 d180 dT15001.44±0.04b2.26±0.06a1.67±0.04a2.01±0.05a2.30±0.06ab2.69±0.06aT21 5001.84±0.05a1.61±0.04b1.20±0.02b1.78±0.05b2.16±0.04b2.49±0.06bT33 0001.98±0.07a1.63±0.04b1.16±0.04bc1.62±0.03bc2.44±0.04a1.90±0.05dT44 5001.33±0.04bc1.45±0.04bc1.07±0.02bc1.47±0.04c2.16±0.06b2.21±0.05cT56 0001.14±0.02c1.28±0.03c0.97±0.02c1.27±0.02d1.94±0.04c2.10±0.04c
1)同列中不同的小写字母表示差异显著(P<0.05)Different lowercases in the same column indicate the significant (P<0.05) difference.
2.3 不同光照度对金线莲药用成分的影响
经不同光照度处理30~180 d金线莲中多糖、总黄酮和生物碱含量的变化见表8。结果显示:在不同光照处理下,金线莲中多糖、总黄酮和生物碱含量均呈波动的变化趋势;其中,随处理时间的延长,总黄酮和生物碱含量总体升高,除T1(光照度500 lx)处理组外,其他处理组的多糖含量也总体升高。
从不同处理时间多糖含量的变化看,在处理30 d时,T1和T4(光照度4 500 lx)处理组的多糖含量显著高于其他处理组,但此后T1处理组的多糖含量均不同程度降低,在处理120~180 d时较低;而其他处理组的多糖含量均不同程度升高,其中T4处理组的多糖含量在处理30、60、90、150和180 d时均最高并与多数处理组间差异显著,在处理120 d时也仅低于T3(光照度3 000 lx)处理组但无显著差异。总体上看,T4处理组的多糖含量维持在较高水平。
从不同处理时间总黄酮含量的变化看,在处理30、90和150 d时,各处理组的总黄酮含量无显著差异;在处理60 d时,仅T1和T4处理组的总黄酮含量显著高于T2(光照度1 500 lx)处理组;在处理120 d时,T3处理组的总黄酮含量显著高于T1、T2和T4处理组;在处理180 d时,T3处理组的总黄酮含量显著高于T1、T4和T5(光照度6 000 lx)处理组。总体上看,T3处理组的总黄酮含量维持在较高水平。



处理组Treatment group光照度/lxIlluminance不同处理时间的多糖含量/(mg·g-1) Polysaccharide content at different treatment times30 d60 d90 d120 d150 d180 dT150016.2±0.2a11.5±0.2c12.5±0.2d11.3±0.3b11.7±0.3c13.9±0.2cT21 50013.7±0.2b11.1±0.4c14.7±0.3c12.1±0.4b14.0±0.4b15.0±0.3bcT33 00013.9±0.3b12.9±0.3b10.7±0.2e15.2±0.3a14.810.4b15.9±0.2abT44 50016.8±0.3a15.0±0.3a18.2±0.3a14.5±0.2a16.7±0.3a17.2±0.4aT56 00013.3±0.2b13.3±0.2b16.6±0.2b12.3±0.3b13.9±0.2b15.1±0.4bc处理组Treatment group光照度/lxIlluminance不同处理时间的总黄酮含量/(mg·g-1) Total flavonoid content at different treatment times30 d60 d90 d120 d150 d180 dT150017.8±0.4a20.0±0.4a19.5±0.3a19.3±0.3c23.7±0.3a21.3±0.2cT21 50017.4±0.5a17.6±0.3b19.5±0.5a18.8±0.4c22.8±0.3a24.8±0.2abT33 00017.6±0.4a18.9±0.2ab20.2±0.3a24.6±0.5a24.7±0.4a26.4±0.4aT44 50017.5±0.3a20.1±0.3a19.8±0.4a21.5±0.4bc24.5±0.3a24.3±0.4bT56 00017.9±0.3a18.8±0.4ab20.0±0.3a23.0±0.4ab22.3±0.3a22.3±0.3c处理组Treatment group光照度/lxIlluminance不同处理时间的生物碱含量/(mg·g-1) Alkaloid content at different treatment times30 d60 d90 d120 d150 d180 dT150015.5±0.2c15.3±0.3a14.6±0.4bc16.9±0.5b17.3±0.5b18.6±0.3aT21 50016.2±0.3b15.4±0.2a14.3±0.2c16.5±0.3c16.9±0.4b18.5±0.4aT33 00016.3±0.5b15.3±0.2a14.8±0.3b17.5±0.4a19.2±0.4a18.7±0.5aT44 50017.0±0.3a15.3±0.3a15.3±0.3a17.6±0.3a19.4±0.3a18.7±0.3aT56 00016.8±0.2a15.6±0.3a14.4±0.5c16.6±0.2c17.2±0.4b18.6±0.3a
1)同列中不同的小写字母表示差异显著(P<0.05)Different lowercases in the same column indicate the significant (P<0.05) difference.
从不同处理时间生物碱含量的变化看,在处理60和180 d时,各处理组的生物碱含量无显著差异;在处理30 d时,T4和T5处理组的生物碱含量差异不显著,但显著高于其他处理组;在处理90 d时,T4处理组的生物碱含量最高,且显著高于其他处理组;在处理120和150 d时,T3和T4处理组的生物碱含量无显著差异,但显著高于其他处理组。总体上看,T3和T4处理组的生物碱含量维持在较高水平。
与处理30 d时相比,处理结束(180 d)时各处理组金钱莲的总黄酮和生物碱含量分别增加19.7%~50.0%和10.0%~20.0%, T2、T3、T4和T5处理组的多糖含量增加2.4%~14.4%,仅T1处理组的多糖含量降低14.2%,表明较长时间的光照可以使金线莲叶片中总黄酮含量较大幅度增加。此外,处理结束时T3处理组的多糖、总黄酮和生物碱含量分别较处理30 d时增加14.4%、50.0%和14.7%,增幅均较大,说明适度的光照有利于金线莲叶片中各药用成分的合成和积累。
3 讨论和结论
以金线莲为代表的全草类、阴生药用植物生产明显有别于大多数喜光药用植物的生产,其产量构成更多来源于全株的营养器官。金线莲的叶片、茎及地下肉质根是构成其产量的主体部分,特别是其叶片占全株的比例较大,因此,合理调控金线莲株型、促进茎叶长势及增加叶片数量有利于提高金线莲的产量和品质。相关研究结果[8]表明:光照是影响和调控金线莲产量构成的核心支配因子。陈黎明等[15]发现,在三七〔Panaxnotoginseng(Burkill) F. H. Chen ex C. Chow et W. G. Huang〕的栽培过程中,随光照强度的增加,其植株茎部矮化、变粗,适宜的光照强度可以显著促进三七地上部干物质的积累。本研究中,经500 lx光照处理后金线莲的株高较高,但其他的产量构成因子(如单株干质量)较低;经4 500 lx光照处理后金线莲的单株叶片数较多、叶片较长,单株鲜质量、单株干质量和折干率均较高;在6 000 lx光照条件下处理120~180 d,金线莲的根长、茎直径、单株鲜质量和单株干质量均明显高于其他处理组,但其叶绿素a、叶绿素b和总叶绿素含量均明显低于其他处理组;在实验设置的5组光照条件下,金线莲的根直径、茎直径、单株茎节数、单株叶片数、叶长和叶宽总体差异不明显。从上述结果中可以看出:在金线莲的生长过程中,不同器官生长和发育适宜的光照度并不一致,且其各产量构成指标对光照度变化的敏感性存在差异,其中,株高对光照度变化的响应较明显。因此,在进行金线莲生产设施配置时,需要综合考虑光照强度对其不同器官生长发育的影响。
目前,金线莲栽培所用种苗均为组培苗,从组培苗移栽到栽培大棚或林下环境中需要经历长时间、复杂的炼苗过程。特别是林下栽培的环境较为恶劣,环境胁迫因子较多,且金线莲的肉质根系及其生存所需要的过饱和湿度环境往往会使环境中的病原菌大量增殖[16],导致金线莲幼苗在林下等仿野生环境中难以生存,植株成活率较低。在各类逆境诱导因子中,光照能够有效提升植株体内抗逆生理效应[17]。在弱光条件下,因抗逆性机制的差异植物体内保护酶等相关抗逆性指标会发生不同程度变化[18]。本研究结果显示:金线莲体内不同的抗氧化酶对光照度变化的响应时间各异,SOD和POD活性的变幅在处理150 d时较大,CAT活性则在处理90 d时大幅度升高;此外,在多数时间各处理组间POD和CAT活性总体差异显著,在处理150和180 d时, 光照度6 000 lx处理组的SOD和CAT活性高于其他处理组,说明光照度增大可激发金线莲体内的自我保护系统。因此,在阴生植物的栽培过程中,可对光照条件进行合理调控以促进阴生植物抗逆能力的提高。
光照不仅对阴生植物的形态结构塑造具有重要的调控作用,对其内在的生理生化效应和次生代谢产物合成也有明显的诱导效应[19]。郑连金等[20]认为,光照强度过高可抑制金线莲总黄酮的积累,说明过高的光照强度不利于金线莲部分药用成分的积累。本研究结果显示:在光照度500 lx的条件下处理60~180 d,金线莲的多糖含量均较低;而在光照度3 000 lx的条件下处理180 d,金线莲的多糖、总黄酮和生物碱含量分别增加14.4%、50.0%和14.7%,增幅均较大;此外,光照度4 500 lx有利于金线莲多糖的积累,光照度3 000 lx有利于金线莲总黄酮的积累,光照度3 000和4 500 lx对金线莲生物碱含量均有一定的提升作用,表明金线莲的不同药用成分对生境中光照强度变化的敏感性存在明显差异,适度的光照有利于金线莲体内多糖、总黄酮和生物碱的积累。因而,在实际生产过程中,应充分考虑光照对各类药用成分代谢的作用机制,以期定向筛选出适宜的光照条件。
综合分析结果表明:光照度500 lx有利于金线莲幼苗株高的增加,但不利于其物质积累;光照度6 000 lx对金线莲根长等生长指标有促进作用,但对叶片中叶绿素的积累有明显的抑制作用;在光照度3 000和4 500 lx的条件下,金线莲植株的株高适宜、叶片数较多、叶片较长,且可使其物质积累量增加,并能促进多糖、总黄酮和生物碱的积累,在维持一定生长量的同时能提升金线莲的药用品质,因此,在金线莲实际栽培过程中采用光照度3 000~4 500 lx较为适宜。
