燃烧反应机理构建的极小反应网络方法
----氢氧燃烧
2020-04-13李象远申屠江涛李宜蔚李娟琴王静波
李象远,申屠江涛,李宜蔚,李娟琴,王静波
(四川大学化学工程学院,空天动力燃烧与冷却教育部工程研究中心,成都 610065)
燃烧反应是以燃料和氧化剂为初始反应物的混合体系的典型复杂反应,在一定情况下反应体系自发进行的终点是化学平衡,化学平衡态是一个同时平衡状态.
为了描述燃烧反应的动力学过程,建立起了以基元反应为特征的复杂反应机理.随着对动力学模拟精度要求的进一步提高,引入越来越多的基元反应步骤,从最简单的氢气到目前的航空煤油燃烧,基元反应步骤数目越来越庞大,如AramcoMech 3.0机理[1]包含了C4以下的基元反应数超过2000个,而对一个航空煤油混合三组分替代燃料,详细基元反应近万步骤[2].由于反应类型和反应网络的选择不同,导致燃烧反应机理的基元反应数目大幅增加且缺乏通用原则[3].一般机理的基元反应只包含基态反应.燃烧反应中包含着大量激发态过程[4],燃烧发光便是激发态物种存在的表现,但目前的详细机理基本不包括这些激发态反应.可见,试图对燃烧过程的反应网络进行详尽描述目前是不可能的,任何详细燃烧反应机理都无法将所有可能的基元过程包含进来.
越来越详细的反应机理对帮助了解化学反应细节具有重要意义[5~8],但是,试图构建完整的化学反应网络的处理方式也带来其它问题.首先,考虑基态反应、激发态反应和各种中间物种的完整反应网络目前难以做到; 其次,动力学模拟的可靠性除了反应网络,还取决于热力学和动力学参数.目前的实验和计算水平数千焦耳的活化能垒计算误差将带来数倍的速率常数偏差,由于受限动力学和热力学参数精度,目前构建的详细机理要对标点火延迟及层流火焰速度等实验结果进行整体优化[9].另外,燃烧机理构建仍以反应和流动耦合的燃烧流场的数值计算应用为主,因为计算能力所限,燃烧流场计算要求燃烧反应机理尽量简单,所以越来越庞大的燃烧反应机理与实际应用存在较大差距.
尽管燃烧反应机理研究得到了快速发展,但由于机理构建缺乏统一规则,同种燃料,不同发展燃烧机理一般不相同.这种多样化机理由于反应类型、反应途径和动力学参数等没有可比性和可迁性,对机理的可靠性分析、判断和优化存在困难.
1 同时化学平衡和极小反应网络方法
任何复杂的化学反应进行的方向都是化学平衡.如氢氧燃烧的总包反应:

(1)
燃烧完成时,3种气相组分H2(g),O2(g)和H2O(g)的浓度由化学平衡常数确定.如果考虑这3个物种达成的化学平衡体系,在给定初始投料量情况下,式(1)所示的一个反应就足以确定体系的最终平衡浓度.从化学平衡角度看,要确定N个物种的化学平衡体系的平衡浓度,独立化学反应的数目是有限的,其它所有反应均可通过独立反应的线性组合得到.对于一个化学反应:
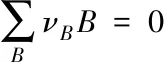
(2)
根据化学势判据,反应达到平衡时,各物种化学势满足:
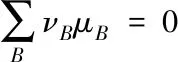
(3)
式中:B为化学物种;νB为计量系数.可将M个化学反应达到同时平衡时的化学势表示为如下齐次方程组:
Aμ=0
(4)
式中:A为反应计量系数矩阵;μ为化学势列矩阵.A矩阵的秩为该反应体系的独立反应方程数.确立独立反应数的另一种方法是对于N个物种的复杂反应机理,独立反应数F为[10]
F=N-L
(5)
式中:N为物种数目;L为体系原子矩阵的秩.如对于目前大量使用的氢氧燃烧机理[4,11~13],一般采用H,O,H2,O2,OH,HO2,H2O2和H2O等8物种,构建的机理无论多么复杂,但确定同时化学平衡的独立反应数只有6个.
一个化学反应,物种标准态化学势满足如下关系,且唯一地确定了反应的标准平衡常数,即
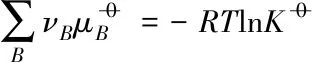
(6)
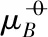
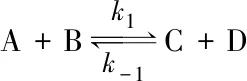
(7)
反应达到平衡时,
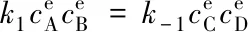
(8)
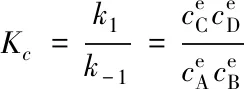
(9)
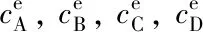
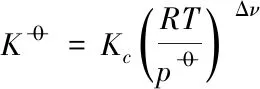
(10)
式中:p0 —为标准压力; Δν为反应的计量系数代数和.
可以注意到,上述F个独立反应的确定方式是热力学处理,不包含动力学信息.从初始状态(初始投料)经历足够长时间后,所有反应均达到化学平衡.化学反应的过程是各物种从初始浓度向最终平衡浓度变化的过程,这个过程的推动力就是化学势.化学势对反应方向的判据是吉布斯自由能判据在多组分反应系统的应用,本质上是熵增原理在等温等压条件下的判据形式,而燃烧反应动力学就是以研究这个过程为目的.
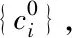
这种从热力学平衡原理导出的复杂反应的极小化反应网络方法(Minimized Reacrion Network,MRN),是一种基于热力学确定极小反应网络、进而确定动力学参数的机理构建方法.由于反应速率常数的实验测量存在较大误差,不同的速率常数值相差数倍属于正常,因此,假设将多个反应通道反应的贡献压缩到一条通道表示,即便将压缩后通道的反应速率常数放大数倍,仍然在实验误差范围内.这便是极小化反应网络方法压缩反应通道数的合理性保证.这样将在保持化学物种数不变的条件下大量压缩基元反应数目,对机理的实际工程应用具有重要意义.
2 氢氧燃烧反应机理
从核心机理到大分子燃烧机理都包含了氢氧燃烧子机理.已有对氢氧燃烧的详细研究.如Olm等[14]考察了1999~2013年期间发布的19个包含氢氧燃烧相关的机理在模拟不同工况时与实验值的误差,认为其中Kéromnès等[12]的机理能最好地预测实验结果.Konnov[4]论述了激发态在氢氧燃烧中的作用,随后对原先的氢气机理进行优化[13].而构建完整的反应网络尤其对大分子燃料而言是一项难以完成的任务,为匹配工程实际应用需求应尽可能缩小燃烧反应机理的尺寸.氢氧燃烧是最基础的反应系统,因此本文首先将极小反应网络方法应用到氢氧燃烧机理构建中,并通过动力学模拟论证方法的可行性.
2.1 机理构建
2.1.1 反应网络构建 针对已知物种未知反应网络复杂体系,确定独立反应比较通用的方法是原子系数矩阵法[10].针对已知物种的已知反应网络复杂体系,可以通过化学计量系数矩阵法[15]确定独立反应.
通过一种比较简便的方法快速写出所有独立反应.首先需确定机理的物种组成,目前大部分氢氧燃烧机理的物种包括H2,O2,H,O,OH,HO2,H2O2和H2O等8个物种,由于这些物种都由H和O原子组成,只需选定2个合适的起始物种,并保证其它物种均能由这2个起始物种生成.需要注意的是,独立反应与起始物种选择有关.对于燃料燃烧反应,一般选取主燃料和O2作为起始物种.对于氢氧燃烧,将H2和O2确定为起始物种是合适的,可得到由这2个物种反应生成其它物种的可能的计量方程式如下:

(11)

(12)

(13)

(14)

(15)

(16)
此即包含8个物种化学平衡体系的6个独立反应.独立反应数由式(5)确定.
通过对现有的反应机理做代数处理也可以得到独立反应,条件是原机理的反应计量系数矩阵A的秩要保证齐次方程组[式(4)]有非零解.将AramcoMech 3.0[1],UCSD[16],USC-Mech Ⅱ[17]等机理中共同包含的氢氧燃烧19步反应列于表1,产物化学计量系数为正,反应物化学计量系数为负.为了简便,可将H2和O2代表的化学计量系数置于矩阵最后两列(起始物种).
对表1所示化学计量系数矩阵进行处理,结果如表2所示.由表2可得矩阵的秩为6,即表明19步反应构成的氢氧燃烧机理独立反应数为6,与式(5)的结论一致.显然,表2是一个阶梯型矩阵,给出的6个独立反应和上述6个独立反应相同.可见,根据式(4)齐次方程组如果选择相同起始物种,可以得到相同的独立反应.表1中19个基元反应均可通过这6个独立反应线性组合得到.
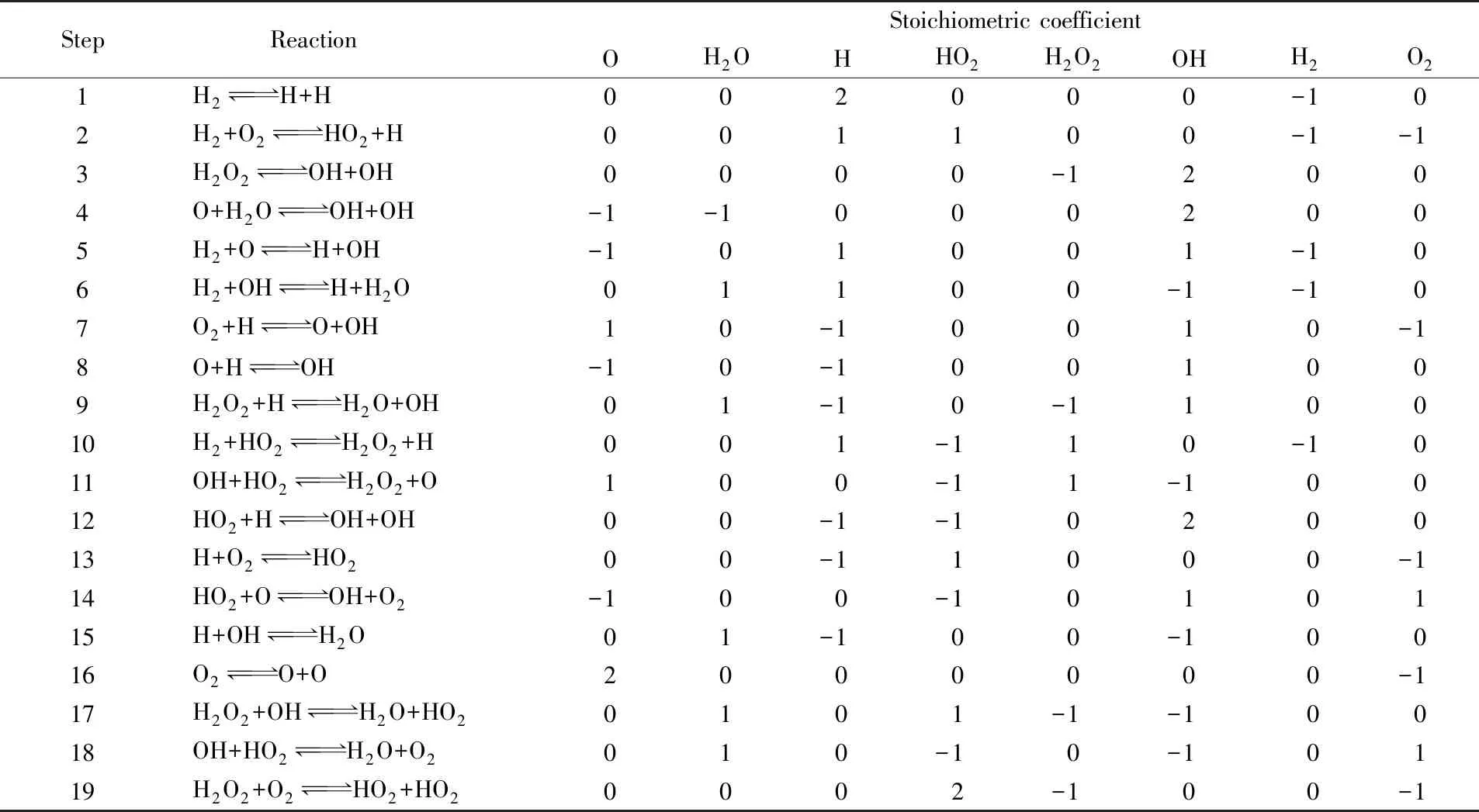
Table 1 Stoichiometric coefficient matrix of 19 reactions in hydrogen combustion mechanism

Table 2 Matrix reduction of hydrogen combustion mechanism
从热力学角度考虑,用6个独立反应平衡常数可以获得8个组分的燃烧反应末态浓度,但根据平衡常数与正逆反应速率常数的关系式[式(9)],要描述一个反应的动力学过程还需要获得反应的k1或k-1,如果可以获得这6个反应的速率常数即完成了反应机理的构建.但是,由于6个独立反应中有总包反应或非基元反应步骤,缺乏这类反应的k1或k-1数据,要实现燃烧机理的动力学描述,只能将缺乏速率常数的反应拆分成能获得速率常数的反应步骤的组合.这样,机理的反应数目可能会适当增加到f个(f≥F),为了获得反应步数较少的反应机理,应尽量避免这种取代,因为这种组合取代不唯一.

2.1.2 动力学参数 动力学参数决定燃烧反应随时间的演变和体系达到化学平衡的时间.文献[18~20]报道了大量的基元反应动力学数据,包括实验数据和理论计算数据.随着互联网及数据技术的发展,动力学数据的在线获取变得非常便捷.在化学动力学数据方面,NIST数据库[21]被广泛使用,四川大学开发的燃烧数据库平台也已经上线运行[22].
随着实验手段的发展、理论的完善和计算水平的提升,理论和实验得到的动力学参数精度都得到了一定提升.由于理论方法和测量技术的限制,高精度反应动力学参数的获得仍较困难,大量基元步骤的速率常数都存在一定的不确定度.
目前的燃烧反应机理体系,包括Chemkin-Pro[23]等化学动力学模拟软件的速率常数均采用所谓扩展Arrhenius方程的三参数形式,即
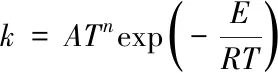
(17)
式中,A为指前因子;T(K)为温度;n为温度指数;E(J/mol)为活化能;R(8.314 J·mol-1·K-1)为普适气体常数.为了还原活化能E的物理意义和压缩变量空间以利于机理整体优化,本文提出将反应速率常数采用如下所示的Arrhenius双参数形式:

(18)
这样有利于燃烧机理的构建和简化[24].结合表3中反应R1~R9反应速率常数的实验和计算结果,对这9步反应的动力学参数进行了整体优化,构建的氢氧燃烧机理及反应动力学参数列于表3,表中M为第三体,Third-body efficiencies为三体碰撞系数,Low pressure limit为低压极限速率常数,动力学参数的具体处理过程见表S1~表S9和图S1~图S9(见本文支持信息).

Table 3 Kinetic parameters of reaction mechanism for hydrogen combustion through
为区别于其它机理,基于极小化反应网络方法(MRN)的机理简称为MRN-C0.构建的氢氧燃烧机理中所有物种的热力学参数和输运参数均来自AramcoMech 3.0机理[1].基于上述处理,初步形成了氢氧燃烧的8个物种9步反应双参数机理.氢氧燃烧机理是MRN-C0燃烧机理的基础,在氢氧燃烧基础上可进一步构建更大分子燃料的详细机理.
2.2 机理验证
燃烧反应机理的可靠性需要通过动力学模拟对标准实验数据进行验证,目前,已报道了大量氢氧燃烧相关的实验数据[25~30].本文对采用MRN方法构建的氢氧燃烧机理进行了点火延迟时间和层流火焰速度的模拟验证,并与实验值和AramcoMech 3.0[1],UCSD[16],USC-Mech II[17]等核心机理的模拟结果进行了对比,所有机理模拟工作均采用Chemkin-Pro程序包[23]完成.
2.2.1 点火延迟时间 点火延迟时间用于衡量燃料实际燃烧特性,同时也是验证燃烧反应机理合理性和正确性的重要指标,测量点火延迟时间的实验设备主要有激波管和快速压缩机.本文所构建的氢氧燃烧机理与其它核心机理在Herzler等[31]和Zhang等[32]所做激波管实验工况下的点火延迟时间模拟结果分别见图1和图2.总之,本文构建氢氧燃烧机理的点火延迟时间基本上与其它几个机理有相同精确度,能够再现高温区点火延迟时间的实验结果.
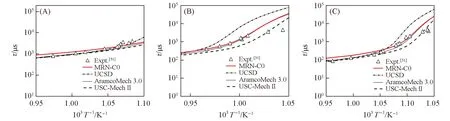
Fig.1 Ignition delay time predicted by different mechanisms compared with experiment data(A) H2/O2/Ar=3.46%/3.49%/93.05%,p=0.1 MPa; (B) H2/O2/Ar=3.46%/3.49%/93.05%,p=0.4 MPa; (C) H2/O2/Ar=5.87%/2.95%/91.18%,p=0.4 MPa.
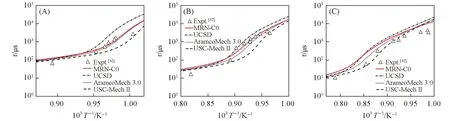
Fig.2 Ignition delay time predicted by different mechanisms compared with experiment dataH2/O2/Ar=3.47%/3.47%/93.06%.(A) p=0.5 MPa; (B) p=1 MPa; (C) p=2 MPa.
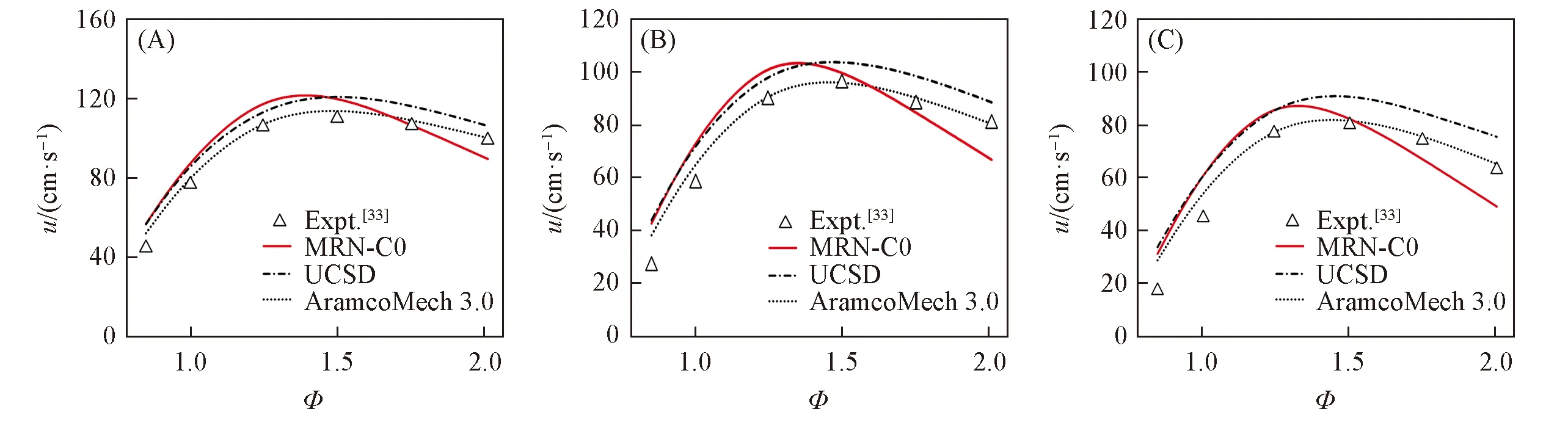
Fig.3 Laminar flame velocity predicted by different mechanisms compared with experiment dataT=298 K,O2/(O2+He)=0.08; (A) p=1.013 MPa; (B) p=1.520 MPa; (C) p=2.026 MPa.
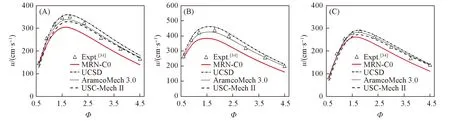
Fig.4 Laminar flame velocity predicted by different mechanisms compared with experiment dataT=298 K,p=0.1013 MPa; (A) O2/(O2+Ar)=21%; (B) O2/(O2+He)=21%; (C) O2/(O2+N2)=21%.
2.2.2 层流火焰速度 火焰传播速度对于研究机理的燃烧特性和研究传质传热过程有重要作用.进一步考察了MRN方法构建的氢氧燃烧机理在预测层流火焰速度方面的性能.本文给出了对所构建的氢氧燃烧机理及其它核心机理在一些工况下层流火焰速度随摩尔比变化的模拟结果,在Tse等[33]所做实验工况下的层流火焰速度(u)随燃料当量比(Φ,燃料-氧气实际燃烧的体积比除以燃料-氧气实际燃烧的化学恰当体积比)变化的模拟结果见图3,在Kwon等[34]所做实验工况下的模拟结果见图4,本文构建的机理总体能再现实验趋势,对层流火焰速度的预测性能还有待进一步优化.
3 结 论
基于复杂化学反应的同时平衡原理和化学势判据,确定描述复杂燃烧反应体系化学平衡状态所需的最小化学反应数目即独立反应数.理论上,燃烧反应的动力学过程可通过这些独立反应的正逆反应速率常数来描述.提出的极小化反应网络方法MRN能够大幅度减少化学反应基元步骤的数量,压缩机理整体优化的变量空间,降低详细机理的简化难度.将MRN方法应用于氢氧燃烧的机理构建,实践表明,通过合理的速率常数调整,可以在保持机理物种种类和数目不变的同时保证机理的模拟精度.此外,反应速率常数还原为回归化学反应活化能物理意义的Arrhenius方程的双参数形式,保证了速率常数的物理意义和可迁性.确定由8个物种组成的氢氧燃烧独立反应数F=6,对缺乏速率常数的反应做了组合替代,构建了f=9的燃烧详细机理MRN-C0.模拟结果表明了极小化反应网络方法构建燃烧反应机理的可行性.
支持信息见http://www.cjcu.jlu.edu.cn/CN/10.7503/cjcu20190568.