羟基改性聚对亚苯基苯并二唑单体3,3′-二氨基-4,4′-二羟基联苯盐酸盐的合成
2020-04-11吴纯鑫常雨淅陈迪超张建庭金宁人赵德明
吴纯鑫,常雨淅,陈迪超,张建庭,金宁人,赵德明
(浙江工业大学化学工程学院,浙江杭州310014)
关于DADHBP·2HCl 的合成,现有文献以4,4′-二羟基联苯为原料经硝化后,以水合肼为还原剂,钯碳为催化剂进行催化还原制得目标产物,但该路线存在反应时间长,成本高等缺点[9]。因此,本文以缩短合成时间和减少生产成本为目标,以4,4′-二羟基联苯为原料,经硝化,七水合硫酸亚铁为助剂还原合成DADHBP·2HCl。路线中采用水合肼,七水合硫酸亚铁还原方法较水合肼钯碳还原方法的优势为价格更为便宜,其对硝基还原的选择性好,对比钯碳还原降低成本,且还原效果显著。其工艺路线如图1所示[14]。经实验优化后,得到高纯度中间体3,3′-二硝基-4,4′-二羟基联苯(DNDHBP)和单体3,3′-二氨基-4,4′-二羟基联苯盐酸盐(DADHBP·2HCl),中间体和产品结构经红外光谱、核磁氢谱和电喷雾质谱表征确认。
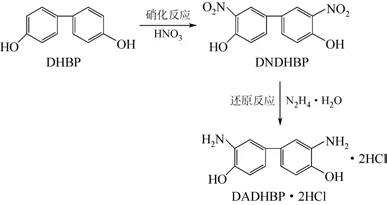
图1 单体3,3′-二氨基-4,4′-二羟基联苯盐酸盐的合成路线
1 实验部分
1.1 主要试剂与仪器
4,4′-二羟基联苯(DHBP)、氯化亚锡、乙醇,均为分析纯,上海麦克林生化科技有限公司;甲苯,分析纯,华东医药股份有限公司;冰乙酸、甲醇,均为分析纯,永华化学科技(江苏)有限公司;N,N-二甲基甲酰胺、浓盐酸,均为分析纯,西陇科学股份有限公司;浓硝酸,分析纯,浙江中星化工试剂有限公司;活性炭、水合肼,均为分析纯,上海阿拉丁生化科技股份有限公司;七水合硫酸亚铁,分析纯,国药集团化学试剂有限公司。
Avance-2型核磁共振仪(1H NMR),瑞士布鲁克公司; Jasco FT/IR-460plus 型红外光谱仪(FTIR),美国Thermo Scientific 公司;ITQ 1100TM直接进样杆离子阱质谱仪(ESI-MS),美国Thermo Scientific 公司;高效液相色谱LC-20A型液相色谱仪(HPLC,面积归一法,室温流动相40%乙腈-水缓冲溶液,流速1.0mL/min,检测波长254nm),岛津(中国)有限公司。
1.2 实验过程及方法
1.2.1 DNDHBP的合成
在装有温度计及球形冷凝管的250mL 四口烧瓶中,依次加入5.00g 4,4′-二羟基联苯、25mL 甲苯、35mL 冰乙酸,搅拌,5℃下加入3.8mL 硝酸(质量分数为65%),然后反应2.5h,冷却至室温,抽滤,用水、甲醇分别洗涤滤饼,滤饼烘干得到黄色产物3,3′-二硝基-4,4′-二羟基联苯,HPLC 分析得质量分数92.43%,以4,4′-二羟基联苯计收率81.39%,重结晶后备用。
分析反应机理以及DNDHBP 的质谱图可推知,该步硝化反应的副产物为3-硝基-4,4′-二羟基联苯,表征结果如下。
FTIR(KBr,cm-1):3224(s)、3090(s)、1520(s)、1310(s)、1239(s)。
1H NMR(二甲基亚砜DMSO,化学位移δ):11.13(s,2H,OH),8.14(2H,s,ArH),7.86(2H,s,ArH),7.20(2H,s,ArH)。
C12H8N2O6ESI-MS:[M H]+=275.0。与DNDHBP理论相对分子质量相同
1.2.2 DADHBP·2HCl的合成
在装有温度计及球形冷凝管的250mL 四口烧瓶中,依次加入2g DNDHBP、0.60g活性炭、0.20g七水合硫酸亚铁和20mL 无水乙醇,回流搅拌,缓慢滴加1mL 水合肼,反应9h 后停止,热过滤,将滤饼溶于12mL 5%(质量分数)稀盐酸,过滤除去杂质,盐析,抽滤,滤饼真空干燥,得到白色固体产物3,3′-二氨基-4,4′-二羟基联苯盐酸盐,HPLC分析质量分数98.20%,以DADHBP计收率为67.16%,表征结果如下。
FTIR(KBr,cm-1):3371(s)、3291(s)、2954(s)、1600.3(s)、1219(s)。
1H NMR(DMSO,δ):10.96(2H,s,OH),10.13(3H,s,NH2·HCl),7.57(2H,s,ArH),7.40(2H,s,ArH),7.18(2H,s,ArH)。
C12H12N2O2ESI-MS:[M+H]+=217.1。与3,3′-二氨基-4,4′-二羟基联苯(DADHBP)理论相对分子质量相同。
2 结果与讨论
2.1 DNDHBP的合成
2.1.1 反应溶剂种类对DNDHBP合成的影响
反应溶剂种类对硝化反应的选择性和反应速率影响较大,为提高硝化反应收率和产物纯度,在反应温度、物料配比和反应时间一定的条件下,考察反应溶剂种类对硝化反应的影响,结果见表1。
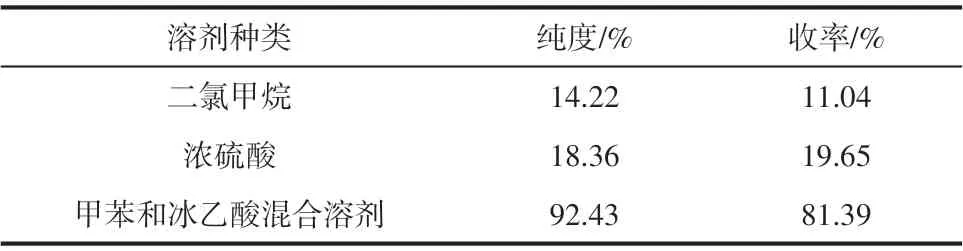
表1 反应溶剂种类对DNDHBP合成的影响
2.1.2 混合溶剂配比对DNDHBP合成的影响
混合溶剂配比对硝化反应有一定影响,选择合适的配比可以提高硝化反应的纯度和收率,结果见表2。
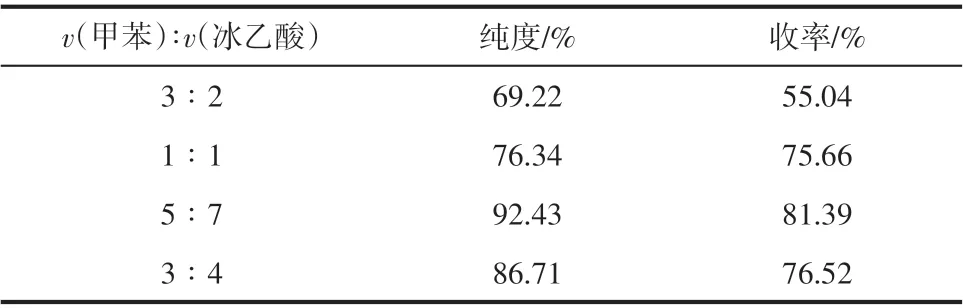
表2 混合溶剂配比对DNDHBP合成的影响
当甲苯与冰乙酸体积比为3∶2 时,硝化反应的收率较低,且后处理过程中有较多产品附着在杯壁上,乙酸有脱水剂的作用,一定程度上影响反应进行,乙酸含量过高时硝化反应不易控制,容易产生副产物导致产物和收率较低,乙酸含量较低时反应不完全,生成较多单硝化化合物。根据表2选择甲苯与冰乙酸体积比5∶7 为较佳溶剂配比进行硝化反应。
2.1.3 硝酸与DHBP 原料配比对DNDHBP 合成的影响
理论的硝酸与DHBP原料摩尔比为2∶1,在工业生产中硝酸用量常常高于理论量,以促进反应进行完全,但过量的硝酸又会产生多硝化副产物及污染环境,提高生产成本。探讨硝酸用量对硝化反产物纯度以及收率的影响,结果见表3。

表3 硝酸与DHBP原料配比对DNDHBP合成的影响
由表3可知,当硝酸配比低于2∶1时,硝化产物收率较低,而硝酸浓度较高时又会得到较多的副产物,且重结晶的方法无法去除这些杂质,故较佳的配比为理论配比,并且在此硝酸比条件下,4,4′-二羟基联苯与硝酸反应较充分,体现出较好的原子经济性。
2.1.4 反应温度对DNDHBP合成的影响
硝化反应是一个强放热反应,如果不及时移除热量,会使反应温度迅速上升,引起多硝化副产物的产生,因此探讨合适的反应温度,减少副产物的生成至关重要。探讨反应温度对硝化反应纯度及收率的影响,结果见表4。
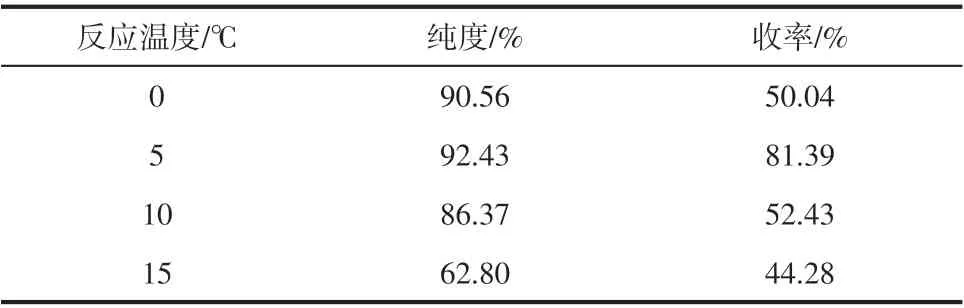
表4 反应温度对DNDHBP合成的影响
由表4 可知,温度为0℃的条件下反应已经发生,温度过低反应不完全导致纯度和收率都不够高,随着反应温度升高,产物收率逐渐提高,当反应温度高于5℃时,继续升高温度会引发其他副反应,导致反应的选择性下降。因此较佳反应温度为5℃左右。
2.1.5 反应时间对DNDHBP合成的影响
硝化反应时间的控制也很重要,反应时间较短会导致硝化反应不完全,而硝化时间过长又会发生副反应,生成多硝基产物,导致产率降低,且难以除去。故考察反应时间对硝化产物纯度以及收率的影响,结果见表5。
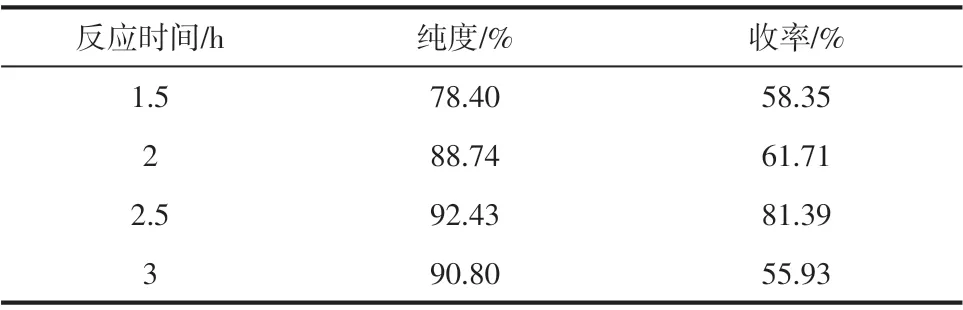
表5 反应时间对DNDHBP合成的影响
由表5可知,随着反应时间延长,产物收率逐渐增加,当反应时间为2.5h时,收率较高,继续延长反应时间收率下降,质谱检测有三硝化及四硝化等副产物生成。因此较佳反应时间为2.5h。
2.2 DADHBP·2HCl的合成
2.2.1 DADHBP还原方法对比
硝基还原的方法有很多,通常使用的方法有水合肼还原法、催化加氢、金属单质、SnCl2-HCl 法和保险粉还原等。各个还原反应各有优缺点,本文选择5种还原方法对DADHBP分别进行硝基还原实验,结果见表6。
表6结果表明,使用铁粉、保险粉和氯化亚锡作为还原剂的实验编号为1、2和3中还原硝基效果不好,主要原因是反应物溶解性较差,反应在非均相中进行,二硝基不能完全还原。而实验4中水合肼钯碳还原的效果不好是因为反应过程中产生的未知副产物难以除去。综合考虑,采用乙醇为溶剂水合肼七水合硫酸亚铁的还原方法。

表6 不同还原方法对产物的影响
2.2.2 七水合硫酸亚铁用量对DADHBP·2HCl合成的影响
考察七水合硫酸亚铁用量对DADHBP·2HCl合成的影响,结果见表7。
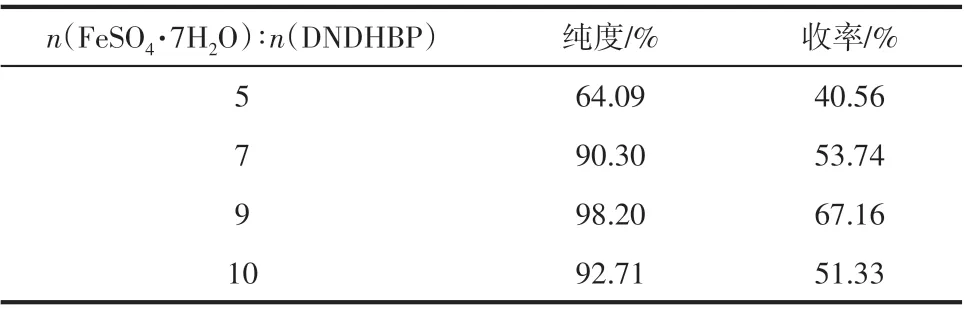
表7 七水合硫酸亚铁用量对DADHBP·2HCl合成的影响
七水合硫酸亚铁的用量对还原反应有一定的影响,由表7 可知,当n(FeSO4·7H2O)∶n(DNDHBP)=5∶1时,反应速度很慢,无法得到较多还原产物,随着七水合硫酸亚铁用量增加,在n(FeSO4·7H2O)∶n(DNDHBP)=9∶1时收率和纯度达到最高,其后再增加七水合硫酸亚铁用量,反应产品的纯度和收率变化不大,因此采用n(FeSO4·7H2O)∶n(DNDHBP)=9∶1为适宜的用量。
2.2.3 水合肼用量对DADHBP·2HCl合成的影响
还原反应一般不易进行且产物易氧化,还原硝基过程与大多数硝基还原成氨基相同,首先产生亚硝基或羟胺中间体,中间体继续被还原为氨基,还原反应需保证拥有足够的氢供体。水合肼在回流温度和助剂影响下完全转化一部分产生的活性氢参与反应,一部分没有参与反应直接逸出,需使用过量的水合肼才能达到较高的纯度和收率。因此探讨水合肼用量对DADHBP·2HCl 合成的影响,结果见表8。

表8 水合肼用量对DADHBP·2HCl合成的影响
硝基还原为氨基需足量的水合肼,由表8 可知,当物料摩尔比采用理论用量1∶4 时还原不完全,随着水合肼与DNDHBP 摩尔比的增大,产物的收率也随之增加,当二者的摩尔比达到1∶5.5时,纯度与收率较优。再继续增加水合肼的用量,收率没有提高。因此DNDHBP 与水合肼的较佳物料配比应以1∶5.5为宜。
2.2.4 反应时间对DADHBP·2HCl合成的影响
反应时间对产物制备的纯度及收率的影响尤其重要,反应时间过长会导致产物中杂质增加,反应时间过短还原反应不完全。探讨反应时间对DADHBP·2HCl合成的影响,结果见表9。
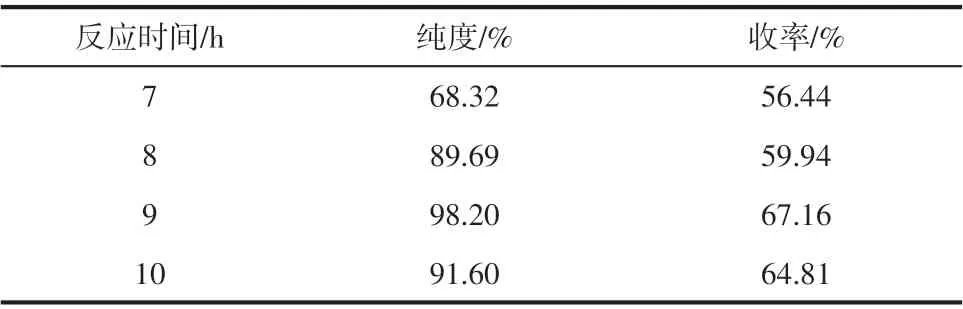
表9 反应时间对DADHBP·2HCl合成的影响
由表9可知,随着反应时间的延长,产物的收率也逐渐增大,反应时间9h 时产物的纯度及收率较佳,还原较完全,继续延长反应时间,收率略有降低。因此还原反应较佳的反应时间为9h。还原产物经质谱检测含有小于2%的单还原杂质3-硝基-3′-氨 基-4,4′-二 羟 基 联 苯,目 标 产 物DADHBP·2HCl 的纯度大于98%,达到聚合要求,可进行后续聚合反应。
3 结论
本文成功地以4,4′-二羟基联苯为原料制得了中间体DNDHBP、DADHBP·2HCl,并对其合成工艺条件进行了优化,产物用FTIR、1H NMR 和MS等方法定性表征,均符合其分子结构[15]。结果如下。
(1)DNDHBP 的合成 以4,4′-二羟基联苯为原料,甲苯冰乙酸为反应溶剂,反应温度5℃,反应时间2.5h,n(DHBP)∶n(HNO3)=1∶2,反应中缓慢滴加硝酸,防止温度升高,便于控制反应,得到3,3′-二硝基-4,4′-二羟基联苯,HPLC 分析得质量分数92.43%,收率81.39%。
(2)DNDHBP·2HCl 的合成 以DNDHBP 为原料,乙醇为反应溶剂,七水合硫酸亚铁为助剂,n(DNDHBP)∶n(N2H4·H2O)=1∶5.5,反应温度78℃,反应9h后,经热过滤和盐析,得到DADHBP·2HCl,收率67.16%,HPLC分析得质量分数为98.20%。
