韶关再次无偿献血者血液六个项目检测现状及对策
2020-04-09霍宝锋李慧文林奕斌刘智敏张天弼
霍宝锋 李慧文 林奕斌 刘智敏 张天弼
广东省韶关市中心血站,广东韶关 512026
随着韶关市医疗临床技术水平的不断提高,医疗临床对血液需求量持续增长,平均每年增长15%~20%。2017 年,全市无偿献血人数达49 894人次,总采血量达9.98 吨,与上年同期相比实际采血量增长0.8%。虽然供需矛盾日益增长,但为临床提供安全合格的血液的初衷不能改变。因此如何在保障安全的同时更大程度的满足临床需求成为我们血站亟待解决的难题。血液供应的源头在于无偿献血者,所以建立具备一定规模的低危自愿无偿献血者队伍,提高招募成功率和工作效率、成为切实解决血液短缺的有效举措。我们对韶关市中心血站近三年来,初次和再次无偿献血者的血液检验结果进行分析,比较初次和再次献血者不合格项目的差异,分析研究再次无偿献血者的优势、血液检测不合格因素和制订针对性招募策略,以便更好得保留固定无偿献血队伍,建立低危、逐渐强大的固定无偿献血者队伍,现报道如下。
1 资料与方法
1.1 一般资料
采用简单随机抽样法随机抽取2015 年1 月1日~2017 年12 月31 日韶关市中心血站92 549 人份无偿献血者血液标本的检测结果作为研究对象。纳入标准:年龄18 ~60 周岁、身体条件符合《献血者健康要求》(GB18467-2011)中的规定、采血后留取血液标本合格、规定时间内完成相关检测。按照是否第一次无偿献血将献血者分为初次献血者组和再次献血者组(再次献血者是指曾无偿捐献过一次及以上血液者;初次献血者为第一次无偿捐献血液者、包括成分献血者);按年份对比六个检测项目不合格情况。
1.2 试剂与仪器
初筛仪器、试剂:谷丙转氨酶(ALT)检测试纸(罗氏诊断产品有限公司)、乙型肝炎病毒表面抗原(HBsAg)检测试剂盒(英科新创科技有限公司)。血液筛查实验室使用试剂:谷丙转氨酶(ALT)检测试剂(贝克曼库尔特)、HBsAg 试剂(珠海丽珠、北京万泰)、抗-HCV 试剂(珠海丽珠、北京万泰)、抗-HIV 试剂(北京万泰、Bio-Rad)、抗-TP 试剂(珠海丽珠、北京万泰)。核酸试剂为中山大学达安生物科技有限公司配套试剂。HBsAg、抗-HCV、抗-HIV和抗-TP 的室内质控物均来自康彻斯坦有限公司,以上试剂均经过批批检定合格,且在有效期内使用。血液筛查实验室仪器:贝克曼4800 生化分析仪、KH80 型离心机、TECAN Evo/200 全自动加样器、BEP Ⅲ全自动酶免分析仪,核酸提取仪为中山大学达安生物科技有限公司DA3000、核酸扩增仪为ABI7500。
1.3 方法
初筛项目检测:ALT 采用干化学法,HBsAg 采用试纸条法。血液筛查:ALT 检测采用速率法,检测数值>50U/L 判为阳性。HBsAg、抗-HCV、 抗-HIV、抗-TP 采用ELISA 法,同时采用2 种不同厂家试剂检测,严格按说明书要求进行操作,核酸检测为HBV/HCV/HIV 8 混样分项目检测模式。结果<cutoff 值判为合格,结果≥cutoff 值判为反应性;如果只有1 种试剂反应性而另1 种试剂合格,则判定为该标本待查,需用两种试剂分别做双孔复检,复查结果任何一种试剂任一孔反应性或2 孔均反应性均判为不合格,两种试剂两孔均无反应性判为合格。HIV 筛查反应性标本送韶关市疾控中心确认。
1.4 统计学处理
应用SPSS19.0 软件,采用χ2检验,P <0.05 表示差异有统计学意义。
2 结果
2.1 初次与再次献者血液检测不合格结果比较
初次献血者中六个项目合计不合格率高达5.57%。其中HBsAg 不合格率最高(1.96%),其次为ALT(1.38%)、抗-TP(1.18%),核酸检测不合格率最低(0.21%);再次献血者中六个项目不合格率为1.89%。其中ALT 不合格率最高(1.33%),其次为核酸检测(0.13%)、HBsAg(0.12%)、抗-HCV(0.12%)、抗-TP(0.10%),抗-HIV 不合格率最低(0.09%)。再次献血者因为经过上次献血时的筛选,故合格率较高。初次献血者HBsAg、抗-HCV、抗-TP、抗-HIV 及核酸不合格率高于再次献血者,差异有统计学意义(P <0.05)。见表1。
2.2 再次献血者血液检测不合格项目情况
2015 ~2017 年再次献血者血液检测总不合格率为1.16%,其中ALT 占比最大(0.83%),其次为核酸检测(0.09%),HBsAg 不合格率最低(0.05%)。三年间再次献血者ALT、HBsAg、抗-HCV、抗-TP、抗-HIV 不合率相比较,差异无统计学意义(P >0.05)。三年间再次献血者核酸不合格率逐年升高,相比较差异有统计学意义(P <0.05)。2015 年底开展核酸检测,随着检测系统的稳定和实验条件的优化,检出率有所提高;另外检测试剂的高敏感性带来的假反应性不容忽视。见表2。
2.3 再次献血者血液检测单试剂不合格项目比较分析
2015 ~2017 三年中再次献血者HBsAg 单试剂不合格者合计5 例,占此项目不合格人数的71.43%(5/7);抗-HCV 单试剂不合格者合计9例,占此项目不合格人数的100%(9/9);抗-HIV单试剂不合格者合计7 例,占此项目不合格人数的87.50%(7/8);抗-TP 单试剂不合格者合计8 例,占此项目不合格人数的88.89%(8/9)。三年间再次献血者血液检测单试剂不合格项目相比较,差异无统计学意义(P >0.05)。见表3。
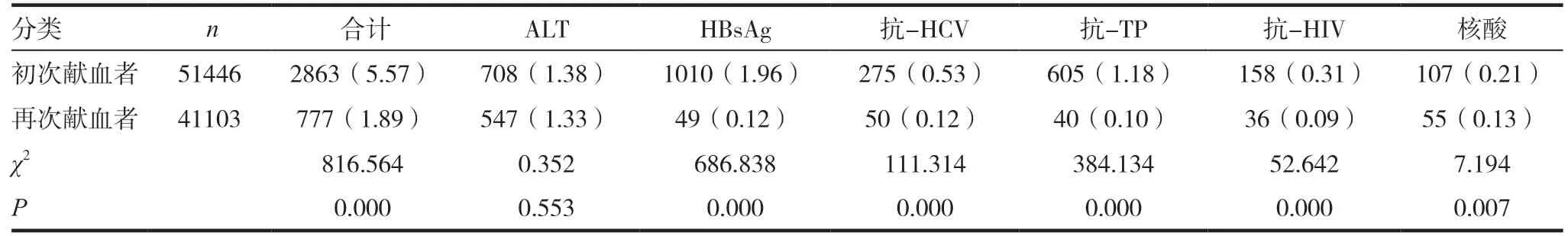
表1 2015~2017初次与再次献者血液检测不合格结果比较[n(%)]
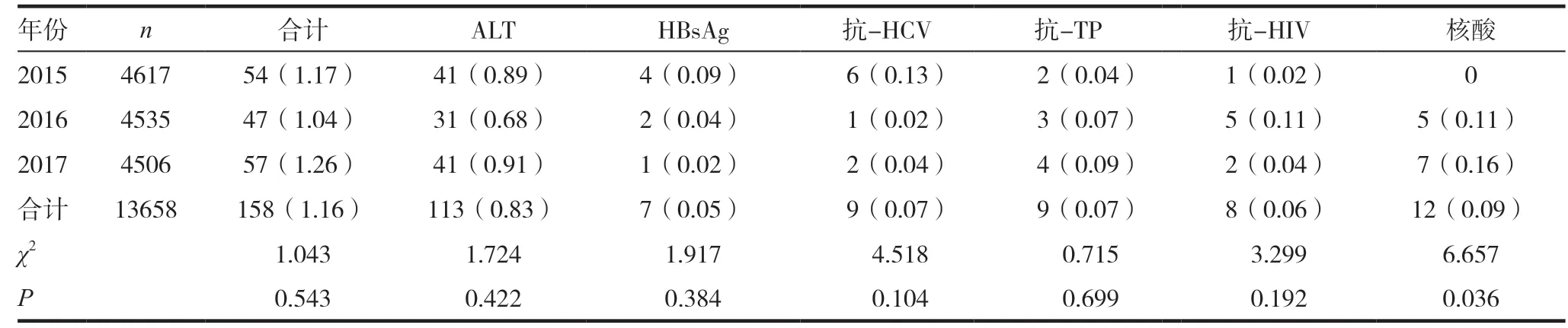
表2 2015~2017再次献血者血液检测不合格项目比较[n(%)]
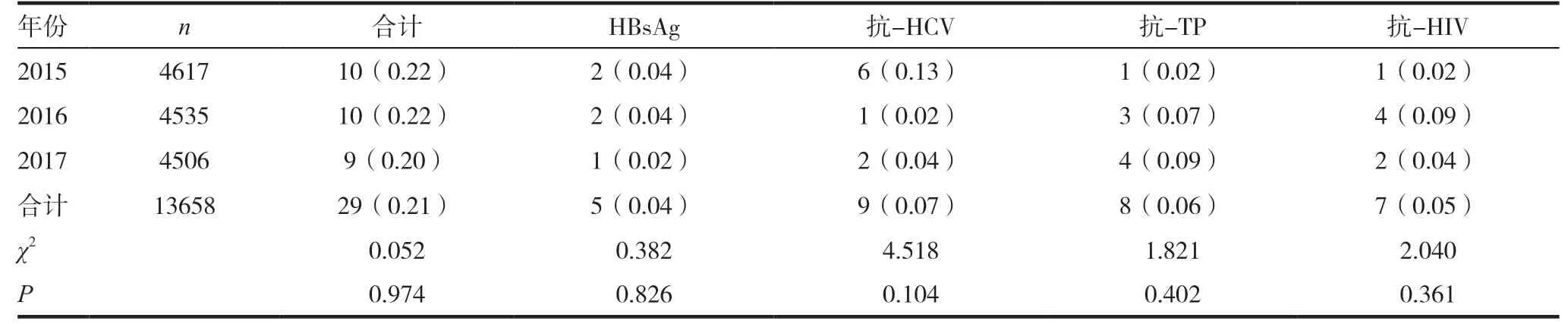
表3 2015~2017再次献血者血液检测单试剂不合格项目比较[n(%)]
3 讨论
本研究数据显示:本站2015 ~2017 初次献血者51 446 人,占比55.59%,比同期北京地区(53.5%)略高[1];再次献血者41 103 人,占比44.41%。可见本单位对新献血者的招募工作做的很好,但献血者的保留工作有待提高。初次献血者中六个项目合计不合格率高达5.57%。其中HBsAg不合格率最高(1.96%),虽然献血前用金标试纸进行初筛,但HBsAg 筛查不合格率还是占不合格项首位,其原因可能是一些大型采血前初筛量大,为避免拟献血者等待时间过长,临时取消了采血前初筛HBsAg;金标试纸的使用和保存等不恰当因素影响结果判定;结果还发现初筛抽血出现溶血,标本量过多、过少,会影响整个实验检测结果。研究还发现,由于金标试纸条本身灵敏度不高;也可导致工作人员观察未按要求在15 ~30min 内判读,进行也可造成漏检。可以采取以下措施:大型采血时增加,进行采血前初筛HBsAg 的工作人员,确保对每个献血者做HBsAg 初筛。再次献血者中六个项目合计不合格率为1.89%。其中ALT 不合格率最高(1.33%),因为ALT 影响因素比较多,需要我们对再次献血者进行献血前应注意事项的告知工作。大型采血时增加,进行采血前初筛ALT 的工作人员,确保对每个献血者做ALT 初筛[2]。
2015 ~2017 年三年中再次献血者单试剂不合格项目按从高到低的顺序为:抗-HCV(100%)、抗-TP(88.89%)、 抗-HIV(87.50%)、HBsAg(71.43%)。可见,ELISA 实验中单试剂反应性是再次献血者血液检测不合格的主要原因,特别是抗-HCV(100%)。丙肝是输血后肝炎的主要类型,占输血后肝炎80%以上[3-4]。2004 ~2016 年我国居民病毒性肝炎发病率呈小幅下降后走平趋势,但仍然处于高位,丙肝发病率呈上升趋势,年均增长14.4%[5-7]。再次献血者不合格项目传染性指标以核酸检测、抗-TP 和抗-HIV 为主,分别占不合格人数的0.09%、0.07%和0.07%。再次献血者短期内传染性指标检测理应不会太大变化。产生变化的原因[8]有:(1)献血者感染了相应的病毒并产生了抗体,或者上次献血时处于窗口期;(2)此次检测结果假阳性。本研究数据中再次献血者单试剂不合格所占比值也说明了这一问题[9-11]。(3)操作失误造成不正确结果。核酸检测不合格者在初次和再次献血者中所占比例都很高,主要是HBV 检测不合格。其主要原因为:(1)献血者隐匿性HBV 感染(OBI)客观存在。(2)核酸检测技术用于血液筛查其检测灵敏度明显高于ELISA 血清学检测方法[12-13]。除了方法学原因造成的假阳性之外,也有检测系统稳定性、国产试剂质量和操作不当等引起的假阳性[14]。(3)捐献血液之后感染了病毒[15]。
综合上述结果,再次献血者中以ALT 和核酸检测不合格为主。ELISA 实验中单试剂反应性是再次献血者血液检测不合格的主要原因。为了尽可能的降低检测不合格率,避免血液资源的浪费,应做到加强宣传教育,提高献血人群对献血的认知度,了解经血传播疾病,倡导健康的生活方式。保持一个有充足数量的低危无偿献血者队伍,加强固定献血者队伍建设。改进献血者的初筛和血液检测过程,加强专业人员的责任心,杜绝因工作失误造成漏检。选择质量好的酶免检测试剂,结合核酸检测技术,提高检测的特异度。制订针对再次献血者的招募策略以及保留固定献血队伍的有效措施,并且针对固定献血者制定归队程序。
