超积累植物伴矿景天镉耐受基因SpMT2的分离及功能鉴定
2020-04-09彭佳师易红英龚继明
彭佳师,易红英,龚继明
1 湖南科技大学 生命科学学院 重金属污染土壤生态修复与安全利用湖南省高校重点实验室,湖南 湘潭 411201
2 中国科学院分子植物科学卓越创新中心/植物生理生态研究所 植物分子遗传国家重点实验室,上海 200032
重金属超积累植物由于其高积累与高耐受重金属的特性,不仅可以直接用于环境污染的植物修复,还可以在深入解析其高富集和高耐受重金属机理的基础上为植物修复技术提供基因资源和研究思路。对十字花科“模式超积累植物”叶芽鼠耳芥 Arabidopsis halleri和天蓝遏蓝菜 Thlaspi caerulescens的研究表明,除了关键的转运蛋白如ZIP (ZRT and IRT-like protein) 家族蛋白、HMA4(Heavy metal ATPases 4) 和MTP (Metal Transport Protein) 等的组成型高表达外,一些金属螯合物如组氨酸 (Histidine) 和NA (Nicotinamine) 等在超积累植物耐受和富集重金属的过程中也发挥着重要的作用[1]。然而,人们对另一类广泛存在于植物体内的金属螯合蛋白——金属硫蛋白(Metallothioneins,MTs) 在超积累植物耐受和富集重金属的过程中所发挥的作用却知之甚少。
金属硫蛋白是一类富含半胱氨酸(Cys)并能够结合多种重金属如锌 (Zn)、镉 (Cd) 以及铜(Cu) 等的小分子蛋白。已有的证据表明,MTs在植物体内金属离子胁迫的解毒过程中发挥着重要作用[2]。植物金属硫蛋白家族在序列和功能上虽具多样性,但大多数被子植物MTs在序列的两端富含Cys,并且一般具有4种相对保守的Cys排列顺序,从而将植物 MTs分为 4种类型[2-3]。而对于重金属超积累植物,大量的研究证实一些MTs家族成员的表达水平远高于其近亲非超积累植物,这暗示它们可能参与了其超富集和超耐受重金属的过程[4-7]。这些 MTs在酵母、拟南芥或烟草中表达后能提高对重金属的抗性[6-11]。然而,遗传学的证据表明MTs的高表达并没有与超积累植物对重金属的超耐受性连锁[7,11-12]。这也就使MTs在超积累植物富集和耐受 Cd的过程中的作用至今仍未被人们所解析。
伴矿景天Sedum plumbizincicola是近期在中国发现的景天科超积累植物新种[13-14]。地上部重金属超量积累以及较大的生物量和实验室种植方便等特性使伴矿景天成为较为理想的模式超积累植物。为了鉴定其富集和耐受重金属Cd的关键基因,我们通过筛选伴矿景天的 cDNA文库得到一个富含Cys的金属硫蛋白家族基因SpMT2。通过酵母异源表达系统解析了其介导Cd耐受性的机制,并结合其在植物中的亚细胞定位和表达模式,推测 SpMT2可能通过在伴矿景天细胞质内螯合 Cd以增强对 Cd的耐受性,同时这种螯合减少了 Cd向液泡中的区隔化从而保持了 Cd在植物体内的流动性,促进了 Cd的高效长途转运。
1 材料与方法
1.1 植物材料及培养条件
伴矿景天采集自浙江省衢州市一处废弃的锌/铅矿 (N29°14′29″,E118°50′32″)。实验室条件下,选择生长良好、茎部粗细基本一致的植物材料,截取含顶芽的3–5 cm长带叶枝条,扦插进行土壤培养,或进行营养液培养。伴矿景天营养液培养配方:1 L 营养液中含 2 000 μmol Ca(NO3)2、100 μmol KH2PO4、500 μmol MgSO4、100 μmol KCl、700 μmol K2SO4、10 μmol H3BO3、0.50 μmol MnSO4、1 μmol ZnSO4、0.20 μmol CuSO4、0.01 μmol (NH4)6Mo7O24、100 μmol Fe-EDTA,pH 5.5–5.8。生长环境为相对湿度60%–70%,恒温22–24 ℃,光照周期为16 h光照/8 h黑暗[15]。
1.2 cDNA文库构建及抗Cd基因筛选
用不同浓度梯度以及时间梯度处理的伴矿景天分根和地上部取材后利用CTAB法 (2% CTAB,25 mmol/L EDTA-Na2,0.1 mol/L Tris,pH 8.0,1.4 mol/L NaCl) 提取伴矿景天总RNA[15]。按照试剂盒说明书(Invitrogen公司)步骤构建酵母表达全长cDNA文库,酵母表达载体为半乳糖诱导表达载体pYES-DEST52。将文库转化大肠杆菌进行扩增,提取质粒后,按照Gietz & Schiestl的方法[16]转化对Cd敏感的酵母ycf1突变体,涂布200个平板 (碳源为葡萄糖),每块大平板 (150 mm×15 mm)涂布约5 000个酵母转化子。收集平板上的转化子,混合后涂布到含有相应浓度 Cd的培养基平板上 (碳源为半乳糖),每块平板涂布约 10万个细胞,涂布约200块平板。30 ℃培养7 d左右,对阳性转化子进行筛选鉴定。
1.3 酵母表型鉴定
将目的基因连入酵母表达载体pYES2,并转化酵母[17]。挑取单克隆培养至OD600为1.0左右。用 2 mL新鲜的液体培养基将适量菌液稀释至OD600为0.2左右,培养至OD600为0.6。取1 mL菌液,12 000×g离心收集菌体,用无菌水重悬菌体。将菌液依次稀释至 OD600=1、0.1、0.01。分别取10 μL菌体悬液滴至含有不同浓度重金属的培养基平板上,28–30 ℃培养4–7 d。并拍照。
1.4 酵母液泡提取
酵母液泡提取参考Li等的方法[18],并略有改动。简要步骤如下:从平板上刮取适量的酵母接种到20 mL液体培养基中,培养至OD600为1–1.5左右。将培养液倒入 400 mL新鲜培养基中,培养至OD600为1时加入相应浓度的重金属处理,并继续培养6 h。1 800×g离心5 min,收集细胞。用30 mL含有 100 mmol/L Tris-SO4(pH 9.3)和10 mmol/L DTT的溶液重悬细胞至OD600为10,30 ℃静置 10 min。离心,弃上清,菌体沉淀用缓冲液(1.2 mol/L 山梨醇,20 mmol/L 磷酸钾,pH 7.4) 洗一次。加入20 mg/mL酵母细胞壁裂解酶 (Sigma公司),30 ℃静置 30 min 以上。1 000×g、4 ℃离心5 min,用3.5 mL预冷的15% 菲可缓冲液 (15%菲可,0.2 mol/L山梨醇,10 mmol/L PIPES-KOH,pH 6.8) 将无壁细胞悬起 (至OD600=70)。加入二乙胺乙基葡聚糖至50 mg/mL,冰上3 min,30 ℃5 min,加入MgCl2至终浓度为1.5 mmol/L。裂解液转至离心管中,上面依次覆盖3 mL 8%菲可、4 mL 4%菲可和1 mL 0%菲可缓冲液 (10 mmol/L PIPES-KOH,pH 6.8,1.5 mmol/L MgCl2,0.2 mol/L山梨醇),110 000×g、4 ℃离心90 min,收集0%和4%菲可的液相界面间的液泡。提取得到的液泡分为两份,一份用BSA法测定其总蛋白含量,另一份测定重金属含量。
1.5 荧光蛋白融合构建及亚细胞定位
以eGFP-L和eGFP-R为引物扩增eGFP (表1),并利用 KpnⅠ和 SacⅠ酶点连入酵母表达载体pYES2得到pYES2-eGFP载体。以SpMT2-L1和SpMT2-R2为引物扩增 SpMT2 (表 1),通过Hind Ⅲ和KpnⅠ连入酵母表达载体pYES2-eGFP得到酵母亚细胞定位载体pYES2-SpMT2-eGFP,并转化酵母,用共聚焦显微镜 (Olympus-FV1000)观察亚细胞定位,激发光波长488 nm,接受光波长500–550 nm。
以SpMT2-L1和SpMT2-R2扩增SpMT2 (表1),通过 XhoⅠ和 SalⅠ连入植物瞬时表达载体PA7-YFP得到用于拟南芥叶片细胞原生质体瞬时表达的载体PA7-SpMT2-YFP。参考He等[19]的方法转化拟南芥原生质体细胞,用共聚焦显微镜(Olympus-FV1000) 观察亚细胞定位,激发光波长514 nm,接受光波长530–600 nm。
1.6 镉含量测定
待测酵母细胞依次用超纯水、5 mmol/L的EDTA、超纯水各洗2次,每次5 min。清洗好后烘干,称干重,用70%浓硝酸硝解,稀释,用电感耦合等离子质谱 (ICP-MS) 测定镉离子含量[13]。
1.7 qRT-PCR检测基因表达
提取RNA后,去除总RNA中的基因组DNA。精确量取1 μg总RNA进行反转录。将合适浓度梯度的SpMT2/pGEM T-easy质粒和伴矿景天cDNA在同一批次进行实时定量 PCR。将 SpMT2/pGEM T-easy的反应循环数和模板拷贝数制作标准曲线,计算伴矿景天转录组中SpMT2的表达丰度[13]。引物见表1。

表1 本研究中所用到的引物Table 1 Primers used in this study
1.8 序列信息
SpMT2的cDNA序列已经提交至GenBank,序列号 (Accession Number) 为MK893990。
2 结果与分析
2.1 伴矿景天cDNA文库筛选及SpMT2的鉴定
酵母具有真核生物基因的优良表达系统、高效的转化方法和可供筛选的丰富突变体、因此是筛选目的外源基因的高效系统。植物中很多抗Cd基因都是利用酵母互补系统对其cDNA文库进行筛选而被鉴定,如拟南芥的AtPCS1和AtPCR1、小麦 Triticum aestivum 的 TaPCS1、TaTM20 和TaHsfA4a、印度芥菜 Brassica juncea的 BjOXS3等[19-25]。伴矿景天由于遗传背景不明,基因序列信息缺失,因此利用酵母的遗传互补系统对其cDNA文库进行筛选以得到抗Cd的关键基因是研究伴矿景天富集和耐受Cd机理的有效方法。
利用均长为1 200 bp的酵母表达cDNA文库转化酿酒酵母 Ycf1突变体 DTY168,得到大于400 000个酵母单克隆。收集这些单克隆并混匀,取部分涂布于含有400 µmol/L Cd的平板上,最终筛选得到约6 000个抗Cd克隆。随机挑取200个克隆分析了其插入片段,发现只有两个基因,命名为 KG7和 KG8。KG8已经发表[13],在此选取KG7作为研究对象。由于KG7符合植物金属硫蛋白特征,因此命名为SpMT2。
SpMT2的CDS 全长240 bp,编码79个氨基酸,其中Cys残基 14个。根据 Zimeri 等[3]通过相邻Cys位置的间距对植物4种类型MTs的表征(表 2),SpMT2 (Cys 排列顺序:1424243…24232)属于植物MT2亚家族。
为了进一步验证SpMT2在酵母中的功能,将其在酵母Cd敏感突变体Δyap1及其野生型Y252中表达,发现能极大地提高突变体以及野生型酵母对Cd的抗性 (图1A)。值得一提的是,SpMT2的表达并没有增强酵母对Zn的耐受性 (图1B)。

表2 植物金属硫蛋白的半胱氨酸数目及分布类型Table 2 Total numbers and spa cing patt erns of cysteine residues in different types of plant MTs

图1 SpMT2的表达增强了酵母对Cd的抗性Fig. 1 Expression of SpMT2 enhanced Cd tolerance in yeast. The cadmium-sensitive yeast mutant Δyap1 and its wild type Y252 (A), zinc-sensitive yeast mutant Δzrc1 and its wild type CM100 (B) were transformed with EV(pYES2 empty vector), SpMT2, and grown on SD plates with indicated concentrations of metals for 7 days.
2.2 SpMT2定位于酵母细胞的细胞质中
由于 SpMT2的分子量远小于绿色荧光蛋白eGFP,为了利用eGFP的融合来观察SpMT2的亚细胞定位,我们先将SpMT2-eGFP的融合载体在酵母中表达,发现其抗Cd功能并未受到eGFP融合的影响 (图 2A)。在此基础之上,我们检测了其亚细胞定位,SpMT2主要定位在酵母细胞质中(图2B),暗示其可能主要在细胞质中发挥作用从而降低了Cd的毒害。
2.3 SpMT2减少了酵母中Cd向液泡中的转运
由于酵母 Δyap1突变体的液泡 Cd区隔化功能受到影响[26],并且SpMT2的表达能提高野生型酵母Y252对Cd的抗性 (图1A),因此用50 μmol/L Cd处理Y252转化子酵母并提取了液泡,通过测定液泡中 Cd含量发现,SpMT2的表达极大地减少了液泡中Cd的含量 (图3A),然而并没有改变酵母中总Cd 的含量 (图3B)。

图3 SpMT2的表达减少了酵母中Cd向液泡的转运Fig. 3 Expression of SpMT2 reduced Cd transport into vacuole. Total Cd accumulation (A) and vacuolar Cd accumulation (B) in yeast containing EV (pYES2 empty vector) or SpMT2. Yeast was treated with 50 μmol/L CdCl2 for 5 hours. Data are x±s, n=3. Statistical significance was indicated by lowercase letters above the bars (ANOVA test, P<0.05).
2.4 SpMT2定位于植物细胞的细胞质
为了探究 SpMT2在植物中是否也具有类似的功能,我们检测了其在植物中的亚细胞定位。将 SpMT2-YFP的融合构建在拟南芥的原生质体细胞表达后,发现其与对照YFP的定位一致,主要位于细胞质中 (图4)。
2.5 SpMT2在伴矿景天中的表达模式
基因的表达模式能够为基因功能的推测提供线索。我们通过分析单位总RNA中SpMT2的mRNA丰度来检测其表达模式。结果表明,SpMT2在伴矿景天根部和地上部都高丰度表达,且表达丰度无显著差异,1 μg总RNA中含有的SpMT2 mRNA的分子数超过108个 (图5)。需要指出的是,SpMT2的表达并不受Cd处理的诱导变化 (图5)。
3 讨论
本研究中我们通过高通量的 cDNA文库筛选,克隆鉴定了金属硫蛋白家族成员SpMT2。并利用酵母系统证实 SpMT2主要在细胞质发挥作用从而降低了Cd的毒害,同时减少了Cd向液泡中的区隔化。由于伴矿景天是新鉴定的物种,其相关遗传操作方法尚未成熟,但是我们根据 SpMT2在植物细胞质定位以及在伴矿景天根部和地上部高丰度表达的结果,推测其可能在伴矿景天富集和耐受Cd过程中发挥了重要的作用。
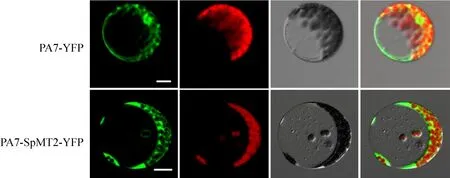
图4 SpMT2定位于植物细胞质Fig. 4 SpMT2 localized to the cytosol in plants. Subcellular location of SpMT2 in Arabidopsis mesophyll protoplasts.Bars=10 µm.
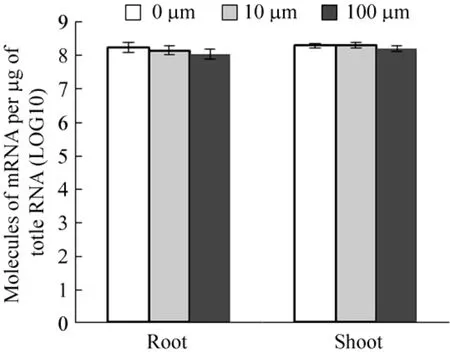
图5 SpMT2在伴矿景天中的表达模式Fig. 5 Expression levels of SpMT2 in S. plumbizincicola.Plants were grown in hydroponics for 6 weeks, and were transferred to solution supplemented with 10 µmol/L CdCl2 and allowed growth for another 3 d. Data are x±s, n=3.
植物体内存在多种类型的金属元素的螯合物,越来越多的研究表明,这些螯合物通过与金属元素形成稳定的复合物,在调节金属元素的液泡区隔容量 (Vacuolar sequestration capacity,VSC) 从而调节它们在体内转运的过程中发挥重要的作用[27]。特别是在超积累植物中,这些螯合物在细胞质中与重金属离子的螯合不仅降低了游离重金属离子造成的毒害,而且减少了根部重金属离子向液泡中的区隔化,保证了重金属离子流动性从而促进其在体内的长途转运。如NA在超积累植物叶芽鼠耳芥中的含量远高于其近亲非超积累植物,在NA含量减少的AhNAS2-RNAi株系中,地上部Zn和Cd的积累量也随之减少[28]。因此,我们推测SpMT2可能通过在伴矿景天细胞质中螯合Cd以增强对Cd的耐受性。同时,减少了Cd向液泡中的区隔化从而促进了Cd在体内的高效长途转运。
我们前期的研究已经证实,伴矿景天根部细胞中Cd的VSC显著小于其近亲非超积累植物[13],而地上部积累的 Cd并不是主要储存于液泡中而更多地储存在细胞壁中[29]。因此,伴矿景天可能存在特殊的调节机制减少了Cd的VSC,SpMT2在根部和地上部都高丰度表达,可能在此过程中发挥作用。SpMT2在根部细胞的细胞质中通过螯合Cd促进了Cd向地上部的转运,而在地上部细胞质中与Cd的螯合可能在Cd向胞外细胞壁部位再分配过程中发挥作用。这一推测需要在未来通过构建和分析伴矿景天的 SpMT2突变体或过表达材料等方式来进一步验证。
