COVID-19 患者粪便核酸检测结果特征及其临床意义
2020-04-09马志强瞿春燕李保萍马云珊吴艳蓉赵金花许娅琳
马志强,王 霖,罗 煜,瞿春燕,李保萍,马云珊,董 睿,吴艳蓉,赵金花,许娅琳
(1)昆明市第三人民医院检验科;2)关怀科,云南昆明 650301)
2019 年12 月,湖北省武汉市部分医院及医疗机构陆续报道新型冠状病毒感染的肺炎病例[1-2],随着新增病例的大量增加,疫情迅速在中国各地蔓延开来并波及全球20 多个国家和地区[3-5]。经研究,其基因特征与SARSr-CoV 和MERSr-CoV 有明显区别,但与蝙蝠 SARS 样冠状病毒(bat-SL-CoVZC45)同源性达85%以上[6-7]。新型冠状病毒由单一的核糖核酸(RNA)构成,属于β属的新型冠状病毒,有包膜,颗粒呈圆形或椭圆形。新冠肺炎的传播途径以经呼吸道飞沫和接触传播为主,同时有证据显示COVID-19 亦可通过气溶胶和消化道传播,且有人群普遍易感的特点。临床表现为发热、乏力、干咳等,少数患者伴有鼻塞、流涕、腹泻等症状,但也可隐匿发病[8]。新冠肺炎确诊主要通过实时荧光定量逆转录聚合酶链反应(revers etranscriptase-polymerase chain reaction,RT-PCR)和病毒基因测序。RT-PCR 特异性强、灵敏度高、快速经济以及应用简便,在COVID-19患者的诊治评估中具有重要意义。《新型冠状病毒感染的肺炎诊疗方案(试行第五版)》将COVID-19 感染核酸确诊检测的生物标本定为呼吸道标本[9]。因此核酸检测标本主要集中在咽拭子和痰等标本上,但是对COVID-19 患者其他类型标本如粪便的核酸检测结果缺少相关的报道,据此本研究旨在利用RT-PCR 的方法检测新冠肺炎患者粪便标本的带毒情况,初步阐明COVID-19 感染后在患者体内的分布特点及其临床意义,为新冠肺炎的诊断和分析传播途径提供实验依据。
1 材料与方法
1.1 研究对象
本研究收集昆明市第三人民医院自2020 年1月30 日至2020 年3 月10 日收治的COVID-19 确诊病例的粪便标本用于核酸检测,昆明市第三人民医院为云南省COVID-19 定点收治医院,也是云南省卫健委第一批确认开展COVID-19 核酸检测的实验室,在此期间共收治了39 例确诊病例,所有生物标本均严格按标准流程密封转运至本院检验科核酸检测实验室。COVID-19 诊断标准:根据《新型冠状病毒感染的肺炎诊疗方案(试行第七版)》[10],符合相关临床表现,及粪便COVID-19 核酸检测阳性[7-9]。本研究所有病例的个人信息均保密,所有生物标本仅用于科学研究和疫情防控。
本研究共纳入COVID-19 确诊病例粪便标本25 例用于核酸检测,其中男12 例,女13 例,平均年龄(49.5±17.3)岁。
1.2 仪器和试剂
主要仪器:NP968-C 全自动核酸提取仪(西安天隆科技有限公司),TL988-IV 实时荧光定量PCR 仪(西安天隆科技有限公司),CFX 96 实时荧光定量PCR 仪(美国伯乐科技公司)。相关试剂:COVID-19 病毒核酸提取试剂盒(EX-DNA/RNA病毒),新冠状病毒(2019-nCoV)ORF1ab/N 基因核酸检测试剂盒(天隆)、2019 新型冠状病毒(ORF1ab/N 基因)核酸检测试剂盒(上海伯杰)。
1.3 引物和荧光探针
引物与荧光探针有2 个靶序列,FAM 区域靶标(ORF1ab 基因)。
正向引物(F):CCCTGTGGGTTTTACACTTAA;反向引物(R):ACGATTGTGCATCAGCTGA;荧光探针(P):5'-FAM-CCGTCTGCGGTATGTGGAAAGGTTATGG-BHQ1-3'。HEX 区域靶标(N 基因);正向引物(F):GGGGAACTTCTCCTGCTAGAAT;反向引物(R):CAGACATTTTGCTCTCAAGCTG;荧光探针(P):5'-FAM-TTGCTGCTGCTTGACAGATT-TAMRA-3'。
1.4 标本处理与检测
标本处理 所有粪便标本先经过56℃30 min 灭活后,取黄豆大小的大便(1g 左右)于1.5 mL EP管中,加入1 mL 生理盐水振荡混匀10 s,3 000 r/min 离心30 s;取200 μL 上清液置于新的EP 管中,12 000 r/min 离心5 min,弃上清液,加入1 mL 生理盐水混匀,12 000 r/min 离心10 min,取下层沉淀50 μL 加入核酸提取试剂盒提取病毒核酸。
标本检测 依次加入30 μL 预先配制好的PCR混合液和20 μL 上述处理后的标本至PCR 反应管,在实时荧光PCR 仪上机进行扩增检测,结束后判读结果。
1.5 结果判读
先观察内标在对应的通道是否有扩增曲线,且扩增产物的荧光信号需达到设定的荧光阈值所对应的扩增循环数(cycle threshold,Ct)≤40。以天隆检测试剂为例,阳性:ORF1ab 和N 基因检测呈典型的S 型扩增曲线,且Ct 值≤37;阴性:无Ct值,内标通道检测结果为阳性。
1.6 统计学处理
采用SPSS 对数据进行分析,计数资料用率(%)表示;计量资料满足正态分布时,采用配对t检验。检验水准取α=0.05,P<0.05 为差异有统计学意义。
2 结果
2.1 不同治疗阶段粪便ORF1ab/N 基因检测
对COVID-19 确诊病例的粪便标本分别进行病毒ORF1ab/N 基因核酸检测。结果显示,治疗中期患者ORF1ab/N基因核酸检测扩增曲线呈S型,治疗后期患者ORF1ab/N基因检测未得到扩增曲线,见图1。
2.2 不同治疗阶段患者粪便核酸检测结果
不同治疗阶段的确诊病例阳性数为:治疗中期12 例,治疗后期3 例,阳性率分别为48%、12%,见表1。
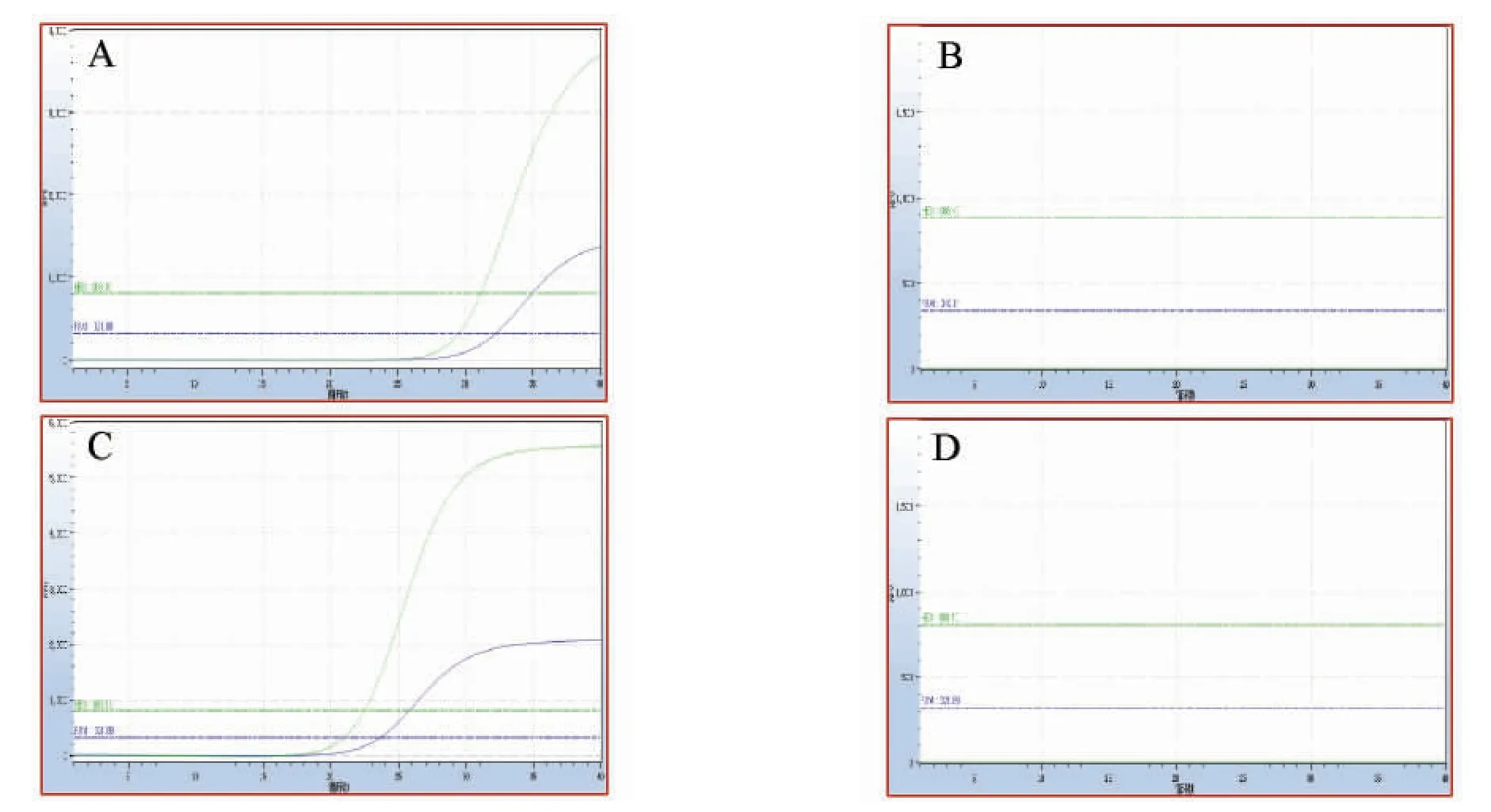
图1 不同治疗阶段粪便ORF1ab/N 基因扩增曲线Fig.1 Amplification curve of ORF1ab/N gene in stool at different treatment stages

表1 不同治疗阶段粪便核酸检测结果[n(%)]Tab.1 The stool nucleic acid test results at different treatment stages[n(%)]
2.3 不同治疗阶段患者粪便核酸检测CT 值结果变化
根据1.4 结果判读作依据分析CT 值,随着病程和治疗时间的推进,患者粪便核酸阳性检出例数有明显的减少,同时CT 值总体有升高的趋势。结果表明,经过抗病毒治疗后,患者病毒载量有所降低,抗病毒治疗效果差异有统计学意义(P<0.05),见表2、图2。
表2 不同治疗阶段粪便核酸检测CT 值结果比较(±s)Tab.2 Comparison of CT results of stool nucleic acid tests in different treatment stages(±s)
与治疗中期比较,△P<0.05。

图2 不同治疗阶段粪便核酸检测CT 值的变化Fig.2 The Changes of CT values in stool RT-PCR at different treatment stages
3 讨论
新冠肺炎疫情在中国已进入最关键的时期,最初有关COVID-19 的报道认为其与早年发生的SARS 冠状病毒存在许多相似之处,多数感染者表现为发热、乏力、呼吸困难等,少数患者以呼吸道症状发病如:流涕、打喷嚏、咽部肿痛等[1,11-13]。在临床诊疗中,仅依靠临床表现或实验室常规检查均不能作为新冠肺炎的准确依据,确诊的金标准是检出COVID-19 病毒核酸。因此,及时准确的病毒核酸检测不仅在早发现、早隔离、早治疗方面发挥至关重要的作用,而且可以为与密切接触、大量观察者的筛查节省宝贵的医疗资源[13]。
对于COVID-19 的实验室检测,笔者依据新型冠状病毒实验室检测技术指南发布的COVID-19 荧光PCR 检测引物和探针对25 例COVID-19 确诊病例的粪便标本进行病毒ORF1ab 基因及N 基因核酸检测。结果表明,在确诊的25 例粪便标本中,根据发热入院时间和治疗时间来划分,治疗中期粪便标本的病毒核酸检测有12 例为阳性,确诊病例中粪便标本COVID-19 核酸阳性检出率高达48%。其中男女比例为1:1.08,性别比例在统计学上无明显差异,因此没有证据证明性别易感性。经过治疗后,患者粪便病毒核酸检测仅有3 例为阳性,同时相应的检测CT 值总体上升,间接反映出病毒载量呈降低的趋势,这说明常规抗病毒治疗效果值得肯定。本研究显示粪便标本COVID-19 核酸检测呈阳性,但是有些呼吸道标本核酸检测却为阴性,这提示笔者在呼吸道标本的采集方法和类型的问题上应当引起足够的重视。粪便标本取材方便,不像呼吸道标本对取样要求较高,并且粪便标本的质和量更容易得到控制。同时在疾病的早期或症状较轻者,呼吸道标本可能病毒载量较低,这可造成核酸检测假阴性结果,而研究表明多数经呼吸道感染的病毒后期有粪便排毒的特点[14],因此选择粪便标本进行核酸检测可防止漏检,对COVID-19 核酸检测具有重要的意义。
综上所述,研究新型冠状病毒粪便标本中的病毒含量及持续时间,是实验室诊断COVID-19 感染及评价治疗效果的重要方法之一。本研究结果对COVID-19 实验室检测标本的选择具有一定的参考价值,在后续的研究中可结合其他类型的标本做出系统的检测和治疗方案。
