人工腹水在膈面、脏面原发性肝癌微波消融治疗中的作用
2020-04-05赵正兴戴建虎袁威威
卞 虎,赵正兴,戴建虎,袁威威
(江苏省淮安市淮阴医院 江苏 淮安 223300)
1 引言
原发性肝癌是临床常见恶性肿瘤,对患者危害较大,由于前期症状不是非常明显,导致疾病发现时已进展为中晚期,仅有少数患者符合手术切除指征,对于不能切除患者可根据实际情况选择栓塞、射频、消融等治疗方式[1]。本次研究纳入48 例膈面、脏面原发性肝癌患者,全部采取微波消融治疗,予以分组后,部分患者在治疗中应用人工腹水技术,研究人工腹水作用。
2 资料与方法
2.1 一般资料
纳入我院2017 年10 月—2019 年10 月期间48 例膈面、脏面原发性肝癌患者,采取分组方式进行对比研究,以“奇偶数字表”将纳入主体分为两组,奇数24 例为对比组:膈面13 例、脏面11 例,男女比例14:10,年龄32 ~70 岁,均值数(53.6±7.5)岁;偶数24 例为研究组:膈面12 例、脏面12 例,男女比例13:11,年龄31 ~71 岁,均值数(54.1±7.7)岁;纳入主体全部符合原发性肝癌诊断指南与标准,具有微波消融指征,对两组患者基本资料信息用统计学软件计算差异较小,P>0.05,研究可行。
2.2 方法
奇数24 例采取微波消融治疗(对比组),治疗过程:协助患者处于合适体位,对其进行麻醉处理,确定穿刺位置及路径,置入微波消融针,如果肿瘤直径小于2.5cm 进行单点消融,反之则进行两点或者多点消融,确保完全覆盖瘤体,在CT 引导下监测消融过程,若存在残留,继续消融,消融结束退针时消融针道,完成治疗。
偶数24 例在微波消融治疗中应用人工腹水技术(研究组),治疗过程:完善术前检查,在超声引导下实施穿刺,置入引流管(肝脏与膈肌之间),往腹腔注入500 ~1000ml 的温生理盐水,分离肿瘤区肝脏和膈肌,充分暴露手术视野,进行微波消融,具体操作与对比组一致。
2.3 观察指标
对比组、研究组一次性完全消融率、相关并发症观察与分析,一次性完全消融判定标准:消融区域覆盖肿瘤空间且无错位,彩超检查无血流信号,CT 检查无异常增强区域[2];并发症主要包括反应性胸水、肠穿孔、活动性出血。
2.4 统计学分析
3 结果
3.1 对比组、研究组一次性完全消融率对比
研究组一次性完全消融率(95.83%)高于对比组(75.00%),差异显著,P<0.05,见表1。

表1 对比组、研究组一次性完全消融率对比(n,%)
3.2 对比组、研究组相关并发症对比
研究组相关并发症发生率(4.16%)低于对比组(29.17%),差异显著,P<0.05,见表2。
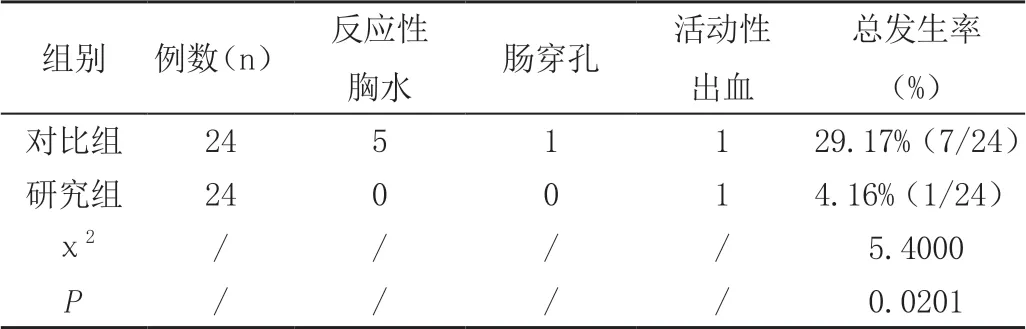
表2 对比组、研究组相关并发症对比(n,%)
4 讨论
微波消融是目前临床治疗原发性肝癌的主要方式,具有定位准确、操作简单、安全性高、效果确切等诸多优势,但是,接近肝脏表面的肿瘤,因毗邻膈肌或肠管及肾脏,消融过程中,因热传导,可引起毗邻脏器损伤,故在消融过程中常有所顾虑,为防止副损伤,需降低微波消融功率或消融时间,导致消融不彻底[3-4]。研究发现,在微波消融前应用人工腹水技术,能够帮助充分暴露手术视野,扩大微波消融适应范围,进一步提高消融安全性、彻底性[5]。
此次研究结果显示,研究组一次性完全消融率(95.83%)高于对比组(75.00%),差异显著,P<0.05;研究组相关并发症发生率(4.16%)低于对比组(29.17%),差异显著,P<0.05;说明人工腹水在膈面、脏面原发性肝癌微波消融治疗中作用较好,分析原因在于人工腹水技术可以使肝脏与毗邻脏器产生隔离,阻止热的传导,另外,随呼吸运动,腹水在腹腔产生流动,带走消融过程中在肝外产生的热量,从而减少对周围组织的损伤,也可以更加合理布针,确保消融彻底。
综上,在膈面、脏面原发性肝癌微波消融治疗中应用人工腹水技术,有助于提高一次性完全消融率,控制与降低相关并发症。
