溃疡型坏疽性脓皮病合并皮肤真菌感染一例
2020-04-03黄舒婷秦思温炬孙大炜广东省第二人民医院皮肤性病科广州5037广东省第二人民医院创伤外科广州5037
黄舒婷 秦思 温炬孙大炜广东省第二人民医院皮肤性病科,广州 5037;广东省第二人民医院创伤外科,广州5037
黄舒婷、温炬现在南方医科大学第二临床医学院,广州 510630
患者男,64岁,因颈背部反复溃疡伴疼痛3年余入院。3年前患者无明显诱因颈部出现数个米粒大小的水疱,伴疼痛,自行外敷中草药后,水疱破溃,周围皮肤糜烂,经当地医院清理创面、换药及自行涂抹多种药膏(具体不详)后,皮损无明显好转,呈潜行性扩大,形成手掌大小的溃疡,累及背部,伴明显疼痛。3个月前双下肢出现凹陷性水肿,当地医院予补充白蛋白后水肿消退,但仍反复发作。2个月前在外院对背部皮损溃疡基底分泌物进行培养示皱落假丝酵母菌(Candida rugosa)阳性,考虑为皮肤真菌感染,予抗真菌及止痛治疗1个月后,效果欠佳。后对右背部溃疡边缘皮肤行病理检查示,浅表表皮缺失,可见痂皮及坏死组织,真皮浅表及血管周围可见中等量淋巴细胞及中性粒细胞浸润,未见上皮细胞团块,未见肿瘤组织,不排除坏疽性脓皮病。患者未予进一步诊疗。近1周皮损较前扩大,局部溃疡深达皮下组织,上覆大片痂皮,疼痛剧烈,伴头晕不适,无法平卧。病程中无畏寒、发热,无乏力、关节疼痛。既往有颈椎增生病史3年余,家族中无类似疾病及传染性疾病史。
体检:一般情况尚可,颈部活动受限,浅表淋巴结无肿大,双肺呼吸音清,闻及双下肺湿啰音。双小腿、踝部及双足背对称性凹陷性水肿(图1A),皮温正常。皮肤科检查:颈背部见大片不规则溃疡,约25 cm×20 cm,深约0.3 cm,呈潜行性,边界清楚,基底凹凸不平,上覆厚层褐色干燥性痂皮,溃疡中央见红色肉芽组织,颈部发际线处溃疡深约1.2 cm,内有黄白色脓性分泌物,触之剧痛,溃疡外周绕以边界尚清的环形红斑,见图1B。
实验室检查:血常规示白细胞13.11×109/L,中性粒细胞比例0.86,C反应蛋白>270.0 mg/L。尿粪常规、肝肾功能、抗HIV抗体和梅毒螺旋体抗体、血培养、自身免疫性抗体、肿瘤标志物检测均未见异常。颈椎及胸部X线片示:①双下肺野病变(考虑感染性病变);②颈椎退行性变。下肢血管彩超示右侧腘静脉、腓静脉、肌间静脉和左侧腓静脉上段血栓形成。颈背部溃疡面分泌物培养示,光滑念珠菌及肺炎克雷伯菌肺炎亚种生长。颈项部皮损组织病理示表皮缺失,可见纤维脂肪组织及少量横纹肌组织,部分区域大片坏死、化脓,其内混杂大量真菌菌丝及孢子,过碘酸雪夫染色、六胺银染色和阿辛蓝染色均阳性,符合真菌感染,见图2。颈项部皮损深部组织培养示诞沫假丝酵母(Candida zeylanoides)生长,无细菌生长。结合临床及以上检查,诊断:溃疡型坏疽性脓皮病(PG)合并皮肤真菌感染、双下肢静脉血栓形成。
治疗经过:入院后予静脉滴注甲泼尼龙40 mg/d及头孢地嗪2 g/d,口服沙利度胺(25 mg每日2次)及雷公藤多苷(10 mg每日3次)、伏立康唑(0.2 g每日2次)和华法林(2.5 mg每日1次)。20 d后溃疡较前愈合,面积缩小,背部大片痂皮脱落,红色肉芽组织生长,颈项部溃疡仍较深,上有约15 cm×10 cm厚层黑褐色痂难以清除。于创伤外科行双下肢血管介入治疗及颈背部清创术,后予大腿取皮及颈背部植皮术,期间予负压吸引及换药治疗,术后2周颈背部淡红色筛状瘢痕形成,颈项部中央见一约15 cm×10 cm的肤色移植皮片(图1C),创面恢复良好出院。

图1 溃疡型坏疽性脓皮病合并皮肤真菌感染患者溃疡治疗前后表现 1A:治疗前双下肢凹陷性水肿;1B:治疗前颈背部大片不规则溃疡,边界清楚,上覆厚层褐色干燥性痂皮,溃疡中央见红色肉芽组织;1C:治疗2个月后,背部形成淡红色筛状瘢痕
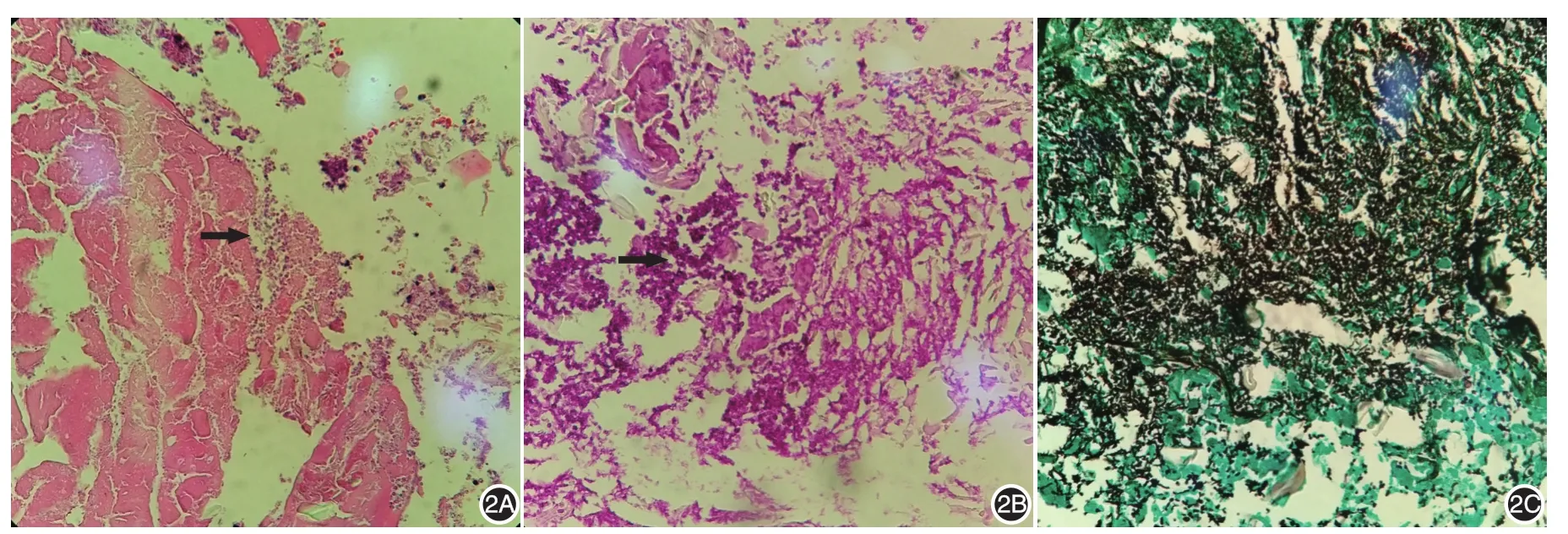
图2 皮损组织病理表现 2A(HE×200)、2B(HE×400):表皮缺失,可见纤维脂肪组织及少量横纹肌组织,部分区域大片坏死、化脓;箭头示大量真菌菌丝及孢子;2C:六胺银染色阳性,见大量呈黑褐色的菌丝及孢子(×400)
讨论PG是一种以皮肤破坏性溃疡和疼痛为特征的非感染性嗜中性皮肤病,临床少见,病情较严重,常伴有潜在的系统疾病。临床上本病按皮损特点分为溃疡型、化脓型、大疱型和增殖型4型[1],本例依据临床特点属于溃疡型。PG的病因及发病机制尚不明确,目前多归于免疫系统疾病。PG的组织病理无特异性,可因皮损的类型、位置及治疗等不同而表现不同。2018年,Delphi共识[2]提出了PG的诊断标准,包括1个主要标准和8个次要标准,主要标准是溃疡边缘活检提示中性粒细胞浸润,8个次要标准包括:①排除感染(组织学染色或组织培养);②病理性反应(外伤部位溃疡);③炎性肠病或炎性关节炎病史;④皮损出现后4 d内有丘疹、脓疱或水疱、溃疡;⑤外周红斑,边界破坏,溃疡部位压痛;⑥多发性溃疡,至少1处位于小腿前侧;⑦溃疡愈合部位呈筛状或“皱褶纸”样瘢痕;⑧使用免疫抑制剂1个月内溃疡变小。除了活检示中性粒细胞浸润外,还必须至少满足4个次要标准才可以诊断PG。
本例经多次分泌物培养提示真菌感染,血培养阴性,但患者皮损自发病以来长期明显疼痛,期间曾自行外用多种药物且外院予抗真菌治疗,效果欠佳。根据病史、体征及外院病理结果(提示嗜中性粒细胞浸润),排除肿瘤性和血管炎性疾病等所致溃疡的可能。入院后经糖皮质激素及免疫抑制剂兼抗真菌治疗3周后,皮损较前缩小,无新发,治疗有效,符合Delphi共识的诊断标准,考虑为PG合并皮肤真菌感染。
目前PG的治疗常以经验性治疗为主,主要分为局部药物、系统药物和其他手段[3]。局部药物治疗适用于早期或轻度PG患者,可联合系统治疗促进溃疡愈合。最近一项针对英国66例PG患者的前瞻性研究[4]显示,0.05%丙酸氯倍他索是最常用的PG局部治疗方法,且43.8%的患者在6个月内通过局部治疗痊愈,33%需要系统治疗。对较为严重的PG病例,需行系统性药物治疗,目前糖皮质激素是治疗PG应用最广且最为有效的药物。在给予充足剂量之后,糖皮质激素能够快速控制临床症状。另外,与免疫抑制剂如环孢素、环磷酰胺、苯丁酸氮芥、硫唑嘌呤、秋水仙碱等联合使用可减少糖皮质激素的不良反应。Del Giacco等[5]报道1例PG患者在常规使用糖皮质激素及免疫抑制剂治疗无效后,联合使用英夫利西单抗治疗12个月,皮损愈合无复发。
对于病情稳定但皮损经久不愈者,可进行外科清创、植皮,联合高压氧治疗[6]。局部手术清创治疗能促进正常组织生长和修复,及时进行清创手术可明显加速疼痛缓解和组织修复[7]。在1篇多中心病例分析报道中,15例PG患者在适当的免疫调节治疗后接受植皮手术和负压创伤疗法(negative-pressure wound therapy)[8],10例皮损完全愈合,3例病情明显改善,90%以上的创面愈合,2例出现轻微复发。Mazokopakis等[9]曾报道1例PG患者经系统药物治疗后溃疡长期不愈,接受多次高压氧治疗后溃疡痊愈。本例患者经抗炎及抗真菌治疗后,疼痛较前稍缓解,但仍反复发作,局部厚层痂皮不易脱落,行清创和植皮手术后,创面恢复良好,形成淡红色筛状瘢痕,无新发潜行皮损。半年后随访本例患者,皮损无复发,偶感头晕,颈部活动度可。
利益冲突所有作者均声明不存在利益冲突
