阿帕替尼联合DOS化疗方案在Ⅲ期胃癌新辅助治疗中的运用
2020-03-31王浩宇闵江钱昆张伟
王浩宇,闵江,钱昆,张伟
(重庆医科大学附属第一医院胃肠外科,重庆)
0 引言
胃癌是近年来中国发病率和病死率最高的恶性肿瘤之一。根据世界卫生组织公布的报告来看,全球胃癌发病率为每10万人中13.9例,在恶性肿瘤中排第2位,同时也是第3大全球癌症病人死亡的主要原因[1]。在中国,每年新增40万胃癌患者,占世界总新增患者数的五分之二以上。尽管在许多国家,胃癌的发病率和死亡率一直在下降,因为胃癌在早期没有明显的症状,当出现明显的症状时,该病通常会进展到晚期,并且大约65%的患者是局部晚期或在诊断时已被诊断为发生了远处转移,并且失去了手术机会。目前手术切除仍是胃癌的综合治疗方案中的主要方法,但是许多患者肿瘤分期太晚,以至于无法切除。同时,手术切除后仍有约60%的复发率。多项研究表明,晚期胃癌患者的术前新辅助化疗能够缓解症状并获得更好地生活质量与更长的生存周期[2]。因此,开展相关的临床新辅助化疗研究对于进一步提高化疗反应率,减少不良反应发生率,提高手术切除率,延长患者生存率具有重要意义。在此基础上,笔者回顾性分析2017-2019年于本科室使用阿帕替尼联合多西他赛(TXT)与奥沙利铂(L-OHP)及替吉奥组(实验组,40例)和仅用多西他赛(TXT)与奥沙利铂(L-OHP)及替吉奥组(对照组,38例)的共78例Ⅲ期胃癌患者,比较两种方案的治疗效果、不良反应、手术切除率及并发症,现汇报如下。
1 资料与方法
1.1 一般资料
选取2017年2月6日至2019年2月24日本院胃肠外科收治的78例ⅢA~ⅢC期胃癌患者,这项研究已经获得本院伦理委员会的批准。纳入标准:(1)通过胃镜和/或腹腔镜检查获得的病理组织确实是胃癌组织,经胸部和腹部增强CT检查证实其临床分期为ⅢA~ⅢC期胃癌;(2)治疗前胃癌病灶均可被测量;(3)第一次不能进行直接手术切除或拒绝手术和化学疗法;(4)血液常规,生化指标,心电图等检查均在正常范围内,无化疗禁忌症;(5)治疗前KPS评分大于或等于70分,且患者的估计生存时间大于4个月;(6)有关知情同意书必须在治疗前自愿签署。根据两种不同的新辅助化疗方案,将78例患者分为两组:阿帕替尼联合DOS组40例,DOS组38例。比较两组患者的一般临床资料,差异无统计学意义(P>0.05)。两组患者具有可比性。有关详细信息,请参见表1。
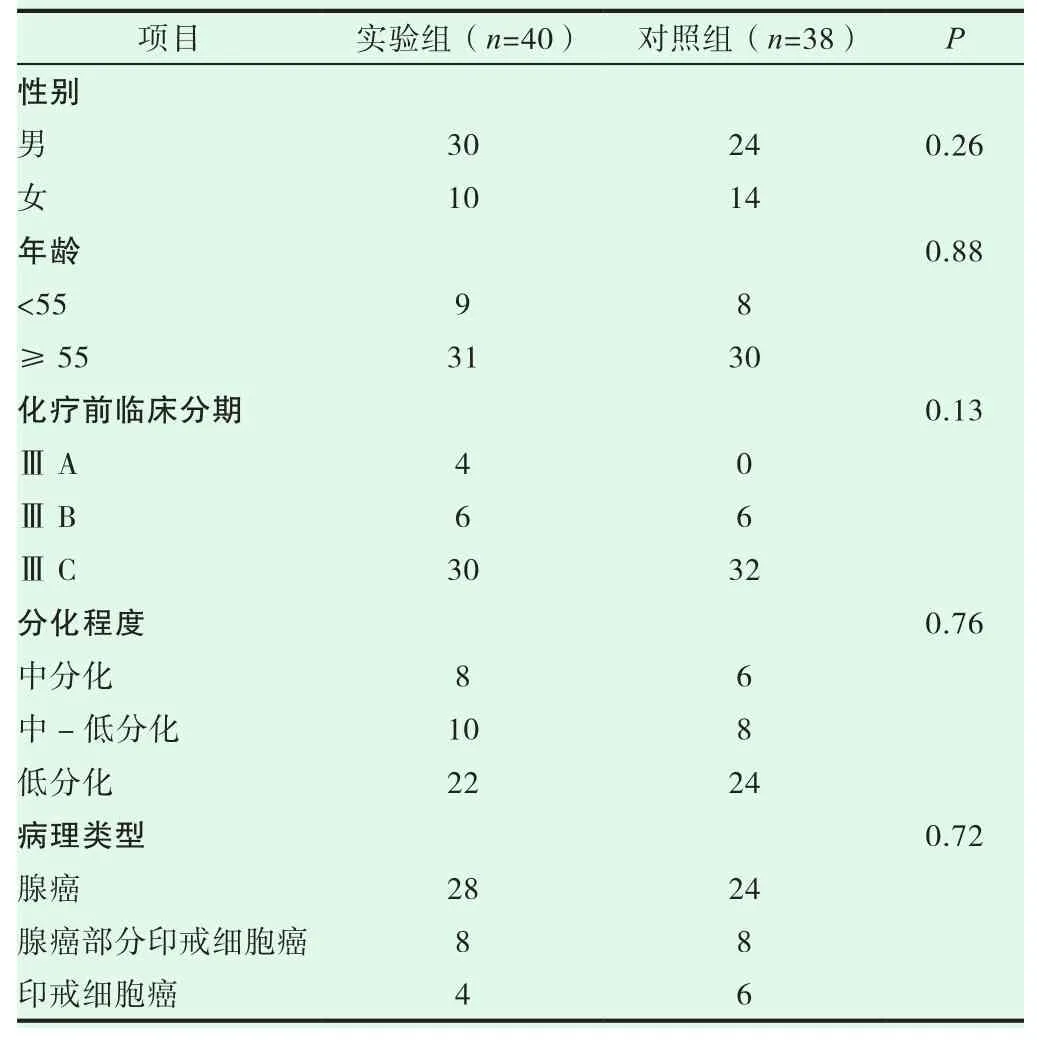
表1 三组患者一般资料比较(n)
1.2 方法
1.2.1 治疗方法
A:DOS方案治疗:多西他赛+奥沙利铂+替吉奥
B:DOS方案+阿帕替尼治疗
第1天,多西他赛60mg/m2静脉滴注1h;第1天,奥沙利铂100mg/m2静脉滴注 3h;第 1-21天,替吉奥胶囊(S-1)30mg/m2,口服,每日2次。连服21d,休息7d,共计28d为1个治疗周期;餐后半小时服用阿帕替尼片250mg,口服,每日一次,用温水送达,如果一个周期后耐受性良好,则将剂量调整为500mg,口服,每日一次。每28天为一个治疗周期,治疗周期与DOS方案的周期平行。
在服药之前,应严格根据患者的体表面积计算每种化疗药物的剂量。对于年老或体弱的患者,应减少剂量(最多减少到70%)。每次化疗前后,患者均常规给予盐酸托烷司琼注射液,并常规服用地塞米松片10 mg,以防止过敏,同时给予患者抑酸,护肝,水化辅助治疗。白细胞减少症降患者常规接受重组人粒细胞刺激因子治疗;对于胃肠道反应大于或等于Ⅱ度的患者给予止吐、止泻、输液等对症支持治疗;当神经毒性出现时,予以大量维生素及营养神经对症治疗。对于疗效评估为疾病进展(PD)的患者,他们将根据自己的意愿接受二线和三线化疗或支持治疗。化疗后胃癌病情缓解的患者将接受根治性或姑息性手术。
1.2.2 疗效及不良反应评价
在每个化疗周期之前和之后,进行三项主要常规检查,肝肾功能,癌症谱图,心电图以及胸部和腹部增强CT检查,以评估疗效和不良反应。根据美国临床肿瘤学会2008年实体瘤反应评估标准(RECIST),确定疗效:完全缓解(CR),所有目标病变消失,无新病变出现,肿瘤标志物正常。任何病理性淋巴结的短轴值必须小于1mm,至少持续4周;部分缓解(PR),根据临界半径的总和,所有病灶半径的总和至少降低了30%,至少持续4周;疾病稳定(SD),基于研究目标病变半径的最小值用作参考,并且既未达到缓解标准,也未达到进展标准。疾病进展(PD),目标病变半径的最小值用作参考,所有目标病变半径的总和至少增加20%。另外,半径总和的增加的绝对值还必须大于5mm,或者有新病灶出现[3]。客观缓解率(0RR)是CR+PR患者的百分比;疾病控制率(DCR)是CR+PR+SD患者的百分比。每个患者的随访时间是从第一次化疗开始到化疗周期结束,肿瘤进展,患者随访失败或死亡。随访截止日期为2019年6月31日。根据美国国家癌症研究所(NCI)2009年通用毒理学评估标准(CTC)4.0版,将不良反应分类,并将不良反应分类为0至IV级[4]。生活质量评估是根据Kamofsky评分(KPS)标准而判定的,如表2所示。治疗后KPS评分增加10分以上的患者被认为生活质量得到改善;治疗后KPS得分变化低于10分的患者被判定为治疗后生活质量稳定。KPS得分降低幅度大于10分的患者被判定为生活质量降低。生活质量的内容包括行为状态评分、体重、患者的主观感受、治疗前后食欲变化。患者新辅助化疗后手术情况主要评价患者手术切除率和患者相应并发症的发生率。

表2 生活质量评分
1.3 统计学处理
使用SPSS 22.0统计软件进行统计分析。使用t检验比较患者一般信息,临床疗效和术后淋巴结阳性率等。化疗不良反应,新辅助化疗后的切除率,术后并发症发生率等使用秩和检验比较。以P<0.05为差异有统计学意义。
2 结果
2.1 两组临床疗效比较
78例Ⅲ期胃癌患者均接受1~3个周期的新辅助化疗。每例患者进行新辅助化疗后临床疗效均可评价。两组内均无临床疗效为CR的患者,实验组中PR 24例(60%),SD 8例(20%),PD 8例(20%),ORR 为 60%(24/40);对照组中 PR 14例(36.8%),SD 12例(31.6%),PD 12例(31.6%),ORR为36.8%(14/38)。实验组ORR、RR 较对照组高,差异有统计学意义(P=0.04<0.05),见表 3。实验组淋巴结阳性率低于对照组,差异有统计学意义(P=0.003<0.05),见表 4。
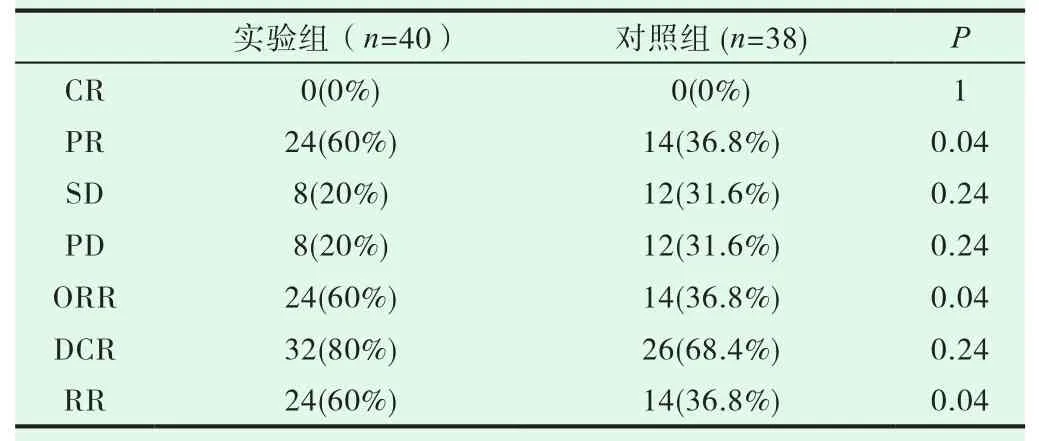
表3 两组临床疗效比较(n)
表4 两组淋巴结比较(n,
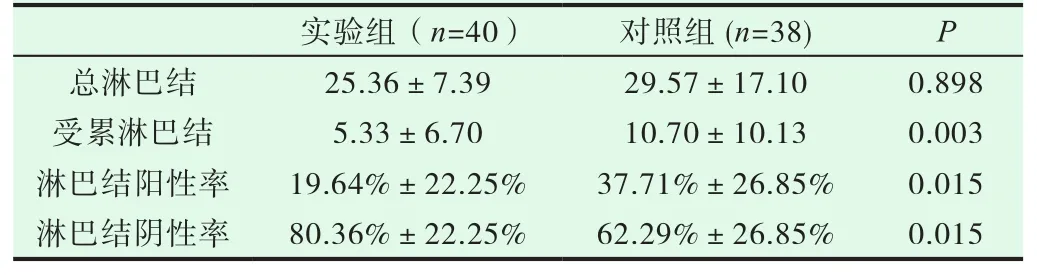
表4 两组淋巴结比较(n,
实验组(n=40) 对照组(n=38) P总淋巴结 25.36±7.39 29.57±17.10 0.898受累淋巴结 5.33±6.70 10.70±10.13 0.003淋巴结阳性率 19.64%±22.25% 37.71%±26.85% 0.015淋巴结阴性率 80.36%±22.25% 62.29%±26.85% 0.015
2.2 两组不良反应发生情况比较
接受两种化疗方案治疗的III期胃癌患者均经历了不同程度的骨髓抑制,胃肠道不良反应(例如恶心和腹泻)以及与新辅助化疗相关的其他不良反应。积极的针对症状支持治疗后均在不同程度上缓解。对78例新辅助化疗后的不良反应进行了评估和分级,两组患者均未终止化疗或因化疗期间的不良反应而死亡。比较了两组新辅助化疗相关不良反应的发生率。实验组骨髓抑制的发生率低于对照组(P=0.04 <0.05),差异具有统计学意义。实验组的皮肤过敏发生率高于对照组。(P=0.02 <0.05),差异具有统计学意义,请参阅表5。

表5 两组化疗后不良反应比较(n)
2.3 两组患者新辅助化疗后手术切除情况的比较
两组在化疗后均可重新评估。胃癌病情缓解的患者可以根据他们的具体情况接受根治性手术或姑息手术治疗。实验组33例(82.5%)接受了根治术,3例(7.5%)接受了姑息性手术,4例(10.0%)没有进行手术;在对照组中,有23例患者接受了根治术(60.5%),有11例(28.9%)接受了姑息手术,其中4例(10.5%)没有进行手术。两组在新辅助化疗后的手术切除率比较具有统计学意义(P=0.03 <0.05),如表 6 所示。
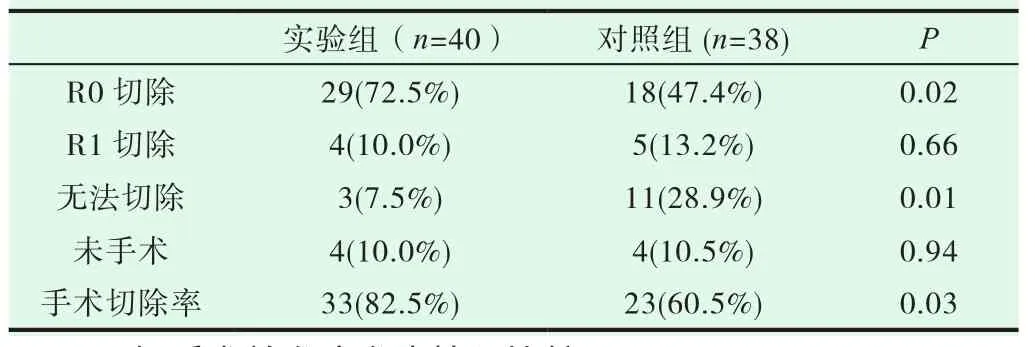
表6 两组手术切除率比较(n)
2.4 两组手术并发症发生情况比较
两组患者手术后主要并发症为手术吻合口瘘、手术吻合口梗阻、术后贫血、术后梗阻性黄疸等,两组并发症的发生率比较,差异无统计学意义(P=0.52>0.05),见表 7。

表7 两组手术并发症发生情况
2.5 两组生活质量比较
化疗后,对两组进行比较。实验组生活质量提高24例、稳定10例、减退6例,对照组生活质量改善18例,稳定7例,降低13例;相比之下,差异无统计学意义(P=0.14> 0.05),请参阅表8。

表8 两组生活质量
3 讨论
目前,胃癌发病率仍处于我国各种恶性肿瘤发病率中的前列,由于其特殊的临床表现,非典型的早期症状,大多数患者会等到自己的身体不适无法忍受后才去医疗机构就诊,等到正式确诊时已经是局部晚期胃癌或已经发生了胃癌远处转移,失去了手术机会。对于晚期胃癌的治疗,目前提倡以综合治疗为主,包括进行手术清除病灶、化学治疗、放疗及分子靶向药物治疗等,但总体的治疗效果至今仍然不算理想,胃癌复发率高,对化学治疗的敏感性差,预后非常的差。因此,临床医生有必要探索针对晚期胃癌的新辅助化疗的研究,这将进一步提高化疗的反应率,减少化疗不良反应的发生率,缩小胃癌肿瘤的大小,降低胃癌的分期并改善胃癌的根治性手术切除率,延长胃癌患者的生存期和改善胃癌患者的生活质量。近年来,晚期胃癌的化疗方案尚无“金标准”,在晚期胃癌的化学治疗中紫杉烷类、铂类、氟尿嘧啶类、丝裂霉素等药物被证实是有疗效的,但是大量临床实践证明,使用这些药物进行单药化学治疗的有效率偏低,疗效并不特别理想,需要更有效的药物或者化疗方案。随着新一代抗肿瘤药物阿帕替尼,多西他赛,替吉奥,曲妥珠单抗和雷莫珠单抗的问世,新的联合化疗方案不断出现并得到了极大改善。晚期胃癌的化疗效果得到了改善。在这项研究中,作者选择了两种多药治疗方案(阿帕替尼联合DOS方案和DOS方案)。这两种方案对晚期胃癌患者有作用,并且患者对这两种化疗方案具有更好的耐受性。艾坦(Apatinib)是世界上第一种针对小分子抗血管生成的药物,已被证明在晚期胃癌中安全有效。同时,该药物是胃癌靶向药物中唯一的口服制剂,可有效改善患者依从性并显著降低治疗成本。它的作用是高度选择性地竞争细胞中VEGFR-2的ATP结合位点,阻断下游信号传导并抑制肿瘤组织中的新血管形成。由于其使用相对简单,顺应性好,副作用少,因此在临床上已越来越多地用于治疗晚期胃癌和其他实体瘤[5]。研究表明,阿帕替尼可以提高胃癌患者对紫杉醇和5-氟尿嘧啶的敏感性,并且多种药物联合化疗的效果相当好[6]。其副作用主要是导致血压升高和蛋白尿,因此患者服药期间应按时规律检查血压及尿常规。多西他赛是一种半合成紫杉烷类抗肿瘤药。其机制是加强微管蛋白聚合并抑制微管解聚,导致形成稳定的非功能性微管束,从而破坏肿瘤细胞的有丝分裂。它是细胞周期M期特异性药物,其微管作用和作用时间均优于紫杉醇。多项临床研究表明,该药物可有效治疗胃癌[7]。因此,多西他赛常在许多化疗方案中被用作联合药物之一[8]。奥沙利铂是一种新的铂类抗癌药物,通过产生水合衍生物形成链内和链间交联来抑制DNA合成。研究表明,与顺铂和卡铂相比,奥沙利铂结合DNA的速度更快,具有广泛的体外细胞毒性和体内抗肿瘤活性,并且对于晚期胃癌患者具有良好的耐受性,并且更容易在床上实施[9]。与多西他赛联用时,效果非常好,患者的肿瘤减退率高于其他化疗方案[10-11]。替吉奥胶囊是一种用于治疗晚期胃肠道肿瘤的新型一线药物。它由替加氟(FT),吉美嘧啶(CDHP)和奥曲西钾组成。替加氟与氟尿嘧啶具有相同的作用,它可以干扰并拮抗抗体中DNA,RNA和蛋白质的合成。吉美嘧啶可以防止氟尿嘧啶活化剂的降解并增强抗癌作用;奥替拉西钾可以保护胃肠道,减少胃肠道反应。临床研究结果表明,替吉奥胶囊在胃癌的综合治疗中显示出更好的疗效,并具有口服方便,不良反应发生率相对较低,患者耐受性好的优点[12]。NCCN(2017 V3)胃癌指南建议,在局部晚期胃癌手术前,是可以进行新辅助化疗的。卫生部2011年版的《胃癌诊断和治疗规范》表明:对于无远处转移的局部晚期胃癌(T3/4、Nx),建议使用新辅助化疗,且应当采用两药或三药联合的新辅助化疗方案,不推荐只单独运用一种化疗药物。ECF方案及其改良方案被建议运用于胃癌的新辅助化疗。新辅助化疗的持续时间一般不应超过3个月。同时,应及时评估疗效,并应谨慎确定是否存在不良反应和不良反应的程度,以免增加手术并发症。对于可切除的胃癌患者,基于多西他赛的三药FLOT方案(Docetaxel(多西他赛)+ Oxaliplatin(奥沙利铂)+ Fluorouracil(氟尿嘧啶)/ Leucovorin(亚叶酸钙))可良好耐受,并且能提高pCR(病理完全缓解)率。当前的NCCN胃癌临床实践指南在2019年增加了“针对无法切除的肿瘤患者的放射化疗方法”(氟尿嘧啶+奥沙利铂),用于治疗无法切除的局部晚期,复发或远处转移的患者。多项Ⅱ期临床试验已经证实了紫杉醇联合顺铂(或奥沙利铂)、氟尿嘧啶(或替吉奥胶囊)的联合疗法(FLOT方案或改良FLOT方案)的有效性及安全性[13-14]。FLOT方案已被美国食品和药物管理局(FDA)批准用于晚期胃癌的一线治疗,但不良反应的发生率很高。目前,晚期胃癌患者的临床应用表明改良的FLOT方案的临床效果与FLOT方案相似,但改良的FLOT方案的不良反应明显少于FLOT方案。美国综合肿瘤网络中心(NCCN)指南已经将改良FLOT方案纳入晚期胃癌的一线治疗。目前,我们正在使用的是的FLOT方案的改良方案:DOS新辅助化疗方案。临床试验表明,该方案更适合亚洲人的体质,对亚洲胃癌患者具有良好的疗效。作者对apatinib + DOS化疗方案和DOS化疗方案进行了比较研究,以探讨两种方案的短期疗效和不良反应之间的区别。研究结果表明,apatinib + DOS方案更好,apatinib + DOS方案和仅DOS方案的ORR分别为60%和36.8%。两种方案的主要不良反应是骨髓抑制、消化道不良反应与其他化疗有关的不良反应(例如肝功能障碍和皮肤过敏),大多为I / II度。比较两组患者化疗相关不良反应的发生率,发现实验组骨髓抑制的发生率低于对照组(P=0.04<0.05),差异有统计学意义。实验组皮肤过敏发生率高于对照组(P=0.02<0.05),差异有统计学意义;新辅助化疗后,大多数患者的生活质量得到改善,身体状况也相应改善,为随后的根治性手术创造了必要条件;新辅助化疗后实验组和对照组的切除率分别为82.5%和60.5%,差异有统计学意义(P=0.03 <0.05)。两组的主要术后并发症(如吻合口瘘,吻合口阻塞,贫血和阻塞性黄疸)的发生率没有显著差异。本研究中没有化疗相关性死亡。
综上所述,阿帕替尼+DOS方案和单纯DOS方案在治疗Ⅲ期胃癌的临床疗效中,阿帕替尼+DOS方案更好,并且可以经积极对症治疗来完全耐受不良反应。这种安全且有效的治疗策略可以提高Ⅲ期胃癌的切除率和根治率,值得临床进一步推广并进行应用。口服阿帕替尼片联合DOS静脉化疗方案有望成为治疗晚期胃癌的一线方案,其可根据患者体质及耐受程度合理选用并进行个体化调整。但是,由于该研究的样本量较小且该研究的患者病情较晚,因此需要进一步论证研究结果。
