携IL-8单克隆抗体靶向造影剂对兔VX2肝癌超声成像的实验研究
2020-03-31陈建福徐飞张湘敏杨寒凝杨媛陆永萍
陈建福,徐飞,张湘敏,杨寒凝,杨媛,陆永萍★
(1.大理大学临床医学院,云南 大理;2. 云南省第二人民医院超声科,云南 昆明)
0 引言
原发性肝癌(Hepatocellular Carcinoma, HCC)是死亡率极高的恶性肿瘤,而我国每年肝癌死亡人数占据全球总构成的50%以上[1-2]。肝癌早期无显著临床特征,多数患者于中晚期检出,失去了肝移植或手术切除的最佳时机[3]。因此,如何早期快速而准确的发现、诊断肝癌已成为临床攻克肝癌的重中之重。
超声显像是肝脏肿瘤的传统检查方法之一,随着现代技术的发展,超声造影已展示出广阔的应用前景,超声造影提高了临床可疑肝脏占位性病变的早期检出率及其良恶性鉴别诊断的准确性,是肝癌早期诊断的主要影像学手段之一[4]。本研究采用IL-8单克隆抗体(简称“IL-8单抗”)偶联SonoVue声学微泡合成新型靶向微泡造影剂,通过肝脏肿瘤组织内靶向造影剂各时相显影分析,研究传统超声造影剂联合IL-8单抗靶向显影在肝癌诊断效能中的应用,为临床研究和治疗奠定基础。
1 材料与方法
1.1 实验动物
健康成年日本大耳兔42只,荷瘤兔2只,雌雄不限,体质量(2.5±0.5)kg,均由昆明医科大学实验动物中心提供。
1.2 实验模型建立
以3%戊巴比妥钠将实验兔麻醉,仰卧位固定,分离皮肤和皮下组织,充分暴露左肝叶并固定,使用15G穿刺针将肿瘤颗粒(取自荷瘤兔)注入肝叶的背离腹壁面,确定肿瘤颗粒包埋于肝组织后退针,同时使用明胶海绵压迫切口止血,术后肌注40万单位抗生素预防感染。采用此改良开腹包埋法[5],对42只日本大耳兔行瘤块种植,建立理想VX2 肝癌模型(肿瘤最大径>1cm)。
1.3 靶向造影剂的制备
IL-8单抗通过异型双功能交联剂(SPDP)偶联SonoVue声学微泡,即共价偶联法。制成微泡悬液,并经玻片凝集实验[6]鉴定,成功制备靶向造影剂。
1.4 仪器设备
意大利百胜公司(EsaoteMylab Twice)超声诊断仪;选用频率为5.0-8.0MHz探头,二维灰阶增益70%。
1.5 实验方法
1.5.1 实验动物分组
对同一实验兔均用普通SonoVue造影剂和携IL-8单抗靶向造影剂行造影检查(前后相隔24小时),前者记为普通组,后者记为IL-8组。
1.5.2 造影检查及图像采集
所有实验兔均经耳缘静脉建立静脉通道,并用体积分数3%戊巴比妥钠注射液(30mg/kg)注射麻醉,常规二维超声检查全肝,清晰显示VX2肿瘤及其周围正常肝组织。实验兔进入麻醉状态后,从静脉通道团注普通SonoVue造影剂(0.2mL/kg),并用2mL生理盐水冲注,注射靶向造影剂前采集图像1次,造影后采集图像11次(前90s内每隔10s1次,90s-150s内每隔30s1次)。共采集图像12帧,时长150s。24小时后,再次从静脉通道团注携IL-8单抗靶向造影剂(0.2mL/kg),并用2mL生理盐水冲注,并在相同的时间点采集图像。使用机器自带软件分析肿瘤组织的上升时间(RT)、达峰时间(TTP)、峰值强度(PI)、平均渡越时间(MTT),回声强度测定点选自肝脏肿瘤中心,所有选取位点均避开坏死区域。分析过程采取盲法,实验动物随机编号。
1.6 统计学分析
采用SPSS 17.0统计分析软件。实验数据为计量资料,用表示。2组间比较采用配对t检验,P<0.05为差异有统计学意义。
2 结果
2.1 模型建立
VX2肿瘤种植时间为2周,42只日本大耳兔中有34只存活并长出肿瘤,2只在肿瘤种植麻醉过程中死亡,6只在肿瘤形成期间死亡,经B超检查证实34只模型兔中有6只肿瘤最大径均≤1cm,最终将28只模型兔(肿瘤最大径均>1cm)纳入实验分析。
2.2 超声显像
2.2.1 二维灰阶显像和CDFI显像
灰阶超声显示肿瘤呈不均质低回声结节,内可见无回声坏死区及多个点状强回声钙化(图1a);CDFI显示肿瘤内可见多个短线状或条索状血流信号(图1b)。
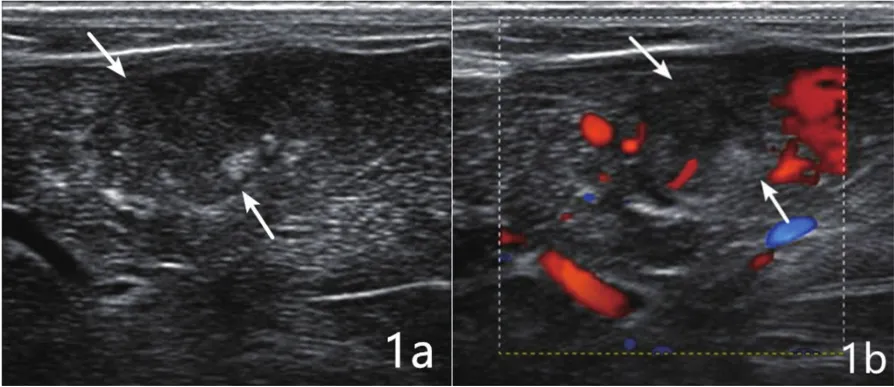
图1 兔VX2肝癌模型造影前超声显像a.灰阶超声显示肿瘤内呈不均质低回声(箭);b.CDFI显示肿瘤内可见短线状血流信号(箭)
2.2.2 造影显像
造影剂经留置针注入兔耳缘静脉后,约10-30s出现动脉相增强,肿瘤周边呈明显“环形”强化,内部呈“片状”或“树枝状”强化,部分坏死区无强化,肿瘤整体强化程度明显高于周边正常组织;约30-120s出现门脉相增强,肿瘤内部仍可见部分强化,整体轮廓更加清晰,因该时相周边正常组织造影进一步增强,而肿瘤组织强化减弱,肿瘤整体强化程度近似或稍低于周边正常组织;120s以后为延迟相,造影剂于该时相已完全退出肿瘤组织,肿瘤呈现低回声,肿瘤整体强化程度明显低于周边正常组织。全部造影过程表现为“快进快出”的特点,是典型恶性肿瘤的增强方式。普通组与IL-8组均于造影剂注入后20s、80s、150s三个时间点取图作为动脉相、门脉相、延迟相的显像。普通组动脉相:肿瘤周边明显强化,内部可见小片状强化(图2a);IL-8组动脉相:肿瘤周边及内部均明显强化,内部可见多个片状及树枝状强化区(图2b);普通组门脉相:肿瘤呈低回声,强化程度低于周边正常组织(图2c);IL-8组门脉相:肿瘤呈稍低回声,强化程度略低于周边正常组织,其内仍可见少量造影剂充填(图2d);普通组延迟相:肿瘤呈低至无回声,强化程度明显低于周边正常组织(图2e);IL-8组延迟相:肿瘤回声明显减低,其内可见极少量造影剂充填(图2f)。
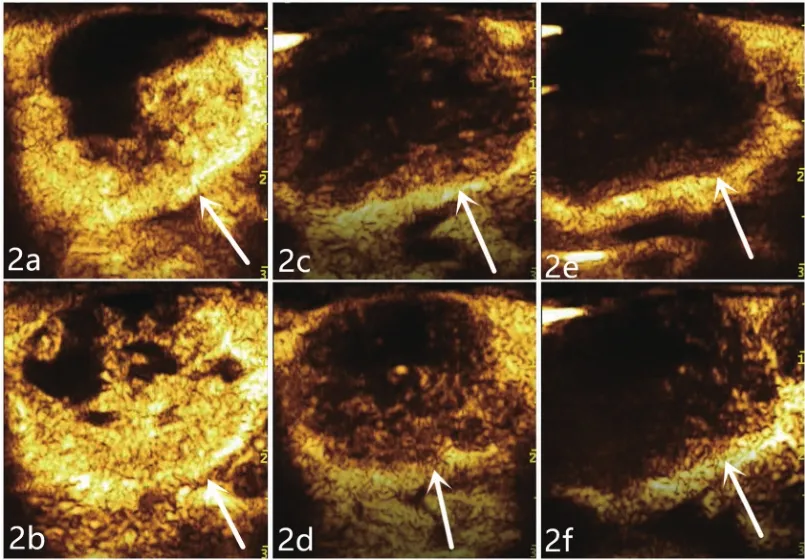
图2 两组兔VX2肝癌模型在三个时相的造影显像 a.普通组动脉相(箭);b.IL-8组动脉相(箭);c.普通组门脉相(箭);d.IL-8组门脉相(箭);e.普通组延迟相(箭);f.IL-8组延迟相(箭)
2.3 造影参数分析
两组不同造影剂进入肿瘤后,其上升时间的比较无统计学意义(P>0.05),而达峰时间、峰值强度及平均渡越时间的比较均有统计学意义(P<0.05),见表1。提示携IL-8单抗的靶向微泡在最初进入肿瘤时的速率及数量与普通脂质微泡相似,在肿瘤显影的初始阶段无明显差异;随后,由于靶向作用,靶向微泡与炎症因子(IL-8)快速结合,IL-8组的达峰时间明显短于普通组,且IL-8组肿瘤组织回声强度随着时间继续増高,当结合达到饱和时,回声强度达到峰值而不再增加,其峰值强度明显高于普通组;全部造影过程中靶向微泡与炎症因子(IL-8)的结合作用持续存在,IL-8组的平均渡越时间较普通组明显延长。

表1 两组造影剂对兔VX2肝癌模型的造影参数比较
3 讨论
近年来,超声造影剂的研究进展主要体现在微泡直径的减小(d<8μm)和稳定性的提高,微泡造影剂可通过无创注射从血液循环到达靶器官或靶组织内持续性显影[7],这些都提高了病灶超声造影诊断的准确性,然而目前大多数超声造影剂不具备靶向选择性[8]。研究表明[9-10],在肝癌发生发展过程中存在大量炎性反应,并在组织内释放多种炎症因子,其中IL-8是参与肝癌炎性反应最重要的炎症因子之一。故此,本实验通过对普通超声造影剂进行特殊改造,将IL-8单抗连接修饰于普通声学造影剂表面[11],通过特殊的结合反应,携IL-8单抗靶向造影剂可快速、准确的到达肿瘤内。相较传统超声造影剂,携IL-8单抗靶向造影剂具备高度靶向选择病灶,与病灶特异性结合且持续显影的优势。
肝脏肿瘤多由肝动脉供血,而正常肝脏主要由门脉供血[12]。超声造影检查利用肝脏肿瘤与正常肝脏供血系统的不同,在注入声学造影剂后,通过两者间增强显影时间及回声强度的差异来进行肿瘤的检测[13]。本实验发现,两种造影剂对VX2肝癌的显影均表现为“快进快出”的增强方式,不同的是,在造影的三期(动脉相、门脉相、延迟相)中,普通造影剂对肿块的显影强度均低于携IL-8单抗靶向造影剂。由此可认为,肿瘤炎症反应中释放的炎性因子IL-8与IL-8单抗之间存在明显的靶向趋化作用。
通过对造影参数的比较,在保持其他实验因素一致的情况下,携IL-8单抗靶向造影剂对肿瘤显影的速度、强度及渡越时间均优于普通声学造影剂。分析其原因可能为普通脂质微泡不具有靶向性,不能与肿瘤的血管内皮细胞特异性黏附,在后继微泡的推动、血流剪切力等外力的作用下被带离肿块,而靶向微泡能与释放IL-8的血管内皮细胞特异性结合,其本质为具有高度特异性抗原-抗体的非共价结合,依靠正、负电荷吸引形成稳定复合物[14],血流的冲击力和剪切力亦不易使其脱离肿块。当携IL-8单抗与IL-8识别且结合后,大量靶向微泡迅速聚集于肿瘤内,其达峰时间大幅缩短但显影强度却明显高于普通微泡;当靶向微泡与肿瘤新生血管内皮细胞结合达到饱和时,病灶区域回声强度不再增强。但由于这种特异性结合持续作用,其渡越时间仍长于普通微泡。由此可说明,携IL-8单抗靶向造影剂对于肝癌的定位和诊断均优于二维超声和普通造影剂,具有高度灵敏性、特异性和靶向性的特点,且造影剂在肿瘤内停留时间更长,不仅可以适当减轻癌灶内的炎症反应,亦可以为肝癌的相关治疗如射频消融治疗等提供更多的定位显影时间。
本实验所采用的靶向微泡在动物实验中应用较为广泛,但仍需解决某些问题,如何对微泡的组成或制备过程进行改进,平衡微泡造影剂与组织细胞损伤之间的关系,使经超声显影的组织不发生实质性的变化,使病灶有效显影,又不致使正常组织细胞受损,这将成为后期实验继续关注的重点之一。
综上所述,携IL-8单抗靶向造影剂可在短时内精准显影于肝癌肿块内,明显提高对肝癌诊断的效率和诊断准确性,同时IL-8单抗与IL-8的结合作用可以缓和一部分肿瘤内的炎症反应,延长显影时间,这有望成为临床上对肝癌诊断、治疗的另一突破点。
