肠道微生物能抗癌吗
2020-03-24张宇
张宇
既往,由于缺乏对肠道微生物的了解,人们一度认为,它们只是一群喜欢吃粪便的细菌而已,似乎与肠道中的寄生虫没什么两样。但实际上,这些小到只有通过显微镜才能看得到的生物,对人体健康有着非同一般的影响。
肠道微生物的影响
这么说吧,无论是从个体数量,还是基因组的体量,肠道微生物都可以用“巨大”来形容。尤其是基因组,因其蕴含的基因,以及可转录的蛋白之重要,更是被称为“第二基因组”和人体“隐形”的器官,其重要性可见一斑。近年来的研究表明,肠道微生物有希望解决现代医学中最棘手的癌症问题,那这又是怎么一回事呢?
众所周知,癌症是人类健康的头号杀手。根据国家癌症中心发布的数据显示,2017年全国恶性肿瘤新发病例数达380.4万例,相当于平均每天有超过1万人被诊断为癌症患者,平均每分钟内就有7人。所以,无论是药物还是治疗方法,只要和抗癌沾上边,那绝对火爆到极点。
2019年1月,世界知名科学杂志《自然》上发表了一篇关于肠道穿孔可以对抗癌症和感染的文章,顿时在全球医学和微生物学界引起了不小的轰动。文章指出,人体肠道中的微生物可以通过增强免疫细胞活性来影响免疫系统,使其具有杀伤细胞的能力,从而达到对抗癌症和防止感染的效果。
微生物抗癌原理发现史
那么,肠道微生物的抗癌原理是现在才被发现的吗?其实不是,人们自意识到肠道微生物对人体可能存在健康效应时起,就已经开始着手关于肠道微生物与癌症相关的研究了。曾有两项研究从侧面印证了肠道微生物可能与抗癌有关。一是科学家们在研究中发现,接受了混合抗生素治疗的模型小鼠,其肿瘤抑制能力明显减弱,抗生素在杀灭肠道微生物的同时,也抑制了肠道微生物的生存。二是科学家将模型小鼠和正常小鼠共同饲养,发现小鼠肠道菌群的特异性逐渐降低,模型小鼠的肿瘤抑制能力居然也同样逐渐消失!这说明当恢复和正常小鼠一起进食后,肠道微生物也恢复了正常,这些都表明了肠道微生物在控制肿瘤的生长中起到了关键作用。但由于当时发现的机制过于复杂,无法阐明具体原因。
目前,包括《自然》在内的多个国际顶级期刊陆续刊发了关于肠道微生物抗癌的文章:
据报道,体内有一种细胞叫作“细胞毒性CD8+T细胞”,它是一种能够表达CD8分子的T细胞,CD8共同受體主要表达在表面的细胞毒性T细胞。同时,它也是一种特效性免疫细胞,可识别并杀死感染细胞和癌细胞。Tanoue等人在《自然》杂志上报道了11种细菌的鉴定。这些细菌存在于一些健康人的肠道中,它们可以驱动CD8+IFN-γ+T细胞在小鼠结肠中的积聚。这些细胞可能是由结肠中现有T细胞的增殖和分化而来,或者是身体其他部位的细胞聚集而成,又或者是两者结合所产生的。CD8+IFN-γ+T细胞能够特异性识别这11种菌株的细菌抗原。Tanoue等人发现的被称为“树突状细胞”的免疫细胞有助于向T细胞提供细菌抗原。而树突状细胞和T细胞之间的这种相互作用有助于激发T细胞应答,从而达到抗感染、抗癌的效果。
发表于国际顶级期刊《科学》上的一篇报道显示,通过给小鼠口服双歧杆菌,也能达到与抗PD-L1免疫抑制剂同等的效果,而联合治疗几乎能完全抑制肿瘤生长。其机制可能是通过启动CD8+T细胞来增强PDL1抗体的抗癌效果。
此外,法国科学家还利用一种环磷酰胺的抗癌药物改变肠道微生物的种群构成,驱使种群中的革兰氏阳性菌进入次级淋巴系统,触发一种特殊的功能,辅助T细胞对肿瘤发动攻击,从而达到杀灭肿瘤的治疗效果。
不仅如此,动物实验还发现增加对调节T细胞的诱导,可加强小鼠反自体炎症的能力,使肠道微生物重塑,维持小鼠肠道内稳态,减少炎症的发生,从而达到预防疾病的目的。
以上这些研究都证明肠道微生物能够调节人体免疫力,最终达到杀伤肿瘤干细胞和预防肿瘤细胞增殖的效果。但是,世间事皆有两面性,肠道微生物与癌症的关系也是如此。
诱发或加重癌症的原因
不正常的肠道微生物也可能会诱发或加重癌症的发生与发展,这又是怎么一回事呢?众所周知,癌症本质上是一类基因病,各种环境和遗传的致癌因素以协同或序贯的方式引起DNA损害,从而激活原癌基因和(或)灭活肿瘤抑制基因,加上凋亡调节基因和(或)DNA修复基因的改变,从而引起表达水平的异常,使靶细胞发生转化。而炎症就是诱发细胞基因改变,进而发生癌症的重要因素。
20世纪90年代,科学家们首次将传染性幽门螺杆菌与胃癌联系起来。从那时起,研究还发现了其他细菌与癌症的发生和发展有关。这些微生物能激活炎症反应并破坏粘液层,保护身体免受外来入侵物的伤害,从而创造出有利于肿瘤生长的环境。这种现象也在结肠中有所发现。健康的结肠上皮细胞覆盖着2层粘液,即粘液内层和粘液外层。粘液外层附着着大量共生菌群,而内层粘液致密,微生物难以渗入,从而阻止了微生物与宿主结肠上皮细胞的直接接触。一旦有保护性的粘液层遭到破坏,微生物伺机进入并与上皮细胞接触形成生物膜,引起炎症性肠病并伴随组织生物学变化,就有可能形成癌症。
研究发现,在癌变的细胞中,微生物还会影响结直肠癌患者机体的免疫细胞。例如,具核梭杆菌产生的一种特殊蛋白质能进入到T细胞和自然杀伤细胞的免疫受体中,从而阻断免疫细胞对肿瘤细胞的毒作用,有利于恶性肿瘤的形成。

在正常稳态条件下,肠道共生菌被Toll样受体识别,在维持肠道上皮细胞内稳态方面发挥至关重要的作用。肠道微生物组与人体免疫细胞之间存在一个动态平衡的相互作用网,肠道微生物一旦失衡或失调就会引起一系列的免疫性疾病、炎症性疾病及癌症的发生。国外研究发现,如果肠道菌群中的白色念珠菌发生突变,其产生的特异性化学物质就会影响免疫应答,使免疫系统过分敏感而产生过敏性疾病。
抗癌药物的筛选
近年来,科学家在以肠道微生物筛选抗癌药物方面也有重大发现。研究发现,某些特定微生物或酶的存在,竟能使特定癌症疗法对某些人群失效。一个人的独特肠道和其他微生物组也能对其具体药物的敏感性造成極大影响。PD-1、PD-L1、CTLA-4等免疫治疗药物的研发成功是这两年肿瘤治疗领域的最大进展,但这些药物并不能让所有人受益,治疗响应率大概只有20%左右,原因可能就和肠道微生物有关。
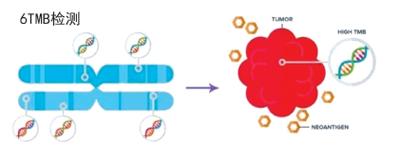
如何在患者用药之前就能判断抗体是否有效,是全世界科学家、临床医生和患者都在关注的问题。除了PD-L1表达、TMB检测、MSI检测、dMMR检测等手段,预先利用肠道菌群的敏感性分析进行抗癌药物的筛选也成了快速选择药物与疗效预评估的重要手段。
治疗癌症的“新”方法
你听说过肠道微生物移植吗?近几年,科学家们还进行了更为大胆的尝试,那就是进行肠道微生物移植。既然肠道微生物对癌症的发生和杀灭有着非常重要的作用,那是否可以基于已发现的成果,将健康人体的肠道微生物移植给容易患癌的人群,或者癌症患者呢?基于这一设想,一项被称为“粪便微生物移植”的技术出现了,其方法为,将来自健康供体的粪便样品移入患者的肠道,让来自于健康人体的肠道微生物在患者肠道内定居、繁殖,从而改善其健康状态。目前,该项研究已经应用于治疗艰难梭菌引发的顽固性结肠感染。在新研究中,粪便移植“辅助”的是免疫检查点抑制剂——PD-1抗体,它是免疫疗法中的热门利器,已获批用于多种难治癌症的治疗。
肠道微生物抗癌之门已经打开,相信将有无限可能等待我们去发现。例如,可以将肠道微生物组及其代谢产物与免疫疗法结合来进行抗肿瘤治疗,也可以和传统的直接靶向治疗恶性细胞的方法结合起来,还可以基于肠道微生物组诱导机体的免疫反应及诱癌机制来筛选高效抗癌菌株,从而开发新型高效的抗癌菌剂等等。
综上所述,肠道微生物的组成、种类、位置和特性等都可能影响抗肿瘤药物的疗效。有关肠道微生物与药物之间多方面关系的研究仍在继续,研究人员已经意识到了肠道微生物在肿瘤药物与肿瘤治疗中至关重要的作用。或许在不远的将来,科学家们能够探清机制,平衡好微生物与药物之间的相互作用,从而敲开针对各类人不同肠道微生物的个性化药物疗法的大门。