mFOLFOX6化疗联合射频消融治疗原发性肝癌的疗效及机制研究
2020-03-24符白玉林怡徐琪张杰伟
符白玉 林怡 徐琪 张杰伟
原发性肝癌发病隐匿,临床确诊时多处于中晚期,大多数失去手术切除机会。射频消融(radiofrequency ablation,RFA)为临床新型微创技术之一,能局部彻底杀灭肿瘤细胞,疗效明确且患者耐受性好[1],在各种实体肿瘤中应用较多,特别是原发性肝癌,被认为是继手术切除、介入治疗后治疗肝癌的第三大方法,且其治疗小肝癌疗效与手术切除相当[2]。但受肿瘤大小、位置等影响,RFA治疗范围受限,可能影响原发性肝癌整体疗效。mFOLFOX6为新辅助化疗方案之一,通过调整药物剂量以达到杀灭肿瘤细胞、增强肿瘤细胞药物敏感度的目的。目前临床关于mFOLFOX6化疗+RFA治疗原发性肝癌相关报道尚少,基于此,本研究通过对照试验分析mFOLFOX6化疗联合RFA治疗原发性肝癌的疗效及对相关血清指标及10号染色体缺失的磷酸酶及张力蛋白同源物((phosphatase and tensin homolog deleted on chromosome ten,PTEN)通路相关基因表达的影响,以为临床肝癌治疗提供新方向,改善患者预后。现报道如下。
1 资料与方法
1.1 一般资料
抽取本院2014年1月至2017年1月收治的原发性肝癌患者94例,随机数字表格法将其分为观察组与对照组,各47例。观察组中男30例,女17例;年龄33~67岁,平均(47.62±10.34)岁;肿瘤直径≥5cm者33例,<5cm者14例;其中单发37例,多发10例。对照组中男28例,女19例;年龄34~68岁,平均(48.10±10.58)岁;肿瘤直径≥5cm者30例,<5cm者17例;其中单发35例,多发12例。上述一般资料2组比较差异均无统计学意义(P>0.05),有可比性。本次研究经医院伦理委员会批准,患者均知情同意。
1.2 纳入及排除标准
纳入标准:符合原发性肝癌诊断标准[2];肿瘤数目不超过3个;未累及邻近器官、无远处转移;符合RFA适应证;均在本院接受治疗。排除标准:凝血机制异常;黄疸、肝外组织器官转移;肝肾原发性疾病;RFA禁忌症;相关药物过敏;相关资料不全者。
1.3 试剂与仪器
奥沙利铂购自南京制药厂有限公司,国药准字H20000686;亚叶酸钙购自江苏恒瑞医药股份有限公司,国药准字H20000584;氟尿嘧啶购自上海旭东海普药业有限公司,国药准字H31020593;血清血管内皮生长因子(vascular endothelialgrowth factor,VEGF)、碱性成纤维细胞生长因子(basic fibroblast growth factor,bFGF)、糖类抗原199(carbohydrate antigen199,CA199)及甲胎蛋白(alpha fetoprotein,AFP)酶联免疫吸附法(Enzyme-Linked ImmunoSorbent Assay,ELISA)试剂盒均购自上海江莱生物科技有限公司,分别为a12871、JL10364、0-009644、JL23952;RNA提取试剂盒购自美国Sigma公司,货号为T9424;RT试剂盒购自美国Roche公司,货号为4655885001;RITA1500X射频消融治疗系统购自美国RITA公司,包括射频发生器、负极板、射频电极等,输出频率460kHz±5%;ZF-6紫外分析仪购自上海市金鹏分析仪器有限公司,波长254 nm、365nm;RDY-SP8型琼脂糖电泳仪购自上海市金鹏分析仪器有限公司,包括凝胶板、缓冲液、电泳槽等;PTEN、VEGF与缺氧诱导因子-1(hypoxia inducible factor-1,HIF-1)引物均购自美国Proteintech公司。
1.4 治疗方法
观察组行mFOLFOX6化疗联合RFA治疗,先给予RFA处理:根据患者肿瘤位置选择合适体位及进针路线,确定穿刺点及深度,局部麻醉成功后于超声或计算机断层扫描(computerized tomography,CT)引导下将射频针穿刺到肿瘤靶位置,依据肿瘤直径及位置确定消融相关参数:温度80℃~100℃,时间10~30min;通常消融范围为肿瘤及正常肝组织(0.5~1.0)cm。RFA治疗7d后给予mFOLFOX6化疗:奥沙利铂85mg/m2静滴,第1d;亚叶酸钙400mg/m2静滴,第1d;氟尿嘧啶500mg/m2静滴,第1、2 d。1个化疗周期2周,连续干预3个周期。对照组仅给予RFA治疗,操作方法同观察组。
1.5 观察指标
1.5.1 近期疗效
以实体瘤疗效评价标准[3]为依据,完全缓解(complete remission,CR):靶病灶全部消失,肿瘤标志物水平降至正常范围,且持续至少4周;部分缓解(partial remission,PR):病灶长径总和缩小30%以上,且持续至少4周;稳定(stable disease,SD):介于PR与疾病进展(progression disease,PD)间;PD:病灶长径总和增大20%以上,或新病灶出现。有效率(response rate,RR)=CR率+PR率;疾病控制率(disease control rate,DCR)=100%-PD率。
1.5.2 血清指标测定
分别于治疗前、治疗后2周空腹抽取患者外周静脉血3mL,以2000r/min速率常规离心,离心15min,血清提取后保存待测。均通过ELISA测定2组患者血清VEGF、b FGF、CA199及AFP水平,严格按照ELISA试剂盒说明书操作。
1.5.3 PTEN通路相关基因测定
包括PTEN、VEGF与HIF-1mRNA表达,于治疗后7d行肿瘤组织活检,检测方法为逆转录-聚合酶链式反应法(reverse transcription-polymerase chain reaction,RT-PCR):依据RNA提取试剂盒说明书提取肝组织标本总RNA,采用紫外分析仪、琼脂糖电泳仪分别对总RNA浓度、完整性进行检测。按照RT试剂盒说明书将总RNA反转录成cDNA。
1.6 统计学处理
应用SPSS 20.0软件处理数据,计数资料以率表示,行χ2检验;计量资料以(±s)表示,行t检验;以P<0.05为差异有统计学意义。
2 结果
2.1 近期疗效
观察组RR、DCR均高于对照组,差异均有统计学意义(P<0.05),见表1。

表1 2组近期疗效比较[n=47,(%)]Table1 Comparison of short-term curative effect between the 2 groups[n=47,(%)]
2.2 血清VEGF、bFGF水平变化
与治疗前比较,2组治疗后血清VEGF、bFGF水平均明显下降(P<0.05);观察组治疗后血清VEGF、bFGF水平均明显低于对照组,差异有统计学意义(P<0.05),见表2。
表2 2组治疗前后血清VEGF、b FGF水平比较[(±s,pg/mL),(n=47)]Table2 Comparison of serum VEGF and bFGF levels before and after treatment in the 2 groups[(±s,pg/mL),(n=47)]
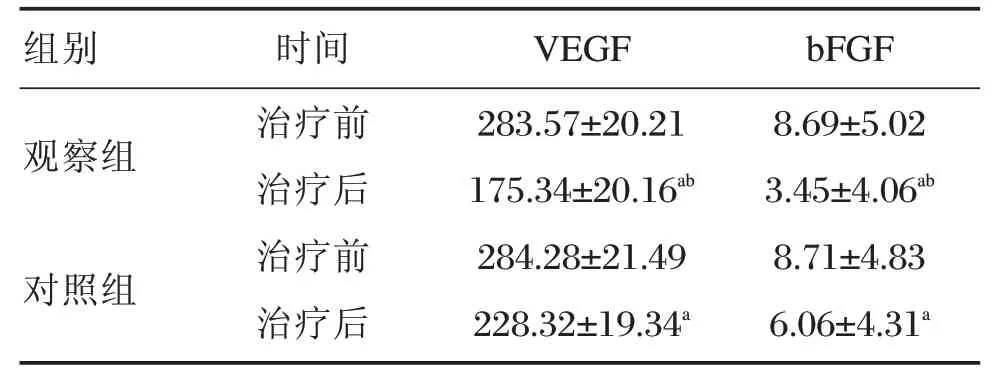
表2 2组治疗前后血清VEGF、b FGF水平比较[(±s,pg/mL),(n=47)]Table2 Comparison of serum VEGF and bFGF levels before and after treatment in the 2 groups[(±s,pg/mL),(n=47)]
注:与同组治疗前比较,aP<0.05;与对照组治疗后比较,bP<0.05。
组别观察组对照组时间治疗前治疗后治疗前治疗后VEGF 283.57±20.21175.34±20.16ab 284.28±21.49 228.32±19.34a bFGF 8.69±5.023.45±4.06ab 8.71±4.836.06±4.31a
2.3 血清CA199、AFP水平变化
与治疗前比较,2组治疗后血清CA199、AFP水平均明显下降差异具有统计学意义(P<0.05);观察组治疗后血清CA199、AFP水平均明显低于对照组,差异有统计学意义(P<0.05),见表3。
表3 2组治疗前后血清CA199、AFP水平比较[n=47,(±s)]Table3 ComparisonofserumCA199andAFPlevelsbefore andaftertreatmentinthe2groups[n=47,(x±s)]

表3 2组治疗前后血清CA199、AFP水平比较[n=47,(±s)]Table3 ComparisonofserumCA199andAFPlevelsbefore andaftertreatmentinthe2groups[n=47,(x±s)]
注:与同组治疗前比较,aP<0.05;与对照组治疗后比较,bP<0.05。
组别观察组对照组时间治疗前治疗后治疗前治疗后CA199(U/L)80.15±9.31 34.26±5.10ab 79.87±10.00 64.13±7.89a AFP(ng/mL)183.16±35.24 73.17±9.38ab 182.94±37.02 130.25±20.11a
2.4 肝组织PTEN通路相关基因表达
观察组治疗后PTENmRNA表达比对照组高,而VEGF、HIF-1mRNA表达比对照组低,差异均有统计学意义(P<0.05)。见表4。
表4 2组治疗后PTEN、VEGF与HIF-1mRNA表达量比较[n=47,(±s)]Table4 Comparison of PTEN,VEGF and HIF-1mRNA expression after treatment in the 2 groups[n=47,(±s)]
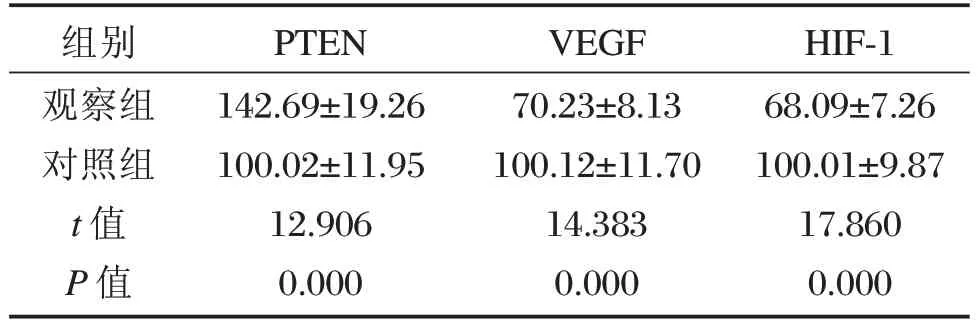
表4 2组治疗后PTEN、VEGF与HIF-1mRNA表达量比较[n=47,(±s)]Table4 Comparison of PTEN,VEGF and HIF-1mRNA expression after treatment in the 2 groups[n=47,(±s)]
组别观察组对照组t值P值PTEN 142.69±19.26 100.02±11.9512.9060.000VEGF 70.23±8.13100.12±11.7014.3830.000HIF-168.09±7.26 100.01±9.8717.8600.000
2.5 不良反应情况
所有患者均无严重RFA相关不良反应发生。观察组化疗期间发生白细胞计数减少1例,轻度肝功能损害3例。
3 讨论
临床发现,受肝动脉解剖、侧支循环形成等多种因素影响,肝动脉化疗栓塞(transcatheter hepatic arterial chemoembolization,TACE)治疗原发性肝癌远期疗效不理想[4]。对此建议寻找新的手段或联合RFA及其他方法治疗[5-7]。
RFA以超声或CT为引导,可直接将电极引入肿瘤内部,经由高频电流生热让局部肿瘤细胞蛋白质变性及凝固性坏死,最终致使肿瘤组织脱落,达到彻底杀伤肿瘤细胞的目的[8]。若温度不能促使肿瘤组织坏死,肿瘤内附近血管组织因射频作用会形成反应带(约10mm),对肿瘤血液供应阻断,以诱导癌组织死亡,减少转移风险[9]。苗同国等[10]研究表明RFA能有效改善原发性肝癌患者细胞免疫功能。由于RFA治疗范围有限,为进一步提高原发性肝癌疗效,我们采取RFA联合化疗方案治疗。mFOLFOX6化疗方案包括奥沙利铂、亚叶酸钙、氟尿嘧啶成分,其中氟尿嘧啶于细胞内转化成脱氧核苷酸,抑制并破坏DNA之胸苷酸合成酶合成,且氟尿嘧啶通过转化进入核糖核酸,对蛋白质合成影响,可对细胞形成各时期作用。临床发现氟尿嘧啶与奥沙利铂、亚叶酸钙合用相对单药干预效果明显,且不显著增加化疗不良反应[11]。
本研究结果显示相比单纯RFA治疗,RFA联合mFOLFOX6化疗治疗近期疗效显著,与胡十齐等[12]研究结果相符。表明RFA联合化疗治疗原发性肝癌疗效更好,这是因为RFA通过高频电流杀灭肿瘤细胞,联合化疗药物能更彻底的杀灭肿瘤细胞。同时本研究发现联合治疗不显著增加化疗毒副反应,患者可耐受。本研究还从血清分子指标及肿瘤生长信号通路方面评价原发性肝癌治疗效果及预后。血清指标指标方面,VEGF为临床常见血管生长因子之一,对血管内皮细胞特异性作用以参与实体瘤血管新生、侵袭及转移过程。bFGF除了对正常组织影响外,还参与肿瘤间质血管新生、侵袭等。张惠洁等[13]研究发现TACE联合索拉非尼相比单纯TACE能明显降低肝癌患者血清VEGF、bFGF水平。本研究结果显示相比单纯RFA治疗,RFA联合mFOLFOX6化疗能进一步降低血清VEGF、bFGF水平,抑制癌细胞活性,阻断其转移。这不但与RFA阻断血供,抑制肿瘤新生血管形成有关,而且与mFOLFOX6化疗药物促使肿瘤细胞死亡,减轻肿瘤负荷,进而促使VEGF、bFGF水平降低有关。为此笔者认为VEGF、bFGF下降可作为原发性肝癌疾病控制评价指标。AFP、CA199为临床常见肿瘤标记物[14],也被认为是肿瘤复发相关指标,其中AFP为原发性肝癌诊断敏感性指标。CA199常用于消化系统肿瘤诊断及观察,相关研究发现大部分原发性肝癌患者血清CA199水平升高,认为CA199可与AFP等指标一同成为原发性肝癌疗效判断指标[15]。本研究结果显示RFA联合mFOLFOX6化疗相比RFA单独治疗能进一步降低原发性肝癌患者血清CA199、AFP水平,可见联合治疗可彻底杀灭肿瘤细胞,促使血清肿瘤标记物趋于正常,也降低了治疗后复发几率。肿瘤生长信号通路方面,PTEN信号通路被发现参与细胞增殖、凋亡,在肿瘤血管生成中发挥至关重要的作用[16]。PTEN为抑癌基因之一,大部分肿瘤内其表达下降。VEGF、HIF-1属于PTEN信号通路下游基因,肿瘤缺氧时,HIF-1可作为转录激活介质,结合于VEGF启动相关因子,促VEGF表达及VEGF受体转录,进而肿瘤血管新生形成[17]。本研究显示,mFOLFOX6化疗联合RFA治疗能有效增强肝癌组织PTEN表达,抑制VEGF、HIF-1基因表达,阻断肿瘤细胞血液供应,进而降低血管形成相关指标VEGF、bFGF水平,促肿瘤细胞凋亡及肿瘤标记物下降,提高治疗效果。受观察时间影响,本研究未分析其复发及远期存活率,有待日后通过延长观察时间进一步探究。
综上,mFOLFOX6化疗联合RFA治疗原发性肝癌近期疗效较好,且较安全,能明显降低血清bFGF、CA199水平,调节PTNE信号通路。
