菱镁矿氨法制备氢氧化镁及活性氧化镁水化动力学研究
2020-03-19黄娜娜李会杰于亚杰王禹博王东意刘云义
黄娜娜,李会杰,仇 龙,于亚杰,王禹博,王东意,李 雪,2,刘云义,2
(1.沈阳化工大学 化学工程学院,辽宁省化工应用重点实验室,辽宁 沈阳 110142;2.辽宁精细化工协同创新中心,辽宁 沈阳 110142)
塑料、橡胶、合成纤维等高分子材料已被广泛应用于居民生产生活的方方面面,其易燃的缺点也逐渐引起人们的关注[1-5]。氢氧化镁是一种无机阻燃剂[6-9],具有广阔的应用前景[10-13]。同时,中国的菱镁矿储量丰富[14-15],这为氢氧化镁和氧化镁的制备提供了丰富的资源。随着科学技术进步和经济的发展,活性氧化镁应用范围会越来越广,需求也会增加,由于利用菱镁矿制备的轻烧氧化镁的活性低,因此,实验研究了以菱镁矿轻烧粉和盐酸反应制得的氯化镁溶液为原料,氨气为沉淀剂,制备氢氧化镁。以氢氧化镁为前驱体通过热分解的方法制备活性氧化镁,并对活性氧化镁的水化动力学进行了研究。
1 实验部分
1.1 氢氧化镁及氧化镁的制备
将轻烧粉与盐酸按照一定比例混合进行酸溶反应,得到酸溶精制氯化镁溶液,向氯化镁溶液中通入氨气制备氢氧化镁产品。以氢氧化镁为前驱体制备活性氧化镁,在N2气氛下,对氢氧化镁产品进行TG-DTG分析,其反应的实质就是氢氧化镁热分解的过程,更好的了解氧化镁的形成过程。
1.2 氧化镁活性的测定
柠檬酸法测变色时间。在20 ℃恒温水浴中,控制搅拌速度恒定,将2.0 g轻烧氧化镁加入到100 mL含有酚酞指示剂的0.2 mol/L柠檬酸溶液中,秒表记录从氧化镁加入到溶液呈现红色的时间,以表示轻烧氧化镁活性。
1.3 氧化镁水化实验
实验所需氧化镁均来源氢氧化镁的煅烧产物。将四口烧瓶固定于恒温水浴锅中,氧化镁和蒸馏水按照1 ∶40的质量比混合,分别在不同温度下进行水化反应,用电动磁力搅拌器设置恒定的搅拌速度。在不同水化温度下,每隔一段时间抽取一次浆液,直至水化4.0 h。用布氏漏斗快速抽滤,并用无水乙醇洗涤滤饼,除去残余的水分,滤饼转移到烘箱中干燥至恒重且准确称重,在800 ℃下煅烧且保温1.0 h,使氢氧化镁完全分解。取出冷却至室温,称重,由此计算出氧化镁的水化率,绘制出氧化镁的水化曲线。
2 实验结果与讨论
2.1 氢氧化镁TG-DTG分析
以1.0 mol/L的酸溶精制氯化镁溶液为原料,氨气为沉淀剂,在80 ℃下进行沉镁反应。并将氢氧化镁产品,在N2气氛下,流速为30.0 mL/min,升温速率分别为5 ℃/min、10 ℃/min、15 ℃/min、20 ℃/min、30 ℃/min,从40.00 ℃加热到1 000.00 ℃的条件下进行TG-DTG分析。氢氧化镁的TG分析见图1(a),DTG分析见图1(b)。
由图1可知,TG曲线只出现一个失重平台,温度在350 ℃~430 ℃之间;DTG曲线出现一个峰,所对应的温度随升温速率的增加向高温移动,说明氢氧化镁的分解一步完成,热分解过程为:
Mg(OH)2→MgO+H2O。


图1 氢氧化镁TG-DTG曲线Fig.1 The TG-DTG curve of Magnesium hydroxide
2.2 氢氧化镁及氧化镁SEM图
氢氧化镁及不同煅烧温度制备的氧化镁SEM图如图2所示。

图2 氢氧化镁及氧化镁SEM图Fig.2 SEM image of magnesium hydroxide and its magnesium oxide
由图2可知,在550 ℃~750 ℃之间,随着煅烧温度的升高,氧化镁的形貌并没有发生明显的变化,其整体保持氢氧化镁前驱体的晶体结构。
2.3 XRD分析
氧化镁的XRD表征结果如图3所示,部分晶面半宽高及峰高变化数据如表1所示。由图3 可知,不同煅烧温度制备的氧化镁谱图与标准氧化镁的谱图基本一致,氧化镁晶体的衍射峰位保持不变。由表1可知,随着锻烧温度的升高,MgO的峰高增加半宽高减小,即XRD图上的特征峰会变尖锐,这说明其晶粒结晶度随着焙烧温度的升高而逐渐增加。
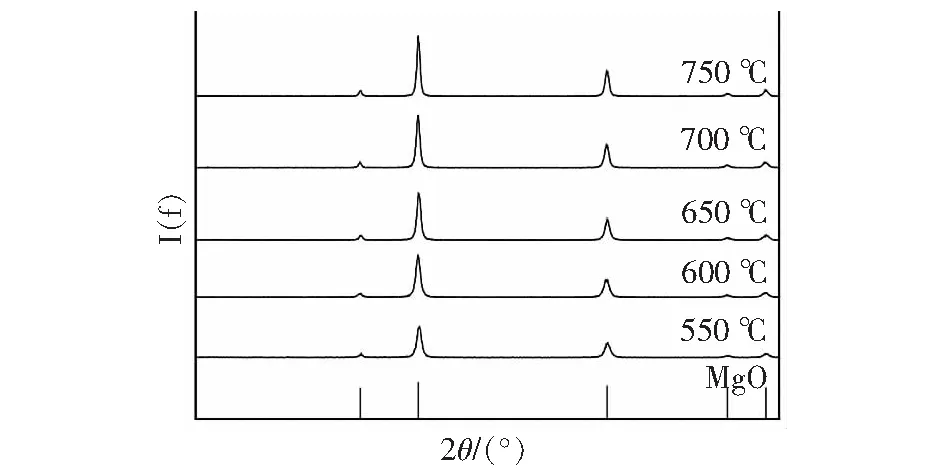
图3 氧化镁XRD图Fig.3 XRD pattern of magnesium hydroxide
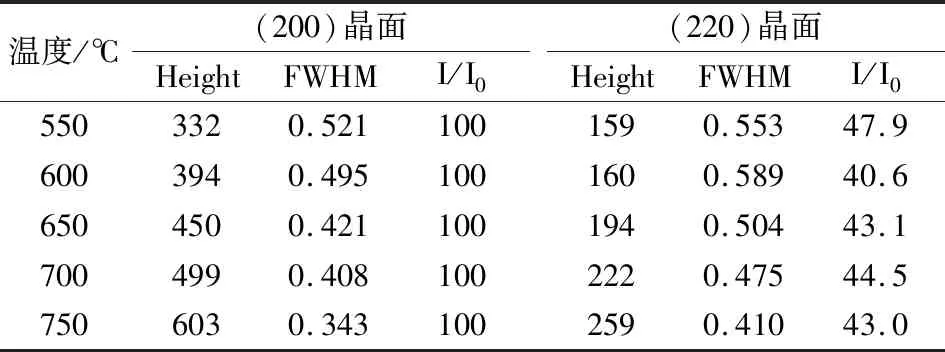
表1 煅烧温度对氧化镁不同晶面半宽高的影响Tab.1 Influence of calcination temperature on the half-width and half-height of different crystal faces of magnesium oxide
注:I/I0是检测峰与最强峰之间的强度比
2.4 煅烧温度对MgO活性的影响
实验结果表明,氢氧化镁分别在550 ℃、600 ℃、650 ℃、700 ℃、750 ℃下煅烧,氧化镁的活性存在一定的差异,部分有关数据如表2所示。

表2 不同煅烧温度所得 MgO活性测试结果Tab.2 Results of MgO activity test obtained from different calcination temperatures
从表2中可以看出,保温时间相同,随着煅烧温度升高,氧化镁与柠檬酸反应变色时间延长。结果表明,煅烧温度越高,生成的MgO的活性越来越低。这是因为在氢氧化镁彻底分解的情况下,刚开始生成的氧化镁晶格不够完善,结构松弛,其活性较高,随着煅烧温度升高,氧化镁的晶格逐渐趋于完善,晶粒之间空隙收缩,结构变得紧密,最终的产品活性降低。
2.5 氧化镁水化率及水化曲线
氧化镁水化率按下式计算:

式中:m1——为水化产物锻烧前质量;m2——为水化产物锻烧后质量。
水化率对水化时间做图,可以得到氧化镁的水化曲线如图4。从表2数据及水化曲线可以看出,氧化镁的活性及水化温度对水化率有很大的影响,不同活性的氧化镁,活性越高,水化速率越快;活性相同的氧化镁,水化温度越高,水化速率越快。


图4 氧化镁的水化曲线Fig.4 Hydration curve of magnesium oxide
2.6 氧化镁水化动力学方程与反应机理
将实验数据带入到各级反应速率方程,经试算可得,氧化镁水化反应符合一级反应动力学。将氧化镁水化数据分别做-ln (1-x)~t图得到其线性关系图,如图5所示。
实验结果表明氧化镁的水化反应符合简单的级数反应,其动力学方程为:-ln (1-x) =kt。
式中:x是氧化镁的水化率;t是水化时间;k是水化反应速率常数(即直线斜率)。不同煅烧温度下制备氧化镁的水化速率常数及其有关数据见表3。


图5 氧化镁水化反应-ln (1-x)~t图Fig.5 Magnesium oxide hydration reaction -ln(1-x)~t diagram
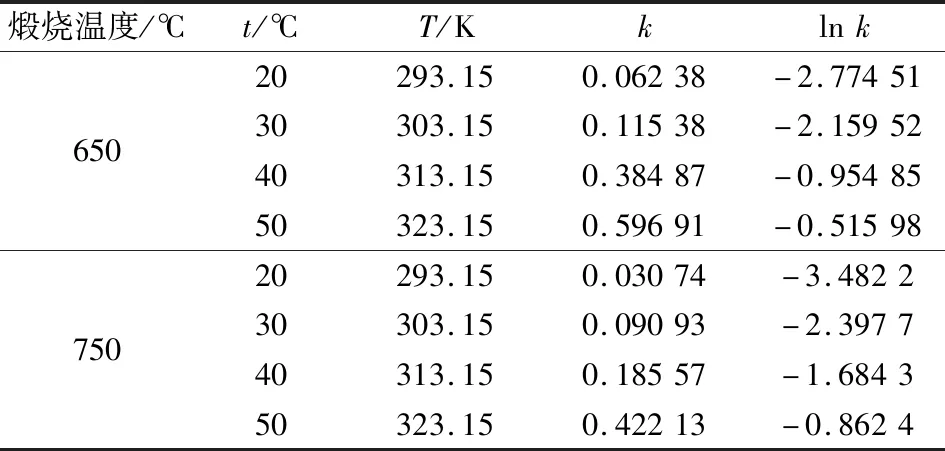
表3 氧化镁的水化速率常数及有关数据Tab.3 Hydration rate constant of magnesia and related data
根据阿伦尼乌斯公式:lnk=-Ea/RT+lnA,转化得到,同一镁源不同煅烧温度下所制氧化镁的活化能,见表4。

表4 不同煅烧温度所制氧化镁的水化反应活化能Tab.4 Activation energy of hydration reaction of magnesia prepared at different calcination temperatures
从表4数据可知,同一种镁源在不同煅烧温度下制备的氧化镁活化能存在一定的差异,随着煅烧温度的升高,氧化镁水化反应的活化能增大。当温度从550 ℃升高到750 ℃,氧化镁反应活化能从43.62 kJ/mol升高到67.91 kJ/mol,根据Bebson提出的关于化学反应和扩散控速的活化能判断依据:E扩散<25.12 kJ/mol 同一镁源,在550 ℃到750 ℃的温度范围内,随着煅烧温度的升高,氧化镁活性降低;氧化镁水化速率与其活性、水化温度及水化时间成正比关系;氧化镁的水化反应符合简单的级数反应,其动力学方程为:-ln (1-x)=kt,煅烧温度从550 ℃升高到750 ℃,氧化镁反应活化能从43.62 kJ/mol升高到67.91 kJ/mol,氧化镁的水化反应属于化学反应控速机理。3 结论
