壳聚糖共混膜的制备及其对Cu2+的吸附*
2020-03-16王淑荣王香爱刘小东
王淑荣,王香爱,曹 强,刘小东
(渭南师范学院 化学与材料学院,陕西 渭南 714099)
壳聚糖是甲壳素脱N-乙酰基的产物,是自然界中第二大的生物多糖[1],在药物研究、化学研究、食品生产、环境保护等诸多方面[2]被大量使用。壳聚糖可用来鳌合吸附多种物质[3]。壳聚糖分子中的氨基和羟基[4]能够与大多数的重金属离子相结合,络合形成稳定的螯合物[5],因此对工业废水、染料废水中的重金属离子有很好的去除效果,并且在净化自来水、人类健康保护等方面被广泛使用。日本是第一个用壳聚糖处理废水的国家,使用量达500 t/a,美国环境保护局也授权使用壳聚糖作为吸附介质来净化饮用水。铜是人体中不可或缺的微量元素[6]之一,其摄入必须满足一定的量,成人摄入量为20 mg/d。随着工业的发展,由于金属冶炼、合成产品等化工行业的发展,含有重金属离子的工业废水直接排入大江大河,使水中的动植物体内积攒大量的重金属离子,对人类和人类所生存的环境造成了无法估量的损害[7]。目前处理水中重金属离子的方法较多,吸附法[8]是最简单方便且容易实现和广泛运用的方法[9]。当人体内积攒了大量的重金属离子之后,这些金属离子就会对身体的内脏和其他器官造成极大的伤害,尤其是肝脏,如果肝脏受到伤害,新陈代谢就会失调,甚至会产生肝硬化、肝腹水等病症,对人体造成更大的伤害。作者以壳聚糖、聚乙烯醇、甘油制备共混膜[壳聚糖(CAS)和聚乙烯醇(PVA)之间以氢键结合,甘油增加了CAS/PVA共混膜的塑性],并研究其对水中的Cu2+的吸附。
1 实验部分
1.1 试剂与仪器
壳聚糖:脱乙酰化≥90.0%,上海蓝季生物;聚乙烯醇:分析纯,平均聚合度1 750±50,天津市天力化学试剂有限公司;乙酸:分析纯,质量分数36%,开封化学试剂;甘油、四氯化碳、硝酸、氯化铵、HCl:质量分数3%,氢氧化钠:质量分数3%,渭南师范学院;二乙基二硫代氨基甲酸钠:分析纯,天津市科密欧化学试剂有限公司;氨水:分析纯,质量分数25%,天津市滨海科迪化学试剂有限公司;氯化铵:分析纯,开封化学试剂总厂;铜粉:试剂级,天津市大茂化学试剂厂。
磁力加热搅拌器:GR-18,巩义市子华仪器有限责任公司;电热恒温鼓风干燥箱:DHG-9070A,上海一恒科学仪器有限公司;恒温水浴锅:HH-1,金坛市华城海纳仪器厂;搅拌器:上海梅颖浦仪器仪表制造有限公司;分析天平:赛多利斯科学仪器有限公司;分光光度计:UV-5200,上海元析有限公司;超声波清洗器:KH-100E,昆山禾创超声仪器有限公司。
1.2 实验方法
1.2.1 制膜液的制备
壳聚糖/乙酸溶液的制备:配制350 mL质量分数2%冰醋酸溶液。称取14 g CAS于500 mL烧杯中,加入配制的冰醋酸溶液,控制转速200 r/min搅拌2 h,去除不溶物,静止脱泡,即得到350 mL质量分数4%的壳聚糖/乙酸溶液。
聚乙烯醇/水溶液的制备:称取16 g PVA于500 mL烧杯中,加400 mL水,在85 ℃水浴中搅拌1 h(转速设置为200 r/min),去除不溶物,静止脱泡,即得到400 mL质量分数4%的聚乙烯醇水溶液。
1.2.2 共混膜的制备
壳聚糖/聚乙烯醇混合比例见表1。

表1 壳聚糖/聚乙烯醇混合比例
按照表1的实验方案取一定体积的壳聚糖/乙酸溶液和聚乙烯醇水溶液混合至100 mL,以单一聚乙烯醇膜为空白对照组,加入一定量质量分数10%的甘油(0.8、1.6、3.2 mL分别用1#、2#、3#表示),以200 r/min的转速搅拌1 h后取出,静置消泡,将其均匀涂抹在玻璃板上,放入烘箱,温度设置为40 ℃烘6 h。
1.2.3 溶胀性测定方法
将制得的共混膜裁剪为边长为2 cm的正方形,测其质量为m,放入装有50 mL蒸馏水的锥形瓶中静置6 h,用滤纸擦干吸附后的共混膜表面的蒸馏水,测其质量为m1溶胀性计算见式(1)。
溶胀性=(m1-m)/m×100%
(1)
式中:m为测定前膜质量,g;m1为测定后膜质量,g。
1.2.4 吸附实验
将制得的共混膜裁剪为所需大小,并放入配置好的废水水样中,采用控制变量法,分别控制pH值、温度、吸附时间进行浸泡吸附。
1.2.5 铜标准溶液的配制
配置质量浓度为5.00 μg/mL的铜标准溶液,静置待用。
1.2.6 模拟废水水样的配制
使用质量浓度为5.00 μg/mL的铜标准溶液配制质量浓度为0.2 μg/mL的模拟水样,静置保存待用。
1.2.7 显色萃取
取10 mL吸附后的样液于50 mL容量瓶中加水稀释至标线。取稀释后的试样和氯化铵氨性缓冲液按体积比1∶1于分液漏斗中混合,再加入5 mL显色剂,摇匀后放置5 min,最后加入10 mL CCl4,充分摇匀后静置分层,取下层淡黄色有机溶液进行吸光度测量。
1.2.8 吸光度的测定
在440 nm的波长下,先将比色皿进行3次润洗,再向比色皿中加入显色萃取后的待测液,保证比色皿内部无气泡,外部无水珠,再将其放入分光光度计中,以CCl4作为参比,测量其吸光度,并记录实验数据。
1.2.9 标准曲线的绘制
5个50 mL容量瓶中,分别加入0、1.0、2.0、3.0、4.0、5.0 mL的铜标准溶液,用蒸馏水定容,分别按照显色萃取的步骤,以模拟吸附后测量吸光度的环境,测定其吸光度,用CCl4作为参比,绘制标准曲线见图1。
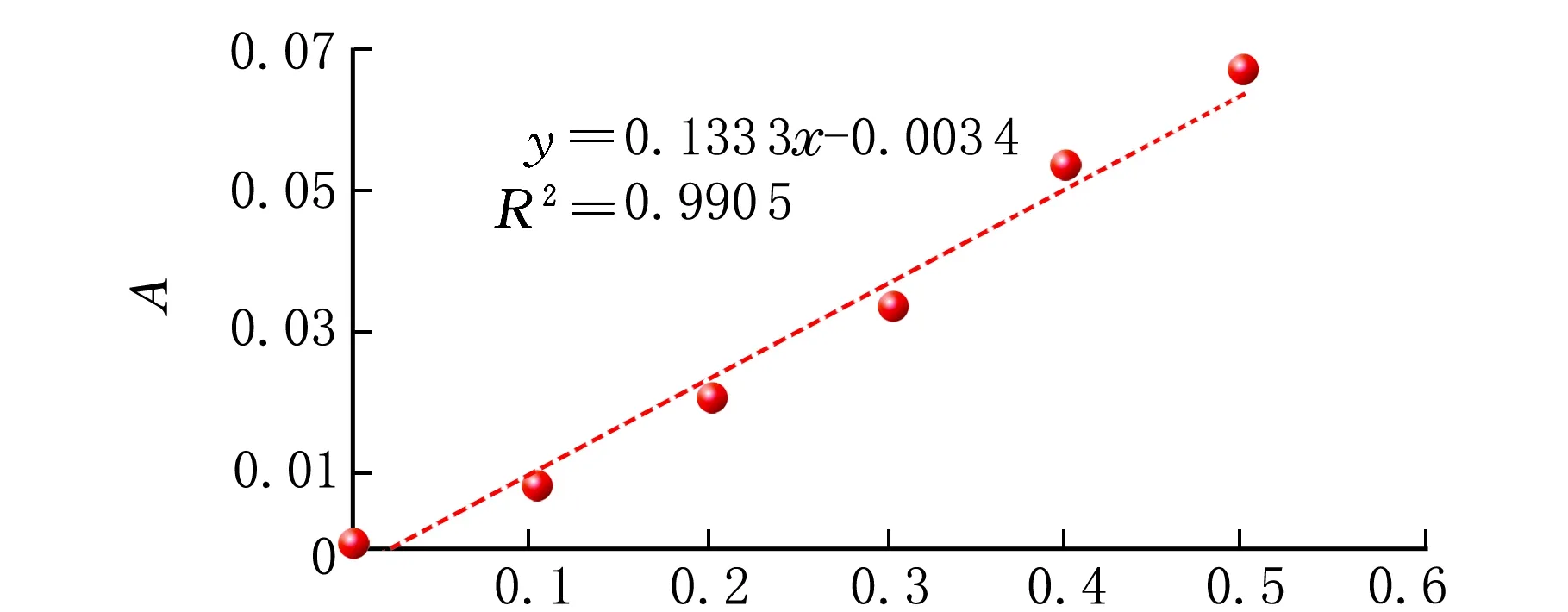
ρ(Cu2+)/(μg·mL-1)图1 Cu2+标准曲线图
由图1可知,此离散数据的相关性较好,可用该方程来描述实验所得数据的变化趋势。
2 结果与讨论
2.1 共混膜性能的分析
共混膜溶胀性的测定结果见表2。
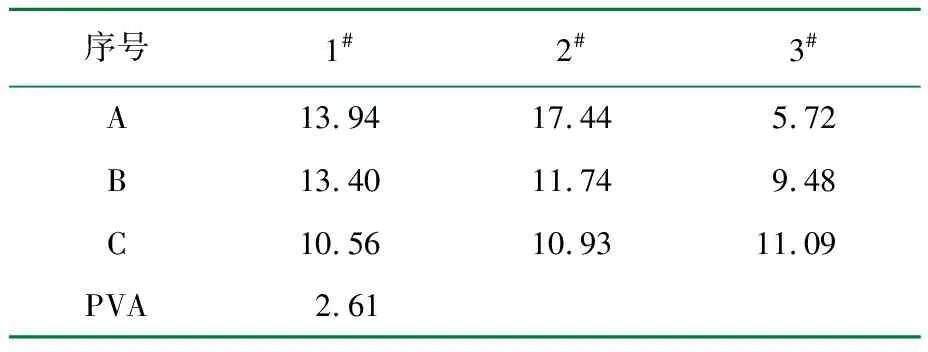
表2 共混膜溶胀性的测定结果 %
由表2可知,当V(CAS/乙酸)∶V(PVA)=1∶2,每100 mL共混液加入3.2 mL质量分数10%甘油所制得的共混膜的溶胀性最低,为5.72%,共混膜性能较优。
2.2 共混膜吸附性的分析
吸附率计算见公式(2)。
θ=(A1-A2)/A1×100%
(2)
式中:θ为共混膜对水样中Cu2+的吸附率;A1为测量模拟水样的吸光度;A2为共混膜吸附后水样的吸光度。
2.2.1 pH值对吸附性能的影响
固定吸附温度为25 ℃,吸附时间为1 h,甘油壳聚糖聚乙烯醇共混膜面积为2 cm×2 cm,改变模拟废水水样的pH值,用质量分数3%的HCl溶液和质量分数3%NaOH溶液调节pH=5、6、7、8、9、10、11,进行吸附,显色萃取,测量其吸光度,吸附率随pH值的变化见图2。
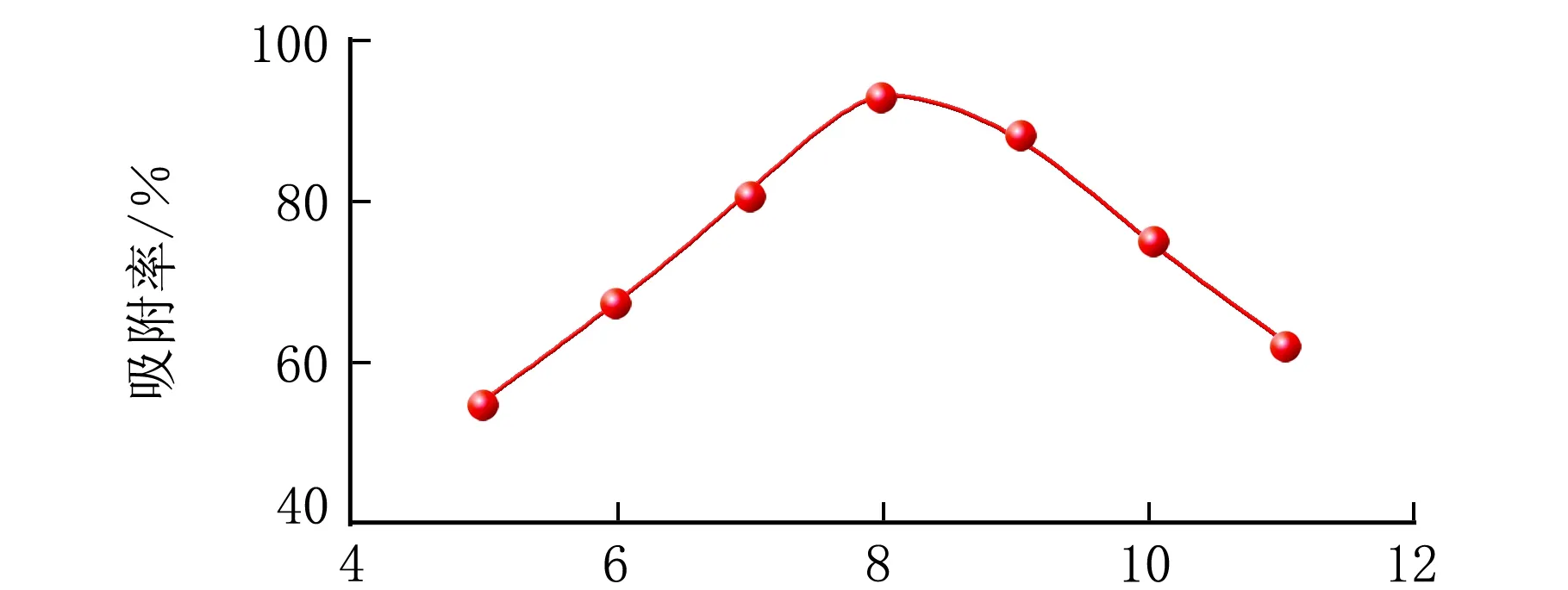
pH图2 pH值对吸附率的影响
由图2可知,随着pH值的逐渐升高,共混膜的吸附率也在随着升高;当pH=8,共混膜的吸附率达到最大,最大吸附率为93%;当pH>8,共混膜对Cu2+的吸附效果逐渐降低。pH值较低时,壳聚糖易溶于酸,溶解度较大,另外,H+浓度较大,共混膜上的—NH2质子化程度较大,削弱了氨基的螯合作用,最终导致共混膜吸附率较低。pH>8,溶液带负电,正电荷浓度降低,电中性作用减弱,吸附率较低。
2.2.2 温度对吸附性能的影响
固定吸附时间为1 h,pH=8,甘油壳聚糖聚乙烯醇共混膜面积为2 cm×2 cm,控制水样温度为15、20、25、30、35、40、55 ℃,进行吸附,显色萃取,测量其吸光度,吸附率随温度的变化见图3。
由图3可知,随着温度的逐渐升高,共混膜的吸附率也随着升高;当温度升到25 ℃,共混膜的吸附率达到最大,为88%;当温度高于25 ℃,共混膜对Cu2+的吸附效果逐渐降低。温度升高,聚乙烯醇的亲水程度增强,吸附率增大,同时吸附为放热反应,温度过高平衡向吸热反应方向即解吸(吸附率下降)的方向移动,导致吸附率降低。
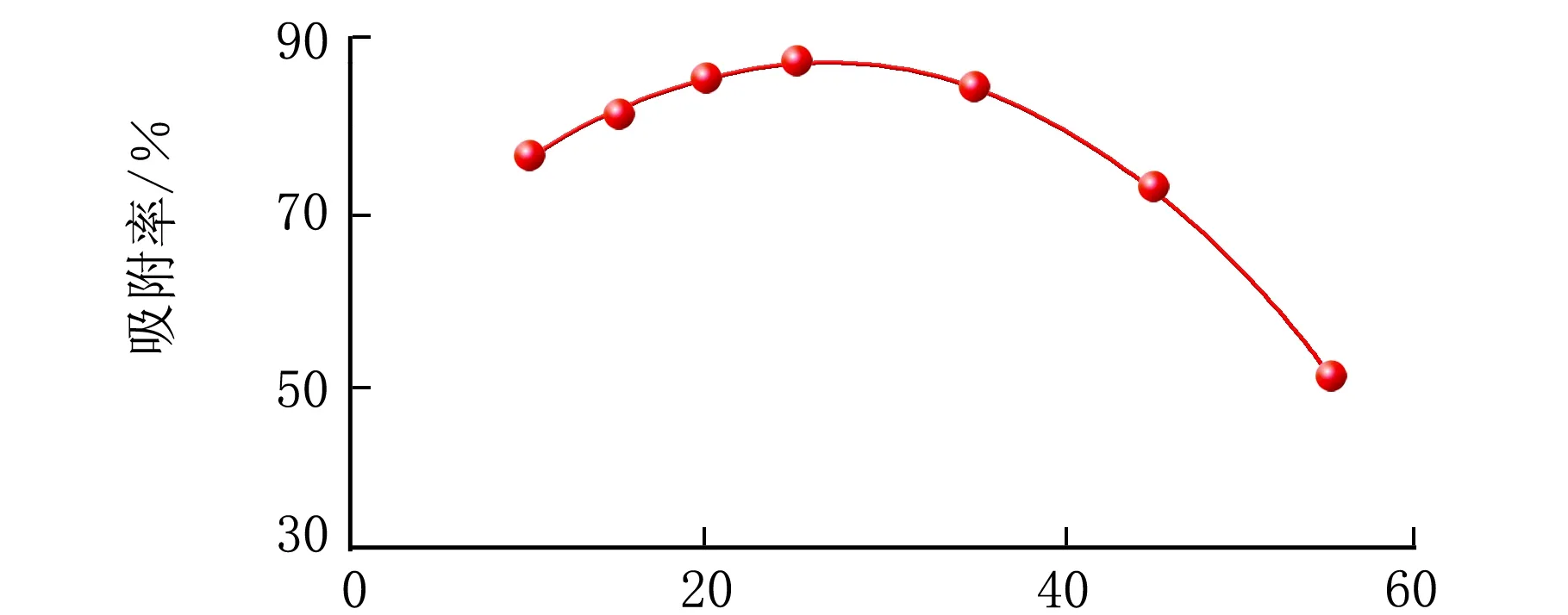
t/℃图3 温度对吸附率的影响
2.2.3 吸附时间对吸附性能的影响
固定吸附温度为25 ℃,pH=8,甘油壳聚糖聚乙烯醇共混膜面积为2 cm×2 cm,控制共混膜的吸附时间为0、0.5、1.0、1.5、2.0、2.5、3.0 h,进行吸附,显色萃取,测量其吸光度,吸附率随吸附时间的变化见图4。

t/h图4 吸附时间对吸附率的影响
由图4可知,随着吸附时间的延长,共混膜的吸附率也随着升高;当吸附时间为1 h,共混膜的吸附率达到最大,为91%;当吸附时间大于1 h,共混膜对Cu2+的吸附效果逐渐降低。可能由于开始溶液中Cu2+浓度较大,共混膜上被吸附的Cu2+浓度较小,吸附速率大于解吸速率,随着时间的延长,共混膜达到了饱和吸附,即吸附速率等于解吸速率,继续延长吸附时间,共混膜表面甘油分子中的—OH和水分子形成氢键,使共混膜有所溶解,部分被吸附的Cu2+可能回到溶液中,导致吸附率逐渐降低。
3 结 论
将壳聚糖与聚乙烯醇、甘油共混复合制得复合膜,当质量分数4%壳聚糖溶液和质量分数4%聚乙烯醇溶液体积比为1∶2时,每100 mL共混液加入3.2 mL质量分数10%的甘油所制得的共混膜性能最优。
用制备的共混膜对水中Cu2+进行吸附,当pH=8、吸附温度为25 ℃、吸附时间为1 h,吸附效果较好,吸附率可达93%。
