基于深度学习的肺炎病灶分割技术用于新型冠状病毒肺炎的定量分析
2020-03-14潘亚玲王晗琦俞勤吉牛镜淇
潘亚玲 王 昊 王晗琦 俞勤吉 牛镜淇 陆 勇
深度学习是目前机器学习领域的研究热点,其中深度卷积神经网络是近年来发展最为迅速的计算机视觉技术,被广泛应用于医学图像分析。病灶分割问题要求对医学图像中的特定异常区域进行像素级分类,最终得到病灶区域掩膜。深度卷积神经网络在超声、核磁共振等医学图像中,对处理病灶分割问题展现出很好的能力[1]。据WHO 统计,截至2020 年3月23 日04:03,全球新型冠状病毒肺炎(coronavirus disease 2019,COVID-19)累计确诊病例294110 例,累计死亡病例12944 例,已有187 个国家或地区出现确诊病例。COVID-19 的确诊依赖于核酸检测和血清学检测,但文献报道核酸检测存在一定的假阴性率且肺部影像表现可能早于检测阳性报告[2]。CT 检查密度分辨率和空间分辨率高,有利于检出早期肺部炎性病灶,准确评估病情严重程度,是COVID-19 首选的影像检查方法[3]。为及早发现COVID-19 可疑病例和发掘COVID-19 区别于其他肺炎的影像特征,通过深度学习分割肺炎病灶,探究基于深度学习的肺炎病灶分割模型用于COVID-19CT 影像定量分析的可行性,为COVID-19 鉴别诊断提供帮助。
方 法
1.一般资料
建立肺炎病灶分割模型的数据集由院内采集的86 例不同程度典型肺炎表现的病例组成,导出CT 扫描的Dicom 图像文件,通过ITK-Snap 工具对肺内炎性渗出的实性和磨玻璃病灶进行像素级分割标注。标注分为两轮进行,在窗宽1500HU、窗位-400HU的肺窗下进行观察和标注,第一轮由一名放射科医师初步勾画病灶区域,第二轮由另一名放射科医师独立审核修改病灶区域细节。其中训练集73 例,测试集13 例。
建立肺炎分类模型的数据集由院内采集的胸部CT 图像构成。依据病例中无可疑渗出及实变、存在微小磨玻璃影或条索影及存在大面积实变和磨玻璃影等典型肺炎表现分为三类,由一名放射科医师进行评估。根据比例均衡原则,构建训练集217 例,测试集56 例,见表1。
验证肺炎病灶分割模型和定量分析的CT 影像从2020 年1 月20 日至2020 年2 月1 日在发热门诊就诊并取得上海疾控中心RT-PCR 检测结果的28 例COVID-19 疑似病例中获得。按照核酸检测结果,7 例为COVID-19 阳性,21 例为COVID-19 阴性。CT 影像数据以Dicom 格式导出,肺炎病灶分割模型预测后,由一名放射科医师对分割结果进行确认,然后用于图像特征定量分析。
2.CT 检查方法
CT 数据由16 排(Lightspeed Pro16,Lightspeed VCT; GE Medical Systems,Milwaukee, IL) 或40 排((uCT 528,Shanghai United Imaging Healthcare Co.,Ltd. China) CT扫描仪采集。扫描参数:管电压120kVp, 自动调节管电流100 ~350mAs,转 速0.75s/r,准直40mm×0.55mm,采用层厚1 ~1.5mm 的肺窗重建。
3.模型训练方法
我们提出的肺炎病灶分割和肺炎分类模型包含两个步骤,见图1。肺炎病灶分割模型在CT 图像中得到磨玻璃和实变等肺炎病灶的精确轮廓,分割结果后续用于对病灶的精确、定量分析。肺炎分类模型根据肺炎病灶分割模型的输出结果,整合CT 图像中所有分割病灶结果,得到一个概率值来评测受检者为肺炎的可能性,此结果有助于优化阅片工作流。
我们使用目前在各类医学图像分割任务中均表现突出的深度学习模型nn-Unet 框架进行肺炎病灶分割[4]。该框架对图像分割中的各个环节,包括图像预处理、网络架构、学习过程和损失函数等都进行了自动化的优化和参数估计,从而针对不同的分割任务和数据集均能达到较优的效果。鉴于在病灶分割基础上进行肺炎分类信息充分,故采用随机森林方法构建肺炎分类模型。根据nn-Unet 输出的肺炎病灶分割结果,进一步计算磨玻璃病灶体积占肺部的比例、实变病灶占肺部的比例和磨玻璃病灶亮度的统计值,以上述三个特征训练随机森林模型,得到CT 影像的肺炎分类预测值。肺炎病灶分割模型和肺炎分类模型参数分别见表2 和表3。

表1 肺炎分类模型的数据集划分

表2 肺炎病灶分割模型参数
4.影像分析方法
使用上述肺炎病灶分割模型, 在28 例COVID-19 疑似患者的CT 影像上进行病灶分割。由1 名放射科医师审核和修正分割结果,计算肺炎病灶分割模型在COVID-19 疑似患者CT 影像上分割病灶的Dice 系数、精准度及召回率。使用一个已报道的基于渐进分割网络的肺叶分割模型将肺炎病灶进行肺叶定位[5]。统计每例COVID-19 疑似患者的病灶平均密度和密度标准差及各个肺叶的受累体积占比。采用独立样本T 检验进行COVID-19 阳性病例与阴性病例组间比较。
结 果
肺炎病灶分割模型采用Dice 分数、病灶像素精准度(Precision)及召回率(Recall)作为评价指标。使用ISBI 中报道的Focal-Tversky Unet 模型[7]作为对比模型。通过对比发现,本研究提出的肺炎病灶分割模型的Dice 系数和精准度较Focal-Tversky Unet模型更高,见表4。
肺炎分类模型采用灵敏度和特异度作为评价指标,并针对典型肺炎病例的检出能力绘制ROC 曲线,见图 2。肺炎分类模型检出肺炎的ROC 曲线下面积为0.990,在切点处灵敏度和特异度分别为95.0%、97.2%。

表3 肺炎分类模型的参数

表4 肺炎病灶分割模型的分割效能
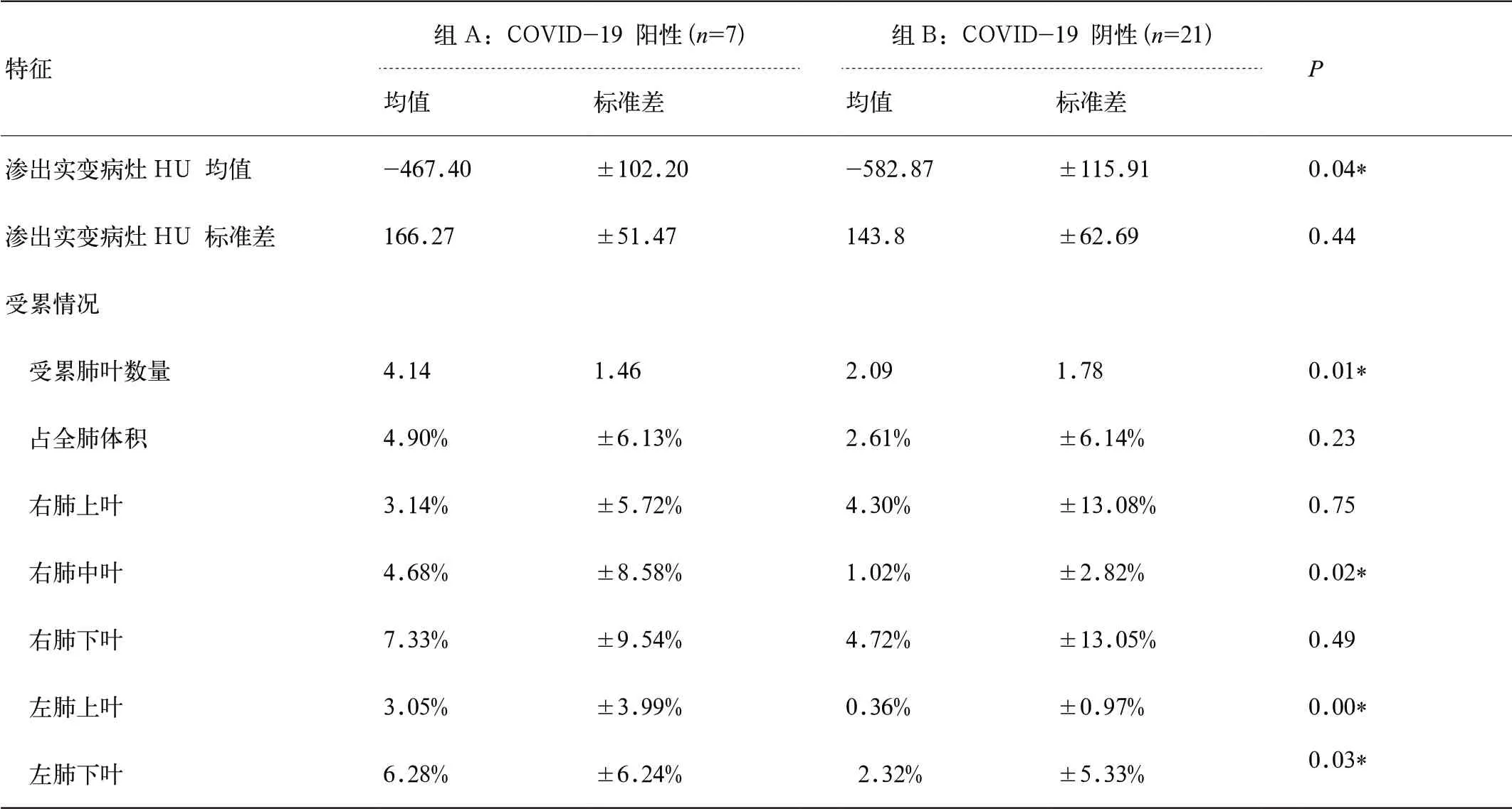
表5 新型冠状病毒肺炎阳性与阴性病例影像学特征比较

图1 肺炎病灶分割与分类的整体流程。

图2 肺炎分类的ROC 曲线。
采用肺炎病灶分割模型对28 例COVID-19 疑似患者的CT 影像进行病灶分割,一名放射科医师对病灶分割结果进行审核和修正,见图3。与修正结果比较,肺炎病灶分割模型的Dice 系数为41.9%,精准度67.7%,召回率40.1%。病灶分割结果修正后,使用肺叶分割模型将肺叶分割结果与病灶分割结果对应,定量、对比分析COVID-19 阳性病例与阴性病例的影像学特征差异,见表5。相较于阴性病例,COVID-19阳性病例中病灶密度均值更高(P=0.04),且受累肺叶数量更多(P=0.01)。
讨 论
本研究采用目前医学图像分割领域先进的nn-Unet 框架建立肺炎病灶分割模型,在病灶分割基础上输入手动设计的特征,采用随机森林方法建立肺炎分类模型,研究结果显示上述方法能够较好的发现肺炎病例。由于磨玻璃渗出病灶的边界在CT 影像中比较模糊,且其在肺炎病灶中占比较大。因此,对该类肺炎病灶分割标注、评估、度量较为困难。从CT 影像中可知,尽管肺炎病灶分割模型的度量指标不高(Dice 系数为0.545),但在分割视觉效果上尚可接受,并且足以支撑肺炎分类结果。

图3 肺叶和肺炎病灶分割和修正结果。A.原始CT 图像 B.肺叶分割结果 C.病灶分割结果 D.经审核和修正的病灶分割结果。
通过普通肺炎病例训练的肺炎病灶分割模型,经COVID-19 患者CT 影像验证发现,尽管CT 数据来源于不同的肺炎患者,但基于深度学习的肺炎病灶分割模型仍然能保持一定水平的准确度,这说明该模型对不同肺炎类型的病灶分割具有一定的鲁棒性。通过基于病灶分割和肺叶分割的结果定量分析,我们发现新COVID-19 的潜在影像学特征。与阴性病例相比,COVID-19 阳性病例的病灶平均密度更高,更容易累及多个肺叶,与其他已报道的影像学特征发现相符合[8-9]。通过计算机辅助病灶分割,有助于肺炎病灶影像学特征定量分析,有望促进COVID-19 的影像学特征研究。
