HILIC-MS/MS测定牛奶中4种含氮化合物的含量*
2020-03-12SONGHANEUN宋汉恩
SONG HANEUN(宋汉恩),任 燕
(滨州医学院,山东 烟台 264003)
三聚氰胺(melamine,MEL)、三聚氰酸(cyanuric acid,CY)、二氰二胺(dicyandiamide,DCD)和尿酸(uric acid,UA)的含氮量如果折合成粗蛋白的含氮量,数值会大大增加[1]。牛奶中的蛋白质的成分特别复杂,一般测定蛋白常用凯氏定氮法,但是这种方法只是检测含氮的多少,不能检测样品中是不是含有非蛋白的氮成分。所以一些不法商家常将上述四种物质添加到牛奶当中,从而使蛋白质的含量测定值上升,严重影响我国奶制品质量安全[2]。但三聚氰胺、三聚氰酸会引起肾结石或膀胱结石等病症,甚至引起肾衰竭,吸入或者摄入二氰二胺后对身体有害,而尿酸会导致人体体液变酸,影响正常细胞的功能,长期发现不了或不治疗将会引发痛风,这四种物质均严重危害人们的身体健康[3-5]。牛奶中有可能存在三聚氰胺、三聚氰酸、二氰二胺和尿酸这些非法添加物。为保证牛奶的安全性,同时检测三聚氰胺、三聚氰酸、二氰二胺和尿酸非常必要[1-9]。
目前检测这四个化合物的分析方法很多,包括气质联用法[10]、高效液相色谱法[11]等。但尚没有对三聚氰胺、三聚氰酸、尿酸、二氰二胺同时进行检测的分析方法。由于三聚氰胺、三聚氰酸、尿酸、二氰二胺的亲水性质,在普通的反相色谱柱上几乎无保留,在不添加任何离子对试剂的条件下,HILIC柱对极性物质有很好的保留能力,因此本实验采用亲水色谱-串联质谱法同时测定牛奶中三聚氰胺、三聚氰酸、尿酸、二氰二胺的含量。
1 仪器与试药
1.1 仪 器
Agilent Hilic色谱柱(4.6 mm×100 mm,3.5 μm);液质联用仪器(包括岛津高效液相色谱仪:检测器为SPD-20A,高压泵LC-20AD,控制器为CMB-20A,柱温箱为CTO-20A和Applied Biosystems API3200质谱仪);TB-215D电子分析天平,丹佛仪器有限公司;DHG-9423A电热恒温鼓风干燥箱,上海精宏实验设备有限公司;涡旋混合器,美国Scientific Industries公司;KG-50B型超声波清洗器,昆山市超声仪公司;HH-4数量恒温水浴锅,常州国华电器有限公司;TG16-WS合式高速离心机,上海卢湘仪离心仪器有限公司。
1.2 试 药
甲醇、乙腈为色谱纯;纯水;9个品牌纯牛奶。
2 方法与结果
2.1 分析条件
2.1.1 色谱条件
亲水性色谱柱Agilent Hilic色谱柱(4.6 mm×100 mm,3.5 μm);流动相A为纯水,流动相B为乙腈,恒度洗脱(纯水:乙腈=50:50);流速为1 mL/min;进样量为10 μL;柱温为25 ℃。
2.1.2 质谱条件
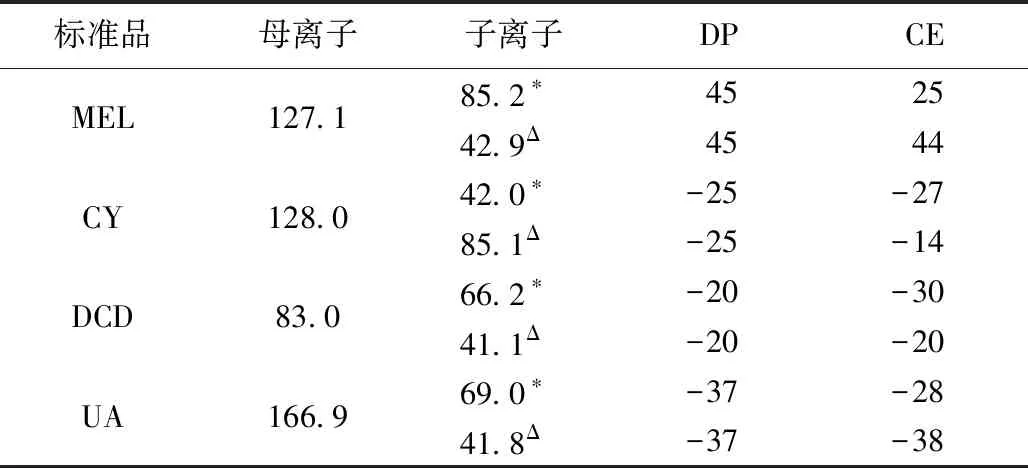
表1 标准品的MRM模式参数
*定量离子,Δ定性离子。
气帘气(Curtain Gas):10 psi;碰撞气(Collision Gas):4 psi;离子喷雾电压(IonSpray Voltage)正离子:5500 V,负离子:-4400 V;离子源温度(turbopray temperature):550 ℃;雾化气(Gas 1):55 psi;加热气(Gas 2):55 psi。标准品的MRM模式参数见表1。
2.2 标准品溶液的制备
分别称取4个化合物适量,加入50%甲醇溶解,最终配制成三聚氰酸、二氰二胺、尿酸浓度均为4.0 μg/mL、2.0 μg/mL、1.0 μg/mL、0.8 μg/mL、0.4 μg/mL、0.2 μg/mL、0.1 μg/mL和三聚氰胺浓度20.0 ng/mL、10.0 ng/mL、5.0 ng/mL、4.0 ng/mL、2.0 ng/mL、1.0 ng/mL、0.5 ng/mL的系列标准品混合溶液。
2.3 供试品溶液制备
分别量取九个不同品牌的牛奶样品100 μL,加入甲醇500 μL,涡旋15 s混合均匀,于4500 rpm离心10 min,取上清液于37 ℃下氮气吹干。然后加入50 μL溶剂(甲醇:水=1:1),超声3 min,13000 rpm离心10 min。取上清液进行分析。
2.4 方法学验证
2.4.1 样品专属性实验
4个化合物在“2.1”质谱色谱条件下所得的谱图见图1,三聚氰胺在正离子模式下检测,三聚氰酸、尿酸、二氰二胺在负离子模式下检测。空白溶剂及样品溶液在“2.1”分析条件下检测所得的谱图见图2、图3。结果表明,空白溶剂不会对标准品的测定产生影响,该实验分析方法的专属性良好。
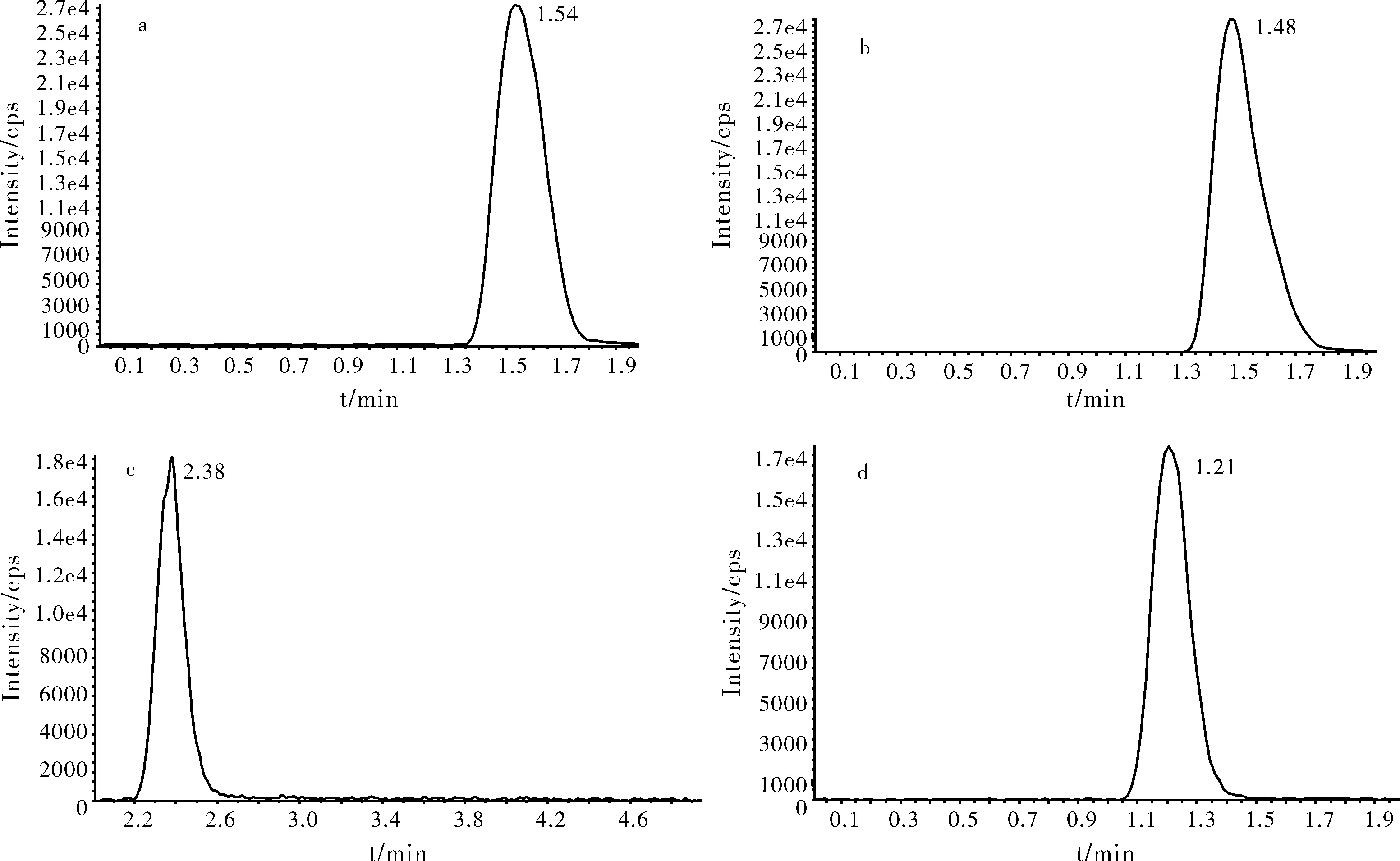
图1 二氰二胺(a)、三聚氰酸(b)、三聚氰胺(c)和尿酸(d)的HPLC-MS图

图2 二氰二胺(a)、三聚氰酸(b)、三聚氰胺(c) 和尿酸(d)的空白溶剂HPLC-MS图

图3 二氰二胺(a)、三聚氰酸(b)、三聚氰胺(c)和尿酸(d)的样品溶液HPLC-MS图
2.4.2 Carryover实验
将4个化合物的最高定量限的标准混合溶液(三聚氰酸、二氰二胺、尿酸的浓度均为4.0 μg/mL,三聚氰胺的浓度为20 ng/mL)进行进样,分析完之后立即分析空白溶液。将空白溶液中标准品的峰面积与最低定量限中标准品的峰面积进行比较,考察其carryover,其值均小于20%,表明高浓度标准品的残留污染不会对样品测定产生影响。
2.4.3 标准曲线与线性关系
分别以四个标准品的峰面积为纵坐标,浓度为横坐标建立标准曲线,三聚氰胺在浓度范围0.5~20 ng/mL内线性良好,三聚氰酸、二氰二胺、尿酸的浓度范围均在100~4000 ng/mL内线性良好,标准曲线方程与R值见表2。
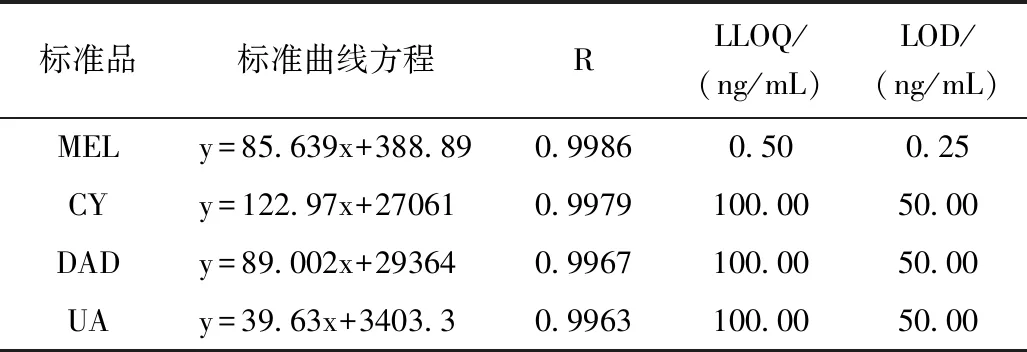
表2 各标准品的标准曲线方程
2.4.4 精密度,重复性和稳定性实验
配制4个化合物的标准混合溶液,三聚氰酸、二氰二胺、尿酸的浓度均为3.2 μg/mL、1.0 μg/mL、0.4 μg/mL,三聚氰胺对应的浓度分别为16.0 ng/mL、5.0 ng/mL、2.0 ng/mL,按照“2.1”的分析条件下用于精密度、重复性及稳定性的考察。连续进样6次考察日内精密度,随后连续三天每天进样6次考察日间精密度考察,配制6份三聚氰酸、二氰二胺、尿酸、三聚氰胺的标准混合溶液重复性考察,分别于0、2、4、6、8、10、12、24 h共进样8次,根据色谱峰面积变化来判断样品的稳定性。结果表明,其RSD值均小于15%,说明该方法精密度、重复性、稳定性良好。实验结果见表3。
2.4.5 加样回收率实验
配制4个化合物的标准混合溶液,三聚氰酸、二氰二胺、尿酸的浓度均为3.2 μg/mL、1.0 μg/mL、0.4 μg/mL,三聚氰胺对应的浓度分别为16.0 ng/mL、5.0 ng/mL、2.0 ng/mL,分别将高、中、低三个浓度的混合标准溶液加入到空白牛奶样品中,每一水平平行制备6份,检测其加样回收率。结果测得三聚氰胺回收率在85.5%~109.0%之间,三聚氰酸回收率在83.8%~109.0%之间,尿酸回收率在88.4%~115.0%之间,二氰二胺回收率在82.5%~115.0%之间,回收率满足样品分析的要求,实验结果见表3。
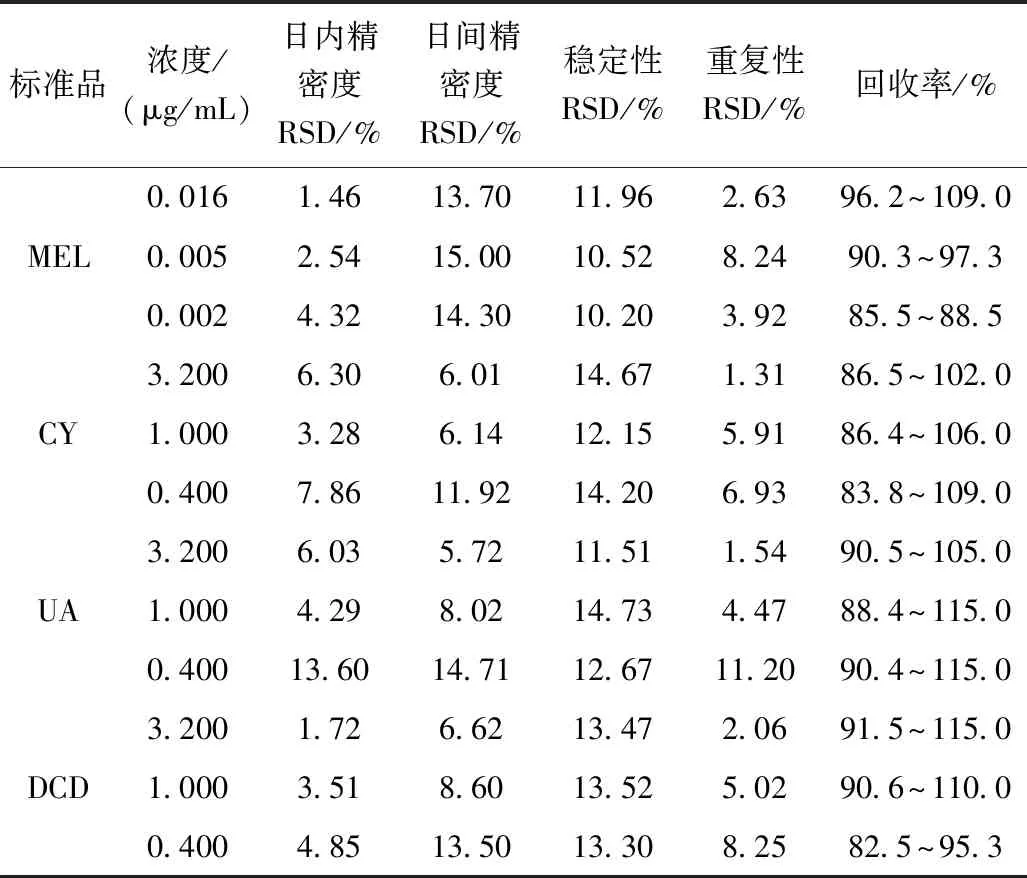
表3 精密度、重复性、稳定性和回收率数据
2.4.6 基质效应

表4 基质效应结果
A组:配制4个化合物的标准混合溶液,三聚氰酸、二氰二胺、尿酸的浓度均为3.2 μg/mL、1.0 μg/mL、0.4 μg/mL,三聚氰胺对应的浓度分别为16.0 ng/mL、5.0 ng/mL、2.0 ng/mL,高、中、低三个浓度每个浓度进样6次,进行液质联用分析。
B组:分别称取空白牛奶样品100 μL,置于1.5 mL离心管中,加入甲醇500 μL,涡旋15 s混合均匀,于4500 rpm离心10 min,取出上清液,于37 ℃下用氮气吹干。然后加入50 μL 标准品混合溶液,涡旋15 s混合均匀,超声3 min,在13000 rpm高速离心10 min。取上清液进样10 μL,每个浓度平行6份,进行液质联用分析。结果如表4所示,由表中结果可以看出样品的基质效应均在87.90%~108.0%之间,符合标准。
2.5 样品测定
分别称取九个不同品牌的牛奶样品100 μL,按供试品操作方法进行制备,然后进行液质连用分析。结果有八个品牌牛奶中含有尿酸,另外一个品牌牛奶中未检测出任何一种违禁物质。结果见表5。

表5 样品含量测定结果
2.6 阳性样品的结果确证
为了避免所测结果出现假阳性,我们根据2002/657/EC进行判定,2002/657/EC是2008年8月12日被欧盟授权执行关于分析方法的运行和结果解释欧盟指令96/23/EC的授权文件。这一授权文件中,描述了相对离子强度最大的允许范围。

表6 阳性样品峰面积比值
根据尿酸标准品计算求得定性离子/定量离子平均值为88.3%,阳性样品的定性离子/定量离子的比值在≥50%范围内,HPLC-MS/MS允许的误差范围为±20%。由表6可知,阳性样品的相对离子强度偏差都在允许的误差范围内,确证该实验所测样品结果为阳性结果。
3 讨 论
3.1 色谱柱的选择
开始选用Agilent ZORBAX SB-C18色谱柱(4.6 mm×150 mm,5 μm)进样,发现几个标准品由于极性太大,在色谱柱上几乎不保留,保留时间比较小,也不能很好地分离。选用亲水性的Agilent Hilic色谱柱(4.6×100 mm,3.5 μm)进行分析,几个标准品得到较好的分离,且保留时间均延后,适于三聚氰胺、三聚氰酸、尿酸和二氰二胺这些极性化合物的分析。
3.2 流动相的选择
选用乙腈-乙酸水和乙腈-水分别作为流动相进行比较分析,结果显示加入的乙酸会抑制三聚氰酸负离子的信号强度,所以选择乙腈-水来作为流动相进行色谱分析。此外分别进行了乙腈:水为95:5、90:10、70:30、60:40、50:50、40:60、30:70、10:90、5:95九种不同比例的流动相进行分析,最终结果显示在乙腈:水为50:50的情况下,各个标准品的色谱峰信号强度最强,峰形最美观,不拖尾,无杂峰。所以最终选用乙腈:水为50:50作为流动相进行色谱分析。
