高盐废水生物阴极MFCs产电及脱氮性能研究
2020-03-12杨茜李轩蒋涛阳王测文付国楷
杨茜,李轩,蒋涛阳,王测文,付国楷,2
(1.重庆大学 城市建设与环境工程学院,重庆 400045;2.重庆大学 三峡库区环境与生态部重点实验室,重庆 400045)
榨菜废水中的大量无机盐对常规微生物的繁殖及生物活性具有抑制作用[1-2],因而常规技术对此类污水的处理效果并不理想[3]。
目前,生物阴极MFCs作为新技术引起了研究者广泛关注[4-7]。崔心冰等[6]、祖波等[8]和Ryu等[9]则在MFCs中实现了畜猪废水中的碳和氮的同时去除。然而在生物阴极MFCs的脱氮过程中容易出现亚硝酸盐和硝酸盐的累积[10-12]。为此,Sotres[13]及赵慧敏等[14]使总氮的去除效果得到明显提升。榨菜废水是MFCs的理想燃料[15],Guo等[16]首次运用MFCs 技术处理榨菜废水。
本文构建了一个双室生物阴极MFCs用于榨菜废水的资源化处理,评估了曝气强度和曝气方式对发电过程中氮和碳去除的影响。
1 实验部分
1.1 材料与仪器
重铬酸钾、纳式试剂、过硫酸钾均为分析纯;榨菜废水,取自重庆涪陵某榨菜厂;阴极、阳极底物皆为厌氧池出水(ARE),保存在 4 ℃的冰箱内,其水质见表1。实验用水为超纯水(电阻率为18.2 MΩ·cm)。

表1 榨菜废水水质情况
PISO电压数据采集器;ZX21旋转式直流电阻箱;78-1 搅拌器;Ag/AgCl/KCl玻璃参比电极;BT100-1L 蠕动泵;ZDX-35BI座式自动电热压力蒸汽灭菌器;DR5000紫外可见分光光度计;便携式pH仪;DRB200型数字式消解仪;UT39A数字万用表;FE30K 基础型台式电导率仪;LZB-3气体流量计;FB1004B 电子天平;SZ-93双重纯水蒸馏器;DL-1万用炉。
1.2 实验方法
1.2.1 实验装置 见图1。
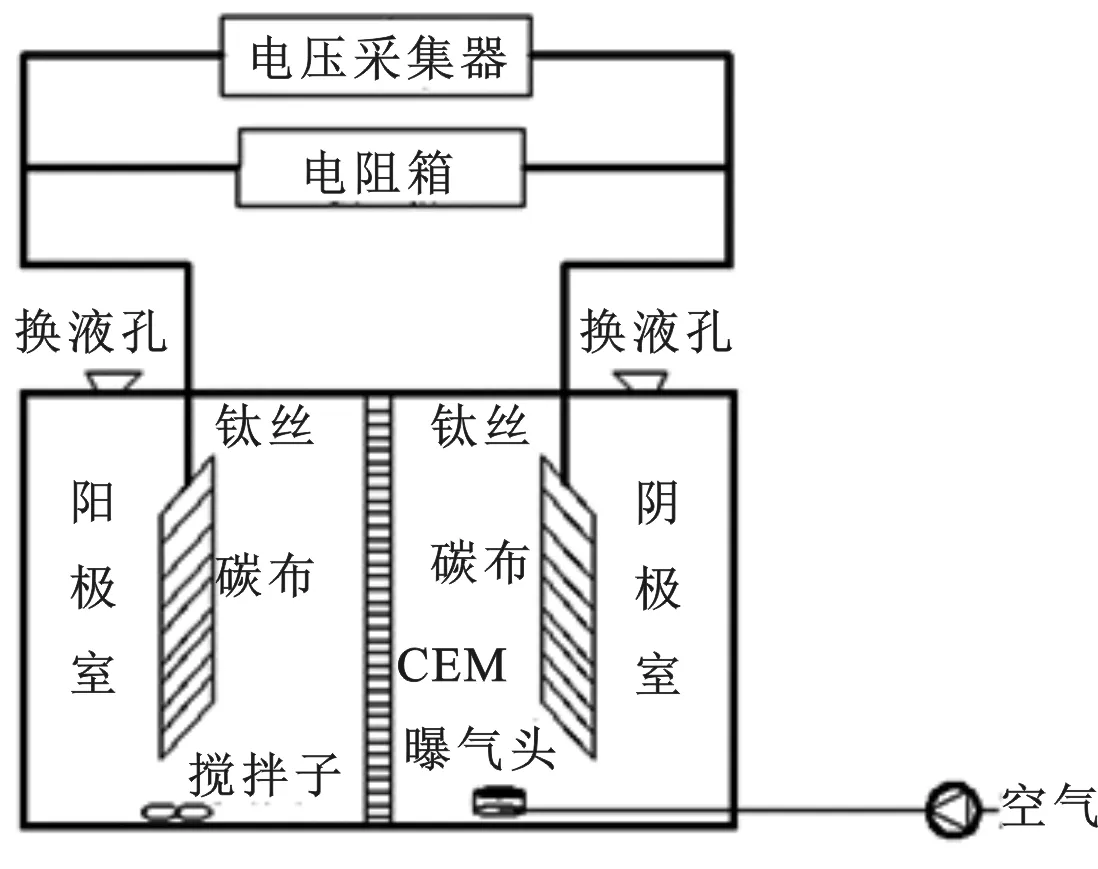
图1 MFCs 实验装置
方形反应器由有机玻璃制作而成。阳极室和阴极室尺寸均为4 cm × 5.5 cm × 4 cm,有效容积均为 80 mL。2个腔体通过质子交换膜从中间隔开,通过面积 22 cm2。阳极和阴极电极材料均为碳布,表面积均为 44 cm2。电极由钛丝导线引出,并用铜线与变租箱( 0 ~9 999.9 Ω) 连接,形成闭合电路。运行过程中采用磁力搅拌器对阳极室底物进行搅拌混匀,阴极外接曝气充氧装置。
1.2.2 电池启动与运行 生物阴极启动阶段,MFCs外接500 Ω电阻。阳极室直接加入厌氧池废水进行启动,并加入厌氧池污泥进行接种。运行过程中保证阳极室的绝对厌氧状态,阴极采用外接曝气充氧设施,保持溶解氧在4.0~5.0 mg/L。当电池电压低于50 mV 时认定完成一个产电周期,之后及时更换新鲜底物和阴极液,在至少连续3个周期电池均能达到相似电压(相差不超过5%)及持续时间时,认为系统启动成功。
反应器启动成功后改变曝气强度为20,40,100,200 mL/min,形成四个运行阶段(P1、P2、P3、P4),阴极溶解氧分别为2.3,4.3,6.3,7.5 mg/L,形成四个不同的溶解氧浓度梯度,最后一个阶段P4的DO浓度接近饱和。考察曝气强度对电池的影响。在逐步改变曝气强度的过程中,要重新获得电池稳定产能状态(连续两个周期获得相似电压),然后对电池进行产电和污染物去除的评估。
随后反应器运行时,固定曝气强度为40 mL/min。通过改变曝气方式为间歇0,1,2,4 h曝气,形成四个运行阶段(S1、S2、S3、S4),考察曝气方式对电池的影响。改变曝气方式时同样要获得稳定产能状态,然后进行电池性能评估。
所有实验采用续批式模式运行,平行检测,实验温度如无特殊说明,均在(25±1)℃下进行。
1.3 电化学分析指标与计算
MFCs系统的输出电压由数据采集模板每分钟采集1次,并保存至电脑。面积功率密度PA=UI/A(I为电流,A为阳极面积),开路电压、内阻RInt、最大功率密度Pmax计算方法依据文献Bruce等[17]。极化曲线和功率密度通过外电阻法测得。
1.4 水质分析方法
COD采用紫外分光光度法测定;常规水质指标如总氮、总磷、氨氮、NO3-N、NO2-N按国标法测定[18]。 pH、电导率、盐度采用便携式仪器检测。
2 结果与讨论
2.1 曝气强度对生物阴极MFCs产电性能的影响
不同曝气强度下,生物阴极MFCs的产电性能见图2。
由图2可知,当曝气强度分别为20(P1),40(P2),100(P3),200(P4) mL/min时,阴极溶解氧分别为2.3,4.3,6.3,7.5 mg/L,MFCs的稳定输出电压分别为205,234,253,215 mV。不同曝气强度下,产电周期均在120 h左右,当曝气强度在40~100 mL/min之间时,系统的产电性能较好。
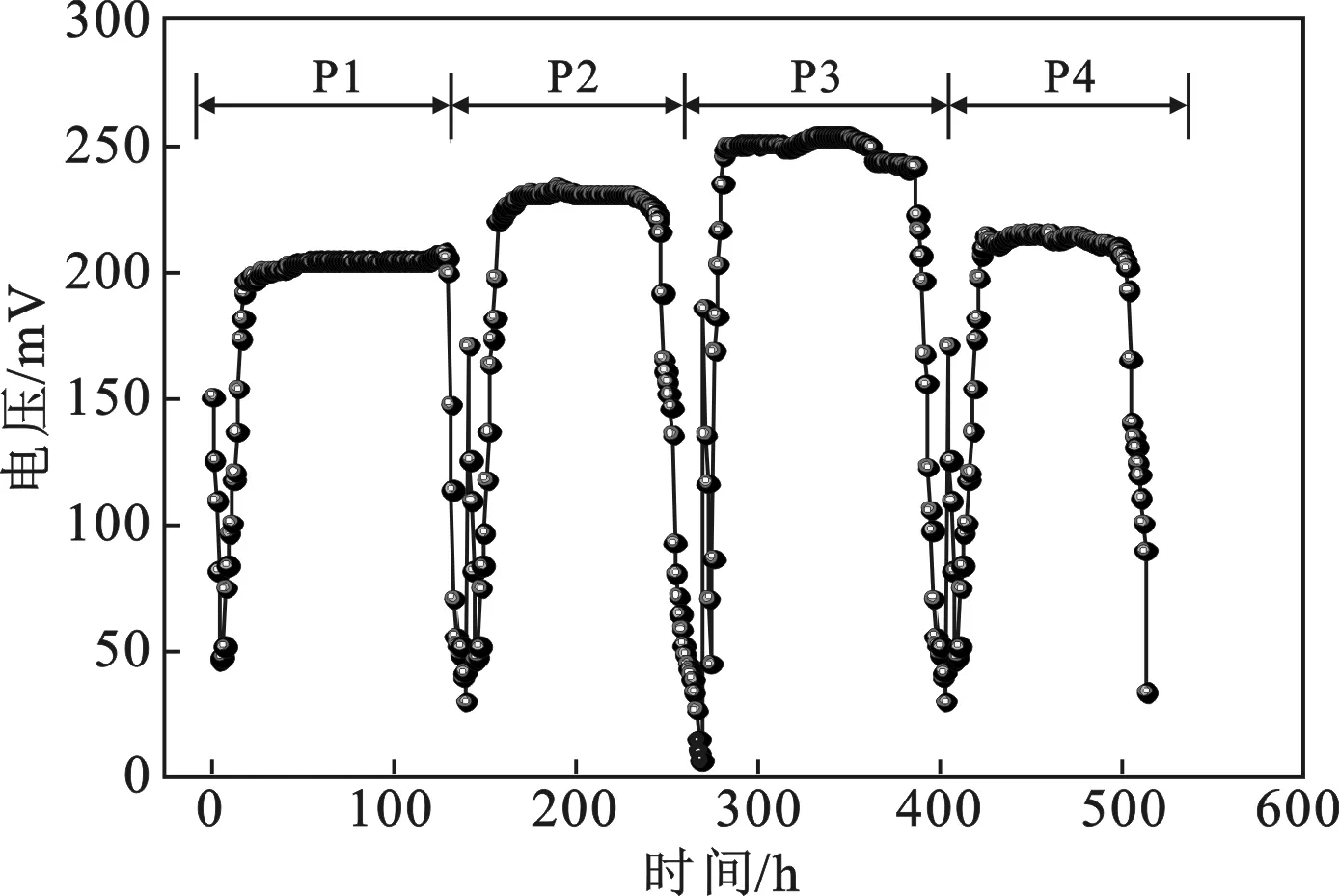
图2 不同阶段生物阴极MFCs的电压输出
由图2可知,一个周期中,输出电压普遍存在先下降再上升的过程。这是由于榨菜废水刚加入阴极时,由于好氧异养生物氧化有机物迅速增殖,阴极有机物作为电子供体消耗氧气[14,19-21]。生物硝化还会消耗阴极中的DO,而氧气是生物阴极MFCs中的主要电子受体,输出电压主要与DO浓度有关,因此生物硝化和异养增值对产电过程的抑制作用,使阴极电位和电池电压都降低,从而电池的产电性能下降[9,22-23]。
在稳定条件下,随着阴极DO的增加,最大输出电压升高,当曝气强度继续增加时,如P4的输出电压反而出现降低。这是由于阴极过量的曝气会导致氧气向阳极扩散,破坏阳极厌氧环境,导致阳极电势上升[24-25],通常,曝气强度在一定范围内,输出电压将随着DO浓度的增加而增加,而继续增加曝气,电池性能反而会降低[26]。同时,过高的DO浓度可以影响有机物分解速率和微生物多样性[27],故控制生物阴极曝气强度在40~100 mL/min之间、DO浓度在4~6 mg/L是电压稳定运行的关键。
由图3a可知,P1、P2、P3和P4 的最大功率密度Pmax分别为1.60,1.93,2.21,2.72 W/m3。由图3b可知,P1、P2、P3和P4的开路电压分别为550,555,568,660 mV;由欧姆定律可得内阻分别为240,236,196,131 Ω。显然,阴极DO的增加使内阻减小,从而Pmax增大[28-30]。最大功率密度为P4阶段,Pmax为2.72 W/m3,内阻为131 Ω。显然,与相关文献中报道的其他生物阴极MFCs,如Ryu等[9]以人工废水为原料,有机玻璃为隔板,最大功率密度为0.17 W/m3并且内部电阻计为 214 Ω;Zhang等[31]以高盐废水为原料,最大功率密度1.45 W/m3内阻为400 Ω相比,本实验功率密度较高,且内阻较小。

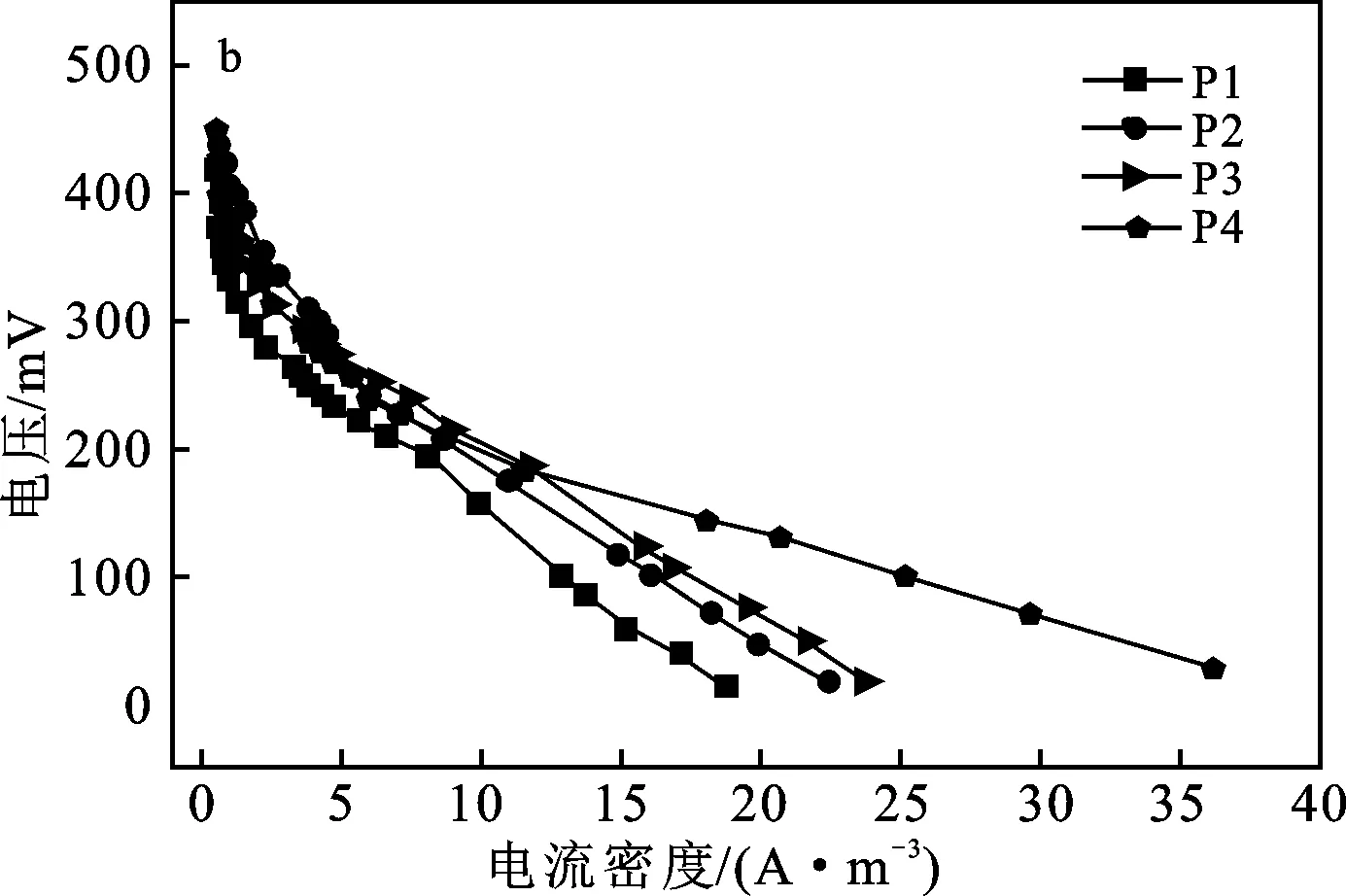
图3 不同阶段生物阴极MFCs的功率密度(a) 和极化曲线(b)Fig.3 Power density (a) and polarization curve (b) of bio-cathode MFCs under different stages
2.2 曝气强度对生物阴极MFCs污染物去除效果的影响
实验考察了曝气强度分别为20(P1),40(P2),100(P3),200(P4) mL/min的曝气强度下生物阴极MFCs污染物的去除效果,结果见图4a。
由图4a可知,P1、P2、P3和P4条件下,阳极COD的去除率分别为88.28%,90.85%,91.14%,88.57%。可知,该去除率在一定范围内随着曝气强度的增加而提高,当曝气强度达到P4条件时COD去除率却有所下降。这是由于,过高的阴极曝气强度会导致氧气扩散到阳极,破坏了阳极厌氧环境[25]。同时,在这四种条件下,阴极COD的去除率分别达到了85.14%,87.14%,88.57%,89.14%。阴极室中的有机物质可能通过以下方式消耗:①用作反硝化的电子供体;②用于异养硝化;③用作好氧反应。多去除途径极大地促进了有机物的降解[22,31-32]。
总体来说,随着曝气强度的提高,COD去除效果有所提升但去除率差距并不巨大,且当曝气强度超过40 mL/min时,曝气强度便不再是COD去除的主要限制因素,若继续增加曝气,还会破坏阳极厌氧环境,使COD去除率有所下降。因而,曝气强度在P2~P3(40~100 mL/min)条件下时,生物阴极MFCs对COD去除效果相对较为理想。
榨菜废水原水中的TN大多以氨氮的形式存在,有大量研究表明,生物阴极具有可以有效完成对碳和氮的同时去除的优点[9,31,33]。P1~P4四种条件下,生物阴极MFCs氮的去除效果见图4b。


图4 不同阶段下MFCs对COD(a)和生物阴极中氮(b)的去除Fig.4 COD concentration and removal rate of inlet and outlet water under different cathode electron acceptors (a),coulombic efficiency of different electron acceptors (b)

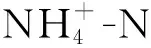
2.3 曝气方式对生物阴极MFCs污染物去除效果的影响
在40 mL/min曝气强度下,通过设置“曝气-停止曝气-曝气-停止曝气…”的间歇曝气方式,并将单周期曝气时长分别设定为0,1,2,4 h,以形成四个对照实验组(即图5中的S1、S2、S3、S4),相应的各组停止曝气阶段平均溶解氧浓度经测量分别为4.6,3.3,1.6,0.4 mg/L。每个实验组均以相应间歇曝气方式持续循环5 d左右(一个产电周期,130 h),最终测量计算其污染物出水去除率,结果见图5。
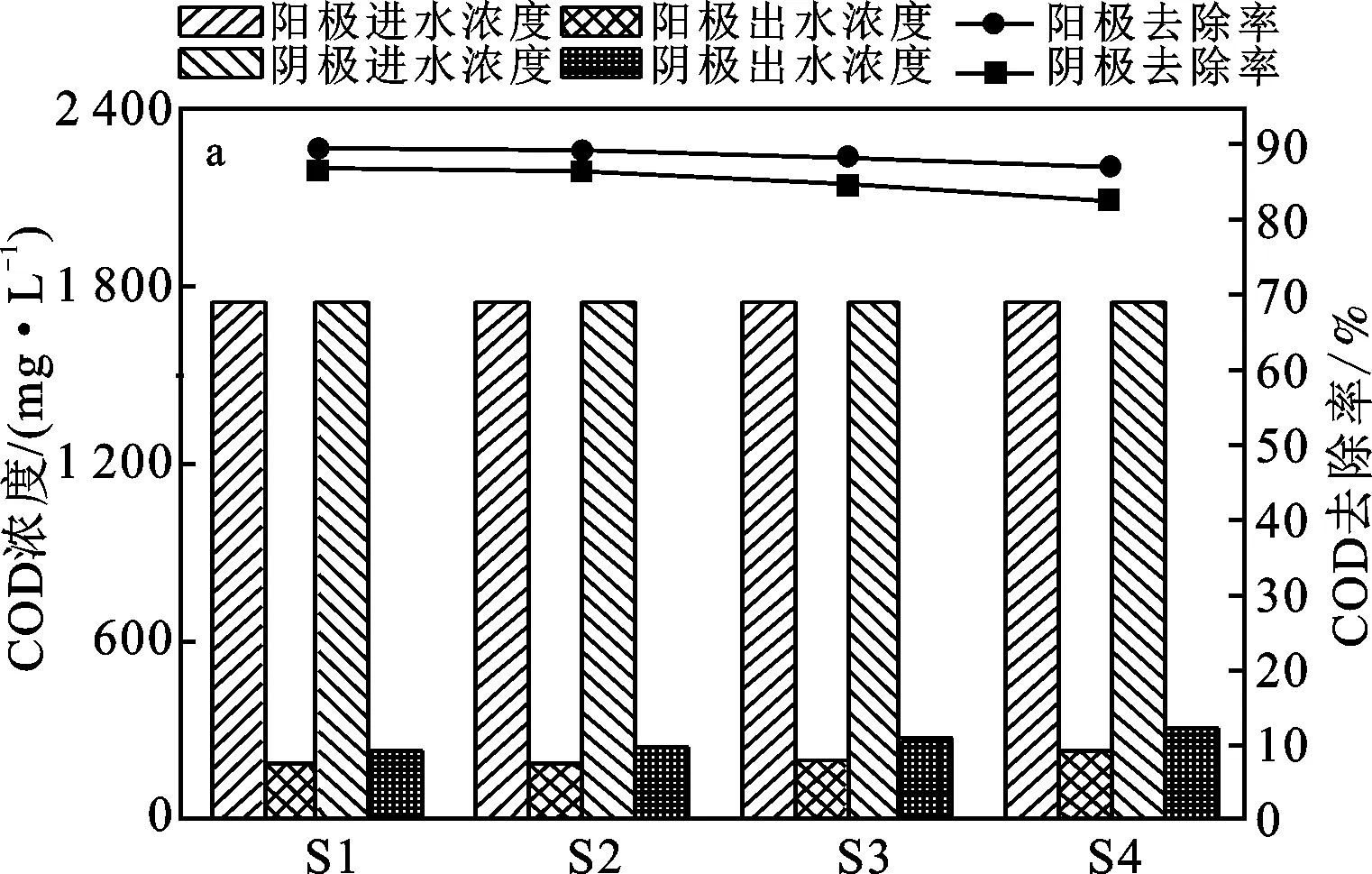
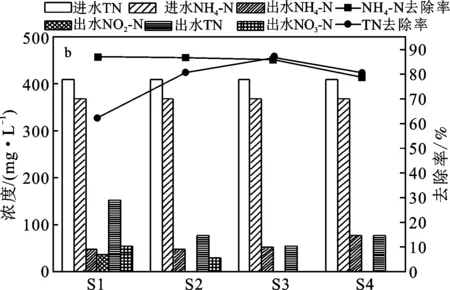
图5 不同曝气方式下MFCs对COD(a) 和生物阴极中氮(b)的去除Fig.5 Removal of COD (a) by MFCs and nitrogen in biological cathode(b) in different aeration modes
由图5a可知,在S1、S2、S3和S4条件下,阳极COD的去除率分别达到了89.71%,89.43%,88.57%,87.14%,即在间歇曝气方式下单周期间歇时长对阳极COD的降解基本没有影响;而相应的阴极COD的去除率则分别为87.14%,86.57%,84.85%,82.86%,可见阴极COD的去除率随着曝气间隔时间的增加略有下降。考虑到在MFCs的阴极环境下主要发生微生物好氧反应,而由前述溶解氧浓度的测量结果可知,随着间歇时长的增加,停止曝气阶段平均溶解氧浓度下降明显,阴极处不得不进行好氧和厌氧交替发生的反应,因而导致图5a中的阴极有机物的降解效率略有降低。
由图5b可知,S1~S4条件下出水中的氨氮去除率,其分别为90%,89.74%,88.95%,82.11%,即氨氮的去除率将随着曝气间歇时长的增加而略有减小,其中以S4条件时该减小最为明显。可能是因为S4阶段每个循环周期内停止曝气的时间过长,使得其对硝化细菌活性的抑制效应比其他三个阶段更为明显,导致氨氮的去除效果显著劣于其他三种条件[11-12,35-36]。由该图同时可知,不同运行条件下的TN去除率分别为68.29%,83.13%,89.52%,83.22%,即总氮的去除率随着曝气间歇时长的增大而大幅提高,特别是S2、S3和S4条件下的去除率均超过了83%。并且在S3阶段较S1提高了21.23%,TN的去除率提高最大。这是因为在间歇曝气的条件下,曝气阶段可以保证氨氮的去除率,非曝气阶段可以减轻氧气对反硝化细菌的抑制作用[37-38]。因而间歇式曝气运行方式既能有效提高生物阴极脱氮性能,又可以减少维持高浓度 DO 的能量输入,这一机理在实验中得以有效验证(S1条件下TN去除率明显大幅低于其他曝气方式)。
由图5b可知,生物阴极MFCs硝化反硝化的最佳运行条件在S3附近,即曝气间歇时长大约采取2 h 时,TN 的去除率最大(即停止供气阶段DO浓度为1.6 mg/L最佳),而其他间歇时长时DO 浓度或偏高或偏低,致使生物阴极MFCs脱氮 TN 的去除率都相对较低[39]。值得注意的是,本实验得出的最佳反应条件为停止曝气阶段DO浓度1.6 mg/L,略高于Third 等[40]提出的最佳硝化-反硝化条件为溶解氧低于1.5 mg/L。有两个可能的原因:①实验水质为高氨氮的废水,其氨氮浓度为380 mg/L,使得硝化过程对氧气需求偏大;②实验进水为高盐废水,而微生物在盐度较高的条件下会生成保护机制,分泌胞外聚合物保护细胞、平衡渗透压、或者改变酶的代谢途径以求生存,这些过程占用了原用于繁殖过程的部分能量,致使微生物繁殖、生长变缓,生物量变少,因而需要更高的氧气浓度去解除盐胁迫[11]。
总的来说,在类似于本实验所涉及的高盐高氨氮电解质条件下,间歇曝气的曝气强度定在40 mL/min,间歇时长2 h附近时,MFCs对污染物TN去除效果最佳。
3 结论
(1)在500 Ω的负载时,生物阴极MFCs在曝气强度20,40,100,200 mL/min下的最大功率密度、开路电压和电池内阻分别为2.72 W/m3、660 mV、131 Ω。控制生物阴极曝气强度在40~100 mL/min之间、DO浓度在4~6 mg/L时,电压输出最大为253 mV,产电周期最长。
(2)当曝气强度控制在40~100 mL/min时,生物阴极MFCs对COD去除效果较为理想。而控制曝气强度在40 mL/min时,氮的去除效果最好。
(3)实验证实了间歇式曝气运行方式既能有效提高生物阴极脱氮性能,又可以减少维持高浓度DO的能量输入。发现曝气方式控制在S3条件(即间歇曝气2 h)时,MFCs对污染物TN去除效果最好,较持续曝气时提高了至少20%。
