Fe(Ⅲ)负载改性橘子皮对Pb2+的吸附性能研究
2020-03-12刘雪梅吴凡章海亮黄晶
刘雪梅,吴凡,章海亮,黄晶
(华东交通大学 土木建筑学院,江西 南昌 330013)
电镀冶金、采矿化工等行业生产会产生含铅废水,铅不可降解累积在生物体中最终通过食物链对人造成危害[1-2]。必须对其加以处理,传统方法在处理低浓度的重金属废水时,处理效率非常低且成本花费特别高[3-5]。但吸附法具有简便经济、高效稳定和吸附容量大等特点。农林废弃物作为吸附剂是目前的研究热点,例如甘蔗渣[6-10]、核桃壳[11-13]、稻壳[14-17]、花生壳[18-22]等。本实验以橘子皮作为生物吸附材料并对其进行改性,研究其对Pb2+的吸附性能,并拟合了动力学方程和等温吸附模型,为橘子皮处理工业废水提供理论基础。
1 实验部分
1.1 试剂与仪器
铅标准储备液(1 000 mg/L)、三氯化铁、氢氧化钠、无水乙醇、盐酸等均为优级纯;实验用水为双重蒸馏水。
美的MJ-PB80Easy218破壁机;DF-101s集热式数显磁力搅拌器;SHZ-82A数显水浴恒温振荡箱;pHS-3E型pH计;AL204型电子分析天平;PE900T原子吸收光谱仪;3-5W低速离心机;DZF系列真空干燥箱;SHZ-D(III)真空抽滤机。
1.2 材料制备
1.2.1 橘子皮的预处理 普通橘子皮(OP)经自来水洗2遍,用去离子水浸泡24 h,再用去离子水清洗3遍,于80 ℃鼓风干燥箱内烘干至恒重,用破壁机粉碎,过40目筛,备用。
1.2.2 橘子皮的改性 称取20 g OP于1 L烧杯里,将300 mL、10% FeCl3加入到处理好的OP中,随后缓慢滴加0.1 mol/L NaOH溶液300 mL。50 ℃恒温搅拌60 min后,搅拌过程中得出系丝状物,离心去除液体部分并用去离子水洗至中性。在80 ℃真空干燥箱烘干备用,得到改性橘皮黑色粉末。
1.3 Pb2+吸附实验
1.3.1 投加量 准确量取铅标准使用液(50 mg/L)50 mL,于8个150 mL锥形瓶中,分别称取普通橘子皮0.02,0.04,0.05,0.06,0.07,0.08,0.09,0.10 g,在30 ℃下恒温振荡2 h,以恒定速率为150 r/min振荡,抽滤取上清液于50 mL的比色管中,然后稀释10倍于原子吸收光谱仪上测定其浓度,计算吸附去除率。
改性橘子皮的实验同上。
1.3.2 pH 准确量取铅标准使用液(50 mg/L)50 mL,于8个150 mL锥形瓶中,称取普通橘子皮0.05 g,用0.1 mol/L的HCl和0.1 mol/L的NaOH分别将溶液的初始pH值调节为2,3,4,4.5,5,5.5,6和7;在30 ℃下恒温振荡2 h,以恒定速率为150 r/min振荡,抽滤取上清液于50 mL的比色管中,然后稀释10倍于原子吸收光谱仪上测定其浓度,计算吸附去除率。
改性橘子皮的实验同上。
1.3.3 吸附时间 准确量取铅标准使用液(50 mg/L)50 mL,于8个150 mL锥形瓶中,称取普通橘子皮0.05 g,将溶液的初始pH值调节为5.5,在30 ℃下恒温振荡20,40,60,70,80,90,100,120 min,以恒定速率为150 r/min振荡,抽滤取上清液于50 mL的比色管中,然后稀释10倍于原子吸收光谱仪上测定其浓度,计算吸附去除率。
改性橘子皮的实验同上。
2 结果与讨论
2.1 投加量对橘子皮吸附Pb2+性能的影响
实验条件同1.3.1节,测定结果见图1。
由图1可知,随着吸附剂的投加量越多,吸附去除率越高,但改性橘子皮的投加量到0.05 g之后就基本不变了,说明吸附达到饱和状态。在投加量为0.05 g时,去除率达到95.66%,考虑到成本问题,确定最佳投加量为1 g/L。
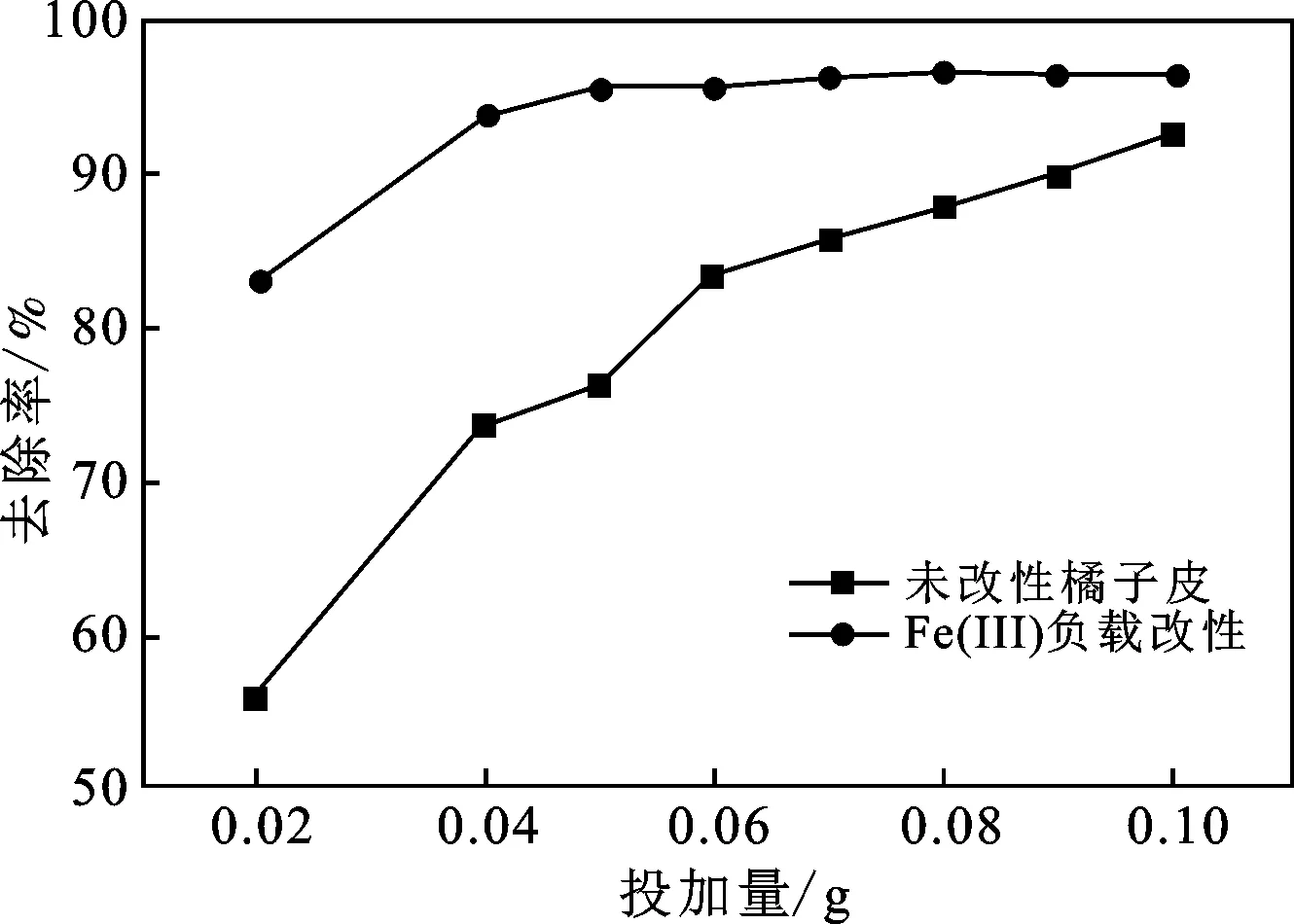
图1 投加量对吸附性能的影响Fig.1 Influence of dosage on adsorption performance
2.2 溶液初始pH值对橘子皮吸附Pb2+性能的影响
由于pH值为7.5时,铅离子会以Pb(OH)2形式沉淀。所以溶液pH值的大小对实验研究有很大的影响,控制pH值是实验的重要因素,按1.3.2节条件进行实验,结果见图2。

图2 pH对吸附性能的影响Fig.2 Influence of pH on adsorption performance
由图2可知,初始溶液的pH较小时,吸附去除率小,造成的原因可能是H+与Pb2+形成竞争吸附,从而降低了吸附率。H+与金属离子Mn+的竞争性吸附是pH影响的主要原因,pH越小时,H+占据了大部分吸附位,阻碍了Mn+的吸附结合,所以H+浓度越高吸附率越小。当溶液pH值增大时,H+浓度减小吸附率变大,pH在5.5之后变化不大。所以控制溶液的pH值为5.5,达到最佳吸附条件。
2.3 吸附时间对橘子皮吸附Pb2+性能的影响
30 ℃下,按1.3.3节条件进行实验,吸附率随时间变化见图3。
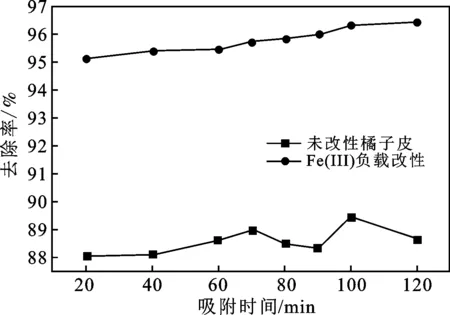
图3 时间对吸附性能的影响Fig.3 Influence of time on adsorptionquasi-secondary performance
由图3可知,改性橘子皮与普通橘子皮对Pb2+的吸附在20 min基本就达到吸附平衡。
2.4 动力学性能研究
取8个150 mL的锥形瓶,每个锥形瓶中,将0.05 g 的普通橘子皮加入到50 mL 50 mg/L的铅离子溶液中,在pH=5.5,30 ℃恒温水浴下,以恒定速率150 r/min振荡,分别振荡20,40,60,70,80,90,100,120 min后,抽滤取上清液于50 mL的比色管中,然后稀释10倍于原子吸收光谱仪上测定其浓度,计算吸附去除率。改性橘子皮的实验同上。用准一级动力学方程、准二级动力学方程及颗粒内扩散方程对实验数据进行拟合。
准一级动力学方程:
ln(qe-qt)=lnqe-k1t
(1)
准二级动力学方程:
(2)
式中 k1——准一级吸附速率常数,h-1;
k2——准二级吸附速率常数,g/(mg·h);
qe和qt——分别为平衡吸附量和在t时的吸附量,mg/g;
t——时间,min。
在生物吸附动力学的研究中,通常用准二级动力学方程对实验数据进行模拟[23]。利用方程式(2)对图3数据模拟,结果见图4。
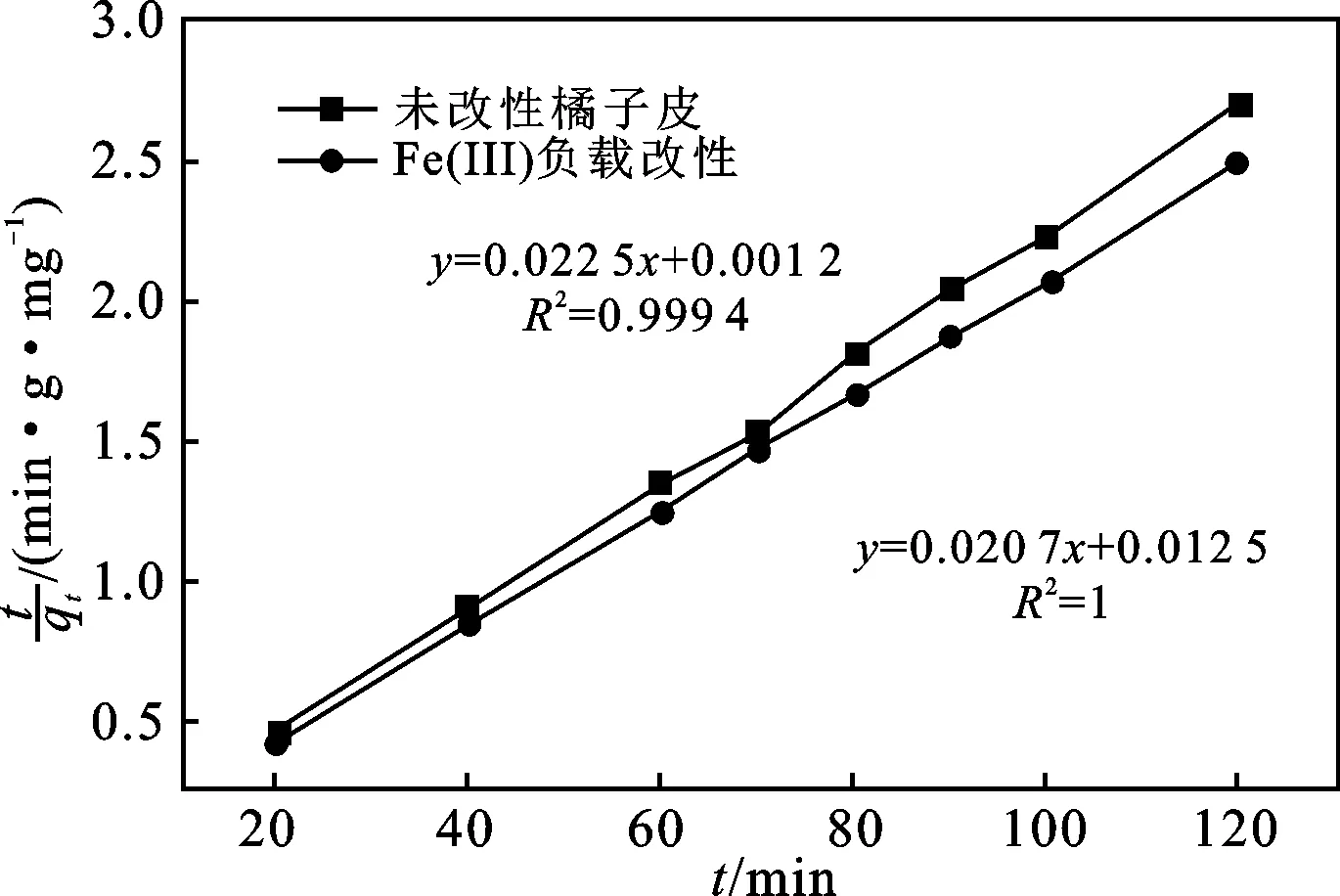
图4 准二级吸附动力学方程模拟结果Fig.4 Simulation results of adsorption kinetic equation
由图4可知,实验结果可以很好地用准二级动力学方程进行模拟,Fe(Ⅲ)负载改性的橘子皮比普通橘子皮相关系数要大,可以更好地描述其吸附过程。

表1 准一级动力学、准二级动力学和内扩散模拟实验数据的相关系数Table 1 The correlation coefficient R2 of quasi-first-order dynamics,quasi-second-order dynamics and internal diffusion simulation data
由表1可知,普通橘子皮与Fe(Ⅲ)改性橘子皮的吸附过程都遵循准二级反应机理,属于化学吸附。
2.5 等温吸附性能研究
取8个150 mL的锥形瓶,每个锥形瓶中,将0.05 g的普通橘子皮加入到50 mL,铅离子溶液初始浓度分别为10,20,40,50,60,80,100,150 mg/L中,在pH=5.5,30 ℃恒温水浴下,以恒定速率150 r/min振荡2 h后,抽滤取上清液于50 mL的比色管中,然后稀释10倍于原子吸收光谱仪上测定其浓度,计算吸附去除率。改性橘子皮的实验同上。得出的实验数据用Langmuir和Freundlich等温吸附方程进行拟合。
Langmuir等温吸附方程:
(3)
式中Ce——平衡时污染物的浓度,mg/L;
qe——平衡吸附量,mg/g;
qm——饱和吸附容量,mg/g;
KL——Langmuir吸附平衡常数,L/mg。
Freundlich等温吸附方程:
(4)
其中,qe为吸附达到平衡时的吸附容量;KF为Freundlich平衡吸附系数;n为特征常数,反映吸附剂的表面不均匀性,以及吸附强度的相对大小;Ce为吸附达到平衡时溶液中污染物的浓度。
图5为普通橘子皮和改性橘子皮在30 ℃下对Pb2+的吸附等温线。

图5 吸附等温线Fig.5 Adsorption isotherm
由图5可知,平衡吸附量随着金属离子浓度的增加而增加。用Langmuir(式4)和Freundlich(式5)吸附等温模型对图4 数据进行模拟,结果见图6和图7。
由图6和图7可知,改性前后的橘子皮对Pb2+的吸附均符合Langmuir和Freundlich模型,但Langmuir吸附等温模型更符合实验数据,可以认为吸附过程是单分子层吸附,以化学吸附为主[24-25]。
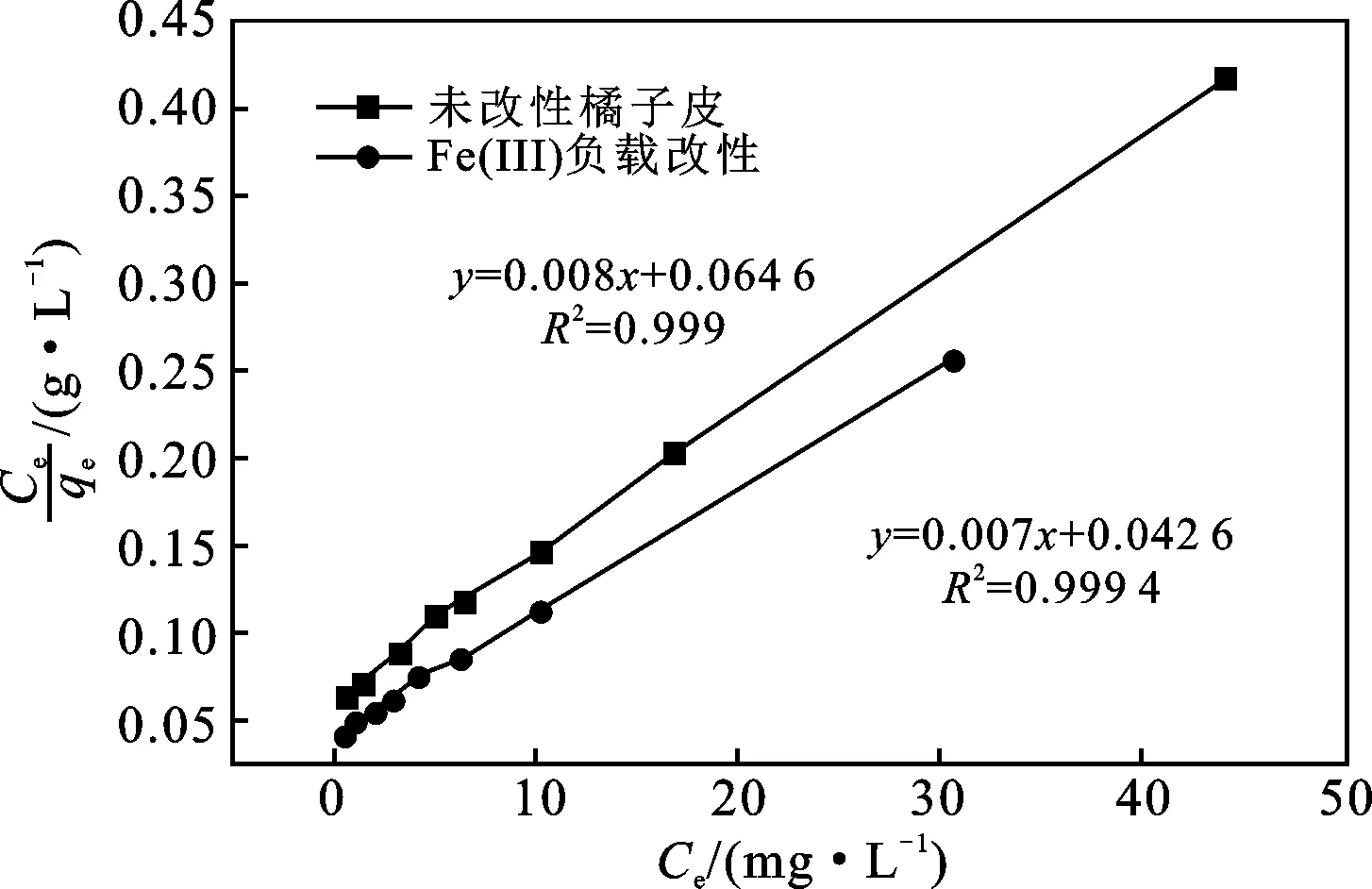
图6 Langmuir吸附等温式Fig.6 Langmuir adsorption isotherm
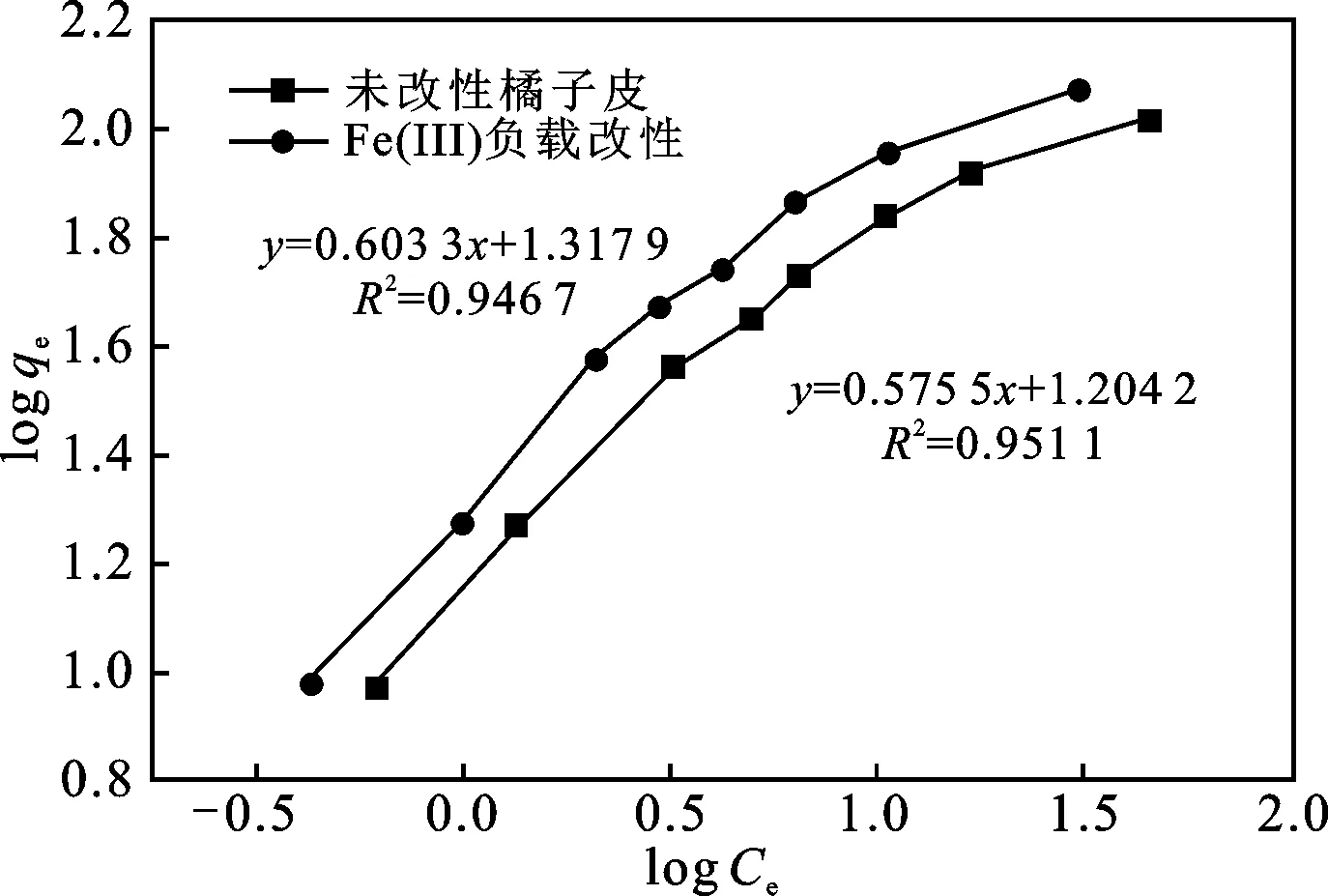
图7 Freundlich吸附等温式Fig.7 Freundlich adsorption isotherm
2.6 其他离子竞争吸附性能的影响
工业废水中含有多种阳离子,会与需要去除的金属离子竞争吸附点位,从而对吸附产生干扰,出现竞争吸附效应。本实验考察了Cd2+、Ni2+和Cu2+对Fe(Ⅲ)改性橘子皮吸附Pb2+的影响。
分别配制50 mg/L+200 mg/L、100 mg/L+200 mg/L和150 mg/L+200 mg/L的Cu2+/Pb2+体系溶液,Cd2+/Pb2+和Ni2+/Pb2+体系溶液同上,各取200 mL。将0.2 g的改性橘子皮加入到上述200 mL的混合溶液,在pH=5.5,30 ℃恒温水浴下,以恒定速率150 r/min振荡2 h后,抽滤取上清液,然后稀释10倍于原子吸收光谱仪上测定其浓度,计算吸附去除率,结果见图8。
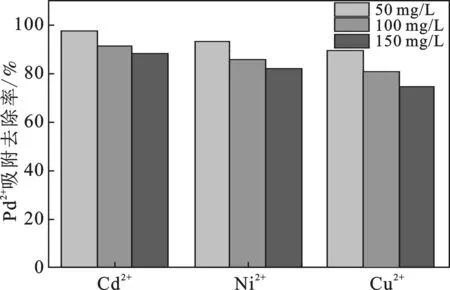
图8 不同阳离子存在时对Pb2+的吸附去除率Fig.8 The adsorption and removal rates of Pb2+ inthe presence of different cations
由图8可知,竞争离子浓度越大,吸附影响就越大。而且不同离子对Pb2+吸附效果影响大小不同,图8中得到的结果是Cu2+>Ni2+>Cd2+,这主要可能是与离子电负性和离子半径有关,对吸附的影响也较大[26]。
2.7 解吸再生实验
向达到吸附平衡的改性橘子皮中加入100 mL 0.1 mol/L的HCl,恒温恒速振荡3 h,过滤水洗至中性,烘干。将0.05 g烘干后的改性橘子皮加入到50 mL 50 mg/L的模拟废水中,恒温恒速振荡2 h,抽滤取上清液于50 mL的比色管中,稀释10倍于原子吸收光谱仪上测定浓度。重复5次上述实验循环。
解吸完再进行吸附性能研究,结果见图9。

图9 吸附性能再生利用Fig.9 The regeneration of adsorption performance
由图9可知,再生后的吸附材料依然具有很好的吸附效果,虽然有所降低,但是吸附能力降低很少。5次循环使用后,吸附率从97.66%降低至91.57%,说明解吸后的吸附材料至少可以循环吸附5次以上。
3 结论
通过橘子皮对Pb2+有效吸附的方法研究表明,得出橘子皮对Pb2+具有良好的吸附性能,而且吸附剂用量少、吸附时间短等优势条件,进一步说明橘子皮在污水处理中具有重要的价值,并为环境减负,实现了农林废弃物的充分利用。
(1)0.05 g的橘子皮和Fe(Ⅲ)负载改性橘子皮对pH 5.5,50 mL 50 mg/L的Pb2+吸附时间为20 min,去除率分别为76.32%,95.66%。改性橘子皮是未改性的1.253倍。
(2)Langmuir等温吸附模型可以很好地模拟实验结果,R2分别为0.999 0,0.999 4。吸附动力学可以用准二级动力学方程描述,R2分别可达0.999 4。表明橘子皮与改性橘子皮对Pb2+的吸附均属于化学吸附过程。
(3)Langmuir等温模型描述出改性后的橘子皮的最大吸附量为119.25 mg/g,高于改性前的105.77 mg/g。这表明Fe(Ⅲ)负载改性的橘子皮吸附性能得到了提高。
