碱性双氧水预处理玉米秸秆性质研究*
2020-03-09侯明韬邢力新郝慧慧
侯明韬,邢力新,郝慧慧
(1. 中国建筑材料科学研究总院,北京 100024;2. 中国建材检验认证集团股份有限公司,北京 100024;3. 北京化工大学,北京 100029)
0 引 言
我国是一个年产秸秆废弃物逾9亿吨的农业大国[1],秸秆废弃物的资源化利用已受到广泛的关注。目前,利用秸秆发酵生产沼气是秸秆资源化利用的重要途径之一,然而由于秸秆中木质素、纤维素及半纤维素具有紧密结合的结构,会影响微生物对纤维素的利用效果[2]。因此,通过预处理提高秸秆的可生化性对促进秸秆资源化利用意义重大[3]。
目前,常见的秸秆预处理手段包括物理法、化学法、物理化学法及生物法等[4-6]。其中,化学处理法操作便捷、经济,在实际应用中受到了广泛的关注。化学处理法是指使用包括酸、碱及氧化剂在内的化学试剂对秸秆进行预处理,其中碱处理在化学处理方式中效果较优,常见的秸秆碱性处理方式包括使用含氢氧化钠、氧化钙等碱性试剂的溶液浸泡秸秆[7-9],利用碱性物质的皂化作用,破坏纤维素、半纤维素和木质素之间的结构,降低木质纤维素原料的聚合度与结晶度,使木质纤维素原料发生溶胀作用[10-11],增加秸秆的酶解及发酵效果[8,12]。此外,利用氧化剂的氧化分解作用,氧化降解生物质中的木质素,降低秸秆的结晶度,也能提高秸秆的水解糖化及发酵效果[13-16]。
近年来,科研工作者使用氧化剂与碱性溶液耦合的方式预处理秸秆亦取得了良好的效果[17-23]。例如,李辉勇等[14]使用臭氧与氢氧化钠耦合预处理秸秆,获得了92.57%的水解糖化率;周殿芳等[24]使用质量分数为2.5%的碱性双氧水处理秸秆,木质素的去除率达到61.52%,酶解糖化率为39.03%。然而,MISHIMA等[25]发现双氧水单独使用不能有效处理秸秆,而在李辉勇的实验中,最优的碱性双氧水使用量仅能使秸秆酶解糖化效果比NaOH单独使用提高10.78%[22],证明氧化剂在碱处理秸秆中的贡献作用有限。
目前,关于氧化剂及碱处理秸秆的机理研究较为充沛,但两者耦合使用时的机理研究较为薄弱。本文使用H2O2和NaOH质量比为5∶8的碱性双氧水对玉米秸秆进行预处理,考察预处理剂对秸秆酶解糖化效果的影响,并优化其预处理参数。随后,对经H2O2、NaOH及碱性双氧水预处理后的秸秆固体及预处理浸出液进行分析,探讨双氧水及氢氧化钠分别在秸秆预处理中的作用。
1 材料与方法
1.1 实验材料与仪器
实验采用的玉米秸秆取自北京昌平区,选取干净完整的玉米叶片,将其剪短为1 ~ 3 cm的片段,使用粉碎机将其粉碎并过60目筛后待用。水解酶为绿色纤维素木酶(上海金穗生物),使用 whatman滤纸测定纤维素酶活(FPA = 159 FPU/g)[26]。实验中所用双氧水(30%)、氢氧化钠(A.R.)购自北京化工厂,二硝基水杨酸(A.R.)购自成都市科龙化工试剂厂。
1.2 实验方法
1.2.1 预处理方法
秸秆预处理在烧杯中进行,固液比(m/v%)为5%,使用的预处理剂为H2O2与NaOH的混合溶液(H2O2∶NaOH = 5∶8,质量比)。将秸秆置于烧杯中,加入一定量碱性双氧水搅拌均匀后迅速用封口膜封口,随后将烧杯置于恒温油浴中控温预处理一定时间,反应结束后,用去离子水清洗秸秆至中性,抽滤分离秸秆,于60℃烘箱中干燥至恒重待用。
1.2.2 秸秆水解方法
秸秆水解实验在装有100 mL柠檬酸缓冲液(50 mmol/L,pH = 4.8)的碘量瓶中进行,秸秆用量为1.00 g,纤维素酶使用量为48 FPU。将碘量瓶置于恒温气浴摇床(荣华仪器制造有限公司,SHZ-82气浴恒温振荡器)中进行水解反应,摇床转速为180 r/min,水解温度为40℃,水解一定时间后取样,经离心分离后取上层清液用DNS法测量溶液中的还原糖浓度[27]。
1.2.3 预处理秸秆表征方法
为考察实验所用碱性双氧水预处理玉米秸秆的机理,采用范式法测定秸秆中的木质纤维素含量[28](上海洪纪仪器设备有限公司,FIWE3/6型),使用扫描电子显微镜(SEM)观测预处理前后秸秆的表面形貌(Hitachi,SU 1510)。
1.2.4 预处理浸出液分析方法
用气相色谱−质谱(GC-MS)测定秸秆预处理浸出液成分(岛津,GCMS-QP 2010 SE)。参考文献[29]的方法,取离心后的秸秆预处理浸出液2 mL,加入盐酸调节溶液pH < 2,用4 mL乙醚萃取,随后用微量注射器取 1 μL乙醚相注入气相色谱−质谱测定。
气相色谱条件:色谱柱为 DB-5MS,柱径0.25 mm,膜厚0.25 μm,长30 m;升温程序:初温55℃保持0.5 min,以15℃/min升温到100℃,保持1 min,以20℃/min升温到200℃,保持1 min,以15℃/min升温到280℃,保持1 min;扫描方式:全扫描(Scan),扫描范围(m/z)35 ~ 500。
2 结果与分析
2.1 预处理剂使用量对秸秆酶解糖化的影响
实验首先考察不同碱性双氧水使用量对玉米秸秆水解糖化的影响,预处理温度为40℃,预处理时间为24 h。如图1所示,随碱性双氧水加入量的增加,玉米秸秆水解液还原糖浓度在0 ~ 12 h内提升,并在24 h时达到稳定,随后呈现略微下降的趋势,这可能是还原糖被进一步水解的缘故[15]。因此,随后的实验均采用24 h水解还原糖浓度评价预处理效果。如图1所示,随预处理剂加入量的提高,秸秆24 h水解还原糖浓度逐渐增加,当H2O2与NaOH加入量达秸秆质量的16%与25.6%时(H2O2∶NaOH =5∶8,质量比),还原糖浓度基本维持不变,因此最优预处理剂加入量选为秸秆质量16% H2O2+ 25.6%NaOH。
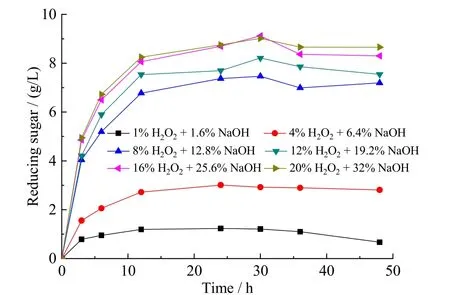
图 1 不同预处理剂加入量对玉米秸秆酶解效果与反应时间的关系Fig. 1 The concentration of reducing sugar as a function of time under different pretreating dose
2.2 预处理时间对玉米秸秆水解糖化的影响
选用上述得到的最优预处理剂使用量,在预处理温度为40℃条件下,考察预处理时间对玉米秸秆水解糖化效果的影响。如图2所示,随预处理时间从3 h延长到24 h,酶解还原糖量由7.84 g/L逐步提高到8.69 g/L。当预处理时间达到48 h时,秸秆的水解还原糖量基本恒定(8.78 g/L)。考虑到预处理时间从3 h延长到24 h不会显著增加预处理成本,因此随后均采用24 h为预处理时间进行实验。
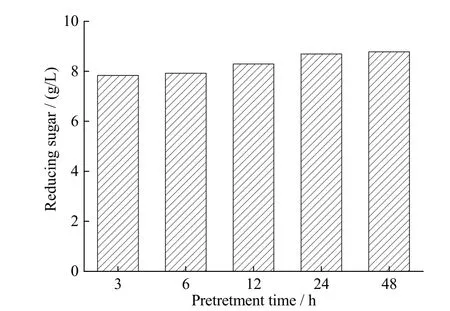
图2 不同预处理时间对玉米秸秆24 h酶解的影响Fig. 2 Effect of pretreating time on the enzymolysis of corn straw at 24 h
2.3 预处理温度对玉米秸秆水解糖化的影响
选用秸秆质量16% H2O2+ 25.6% NaOH的预处理剂量,预处理24 h,考察预处理温度对预处理后秸秆酶解糖化的影响。可以发现,在预处理温度为20 ~ 40℃范围内,随预处理温度的升高,秸秆的水解糖化效果有一定的提高,24 h酶解还原糖量由7.03 g/L逐步提高到8.67 g/L。但是,当预处理温度超过40℃时,预处理温度的提高反而引起还原糖浓度的下降(50℃下酶解还原糖量为8.53 g/L,60℃下为8.59 g/L),这是由于过高的预处理温度增加了过氧化氢的热不稳定性,导致其木质纤维素脱除效果降低的缘故[30]。因此,后续试验均在预处理温度40℃下进行。

图3 不同预处理温度对玉米秸秆24 h酶解效果的影响Fig. 3 Effect of pretreating temperature on the enzymolysis of corn straw at 24 h
本实验中,预处理温度对于秸秆预处理效果的影响不明显,类似的现象也有诸多科研工作者观察到[19,21-22],这可能是预处理剂(H2O2、NaOH)与木质纤维素的反应受温度影响较小的缘故。另外,实验发现,向秸秆中加入碱性双氧水后,烧杯中立即产生大量的泡沫,约2 h后泡沫逐渐消失,说明双氧水已反应完全,由此可见,双氧水主要在预处理初期发挥作用,预处理时间延长带来的酶解效果提高应该是氢氧化钠存在引起的结果。
2.4 强碱性双氧水预处理玉米秸秆机理研究
为考察碱性双氧水与秸秆作用的过程,分别对比未处理(Blank)、去离子水(H2O)、H2O2(16%)、NaOH(25.6%)及碱性双氧水(16% H2O2+ 25.6%NaOH)处理后的秸秆酶解糖化效果(预处理剂量皆以秸秆质量的百分比计)。预处理温度为 40℃,时间为24 h。如图4可知,秸秆水解糖化效果优劣顺序为 Blank ≈ H2O ≈ H2O2< NaOH < 碱性双氧水,其24 h水解还原糖量分别为1.35 g/L、1.35 g/L、1.59 g/L、7.48 g/L、8.26 g/L,H2O2单独使用时的秸秆预处理效果与H2O相似,皆不能有效提高秸秆酶解效果。
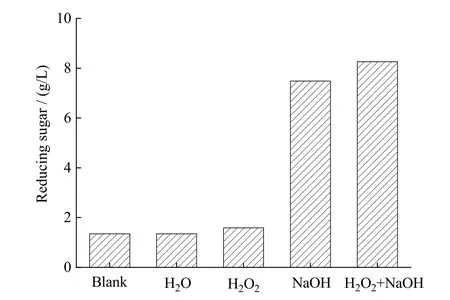
图4 不同预处理剂对玉米秸秆24 h酶解效果的影响Fig. 4 Effect of different pretreating agents on the enzymolysis of corn straw at 24 h
对经以上 4种预处理后的秸秆成分进行分析(图5)可以发现,经H2O与H2O2处理后,秸秆中的木质纤维素及杂质含量相似,与空白试验相比,主要表现为杂质成分的降低,说明H2O2单独使用无法对秸秆木质纤维素成分产生明显影响。而 NaOH处理明显提高了纤维素含量,降低了半纤维素与木质素含量,H2O2的加入则进一步强化了该效果。
SEM分析预处理前后秸秆表面形貌(图6),发现未经处理(Blank,图6a)与经过水浸泡(H2O,图6b)的秸秆表面结构较为平整,未被明显破坏。经过双氧水处理后(H2O2,图 6c),秸秆表面产生一定破碎,这是双氧水的氧化作用破坏了纤维素、半纤维素和木质素之间的连接键,使得秸秆中质地较疏松的部分被破坏,产生较大空隙,比表面积增大。经过NaOH处理后(图6d),秸秆中半纤维素及木质素成分被大量溶出(图5),秸秆表面变粗糙并出现少量的破损,这同样增大了秸秆的表面积,且有利于纤维素水解酶与秸秆内部发生作用。经碱性双氧水处理后的秸秆表面(H2O2+NaOH,图6e)同样表现为严重破损,这应该是NaOH与H2O2联合作用的效果。
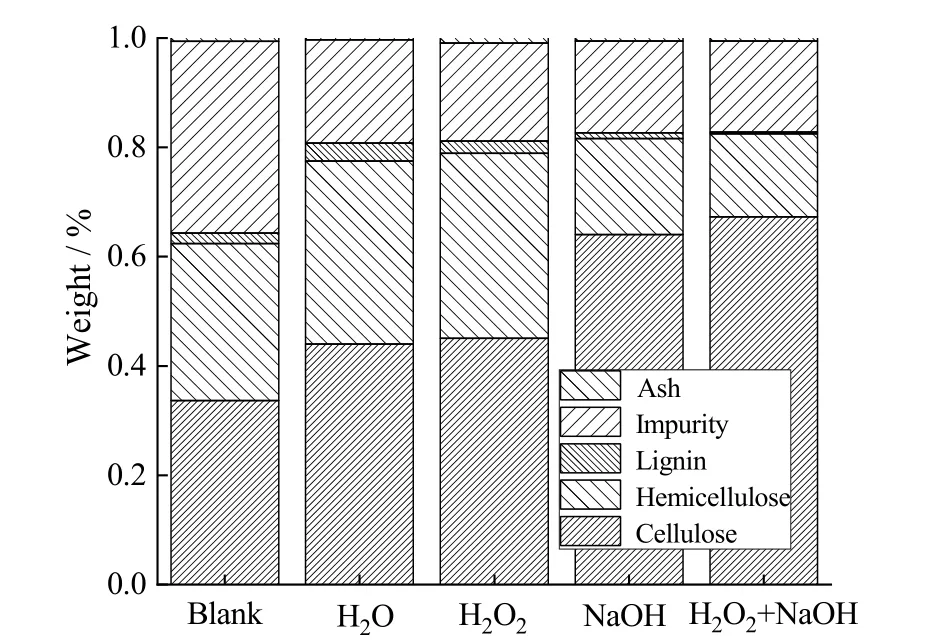
图 5 不同预处理剂预处理后秸秆木质纤维素含量Fig. 5 Lignocellulose content of straw pretreated by different pretreatment agents

图6 不同预处理剂处理后秸秆表面SEM图像:(a)未处理(Blank),(b)经H2O处理,(c)经H2O2处理,(d)经NaOH处理,(e)经碱性双氧水处理;(f)不同预处理秸秆浸出液Fig. 6 Images of scanning electron microscope (SEM) of straw surface pretreated by different pretreatment agents: (a) untreated straw (Blank), (b) H2O, (c) H2O2, (d) NaOH, (e) alkaline hydrogen peroxide; (f) leaching liquor picture of straw pretreated by different pretreating agents
以上结果证实,H2O2主要破坏秸秆结构,NaOH则作用于秸秆成分。碱性H2O2对秸秆的预处理效果主要由NaOH提供,H2O2辅助提高了NaOH对秸秆的预处理效果。实验中发现,秸秆经NaOH与碱性H2O2预处理前后质量损失(TS损失率分别为47.6%与50.0%)及木质纤维素含量(图5)相似,然而经 NaOH处理后的秸秆浸出液为棕黑色,经碱性H2O2处理后的秸秆浸出液为深棕色(图 6f),说明H2O2的存在虽然没有对秸秆成分产生明显影响,但其却与被NaOH溶解的木质纤维素发生了反应。
使用乙醚萃取秸秆浸出液并进行GC-MS分析。如图7所示,经H2O、H2O2及NaOH预处理后的秸秆浸出液GC-MS总离子流图(TIC)中未发现明显出峰(图7 a ~ 图7c),而经碱性双氧水处理后的秸秆浸出液提取物TIC图中可以检测到若干明显响应(图7d)。这可能是由于NaOH虽然可以溶解秸秆中的木质素及半纤维素,却未能破坏其大分子结构,因此不能被乙醚溶解,而H2O2可以与被NaOH溶解的大分子有机物发生氧化还原反应,其产物能够被乙醚溶解并在GC-MS中能被检测到。对峰强度(H)大于50 000的组分进行检索,表1列举了相似度 >80的物质。可以发现,检索结果主要为携带双键及羟基的各类环状及直链有机化合物,这应该是木质纤维素被氧化分解的结果。
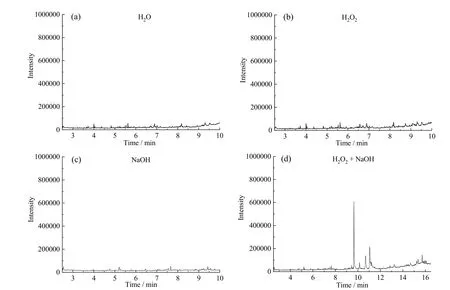
图7 秸秆浸出液GC-MS分析:(a)H2O处理;(b)H2O2处理;(c)NaOH处理;(d)H2O2+NaOH处理Fig. 7 GC-MS image of straw leach liquor: (a) H2O; (b) H2O2; (c) NaOH; (d) H2O2 + NaOH
3 结 论
碱性双氧水预处理秸秆可以显著提高秸秆的酶解糖化效果,试验发现NaOH在预处理过程中起溶解秸秆中木质素及半纤维素的作用,对秸秆预处理效果的优劣起决定作用。H2O2的加入虽然不能对秸秆中的木质纤维素成分产生明显影响,却可以破坏秸秆表面结构,辅助提高NaOH的秸秆预处理效果。此外,当H2O2与NaOH共同使用时,H2O2可作用于被NaOH溶解的大分子物质,将其分解为多种小分子有机物,这为秸秆资源化利用提供了新途径。
