稻壳炭制备工艺参数对吸附性能的影响
2020-03-05刘晓刚李翠清宋永吉
田 雨,刘晓刚,赵 玉,詹 华,王 虹※,李翠清,宋永吉
稻壳炭制备工艺参数对吸附性能的影响
田 雨1,2,刘晓刚1,赵 玉1,詹 华1,王 虹1※,李翠清1,宋永吉1
(1. 北京石油化工学院化学工程学院/燃料清洁化及高效催化减排技术北京市重点实验室,北京 102617;2. 北京工业大学环境与生命学部,北京 100124)
以稻壳为原料,采用水热法制备稻壳炭,将稻壳炭用于吸附印染废水中亚甲基蓝。利用XRD、SEM、TG、FT-IR等手段对稻壳炭进行表征分析,探究炭化温度和炭化时间对稻壳炭理化性质和亚甲基蓝吸附性能的影响。结果表明,炭化温度是影响稻壳炭吸附性能的重要因素。炭化时间为4 h,炭化温度为180~220 ℃,稻壳炭对亚甲基蓝去除率大于90%,亚甲基蓝的吸附量大于6.27 mg/g,其中,炭化温度为200℃、炭化时间为8 h,即(RH-200-8)的稻壳炭结构完整,稻壳炭产率较高为65.20%,亚甲基蓝的去除率和吸附能力分别为93.04%和6.62 mg/g。炭化温度为180~220 ℃,纤维素未完全分解,孔隙结构良好,孔径适中,有利于亚甲基蓝分子的扩散与吸附,含氧官能团数量较多,吸附活性点位较多,对亚甲基蓝吸附性能较好。炭化温度大于220 ℃,随着炭化温度的升高,纤维素和富氧官能团的分解加速,吸附活性点位减少,稻壳炭结构发生改变,比表面积增加,但最可几孔径减小,不利于亚甲基蓝分子的扩散,导致稻壳炭对亚甲基蓝的去除率和吸附能力降低。RH-200-8稻壳炭再生循环使用实验表明,RH-200-8稻壳炭再生次数增加,稻壳炭对亚甲基蓝去除率略有下降,RH-220-8-3(即稻壳炭使用第3次)的亚甲基蓝去除率达82.20%(10 h)。
生物质炭;吸附;水热炭化;稻壳;亚甲基蓝
0 引 言
随着印染技术的发展,中国造纸、纺织、皮革和制造等行业使用染料时产生大量印染废水,印染废水排放造成水污染,破坏生态环境,危害人体健康[1-3]。随着环保意识加强,处理印染废水已刻不容缓。印染废水具有水量大、有机毒物含量高[4-5]、成分复杂及难降解[4]等特点,是国内外公认较难处理的工业废水之一。印染废水的处理方法主要有物理法、化学法和吸附法[6]。其中,吸附法具有效率高、成本低、易开发等优点,是目前污染治理技术中广泛应用的方法之一[1-2,6]。
生物炭具有比表面积较大、孔隙度较高等特点,表现出良好的吸附性,广泛应用于吸附废水中有机污染物和无机污染物等。水热炭是生物质经过一系列的水解、缩合、脱羧和脱水反应形成以脂肪族化合物为主的生物炭[7],热解炭是以芳香族化合物为主的生物炭[8-9]。水热炭化(HTC)是在封闭的系统中将生物质置于水悬浮液中加热到180~260 ℃,把生物质转化为热化学更稳定的、纳米结构的水热炭[8-10]。相比于热解炭化,水热炭化是一种环境友好的新兴环保技术,因其具有产率高[11]、反应条件温和[12]、成本低和工艺简单环保[8,12]等优点,受到国内外学者的广泛关注。
稻壳是稻米加工的副产物,来源广泛、价格低廉,是可再生的富碳生物质资源[13],稻壳生物炭是一种良好的生物质基污染物去除吸附材料[6,14-15],是稻壳高附加值资源化利用途径之一。王洪杰等[16]研究发现,使用KMnO4改性的水热稻壳炭吸附孔雀石绿和甲基橙,其去除率可以达到90%。Jian等[17]考察了不同炭化温度对水热稻壳炭和热解稻壳炭的亚甲基蓝吸附性能,结果表明,水热稻壳炭对亚甲基蓝表现出更强的亲和力。稻壳炭作为吸附剂具有较好的应用前景,但是稻壳炭的处理和再生过程的损失限制了其发展。
本研究以稻壳为原料,采用水热法制备稻壳炭,运用XRD、SEM、TG和FT-IR等手段对稻壳炭的理化性质进行表征,系统考察炭化温度和炭化时间稻壳炭对亚甲基蓝吸附性能的影响及其稻壳炭再生循环使用吸附性能。
1 材料与方法
1.1 试剂与仪器
稻壳,采购于三聚环保公司;亚甲基蓝(C16H18ClN3S,纯度>97%),美国Aladdin公司。
热重分析,STA449F3型,耐驰科学仪器商贸(上海)有限公司;X射线粉末衍射仪,XRD-7000型,日本岛津株式会社;pH计,pH525型,天津市赛得利斯;水浴恒温振荡器,SHA-C型,巩义予华仪器有限责任公司;紫外可见分光光度计,7890B型,Agilent;扫描电子显微镜,S-4800型,日本日立公司;傅里叶红外光谱仪,Vector22型,德国Bruker公司。
1.2 稻壳炭的制备
采用水热法制备稻壳炭。稻壳经干燥研磨成粉末状,冲洗干燥备用。稻壳炭典型制备过程如下:称取4 g稻壳,加入80 mL去离子水,置于内衬为100 mL的聚四氟乙烯反应釜中,在电热恒温鼓风干燥箱(DF-101S)中升至目标温度(180、200、220、240和260 ℃),停留规定时间(2、4、6、8和10 h),冷却至室温,3 500 r/min离心5 min、乙醇和水洗数次后,置于干燥箱中100 ℃干燥7 h后得到稻壳炭,称量计算稻壳炭产率(即反应后稻壳炭质量与原料质量之比)。稻壳炭标记为RH-,RH代表原料为稻壳(Rice Husk),为炭化温度,为炭化时间。
稻壳炭再生:将亚甲基蓝吸附性能最佳的稻壳炭置于烧杯中,加入10 mL乙醇超声10 min,离心3 min,重复3次;再加入10 mL甲苯重复超声洗涤3次后,移入旋转蒸发器中60 ℃真空干燥,恒温干燥箱80 ℃干燥6 h,取出备用。RH-200-8-(=1、2、3,定义为稻壳炭再生次数)。
1.3 稻壳炭表征方法
采用日本岛津XRD-7000型X射线衍射仪(XRD)检测稻壳炭的晶相结构。试验条件为:Cu-K靶,管电流30 mA,电压40 kV,扫描速度4(°)/min,扫描步长0.02º,扫描范围10°~80°。
采用日本日立S-4800型扫描电子显微镜(SEM)观察稻壳炭形貌。
热失重(TG)分析采用耐驰科学仪器商贸(上海)有限公司STA449F3型热重仪器测量。试验条件为:高纯氮气为载气,气体流速为100 mL/min,以10 ℃/min的升温速率从40 ℃升温至1 000℃。
采用pH525型pH计测定稻壳炭的pH值。稻壳炭和水以1∶10的比例混合,室温下震荡4 h,离心取上清液。
采用德国Bruker公司Vector22型傅里叶变换红外(FT-IR)光谱仪进行测定。试验条件为:扫描范围400~4 000 cm-1,分辨率4 cm-1,扫描次数64次。稻壳炭与KBr质量比为1∶100压片。
采用北京金埃普科技公司的比表面积及孔径分析仪(V-Sorb 2800型)测定比表面积(BET)及孔结构。0.15 g稻壳炭粉末预处理:第一阶段40 ℃处理30 min,第二阶段80 ℃处理60 min;-196 ℃进行N2吸附。
1.4 稻壳炭吸附亚甲基蓝试验
模拟印染废水配制:以亚甲基蓝为印染废水中模型化合物,去离子水为溶剂,配制3.5 mg/L亚甲基蓝溶液,密封置于冰箱中备用。
亚甲基蓝吸附试验:称12.5 mg稻壳炭置于50 mL锥形瓶中,加入25 mL模拟印染废水,混合均匀,30 ℃下恒温震荡10 h,每隔2 h使用带有孔径为0.45m聚四氟乙烯滤头的注射器吸取3 mL亚甲基蓝溶液,采用紫外-可见分光光度计(SOPTOP-752型)在波长为665 nm处测量亚甲基蓝浓度,按公式(1)和公式(2)计算亚甲基蓝去除率()和吸附量(Q),以亚甲基蓝去除率评价稻壳炭的吸附能力。


式中为亚甲基蓝去除率,%;Q为时刻稻壳炭对亚甲基蓝的吸附量,mg/g;0、C分别为亚甲基蓝的初始浓度和时刻质量浓度,mg/L;为溶液的体积,L;为稻壳炭的质量,g。
2 结果与讨论
2.1 稻壳炭吸附亚甲基蓝性能
图1是炭化温度和炭化时间与稻壳炭吸附亚甲基蓝关系曲线。由图1a可知,炭化时间为4 h,随着炭化温度升高,亚甲基蓝去除率先升高后下降。炭化温度为180~220 ℃,稻壳炭吸附性能较好,亚甲基蓝去除率均高于90%,稻壳炭对亚甲基蓝吸附量为6.27 mg/g,其中炭化温度为200 ℃,亚甲基蓝去除率较高,为91.35%,吸附量为6.44 mg/g;当炭化温度高于220 ℃,亚甲基蓝去除率和吸附量急剧下降,主要原因是炭化温度过高(>220 ℃),纤维素过度分解,形成较大的炭颗粒附着并粘连在稻壳炭表面,使稻壳炭孔隙减少,同时,含氧官能团分解、缩合、芳香化,吸附活性点位减少,导致稻壳炭吸附亚甲基蓝性能变差[2]。
由图1b可知,炭化温度为200 ℃,随着炭化时间延长,稻壳炭对亚甲基蓝去除率和吸附量先升高后降低,但整体去除水平较高。去除率高于91.14%,消耗量大于6.38 mg/g,其中RH-200-8稻壳炭的吸附性能较好,亚甲基蓝去除率为93.04%,吸附量为6.62 mg/g,但吸附量低于文献[17](9.7 mg/g)。原料来源及制备方法和条件等均影响稻壳炭对亚甲基蓝的吸附性能。
图2为RH-220-8-(=1、2、3,为RH-220-8样品使用次数)稻壳炭上亚甲基蓝去除率与吸附时间关系曲线。由图2可知,随着反应时间的增加,RH-200-8稻壳炭对亚甲基蓝去除率逐渐增大。吸附时间为0~2 h,稻壳炭对亚甲基蓝去除率快速增加;吸附时间为2~10 h,稻壳炭对亚甲基蓝去除率缓慢增加,逐渐趋于平衡。由图2看到,RH-200-8稻壳炭再生后,对亚甲基蓝的吸附性能不能完全恢复,且随着再生次数增加,亚甲基蓝去除率降低,吸附时间为10 h,第1次吸附到第3次吸附,亚甲基蓝去除率分别为95.85%、88.81%、82.20%。
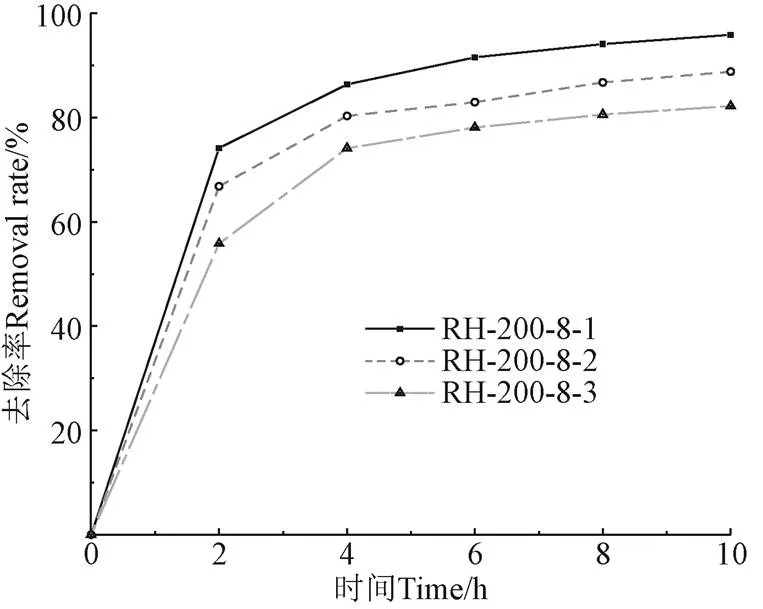
图2 RH-220-8-n(再生次数n=1、2、3)稻壳炭上亚甲基蓝去除率与吸附时间关系曲线
2.2 稻壳炭结构表征
2.2.1稻壳炭产率
图3为炭化温度和炭化时间对稻壳炭产率的影响。由图3稻壳炭产率与炭化温度关系曲线可知,炭化时间为4 h,随着炭化温度升高,炭化温度由180 ℃升至200 ℃,稻壳炭产率略有降低,由69.13%降至68.80%,仅下降0.33个百分点,变化率为0.17%/℃;炭化温度由200升至240 ℃,稻壳炭产率由68.80%降至51.50%,下降17.30个百分点,变化率为0.43%/℃;炭化温度由240升至260 ℃,稻壳炭产率下降缓慢,由51.50%降至50.09%,下降1.41个百分点,变化率为0.07%/℃。稻壳炭产率在200~240 ℃之间变化显著,稻壳炭产率随炭化温度变化趋势和文献[18]研究成果一致。稻壳主要组成成分为纤维素、半纤维素和木质素[19]。炭化时间为4 h,炭化温度低于200 ℃,稻壳中半纤维素分解为低分子有机物,炭化温度达220 ℃,稻壳炭产率急剧下降,纤维素发生脱水缩合反应,分解成为小分子气体和有机物[20],随着炭化温度升高,固体有机物发生二次分解,高度缩合转化为不可缩合的气体,炭化温度为240~260 ℃,未分解的纤维素继续分解,而木质素由复杂苯环聚合物组成,其结构基本保持不变[18]。
由图3稻壳炭产率与炭化时间关系曲线看到,炭化温度为200 ℃,炭化时间由2 h延长至10 h,稻壳炭产率由69.58%降至65.20%,仅降低4.38个百分点,炭化时间延长,仅使纤维素分解更完全,挥发性物质逐渐减少,稻壳炭产率趋于稳定[21]。由此可见,炭化温度是影响稻壳炭产率的主要因素,炭化时间对稻壳炭产率影响不显著[22-23]。

图3 炭化温度和炭化时间对稻壳炭产率的影响
2.2.2TG表征分析
图4为稻壳炭TG曲线图。由图4a可知,RH-T-4稻壳炭重量损失主要为2个阶段[24]:第一阶段,小于150 ℃的质量损失主要为水分蒸发,其水分损失为大气含水和稻壳本身;第二阶段,200~600 ℃,稻壳炭的质量损失为纤维素、半纤维素和木质素的挥发和分解[19],半纤维素最不稳定,主要在220~315 ℃阶段分解,其次是纤维素,主要在315~400 ℃阶段分解,木质素最稳定,分解温度范围宽达至900 ℃。随着炭化温度升高,RH-T-4稻壳炭最大失质量率逐渐降低,表明炭化温度升高,稻壳在水热炭化中纤维素等物质分解更加完全,稻壳炭的热稳定性提高[24]。
由图4b可以看出,炭化温度为200 ℃,随着炭化时间延长,RH-200-稻壳炭质量损失率逐渐降低。RH-200-稻壳炭(为2、4、6、8和10 h)最大质量损失率分别为76.89%、70.98%、68.28%、64.57%和63.21%,表明炭化时间延长,纤维素等物质分解更完全,炭化时间大于8 h,稻壳炭的热稳定性逐渐增强,表明稻壳炭结构已趋于稳定[24]。
2.2.3XRD表征分析
图5为稻壳炭XRD谱图。由图5a可知,炭化时间为4 h,炭化温度为180~220 ℃,稻壳炭在2为16°和22°出现归属纤维素的特征峰(2为22°也可能是SiO2特征峰,与纤维素存在重叠峰),且随着炭化温度升高,峰强度无明显变化,表明较低炭化温度未能破坏纤维素结构[25]。炭化温度达240 ℃,纤维素的特征衍射峰明显减弱,表明较高的炭化温度破坏了纤维素结构,炭化温度对稻壳炭组成和结构影响较显著。稻壳炭在2值为44°和77°附近的特征峰归属于炭结构(PDF#99-0043),炭的形成有利于稻壳吸附亚甲基蓝[6]。由图5b可知,炭化温度为200 ℃,炭化时间对纤维素结构没有显著影响。

注:图a中的数字为炭化温度,℃;图b中的数字为炭化时间,h。下同。
2.2.4SEM表征分析
图6为稻壳炭SEM照片。由图6可知,炭化温度不同,RH-T-4稻壳炭形貌存在差异性。RH-200-4稻壳炭基本保留纤维状结构,表面结构光滑,稻壳炭部分炭化和挥发性气体释放,表面具有明显的凹槽和团聚的大块颗粒,大大增加稻壳炭吸附亚甲基蓝的活性点位[5]。RH-220-4稻壳炭纤维状结构粗糙坍塌,出现大量裂隙,炭球尺寸增大,纤维素开始分解。RH-240-4稻壳炭纤维素逐渐分解,形成大量的炭球发生粘连附着在孔隙上[21]。RH-260-4稻壳炭表面产生不同形状的炭球覆盖在稻壳炭表面。随着炭化温度升高,纤维素和半纤维素水解聚合反应加快,导致炭球粘连、覆盖在稻壳炭上,进而导致孔隙减少,活性点位减少,稻壳炭的吸附性能下降,与稻壳炭吸附亚甲基蓝结果一致。


图6 不同炭化温度稻壳炭SEM照片
2.2.5BET表征结果
图7为稻壳炭的等温吸附曲线(图7a)和孔径分布(图7b)。根据国际纯粹与应用化学联合会对孔径大小的规定表示介孔范围为2~50 nm。由图7a可知,稻壳炭的吸附脱附等温曲线为典型的带有明显H4型滞后环的第IV型的等温曲线类,表明不同炭化温度下,制备的稻壳炭均为介孔结构。由图7b可知,炭化温度为180~220 ℃,稻壳炭为明显的介孔结构。随着炭化温度的升高,比表面积和孔径增加(见表1),炭化温度为240 ℃,比表面积达到最大,为30.621 m2/g;炭化温度为220 ℃,最可几孔径最大,为6.743 nm,炭化温度继续升高,孔径范围较为分散,最可几孔径大幅度减小,炭化温度为240 ℃,最可几孔径仅为2.486 nm。炭化温度为240 ℃,RH-240-4样品虽然比表面积较大,但对亚甲基蓝吸附性能较差;而炭化温度为200 ℃和220 ℃,即RH-200-4和RH-220-4虽然比表面积较RH-240-4样品小,亚甲基蓝吸附性能较好。稻壳炭对亚甲基蓝的吸附性能同时与孔结构和表面含氧官能团有关[2],随着炭化温度的升高,有利于孔隙的形成,但是炭化温度过高也加速了含氧官能团的分解,所以比表面积不是影响稻壳炭吸附性能唯一因素。

注:为系统压力;0为大气压力。
Note:is system pressure;0atmospheric pressure.
图7稻壳炭的N2等温吸附曲线和孔径分布图
Fig.7N2adsorption-desorption isotherms and pore size distribution of rice husk carbon

表1 稻壳炭的物性分析结果
2.2.6pH值测定结果
图8为稻壳炭的pH值曲线图。由图8可知,随着炭化温度升高和炭化时间延长,由于稻壳中纤维素等分解成各种有机酸,如甲酸、乙酸和乳酸等[26],稻壳炭pH值均呈现下降趋势。RH-T-4稻壳炭,炭化温度由180 ℃升至260 ℃,稻壳炭pH值从4.47降至4.16,降幅为0.31。RH-200-h稻壳炭,炭化时间由2 h延长至10 h,稻壳炭pH值从4.40降至4.25,降幅为0.15。pH值测定结果显示,炭化温度升高加速纤维素的分解,炭化时间达到8 h后,再延长炭化时间,对纤维素等分解影响不显著,与TG表征结果一致。
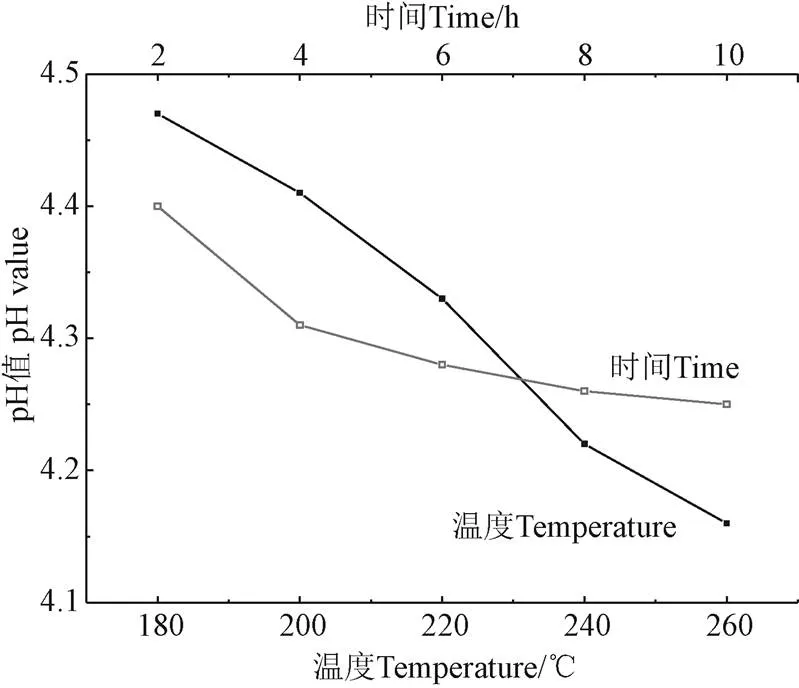
图8 稻壳炭的pH值变化
2.2.7FT-IR表征分析
图9为稻壳炭的FT-IR谱图。由图9可知,3 419 cm-1处的吸收峰归属于O-H的伸缩振动[27];2 925 cm-1处的吸收峰归属于脂肪族C-H的伸缩振动[27];2 379 cm-1处的吸收峰归属于C≡C的伸缩振动;1 730 cm-1处的吸收峰归属于羧基、醛、酮和酯类基团上的C=O振动[26];1 598 cm-1处的吸收峰归属于芳香C=C振动[27];1 435 cm-1处的吸收峰归属于COOH或CH=O的振动[28];1 160 cm-1吸收峰归属于C-O振动;798和466 cm-1的吸收峰归属于Si-O键振动[29]。
由图9a可知,炭化时间为4 h,随着炭化温度升高,在官能团区(3 500~1 500 cm-1),3 419 cm-1(-OH)峰强度降低,表明稻壳炭脱水脱氢缩合和不饱和程度加剧;而2 925 cm-1(C-H)、2 852 cm-1(C-H)、2 379 cm-1(C≡C)、1 730 cm-1(C=O)和1 598 cm-1(C=C)峰强度增加,表明稻壳炭逐渐脂肪化和芳香化。在指纹区(1 500~500 cm-1),RH-T-4稻壳炭的峰强度较高,分别有葡萄糖醇基(C-OH)、纤维素糖苷键(C-O-C)、木质素芳基醚(-OCH3)、半纤维素酮基(C=O)等含氧官能团。炭化温度为200 ℃时,稻壳炭中的纤维素结构基本完整,具有较多的丰富的含氧官能团,稻壳炭表面-OH、COOH等官能团充当吸附活性点位,而亚甲基蓝(染料阳离子)通过静电作用相互吸引[6],进而增强稻壳炭吸附亚甲基蓝[2,28],当炭化温度达到240 ℃,稻壳炭中的含氧官能团分解、缩合和芳香化而明显减少,致使稻壳炭的吸附性能降低。此外,随着炭化温度升高,798 cm-1(Si-O)峰强度增加,表明SiO2在稻壳炭中富集,这与XRD相符合。
由图9b可知,炭化温度为200 ℃,随着炭化时间延长,在2 379 cm-1(C≡C)呈现先增强后平稳的趋势。表明稻壳炭脱氢缩合程度加剧,炭化时间达到8 h后稳定。3 419 cm-1(-OH)、2 925 cm-1(C-H)和指纹区含氧官能团变化不显著,稻壳炭的吸附性能基本保持在91.14%之上,表明RH-200-稻壳炭中纤维素和木质素未完全分解,稻壳炭中存在丰富含氧官能团。

图9 稻壳炭FT-IR谱图
3 结 论
采用水热法制备稻壳炭,考察炭化温度和炭化时间对稻壳炭理化性质和亚甲基蓝吸附性能的影响,结果表明炭化温度是影响稻壳炭吸附性能的重要因素。炭化时间4 h,炭化温度为180~220 ℃之间,稻壳中半纤维素和纤维素逐渐分解,形成孔隙结构清晰、含氧官能团较多、产率较高的稻壳炭,稻壳炭对亚甲基蓝的吸附脱硫性能维持在较高水平,稻壳炭对亚甲基蓝去除率和吸附量分别高于90%和6.27 mg/g;当炭化温度大于220 ℃,炭化温度的升高,使稻壳炭结构坍塌破碎,纤维素分解加速,稻壳炭中的含氧官能团分解、缩合和芳香化,吸附活性点位减少,稻壳炭结构发生改变,比表面积增加,但最可几孔径减小,不利于亚甲基蓝分子的扩散,稻壳炭的吸附性能降低。炭化温度为200 ℃,延长炭化时间,稻壳炭球化明显,形貌逐渐良好,稻壳炭的吸附性能略有提高,其中炭化温度为200 ℃,炭化时间为8 h,稻壳炭结构完整,含氧官能团较多,活性点位较多,稻壳炭吸附亚甲基蓝性能较好,分别为93.04%和6.62 mg/g。RH-200-8稻壳炭再生循环使用试验表明,随着稻壳炭再生次数的增加,稻壳炭的去除率略有下降,RH-220-8-3稻壳炭的亚甲基蓝最大去除率达82.20%。
[1]Li W, Mu B, Yang Y. Feasibility of industrial-scale treatment of dye wastewater via bio-adsorption technology[J]. Bioresource Technology, 2019, 277: 157-170.
[2]Wang B, Zhai Y, Wang T, et al. Fabrication of bean dreg-derived carbon with high adsorption for methylene blue: Effect of hydrothermal pretreatment and pyrolysis process[J]. Bioresource Technology, 2019, 274: 525-532.
[3]Bu J, Yuan L, Zhang N, et al. High-efficiency adsorption of methylene blue dye from wastewater by a thiosemicarbazide functionalized graphene oxide composite[J]. Diamond and Related Materials, 2020, 101: 107604.
[4]Zhu Y, Xu J, Cao X, et al. Characterization of functional microbial communities involved in different transformation stages in a full-scale printing and dyeing wastewater treatment plant[J]. Biochemical Engineering Journal, 2018, 137: 162-171.
[5]Hou Y, Yan S, Huang G, et al. Fabrication of N-doped carbons from waste bamboo shoot shell with high removal efficiency of organic dyes from water[J]. Bioresource Technology, 2020, 303: 122939.
[6]Shamsollahi Z, Partovinia A. Recent advances on pollutants removal by rice husk as a bio-based adsorbent: A critical review[J]. Journal of Environment Management, 2019, 246: 314-323.
[7]Lu X, Flora J R V, Berge N D. Influence of process water quality on hydrothermal carbonization of cellulose[J]. Bioresource Technology, 2014, 154: 229-239.
[8]Unur E, Brutti S, Panero S, et al. Nanoporous carbons from hydrothermally treated biomass as anode materials for lithium ion batteries[J]. Microporous and Mesoporous Materials, 2013, 174: 25-33.
[9]李音,单胜道,杨瑞芹,等. 低温水热法制备竹生物炭及其对有机物的吸附性能[J]. 农业工程学报,2016,32(24):240-247. Li Yin, Shan Shengdao, Yang Ruiqin, et al. Preparation of bamboo biochars by low-temperature hydrothermal method and its adsorption of organics[J]. Transactions of the Chinese Society of Agricultural Engineering (Transactions of the CSAE), 2016, 32(24): 240-247. (in Chinese with English abstract)
[10]Islam M A, Benhouria A, Asif M, et al. Methylene blue adsorption on factory-rejected tea activated carbon prepared by conjunction of hydrothermal carbonization and sodium hydroxide activation processes[J]. Journal of the Taiwan Institute of Chemical Engineers, 2015, 52: 57-64.
[11]常春,刘天琪,王瑀婷,等. 水热法制备玉米叶基生物炭对亚甲基蓝的吸附性能研究[J]. 环境科学学报,2017,37(7):2680-2690. Chang Chun, Liu Tianqi, Wang Yuting, et al. Hydrothermal preparation of maize leaf based biochar and its adsorption performance for methylene blue[J]. Acta Scientiae Circumstantiae, 2017, 37(7): 2680-2690. (in Chinese with English abstract)
[12]刘慧慧,曲磊,陈应泉,等. 天然微藻水热炭理化特性及热解动力学研究[J]. 农业工程学报,2019,35(14):235-242. Liu Huihui, Qu Lei, Chen Yingquan, et al. Physicochemical characteristics and pyrolysis kinetics of hydrothermal carbon from natural scenedesmus[J]. Transactions of the Chinese Society of Agricultural Engineering (Transactions of the CSAE), 2019, 35(14): 235-242. (in Chinese with English abstract)
[13]Eduah J O, Nartey E K, Abekoe M K, et al. Phosphorus retention and availability in three contrasting soils amended with rice husk and corn cob biochar at varying pyrolysis temperatures[J]. Geoderma, 2019, 341: 10-17.
[14]Hu L, He Z, Zhang S. Sustainable use of rice husk ash in cement-based materials: Environmental evaluation and performance improvement[J]. Journal of Cleaner Production, 2020, 264: 121744.
[15]Zhang Y, Yue X, Xu W, et al. Amino modification of rice straw-derived biochar for enhancing its cadmium (II) ions adsorption from water[J]. Journal of Hazardous Materials, 2019, 379: 120783.
[16]王洪杰,兰依博,李晓东. KMnO4改性稻壳、稻秆水热炭吸附染料的研究[J]. 应用化工,2019,48(6):1344-1350. Wang Hongjie, Lan Yibo, Li Xiaodong. Hydrothermal synthesis of KMnO4modified rice husk and rice straw and its adsorption properties[J]. Applied Chemical Industry, 2019, 48(6): 1344-1350. (in Chinese with English abstract)
[17]Jian X, Zhuang X, Li B, et al. Comparison of characterization and adsorption of biochars produced from hydrothermal carbonization and pyrolysis[J]. Environmental Technology & Innovation, 2018, 10: 27-35.
[18]Gao Y, Wang X, Yang H, et al. Characterization of products from hydrothermal treatments of cellulose[J]. Energy, 2012, 42(1): 457-465.
[19]Kalderis D, Kotti M S, Méndez A, et al. Characterization of hydrochars produced by hydrothermal carbonization of rice husk[J]. Solid Earth, 2014, 5(1): 477-483.
[20]Xu J, Zhang J, Huang J, et al. Conversion of phoenix tree leaves into hydro-char by microwave-assisted hydrothermal carbonization[J]. Bioresource Technology Reports, 2020, 9: 100353.
[21]He C, Giannis A, Wang J Y. Conversion of sewage sludge to clean solid fuel using hydrothermal carbonization: Hydrochar fuel characteristics and combustion behavior[J]. Applied Energy, 2013, 111: 257-266.
[22]Khan T A, Saud A S, Jamari S S, et al. Hydrothermal carbonization of lignocellulosic biomass for carbon rich material preparation: A review[J]. Biomass and Bioenergy, 2019, 130: 105384.
[23]Wang Z, Zhai Y, Wang T, et al. Effect of temperature on the sulfur fate during hydrothermal carbonization of sewage sludge[J]. Environmental Pollution, 2020, 260: 114067.
[24]Li J, Zhao P, Li T, et al. Pyrolysis behavior of hydrochar from hydrothermal carbonization of pinewood sawdust[J]. Journal of Analytical and Applied Pyrolysis, 2020, 146: 104771.
[25]Sun Y, Gao B, Yao Y, et al. Effects of feedstock type, production method, and pyrolysis temperature on biochar and hydrochar properties[J]. Chemical Engineering Journal, 2014, 240: 574-578.
[26]Jain A, Balasubramanian R, Srinivasan M P. Hydrothermal conversion of biomass waste to activated carbon with high porosity: A review[J]. Chemical Engineering Journal, 2016, 283: 789-805.
[27]Wu J, Yang J, Huang G, et al. Hydrothermal carbonization synthesis of cassava slag biochar with excellent adsorption performance for rhodamine B[J]. Journal of Cleaner Production, 2019, 251: 119717.
[28]Reza M T, Rottler E, Herklotz L, et al. Hydrothermal carbonization (HTC) of wheat straw: Influence of feedwater pH prepared by acetic acid and potassium hydroxide[J]. Bioresource Technology, 2015, 182: 336-344.
[29]Adam F, Fook C L. Chromium modified silica from rice husk as an oxidative catalyst[J]. Journal of Porous Materials, 2009, 16(3): 291-298.
Effects of preparation process parameters of rice husk carbon on adsorption performance
Tian Yu1,2, Liu Xiaogang1, Zhao Yu1, Zhan hua1, Wang Hong1※, Li Cuiqing1, Song Yongji1
(1.,,102617,; 2.,,100124,)
Rice husk carbon was prepared by hydrothermal method from rice husk, and used to adsorb methylene blue from printing and dyeing wastewater. Rice husk carbon was characterized by X-ray diffraction(XRD), Scanning Electron Microscope(SEM), Thermo Gravimetric(TG), Fourier Transform Infrared Spectrometer(FT-IR), and the effects of hydrothermal temperature and hydrothermal time, respectively, on the physicochemical properties and adsorption properties of methylene blue in rice husk carbon were investigated. The results showed that hydrothermal temperature was the important factor to affect the adsorption performance of rice husk carbon. In this study, when the hydrothermal time was 4 h and the hydrothermal temperature was 180-220 ℃, the removal rate of methylene blue in rice husk carbon was more than 90% and the adsorption capacity of rice husk carbon to methylene blue was more than 6.27 mg/g. Among them, the hydrothermal temperature was 200 °C and the hydrothermal time was 8 h(RH-200-8), the structure of rice husk carbon was intact and the yield of rice husk carbon was 65.20%. Besides, theremoval rate and adsorption capacity of methylene blue in rice husk carbon were 93.04% and 6.62mg /g in the same condition, respectively. The phenomenon was due to thecellulose was not completely decomposed, the pore structure of rice husk carbon was better and the pore diameter of rice husk carbon was moderate when the hydrothermal temperature was 180-220 °C. In addition, the structure of rice husk carbon was conducted to the methylene blue molecule diffusion and adsorption, and rice husk carbon has more oxygen-containing functional groups with more adsorption active points, so the adsorption performance of rice husk carbon on methylene blue was better. When the hydrothermal temperature was greater than 220 °C, with the increase of hydrothermal temperature, the cellulose would be accelerated decomposition, the oxygen-enriched functional groups were decomposed quickly, the adsorption activity points of rice husk carbon were reduced, the rice husk carbon structure was also changedand the specific surface area was increased, but most probable pore sizes of rice husk carbon were decreased, the phenomenon was not conducted to the methylene blue molecule diffusion in rice husk carbon, so the removal rate and adsorption ability of methylene blue in rice husk carbon decreased. The experiment of rice husk carbon(RH-200-8) regeneration and recycling showed thatthe removal rate of methylene blue in rice husk carbon decreased slightly with the number of rice husk carbon regeneration increased, and the maximum methylene blue removal rate of RH-220-8-3(Rice husk charcoal use 3rd) reached 82.20% (10 h).
biomass carbon; adsorption; hydrothermal carbonization; rice husk; methylene blue
田雨,刘晓刚,赵玉,等. 稻壳炭制备工艺参数对吸附性能的影响[J]. 农业工程学报,2020,36(24):211-217.doi:10.11975/j.issn.1002-6819.2020.24.025 http://www.tcsae.org
Tian Yu, Liu Xiaogang, Zhao Yu, et al. Effects of preparation process parameters of rice husk carbon on adsorption performance[J]. Transactions of the Chinese Society of Agricultural Engineering (Transactions of the CSAE), 2020, 36(24): 211-217. (in Chinese with English abstract) doi:10.11975/j.issn.1002-6819.2020.24.025 http://www.tcsae.org
2020-08-01
2020-11-02
国家自然科学基金(21673290)
田雨,研究方向为环境工程。Email:1583610160@qq.com
王虹,博士,教授,主要从事环境治理技术研究。Email:wanghong@bipt.edu.cn
10.11975/j.issn.1002-6819.2020.24.025
TQ424
A
1002-6819(2020)-24-0211-07
